El extracto de metanol de la cáscara de Beta Vulgaris Rubra L. (remolacha) reduce el estrés oxidativo y estimula la proliferación celular mediante el aumento de la expresión de VEGF en células endoteliales de la vena umbilical humana con estrés oxidativo inducido por H2O2
Feb 22, 2022
Por favor contactaroscar.xiao@wecistanche.compara saber mas
Laila Naif Al-Harbi 1*, Subash-Babu Pandurangan 1, Alhanouf Mohammed Al-Dossari 1, Ghalia Shamlan 1, Ahmad Mohammad Salamatullah 1, Ali A Alshatwi 1 y Amna Abdullah Alotiby 2
Resumen:La capacidad antioxidante de los polifenoles yflavonoidespresente en los agentes dietéticos ayuda a detener el desarrollo de especies reactivas de oxígeno (ROS) y protege las células del músculo liso endotelial del estrés oxidativo/necrosis inducida. La remolacha (Beta vulgaris var. Rubra L.; BVr) es una verdura de consumo común que representa una rica fuente deantioxidantes. Los compuestos bioactivos de la cáscara de remolacha y su papel en las células endoteliales de la vena umbilical humana (HUVEC, por sus siglas en inglés) aún están poco investigados. En el presente estudio, se preparó extracto de metanol de cáscara de remolacha (BPME) y su efecto sobre la bioeficacia, la integridad nuclear, el potencial de membrana mitocondrial, el crecimiento de células vasculares y los niveles de expresión génica relacionados con la inmunorregulación en HUVEC con inducción.oxidativoSe analizó el estrés. Los resultados de la cromatografía de gases-espectroscopia de masas (GC-MS) confirmaron que BPME contiene 5-hidroximetilfurfural (32,6 %), piruvato de metilo (15,13 %), furfural (9,98 %) y 2,3-dihidro{{11} },5-dihidroxi-6-metil-4H-pirano-4-ona (12,4 %). El extracto de BPM mejoró efectivamente la proliferación celular y fue confirmado por el ensayo MTT; la integridad nuclear se confirmó mediante ensayo de tinción con yoduro de propidio (PI); el potencial de membrana mitocondrial (∆ψm) se confirmó mediante el ensayo de tinción JC-1. El ensayo de anexina V confirmó que las HUVEC tratadas con BPME mostraron un 99 % de células viables, pero solo se mostró una viabilidad del 39,8 % en las HUVEC tratadas con H2O2 solo. Además, el tratamiento con BPME de HUVEC durante 48 h redujo la expresión de mRNA de peróxido lipídico (LPO) y aumentó NOS-3, Nrf-2, GSK-3 , GPX, óxido nítrico sintasa endotelial (eNOS ) y los niveles de expresión del ARNm del factor de crecimiento de células vasculares (VEGF). Encontramos que el tratamiento con BPME disminuyó el proinflamatorio (factor nuclear-κ (F-κ), factor de necrosis tisular- (TNF-), receptor tipo toll-4 (TLR-4), interleucina{{37} } (IL-1 ))y vascularinflamación(molécula de adhesión intracelular (ICAM), molécula de adhesión de células vasculares (VCAM), EDN1, IL-1) relacionadas con expresiones de ARNm. En conclusión, el tratamiento con cáscara de remolacha aumentó efectivamente los factores de crecimiento de células lisas vasculares y el desarrollo de microtúbulos, mientras que disminuyó los reguladores inflamatorios vasculares. BPM puede ser beneficioso para la regeneración de células lisas vasculares, la reparación de tejidos y el potencial antienvejecimiento.
Palabras clave:raíz de remolacha; estrés oxidativo; mitocondrias; angiogénesis; inflamación

Haga clic aquí para obtener más información.
1. Introducción
La angiogénesis es el proceso fisiológico de vasculogénesis a partir de la vasculatura existente en el cuerpo [1]. Es esencial no solo para el desarrollo embrionario y la reproducción, sino también para el ciclo celular y la reparación de tejidos [2,3]. Sin embargo, se asocia con la patogenia de diversas enfermedades, como el crecimiento tumoral, la artritis reumatoide y diversas enfermedades isquémicas e inflamatorias [3–5]. El endotelio vascular juega un papel importante en el mantenimiento de la hemostasia vascular al regular el tono de los vasos sanguíneos y las reacciones inmunitarias e inflamatorias [6,7]. Las células endoteliales (EC) son capas monocelulares delgadas que recubren todas las superficies internas de los vasos sanguíneos y producen una variedad de moléculas que actúan localmente o en sitios distantes [7]. El endotelio es fundamental para la homeostasis corporal, y cualquier alteración en la respuesta de las células del endotelio conduce a los eventos primarios de procesos inflamatorios y vasculares, como la aterosclerosis y la hipertensión [6,8,9]. Estas enfermedades provocan estrés oxidativo, que altera la estructura y la función de las EC y conduce a una disfunción endotelial [9]. Las CE de la vena umbilical humana (HUVEC) se han utilizado ampliamente como modelo para estudios relacionados con el endotelio vascular humano. Además, representan un modelo útil para estudiar las principales vías biológicas implicadas en la función del endotelio [10]. Los compuestos bioactivos y los fitoquímicos se encuentran abundantemente en frutas, verduras, hierbas verdes y muchas plantas, que presentan numerosos beneficios para la salud, como propiedades antiinflamatorias, antioxidantes, anticancerígenas y angiogénicas [11–13]. En este sentido, la remolacha roja (Beta vulgaris var. Rubra L.; BVr) pertenece a la familia Amaranthaceae y está catalogada como una de las mejores fuentes de altos niveles de antioxidantes [14,15]. Específicamente, contiene múltiples fitoquímicos que son biológicamente activos, incluidosbetalaínas, flavonoides,polifenoles, enzimas terapéuticas, ácido ascórbico, ácido dehidroascórbico (DHAA) y nitrato inorgánico (NO3) [16–18]. Además, proporciona valiosos nutrientes esenciales, como potasio, calcio, magnesio, sodio, hierro, zinc, fósforo, cobre y manganeso [19]. Varios estudios han informado que el extracto de remolacha roja (raíz) tiene numerosos efectos beneficiosos debido a sus propiedades hipoglucemiantes, hipolipemiantes, antiinflamatorias, antihipertensivas y antiproliferativas [20-22]. Todas estas propiedades beneficiosas pueden estar relacionadas con las capacidades de eliminación de radicales libres de los compuestos bioactivos. Así, el consumo de remolacha roja se ha relacionado con numerosos beneficios nutricionales y para la salud. Debido a su valor nutricional, puede utilizarse como fuente de alimento funcional contra el estrés oxidativo que induce enfermedades metabólicas crónicas, como la diabetes tipo 2 y las enfermedades cardiovasculares [23]. Según la revisión de la literatura, Beta vulgaris posee potentes propiedades antioxidantes, inmunorreguladoras y angiogénicas. Se ha encontrado apigenina en hojas de remolacha; tiene efectos antiproliferativos en el hígado y las células intestinales, y puede mejorar la comorbilidad de la obesidad inducida por una dieta alta en grasas a través de la activación de AMPK [24,25]. De Silva et al., (2020) [26] identificaron que Beta vulgaris protege a las CE vasculares del estrés oxidativo inducido externamente, lo que puede deberse al efecto combinado de varios compuestos bioactivos presentes en esta planta. Hasta ahora, la acción mecánica para la proliferación de EC y el efecto de angiogénesis de la cáscara de raíz de Beta vulgaris ha sido poco investigada. Por lo tanto, nuestro objetivo fue realizar el presente estudio para examinar la proliferación de células vasculares, el desarrollo de microtúbulos, el estrés oxidativo y la capacidad de angiogénesis relacionada con la exfoliación de la raíz de Beta vulgaris utilizando la morfología celular y el análisis de expresión génica en HUVEC. Se exploran los efectos angiogénicos del extracto de metanol de la cáscara de remolacha roja asociados con la integridad nuclear, el desarrollo de microtúbulos, la eficiencia mitocondrial y la estimulación del ciclo celular en EC vasculares humanos.
2. Materiales y métodos
2.1. Preparación de remolachaExtracto de metanol (Beta vulgaris rubra L.) Las muestras de remolacha fresca (Beta vulgaris var. Rubra L.; BVr.) se obtuvieron inicialmente de tiendas de verduras, Riyadh, Reino de Arabia Saudita (KSA). Las remolachas frescas se lavaron con agua destilada para eliminar los tallos y los contaminantes. Se peló la piel exterior para quitarla y cortarla en trozos pequeños. Las muestras se secaron en un horno de aire caliente a 40 ◦C y luego se molieron hasta convertirlas en polvo usando una licuadora electrónica. Luego, se extrajeron 5{{10}}0 g del polvo en un frasco estéril que contenía 1 L de metanol (Sigma, St. Louis, MO, EE. UU.) durante 24 h a temperatura ambiente en una coctelera y se repite tres veces. Posteriormente, se utilizó un filtro Whatmanfifilter (Whatman, Clifton, NJ, EE. UU.) para filtrar el extracto. Finalmente, reduciendo la presión, el solvente se separó del extracto y el extracto se recogió como una sustancia seca sólida después de la evaporación del metanol. La muestra extraída se conservó en nevera a 4 ◦C hasta su uso posterior. 2.2. Cromatografía de gases y análisis de espectroscopia de masas El extracto de metanol de cáscara de remolacha (BPME) se inyectó en una columna capilar de sílice (30 m × {{60}},25 mm DI × 0 0,25 µm de espesor de película) del instrumento GC-MS (Agilent 6890N/5973I, California, CA, EE. UU.) con un detector selectivo de masas para detectar las composiciones químicas. La temperatura del instrumento se fijó como inicial de 7{{90}} ◦C, manteniéndola durante 2 min, a 305 ◦C a 20 ◦C/min, seguida de una retención de 1 min. El tiempo total de funcionamiento del GC se ajustó a 45 min con el gas helio (99,999 %) como gas portador (una tasa constante de 1,2 ml/min), 250 ◦C como temperatura del inyector y 230 ◦C como fuente de iones. la temperatura. Con base en el espectro de GC-MS, se calculó el porcentaje relativo del componente correspondiente y se identificaron los espectros de masas del componente desconocido comparándolos con los 62,000 patrones conocidos disponibles en el Instituto Nacional de Estándares y Tecnología. biblioteca informática (NIST08). 2.3. Materiales de cultivo celular y productos químicos Las HUVEC se adquirieron de la Colección Americana de Cultivos Tipo (ATCC, Manassas, VA, EE. UU.). Los materiales de cultivo celular como el medio Eagle modificado de Dulbecco (DMEM), EDTA, tripsina y otros se obtuvieron de Gibco (Paisley, Reino Unido). La penicilina-estreptomicina (PS) y el suero bovino fetal (FBS) se adquirieron de Hyclone Laboratories, EE. UU. Los productos químicos utilizados en el experimento de biología molecular se obtuvieron de Sigma-Aldrich, especialmente, MTT [3-(4,5-dimetiltiazol-2-il)-2,5- bromuro de difeniltetrazolio], PI y tinción JC-1. La SYBR Green PCR Master Mix y el kit de síntesis de ADNc se obtuvieron de Qiagen (Hilden, Alemania). 2.4. HUVEC Las HUVEC se cultivaron en DMEM y se complementaron con un 1 por ciento de PS y un 10 por ciento de complejo FBS. Las células se incubaron en una atmósfera húmeda a 37 ◦C, 5 por ciento de CO2 y se subcultivaron aproximadamente cada 3 días. 2.5. Viabilidad celular y proliferación celular mediante ensayo MTT Se cultivaron HUVEC (1 × 104 células/pocillo) con un medio de mantenimiento y se permitió que se adhirieran durante la noche en una placa de cultivo de 96-pocillos. Luego, el medio se reemplazó con un nuevo medio de cultivo que contenía concentraciones crecientes de BPME (0, 0,05, 0,1, 0,2, 0,4, 0,8, 1,6 y 3,2 µg/mL) según el mapa de la placa de ensayo MTT y se incubó durante 24 y 48 h; las células no tratadas se usaron como controles. Después del período de incubación, las células experimentales se trataron con 20 µL/pocillo de 5 mg/mL de MTT (3-[4,5-dimetiltiazol-2-il]-2, 5-bromuro de difeniltetrazolio que se disolvió en dimetilsulfóxido (DMSO)) y adicionalmente se incubó durante 4 h a 37 ◦C. Luego, se descartó el medio y el formazán púrpura producido se disolvió en 100 µl de DMSO al 100 por ciento. La absorbancia de la solución se midió utilizando un lector de microplacas (Thermo Scientific, Waltham, MA, EE. UU.) a una longitud de onda de 570 nm. El porcentaje ( por ciento ) de proliferación celular se calculó mediante la siguiente ecuación: (absorbancia de la muestra/absorbancia media del control) × 100. 2.6. Diseño experimental De acuerdo con el presente ensayo de proliferación celular, la concentración inferior probada de BPME (0,1 y 0,2 µg/mL) mostró HUVEC en proliferación y morfología de microtúbulos sin toxicidad. Se seleccionaron volúmenes de dosis de 0,1 y 0,2 µg/ml de BPME y se trataron con HUVEC normales y HUVEC 10 mM de H2O2-inducidas con estrés oxidativo durante 48 h para determinar los potenciales de proliferación celular, antiinflamatorio, angiogénico y apoptótico. (Figura 1). El control del vehículo también se mantuvo durante 48 h en ambos grupos. Se utilizó quercetina (10 µM) como control de referencia en ambos grupos experimentales. Después de la incubación, se analizó la morfología celular y nuclear y el potencial de membrana mitocondrial de las células no tratadas y experimentales utilizando un kit BDTM MitoScreen (JC-1); la apoptosis se determinó mediante el método de clasificación de células basado en Anexina V/apoptosis en citometría compañera. Se investigaron los niveles de expresión génica relacionados con el estrés oxidativo, proinflamatorio y angiogénesis.

2.7. Ensayo de tinción con yoduro de propidio para daño nuclear Morfologías celulares para daño nuclear característico, picnosis o cambios morfológicos apoptóticos después del tratamiento con 0.1 y 0.2 µg/mL de BPME (con o sin H2O2) en HUVEC se determinó usando análisis de tinción PI bajo microscopía de fluorescencia invertida, como se describe por Leite et al. [27].
2.8. Ensayo del potencial de la membrana mitocondrial (∆ψm) por tinción con tinte JC-1 }.1 y 0.2 µg/ml de HUVEC tratadas con BPME (con y sin H2O2). Brevemente, la solución de tinción JC-1 se mezcló con un volumen similar de medio de cultivo y luego se agregó a las HUVEC experimentales y se incubó en la oscuridad durante 20 min a 37 ◦C. Luego, el tinte JC-1 no unido se lavó suavemente dos veces usando 200 µL de tampón de lavado de tinción JC-1 a 4 ◦C. Posteriormente, la acumulación de j-agregado contra la tinción de JC-1 se observó bajo microscopía de fluorescencia usando un microscopio de fluorescencia, y se capturaron imágenes. Además, se midió el potencial de la membrana mitocondrial en citometría de flujo utilizando el Kit BDTM MitoScreen (JC-1).
2.9. Análisis de apoptosis/anexina V mediante citometría de flujo Se utilizó el método del kit de detección de apoptosis/Anexina V basado en citometría (Sigma Chemicals, EE. UU.) para cuantificar células viables, proapoptóticas, apoptóticas tempranas y necróticas. Las HUVEC inducidas por el estrés oxidativo (1 × 105/pocillo) se sembraron en 24-placas de pocillos y se incubaron con BPME (0.1 y 0,2 µg/mL) o vehículo de control para 48 horas Después de la incubación, las células se incubaron en 400 µl de 5 µl de anexina V-isotiocianato de fluoresceína (FITC) y 5 µl de tampón de unión que contenía PI; después de esto, las células se mantuvieron durante 15 min a temperatura ambiente (RT) en la oscuridad. Las células se analizaron mediante citometría (BD Biosciences, San José, CA, EE. UU.) para identificar células apoptóticas (PI negativas y anexina V positivas) y apoptóticas tardías (PI positivas y anexina V positivas) [28].
2.10. Análisis cuantitativo de PCR en tiempo real Se usó el kit Fastlane® Cell to cDNA (Qiagen, Hilden, Alemania) para extraer el ARN total y sintetizar el ADNc del control del vehículo, HUVEC tratados con BPME (con y sin H2O2) usando una PCR cuantitativa (qPCR) semiautomatizada. instrumento (Applied Biosystems, Foster City, CA, EE. UU.). Los niveles de expresión del estrés oxidativo incluyen (peróxido lipídico, NOS-3), antioxidante (Nrf-2, GSK-3 y GPx), proinflamatorio (factor nuclear-κ (NF-κ), factor de necrosis tumoral- (TNF-), interleucina-1 (IL-1 ), factor de crecimiento de células vasculares (VEGF), receptor tipo toll-4 (TLR-4)) , e inflamación vascular (molécula de adhesión intracelular (ICAM), molécula de adhesión de células vasculares (VCAM), EDN1 y óxido nítrico sintasa endotelial (eNOS)) y el gen de referencia, -actina, se analizaron en HUVEC y se cuantificaron por el método de Yuan et al. [29]. Los valores de amplificación (∆Ct) se calcularon por la diferencia entre Ct (tratados) y Ct (control). La expresión génica se trazó utilizando la expresión del valor 2−∆∆Ct.
2.11. Análisis estadístico Todos los experimentos se triplicaron y los datos resultantes se expresaron como valores medios ± desviación estándar (DE). El análisis estadístico de las diferencias entre los grupos se realizó mediante un análisis de varianza (ANOVA) de una vía utilizando el software SPSS (Versión 28.5, SAS Institute Inc., Cary, NC, EE. UU.). Luego, se realizó la prueba de comparación múltiple de Tukey si se encontraban diferencias significativas. Todos los resultados se presentaron como la media ± SD de seis repeticiones en cada grupo. Un valor de p < 0.05="" se="" consideró="" significativo="">
Cistanche para mejorar la inmunidad
3. Resultados
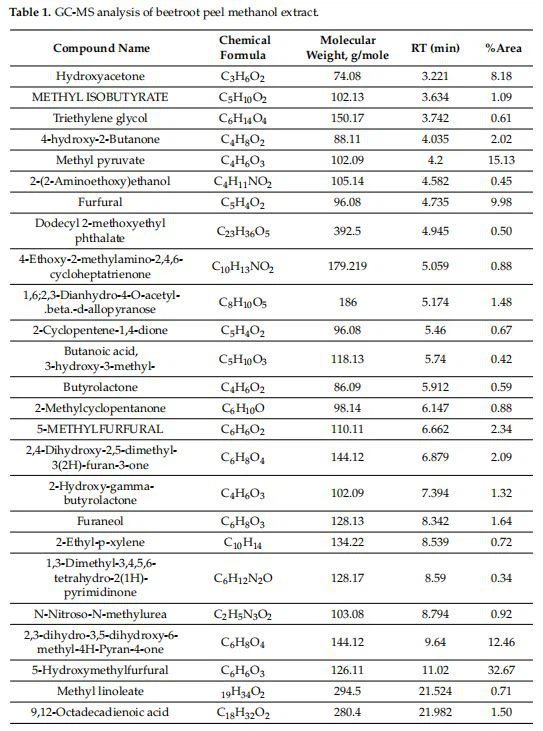
3.1. Moléculas bioactivas en BPME Los componentes químicos de BPME se confirmaron mediante GC-MS (Turbomass, PerkinElmer). La composición química del extracto de cáscara de remolacha se determinó comparando los espectros de masas disponibles con la base de datos espectral del Instituto Nacional de Estándares y Tecnología (NIST). Los resultados de GC-MS confirmaron que el BPME contenía hidroxiacetona (8,18 por ciento), 5-hidroximetilfurfural (32,6 por ciento), piruvato de metilo (15,13 por ciento), beta-d-alopiranosa (1,48 por ciento), furfural (9,98 por ciento), 2-hidroxi-gamma-butirolactona (1,32 %) y 2,3-dihidro-3,5-dihidroxi- 6-metil-4H-pirano -4-uno (12,4 por ciento; Figura 2a, Tabla 1). 3.2. Proliferación celular El potencial de proliferación celular in vitro de BPME contra HUVEC se presenta en la Figura 2b. No se observó una inhibición significativa del crecimiento celular en los grupos experimentales en comparación con el control del vehículo. El presente estudio confirmó que el aumento de la concentración de BPME tratada con HUVEC resultó en una mayor proliferación celular y viabilidad después de 48 h (112 por ciento) en comparación con 24 h (103 por ciento) de tratamiento. Además, las imágenes microscópicas de luz de HUVEC tratadas con BPME después de 48 h confirmaron las células normales con la forma uniforme de la morfología de células adherentes, fue evidente un mayor número de células en proliferación (replicación) sin ningún daño (Figura 2c). 3.3. Análisis de morfología celular y nuclear, formación de microtúbulos y tinción JC-1 en HUVEC La figura 3 muestra la morfología del desarrollo de microtúbulos en imágenes microscópicas de fluorescencia FL. Las HUVEC con estrés oxidativo inducidas por H2O2- mostraron una proliferación deficiente y una morfología irregular de las células adherentes en comparación con las HUVEC de control. Las HUVEC normales tratadas con 0,2 µg/mL de BPME mostraron células en proliferación a través de la replicación o neogénesis con morfología de microtúbulos. Mientras tanto, la dosis de 00,1 µg/mL de células tratadas con BPME mostró un 100 por ciento de células adherentes con etapas tempranas de microtúbulos. Las HUVEC con estrés oxidativo tratadas con 0,2 µg/mL de BPME identificaron la proliferación de nuevas células con morfología de microtúbulos y una disminución del daño celular oxidativo. Además, 0,1 µg/ml de BPME también aumentaron la morfología normal de las células vasculares con células en proliferación.
La Figura 4a muestra la morfología normal de la estructura nuclear, con forma esférica, en las HUVEC de control y tratadas con BPME (0.1 o 0.2 µg/mL). La Figura 4b muestra las imágenes para la tinción con PI de HUVEC normales y con estrés oxidativo inducido por H2O2. Las HUVEC tratadas con H2O{{10}}muestran núcleos con formas irregulares, presentando condensación y picnosis después de 30 min. Sin embargo, 0.2 µg/mL de tratamiento con BPME para HUVEC bajo estrés oxidativo mostró núcleos circulares con morfología normal. En comparación con 0,2 µg/mL de extracto de BPME, 0,1 µg/mL de BPME tuvo un efecto protector menor contra el estrés oxidativo inducido por H2O2- en HUVEC.

Figura 2. Resultados del cromatograma GC-MS del extracto de metanol de cáscara de remolacha (a), proliferación celular in vitro (b) e imágenes de microscopía óptica para la morfología celular (c) en HUVEC, tratadas con una concentración creciente de extracto de metanol de cáscara de remolacha (BPME ) (forma uniforme de células adherentes y proliferantes mencionadas por punta de flecha roja). Todos los valores son medias ± SD (n=6). * p Menor o igual a 0.05 en comparación con el control del vehículo.
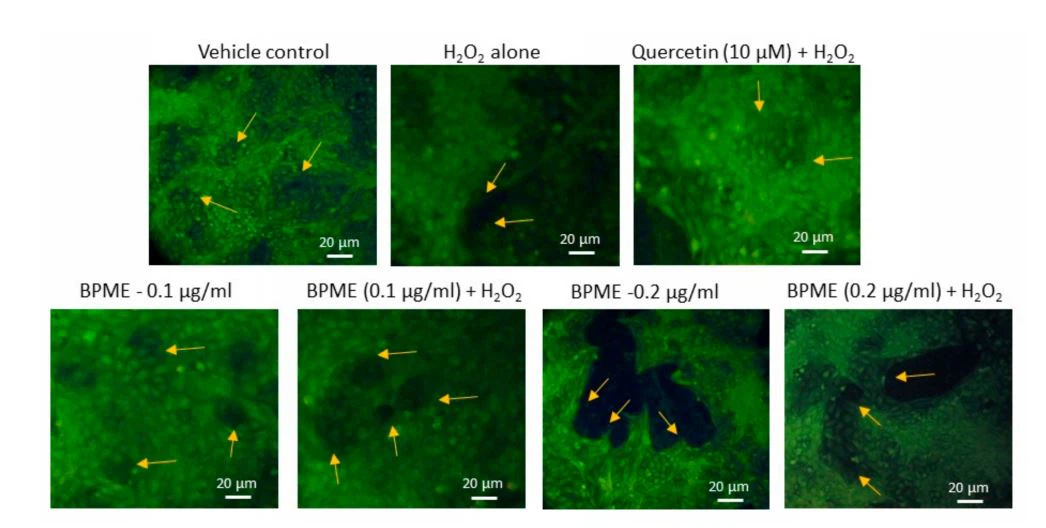
Figura 3. Análisis de formación de microtubos basado en microscopía de fluorescencia en control de vehículo, dosis de 0.1 y 0.2 µg/mL de extracto de metanol de cáscara de remolacha (BPME) tratada normal y H2O{{6} HUVEC inducidas por estrés oxidativo después de 48 h. Después de 48 h, las HUVEC con estrés oxidativo inducidas por H2O2- mostraron una morfología alterada en comparación con el control del vehículo. Volúmenes de 0.1 y 0.2 µg/ml de HUVEC tratadas con extracto de metanol de cáscara de remolacha (BPME) mostraron una morfología normal con microtúbulos vasculares con células en proliferación que se asemejan a la morfología común del comportamiento de las células del músculo liso.

Figura 4. Análisis de tinción con yoduro de propidio (PI) para la morfología nuclear en el control del vehículo, 0.1 y 0.2 µg/mL de extracto de metanol de cáscara de remolacha (BPME) tratado normal (3a) y H2O2-inducidas por estrés oxidativo (3b) HUVEC después de 48 h. En la tinción con PI, el control del vehículo mostró que el núcleo parecía ser normal sin signos de núcleo encogido, picnosis o apoptótico. En H2O2 solo, las células tratadas mostraron una membrana nuclear polarizada después de 48 h. El tratamiento con 0,2 µg/ml de BPME normalizó la polarización de la membrana nuclear inducida por H2O2-en comparación con 0,1 µg/ml de BPME o quercetina 10 µM.
La Figura 5a muestra los resultados de la tinción JC-1 para HUVEC, incluidas las células de control y las tratadas con BPME; la figura ilustra células sanas con mitocondrias activas, como lo confirma la captación de mitocondrias cargadas negativamente del JC catiónico lipofílico extramitocondrial -1 (color verde) y agregados J convertidos con color rojo intramitocondrialmente. La Figura 5b muestra los resultados de tinción de JC-1 para 0.2 µg/mL de BPME administrados a HUVEC con estrés oxidativo inducido por H2O2; los resultados confirmaron que casi el 94 % de las mitocondrias cargadas negativamente convirtieron el JC catiónico lipofílico-1 (color verde) en agregados J de color rojo en comparación con 0.1 µg/ml de tratamiento con BPME (61,4 %) o H2O{{20}}estrés oxidativo inducido en HUVEC (2 por ciento). Se observó que el potencial de membrana mitocondrial (MMP) era mayor en las células tratadas con BPME en comparación con el fármaco de referencia quercetina. 3.4. Análisis de potencial de membrana mitocondrial asistido por FACS (∆ψm; BD MitoScan) y anexina V/apoptosis en HUVEC. y HUVECs con estrés oxidativo inducido por H2O2. Descubrimos que 0,2 µg/mL de tratamiento con BPME aumentó la MMP (∆ψm) al 92,7 % ± 3,7 % en comparación con las HUVEC tratadas solo con H2O2 (27,9 % ± 7,2 %). Por el contrario, las células tratadas con quercetina mostraron un porcentaje de aumento de MMP (∆ψm) del 41,4 % ± 1,6 % en comparación con las HUVEC tratadas con BPME y H2O2 o H2O2 solo.
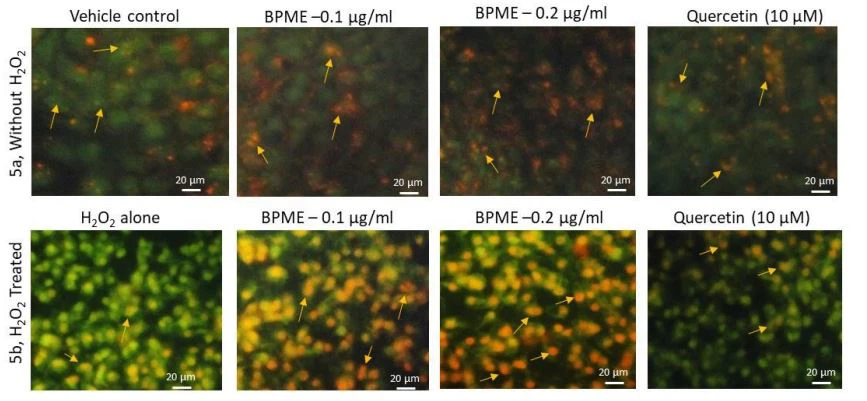
Figura 5. Análisis del potencial de membrana mitocondrial usando tinción JC-1 para el control del vehículo, 0.1 y 0.2 µg/mL de extracto metanólico de cáscara de remolacha (BPME) tratado normal (a ) y H2O2-inducidas por estrés oxidativo (b) HUVEC después de 48 h. JC{{10}}Imágenes de fluorescencia que muestran imágenes fusionadas de las señales roja y verde del tinte, correspondientes a JC-1 en agregados J frente a forma monomérica. Encontramos menos agregados J H2O2 solo tratados con HUVEC. En 0.2 µg/ml de HUVEC tratadas con BPME que muestran agregados j altos que representan directamente (alta MMP, ∆ψm) un alto potencial de membrana mitocondrial en comparación con 0,1 µg/ml de BPME o 10 µM de quercetina.
4. Discusión
Ante el estrés extracelular o intracelular, la biodisponibilidad de las especies reactivas de oxígeno (ROS) supera la defensa antioxidante, y el estrés oxidativo interrumpe la señalización y el control redox [31]. El desarrollo de estrés oxidativo está asociado con la patogenia de trastornos crónicos, como enfermedades neurodegenerativas, diabetes y aterosclerosis. Por ejemplo, el estrés oxidativo inicia la disfunción endotelial y promueve la inflamación sistémica y el reclutamiento de macrófagos [32]. Las células inmunitarias activadas migran hacia la vasculatura y liberan citocinas y quimiocinas asociadas con la vasoconstricción y remodelación de los vasos sanguíneos de las células del músculo liso y la inflamación que afecta a las células del músculo liso vascular y la pared vascular [33]. El aumento del estrés oxidativo vascular termina con daño vascular, rigidez de las células del músculo liso y anomalías estructurales de la elastina. Además, el estrés oxidativo vascular se ha estimulado en otras condiciones patológicas, como la obesidad visceral o la aterosclerosis, debido al aumento de la actividad de la NADPH oxidasa (NOX-2) en el tejido adiposo perivascular [34]. El estrés oxidativo vascular causa los principales cambios epigenéticos que ocurren durante el envejecimiento y termina con un proceso de envejecimiento temprano [35]. El desarrollo de la producción de ROS y el estrés oxidativo en el sistema biológico depende en gran medida de la disfunción mitocondrial, además de NOX-2, xantina oxidasa endotelial, eNOS desacoplada y lipoxigenasa [36]. Las propiedades antioxidantes de los agentes dietéticos pueden neutralizar la generación de ROS a través de una mayor capacidad antioxidante [26]. El extracto de Ginkgo Biloba protege contra el desarrollo de aterosclerosis al reducir la generación de ROS y la actividad de la lipoxigenasa en la disfunción endotelial inducida por OxiLDL [37]. Además, varios compuestos fenólicos yflavonoides delas plantas y los granos comestibles tienen la propiedad de eliminar las ERO y la peroxidación lipídica [38]. El extracto metanólico de la cáscara de remolacha (Beta vulgaris) tiene potencial antioxidante debido a la disponibilidad de alto contenido de fibra, antocianinas y flavonoides como la vitexina y la betanina [39]. En el presente estudio, se seleccionó BPME para identificar el enfoque mecánico dependiente de las mitocondrias para descubrir su efecto sobre el potencial de la membrana mitocondrial, la extinción de LPO y la inhibición de los niveles de expresión de ARNm relacionados con la inflamación vascular. El ensayo MTT confirmó que BPME aumentó significativamente la proliferación celular, como lo confirma el aumento de la integridad nuclear en la tinción de PI con la dosis efectiva de 0,2 µg/mL de BPME versus 0,1 µg/mL probados de BPME. La identificación de la dosis efectiva con baja concentración y máxima actividad puede considerarse fisiológicamente segura. Encontramos tinción microscópica de fluorescencia FL de JC-1, y el potencial de la membrana mitocondrial se restauró tanto en HUVEC normales como en H2O{{10}}inducidas con estrés oxidativo estimuladas externamente después de 0,2 µg/mL de BPME tratamiento. La disfunción mitocondrial altera la fosforilación oxidativa, que no logra transformar los radicales de oxígeno (O2·−) en H2O2 y H2O por la glutatión peroxidasa. Debido a la desintoxicación insuficiente de ROS o la producción descontrolada de ROS, el aumento del estrés oxidativo mitocondrial está relacionado con la aterosclerosis [40]. Los extractos de cáscara de remolacha restauraron efectivamente el potencial de la membrana mitocondrial, lo que aumentó con éxito la desintoxicación de ROS y la generación de H2O2. El análisis de tinción con anexina V/PI confirmó que el tratamiento con BPME mantuvo el porcentaje de células viables y mejoró la etapa de proliferación celular tanto en HUVEC normales como en HUVEC con estrés oxidativo inducido por H2O2. En este contexto, Choo et al. [41] confirmaron que después de la generación excesiva de ROS o H2O2 exógeno en el sitio isquémico, las células madre mesenquimales (MSC) trasplantadas pueden afectar la autoproliferación y la capacidad multilinaje. En la medicina regenerativa, las células del músculo liso vascular son los principales reguladores de las arterias del tono contráctil a través del mantenimiento de la resistencia arterial periférica, los reguladores de la presión arterial, la sangre y la reparación de las arterias [42]. Además, la modulación del fenotipo inducida por la edad de las CE se asocia con una disminución de la contractilidad celular y un aumento de la senescencia celular. Tras el estrés continuo o debido a la mecanosensibilidad reducida, se identifica una menor adaptación de las señales del microambiente en las células musculares lisas envejecidas [43]. Los presentes resultados confirmaron que el tratamiento con BPME mantuvo la población de células viables, como lo demuestra la capacidad de angiogénesis. La capacidad de proliferación identificada de BPME en HUVEC ha sido respaldada por la reducción en la expresión de LPO y el aumento de las expresiones de genes antioxidantes. ROS y LPO se generan inicialmente a partir del complejo mitocondrial (I y III) y NOX-4 durante la proliferación o diferenciación celular [44]. Un exceso de ROS reacciona y daña las biomoléculas, alterando especialmente la integridad del ADN genómico, que es fundamental para la proliferación y las funciones celulares [45]. Sin embargo, se ha confirmado que la ingesta dietética de polifenoles antioxidantes, como la epigalocatequina y el tocoferol, protege a las células del estrés oxidativo y aumenta la capacidad de proliferación [46]. En nuestro estudio, los niveles de expresión de ARNm de LPO disminuyeron, y se encontró que NOS-3, Nrf-2 y eNOS aumentaron dos veces en HUVEC con estrés oxidativo inducido por H2O2. eNOS es la isoforma predominante de NOS, responsable de la mayoría de los productos de NO en las células musculares lisas y los tejidos vasculares. El NO· dilata todo tipo de vasos vasculares y protege la agregación plaquetaria y la adhesión leucocitaria en las CE [47]. Hasta el momento, ha habido muchos informes contradictorios sobre los factores de riesgo cardiovascular, y la disfunción endotelial se ha asociado con una expresión disminuida o aumentada de eNOS [48]. Expresión elevada de eNOS observada en la enfermedad vascular, que probablemente sea una consecuencia de la producción excesiva de H2O2. O2·−, un producto de dismutación, puede aumentar la expresión de eNOS a través de mecanismos transcripcionales y postranscripcionales [49]. La patogenia de la enfermedad vascular se acompaña de una degradación acelerada de NO· después de la reacción con O2·− y, finalmente, de la forma ONOO−, lo que conduce al desacoplamiento de eNOS y a la disfunción de la enzima NOX [50]. El estrés oxidativo ha sido suprimido por enzimas antioxidantes y los niveles de ARNm de GSK-3 y GPX han aumentado después del tratamiento con BPME. BPME contiene múltiples fitoquímicos que son biológicamente activos, incluidas betalaínas, flavonoides, polifenoles, enzimas terapéuticas, ácido ascórbico, ácido dehidroascórbico (DHAA) y nitrato inorgánico (NO3), y estos pueden estar involucrados en la regulación positiva de la capacidad antioxidante en HUVEC. En este contexto, Cha et al. (2014) [51] informó que el ácido clorogénico protege eficazmente contra el daño del ADN inducido por el estrés oxidativo en los queratinocitos humanos. La endotelina-1 (Edn-1), un vasoconstrictor derivado del endotelio, realiza la migración de las células del músculo liso y actúa como un factor antiapoptótico en las células con estrés inducido por el óxido nítrico [52,53]. Los procesos de remodelación vascular, migración, proliferación y acumulación de matriz extracelular han sido estimulados tanto por Edn-1 como por NO [54,55]. Observamos una mayor expresión de Edn-1 después del tratamiento con BPME en HUVEC con estrés oxidativo. Tras el estrés oxidativo o la acumulación de LPO, la etapa temprana de la inflamación vascular es la adhesión de los leucocitos a las células del músculo liso endotelial, es prominente para los eventos críticos de isquemia y aterosclerosis [56]. Está mediado por expresiones VCAM e ICAM; ha sido estimulado por muchas de las quimiocinas y agentes de quimiotaxis, como las expresiones NF-κB, IL-1 y TNF- [57]. La inhibición de la activación de IL-1 seguida de la expresión de moléculas de adhesión se ha logrado mediante el compuesto fenólico dietético ácido elágico [58]. El tratamiento con BPME para HUVEC estimuladas externamente con estrés oxidativo disminuyó significativamente los factores proinflamatorios específicos de células vasculares, como VCAM, ICAM, NF-κB, IL-1 y los niveles de expresión de TNF-. En este contexto, Crespo et al. [59] informaron que el kaempferol y la quercetina inhibían genes proinflamatorios, como las expresiones VCAM, ICAM, NF-κB e IL-1, respectivamente. En general, la inhibición del estrés oxidativo y el potencial de expresión génica relacionado con la inflamación vascular de BPME favoreció la expresión de factores de crecimiento de células vasculares y ayudó potencialmente a la proliferación y el crecimiento de células vasculares.

5. Conclusiones
Los presentes hallazgos confirman que el aumento de la expresión de genes antioxidantes se asoció con la extinción del estrés oxidativo, lo que ayudó a superar el deterioro de la proliferación y la angiogénesis de HUVEC. El ajo negro que contiene hidroximetilfurfural suprime el efecto inflamatorio de la adhesión de células de monocitos inducida por TNF a HUVEC y suprime aún más la generación de ROS, la expresión de VCAM-1 y la activación de NF-κB [60]. Además, Él et al. [61] confirmaron que el hidroximetilfurfural tiene el potencial de proteger las CE de la hipoxia. También se ha identificado que la cáscara de remolacha contiene flavonoides, furano y componentes antioxidantes, como 5-hidroximetilfurfural, metilpiruvato, furfural y 2,3-dihidro-3,5- dihidroxi-6-metil-4H-piran-4-ona; estos componentes son responsables de la capacidad antioxidante mejorada y la supresión de las moléculas de adhesión de células del músculo liso vascular proinflamatorias. La cáscara de remolacha se ha utilizado como estimulante de las reservas de antioxidantes para apagar el estímulo externo o el estímulo patológico interno del estrés celular peroxidativo. Nuestros hallazgos evidenciaron que los componentes de la remolacha ayudan a reducir el estrés metabólico y la inflamación en las HUVEC, lo que puede ser beneficioso para la proliferación de células vasculares y la angiogénesis.
Contribuciones de autor:
Conceptualización, LNA-H. y S.-BP; metodología, LNA-H. y S.-BP; software, SG; validación, LNA-H. y S.-BP; análisis formal, S.-BP, AMA-D., AAA (Ali A Alshatwi) y GS; investigación, LNA-H., S.-BP y AMA-D.; recursos, LNA-H.; curación de datos, S.-BP y LNA-H.; redacción—preparación del borrador original, LNA-H. y S.-BP; redacción—revisión y edición, LNA-H., AMS, GS y AAA (Amna Abdullah Alotiby); visualización, S.-BP y AAA (Ali A Alshatwi); supervisión, LNA-H., y S.-BP; administración de proyectos, LNA-H.; adquisición de financiación, LNA-H. Todos los autores han leído y aceptado la versión publicada del manuscrito. Financiamiento: Los autores extienden su agradecimiento al Decanato de Investigación Científica de la Universidad King Saud por financiar este trabajo a través del grupo de investigación no RG-1442-432. Declaración de la Junta de Revisión Institucional: No corresponde. Declaración de consentimiento informado: No corresponde. Declaración de disponibilidad de datos : Los datos presentados en este estudio están disponibles a pedido del autor correspondiente. Conflictos de interés: No hay conflicto de interés para este estudio.
Referencias
1. Abdolmaleki, Z.; árabe, H.-A.; Amanpur, S.; Muhammadnejad, S. Efectos antiangiogénicos del extracto etanólico de Artemisia sieberi en comparación con su principio activo, la artemisinina. Rev. Brás. Farmacogn. 2016, 26, 326–333. [Referencia cruzada]
2. Yoo, SY; Kwon, SM Angiogénesis y sus oportunidades terapéuticas. mediat. Inflamm. 2013, 2013, 127170. [Referencia cruzada] [PubMed]
3. Folkman, J. Angiogénesis en cáncer, vascular, reumatoide y otras enfermedades. Nat. Medicina. 1995, 1, 27–31. [Referencia cruzada]
4. Hoeben, A.; Landuyt, B.; Highley, MS; Wildiers, H.; Van Oosterom, AT; De Bruijn, EA Factor de crecimiento endotelial vascular y angiogénesis. Farmacol. Rev. 2004, 56, 549–580. [Referencia cruzada]
5. Ferrara, N.; Alitalo, K. Aplicaciones clínicas de los factores de crecimiento angiogénicos y sus inhibidores. Nat. Medicina. 1999, 5, 1359–1364. [Referencia cruzada]
6. Cocina, HF; Webster, NR Fisiología del endotelio. Hermano J. Anaesth. 2004, 93, 105–113. [Referencia cruzada]
7. Onat, D.; Brillón, D.; Colombo, PC; Schmidt, AM Células endoteliales vasculares humanas: un sistema modelo para estudiar la inflamación vascular en la diabetes y la aterosclerosis. actual Diabetes Rep. 2011, 11, 193–202. [Referencia cruzada] [PubMed]
8. Packard, RR; Libby, P. Inflamación en la aterosclerosis: de la biología vascular al descubrimiento de biomarcadores y la predicción de riesgos. clin. química 2008, 54, 24–38. [Referencia cruzada]
9. Esper, RJ; Nordby, RA; Vilariño, JO; Paragano, A.; Cacharrón, JL; Machado, RA Disfunción endotelial: Una evaluación integral. Cardiovasc. Diabetol. 2006, 5, 4. [Referencia cruzada]
10. Baudín, B.; Bruneel, A.; Bosselut, N.; Vaubourdolle, M. Un protocolo para el aislamiento y cultivo de células endoteliales de vena umbilical humana. Nat. Protocolo 2007, 2, 481–485. [Referencia cruzada] [PubMed]
11. Cao, Y.; Cao, R. Angiogénesis inhibida por beber té. Nature 1999, 398, 381. [CrossRef] [PubMed]
12. Yen, G.-C.; Duh, P.-D.; Tsai, H.-L. Propiedades antioxidantes y prooxidantes del ácido ascórbico y del ácido gálico. Química alimentaria 2002, 79, 307–313. [Referencia cruzada]
13. Dhalaria, R.; Verma, R.; Kumar, D.; Puri, S.; Tapwal, A.; Kumar, V.; Nepovimova, E.; Kuca, K. Compuestos bioactivos de frutas comestibles con sus propiedades antienvejecimiento: una revisión integral para prolongar la vida humana. Antioxidantes 2020, 9, 1123. [CrossRef] [PubMed]
14. Baião, DdS; da Silva, D.; Del Águila, EM; Paschoalin, VMF Características nutricionales, bioactivas y fisicoquímicas de diferentes formulaciones de remolacha. Adicto a la comida. 2017, 6. [Referencia cruzada]
15. Lalonde, R.; Roitberg, B. Sobre la evolución del comportamiento de apareamiento en los árboles: ¿Depredación o clima? Soy. Nat. 1992, 139, 6. [Referencia cruzada]
16. Silva, D.; Baião, DDS; Ferreira, VF; Paschoalin, VMF Betanin como modulador de la inflamación y el estrés oxidativo de múltiples vías: un pigmento de remolacha con efectos protectores sobre la patogénesis de la enfermedad cardiovascular. crítico Rev. ciencia de los alimentos. Nutrición 2020, 1–16. [Referencia cruzada]
17. Baião, DDS; Silva, D.; Paschoalin, VMF Vegetal notable: Su contenido de nitratos y fitoquímicos se puede ajustar en formulaciones novedosas para beneficiar la salud y apoyar las terapias de enfermedades cardiovasculares. Antioxidantes 2020, 9, 960. [CrossRef] 18. Abd El-Ghaffar, EA; Hegazi, Nuevo México; Sad, HH; Solimán, MM; El-Raey, MA; Shehata, SM; Barakat, A.; Yasir, A.; Sobeh, M. Análisis HPLC-ESI-MS/MS de hojas de remolacha (Beta vulgaris) y sus propiedades beneficiosas en ratas diabéticas tipo 1. biomedicina Farmacéutico. 2019, 120, 109541. [Referencia cruzada]
19. Singh, B.; Nathan, BS Composición química, propiedades funcionales y procesamiento de remolacha: una revisión. En t. J. Ciencia. Ing. Res. 2014, 5, 679.
20. Ninfali, P.; Angelino, D. Potencial nutricional y funcional de Beta vulgaris cicla y rubra. Fitoterapia 2013, 89, 188–199. [Referencia cruzada]
