Metabolitos secundarios de cianobacterias como ingredientes biotecnológicos en cosméticos naturales antienvejecimiento 2
Aug 24, 2022
Por favor contactaroscar.xiao@wecistanche.compara más información
2.3.Actividades biológicas
2.3.1.Actividad de captación de radicales
El radical anión superóxido es un radical libre fisiológico de extrema importancia para el organismo humano. Cuando existe una sobreproducción de estos ROS durante la respiración aeróbica, o cuando los mecanismos endógenos de desintoxicación fallan o son insuficientes, existe un mayor riesgo de daño oxidativo con efectos deletéreos graves. En este sentido, encontrar mecanismos para inhibir los efectos nocivos de Oz* es de vital importancia, no solo en el campo de la cosmética, sino también al considerar la mejora y prevención de una amplia gama de enfermedades. El comportamiento de eliminación de O2" de los extractos de cianobacterias se muestra en la Figura 1 y los valores de IC se resumen en la Tabla 6.
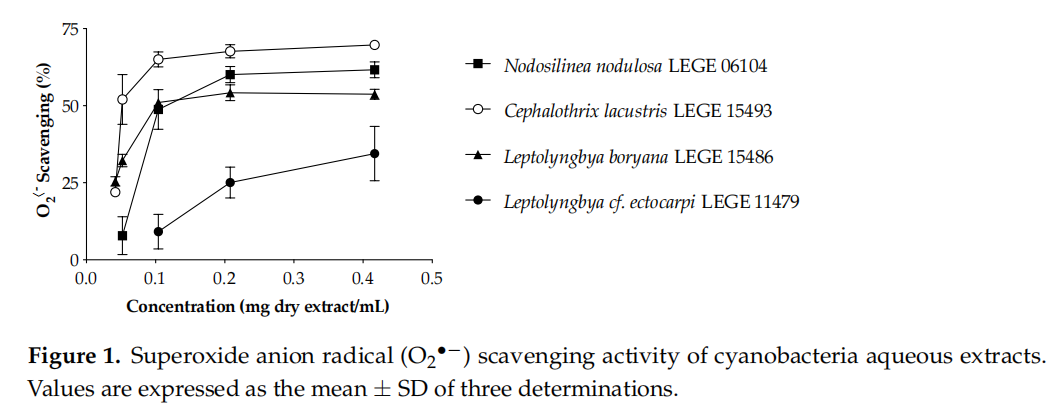

Los extractos acuosos fueron significativamente más efectivos en el barrido de Oz* que los extractos de acetona (Tabla 6) y presentaron una actividad dependiente de la dosis (Figura 1), destacándose las cepas de agua dulce de las marinas. Cephalothorax lacustris LEGE 15493 fue la cepa más efectiva, presentando el valor ICso más bajo (65.5 ug extracto seco/mL, p<0.05), followed="" by="" leptolyngbya="" boryana="" lege="" 15486="" and="" nodosilinea="" nodulosa="" lege="" 06104.="" leptolyngbya="" cf.="" ectocarpi="" lege="" 11479="" was="" the="" only="" strain="" that="" did="" not="" reach="" the="" ic5o="" for="" the="" aqueous="" extract="" (table="" 6).="" on="" the="" other="" hand,="" the="" acetone="" extract="" of="" this="" strain="" was="" the="" most="" effective="" in="" o2*-="">

Por favor haga clic aquí para saber más
Una comparación de las capacidades antioxidantes entre diferentes cianobacterias es un desafío debido a los diferentes métodos aplicados. Morone y colaboradores evaluaron la capacidad de captación de radicales de los extractos de etanol (70 por ciento v/v) de diferentes cepas de cianobacterias [26], siendo el valor ICso más bajo de 822,70 ug/mL para Phormidium sp.LEGE 02 05292, mientras que no Se detectó actividad para Nodosilinea nodulosa LEGE 06102. Lopes y colaboradores informaron actividad de eliminación de O2 para extractos de acetona de Nodosilinea (Leptolynbbya) Antarctica LEGE13457 y Cuspidothrix issatschenkoi LEGE 03282, con valores IC25 de 319 y 286 ug/mL, y ninguna actividad para Leptolynbbya- como sp. LEGE 13412 [27]. Los autores también informaron una mayor eficacia en los extractos de acetona en comparación con los extractos de etanol. Otro estudio realizado por Amaro y colaboradores reveló valores de IC50 de 1394 y 826 ug/mL para Gloeothece sp. y Scenedesmus obliquus (M2-1), respectivamente [37]. Los resultados obtenidos aquí para los extractos de acetona parecen menos prometedores que los informados anteriormente, aunque están dentro del mismo orden de magnitud. Por otro lado, los extractos acuosos revelaron un enorme potencial digno de mayor explotación en cuanto a aplicaciones cosméticas en el campo del envejecimiento de la piel.
2.3.2.Inhibición de enzimas
Las MMP son una familia de enzimas extracelulares dependientes de zinc, cuya función principal es remodelar y degradar la ECM [38], un material similar a un gel esencial para mantener unidas las células y proporcionar una vía para los nutrientes y el oxígeno [39]. Las alteraciones en los componentes de la ECM, como el colágeno y la elastina, inducidas por las MMP son la base del daño de la piel y la formación de arrugas [40]. Junto a estas enzimas, vinculadas a la estructura de la piel y la formación de arrugas, otra asume un papel crucial en el proceso de envejecimiento por su actividad en la melanogénesis: la tirosinasa. Entre otros factores, la exposición a la radiación UV provoca la acumulación de una cantidad anormal de melanina, debido al aumento de la producción de ROS. Estas especies reactivas afectan la actividad de los melanocitos, lo que aumenta la conversión de tirosina en melanina por oxidación, lo que provoca hiperpigmentación y manchas irregulares en la piel [41].

Cistanche puede antienvejecimiento
En la búsqueda de alternativas naturales a los ingredientes antienvejecimiento comerciales, centrándose en las enzimas mencionadas anteriormente, se exploró la actividad de los extractos de cianobacterias (Figura 2). En cuanto a la HAasa, solo tres cepas fueron capaces de inhibir esta enzima, actuando de forma dosis-dependiente: el extracto acuoso de Leptolyngbya cf. ectocarpiLEGE 11479 (IC50=863 ug/mL), y los extractos acetónicos de Cephalothrix lacustris LEGE 15493 y Nodosilinea nodulosa LEGE 06104, estos dos últimos solo alcanzando IC25 (832 y 995 ug/mL, respectivamente). Aunque estos valores parecen altos, su rango de actividad fue similar al del fármaco de referencia cromoglicato disódico (DSCG) (IC50=105 ug/mL). Además, vale la pena mencionar que, para la concentración más alta probada (1 mg/mL), Leptolyngbya cf. ectocarpi LEGE 11479 inhibió esta enzima en un 80 por ciento (Figura 2), lo que hace que este extracto sea prometedor como ingrediente cosmético.
Pocos estudios han informado sobre el efecto potencial de los compuestos y extractos de cianobacterias sobre la actividad de la hialuronidasa, y cualquier comparación sobre el potencial biológico de los extractos debe tener en cuenta que el metabolismo de las cianobacterias sufre una variación significativa según las condiciones de cultivo, lo que influye en la composición química de los extractos. Morone y colaboradores [26] evaluaron el efecto de los extractos etanólicos de Tychonema sp. LEGE 07196 y Cyanobium sp. LEGE 07175 sobre hialuronidasa y encontró una actividad inhibidora más fuerte, con valores de ICso de 182,74 y 208,36 ug/mL, respectivamente. La actividad de extractos etanólicos también ha sido reportada para una fracción insoluble de Spirulina platensis, con una IC5o de 150 ug/mL[42]. Otro estudio, realizado por Yamaguchi y Koketsu [19], mostró que Nostochopsis lobatus MAC0804NAN producía una gran cantidad de polisacáridos con un alto efecto inhibitorio (IC50=7.18 ug/mL). También se informó que un Arthrospira- el péptido derivado puede estar involucrado en la inhibición de la hialuronidasa [4]. Juntos, estos resultados respaldan el potencial de los compuestos y extractos de cianobacterias como ingredientes antienvejecimiento para aplicaciones cosmecéuticas.

Considerando la elastasa, solo los extractos de acetona presentaron bioactividad interesante. Leptolyng-bya cf. ectocarpi LEGE 11479 fue nuevamente la más activa (Figura 2), siendo la única cepa en alcanzar la ICso, con un valor de 391 ug/mL. Nodosilinea nodulosa LEGE 06104, Cephalothrix lacustris LEGE 15493 y Leptolyngbya boryana LEGE 15486 solo alcanzaron IC25, con valores de 126,86 y 99 ug/mL, respectivamente. En cuanto a la hialuronidasa, las cepas marinas han demostrado ser las más prometedoras.
Hasta donde sabemos, no hay informes previos sobre la actividad inhibidora de la elastasa para las cepas exploradas en este documento. Con respecto a otras cepas, se descubrió que Nostoc minutum producía péptidos tipo microviridinas y notopeptinas, con CI50 =1.3 y 11.0 ug/mL [44,45]. Las microviridinas B y contenidas de Microcystis aeruginosa también inhibieron la elastasa de manera eficaz, con valores de ICso de 0.044 y 0,084 ug/mL [46]. La mayoría de los datos disponibles sobre la inhibición de la elastasa se centran en compuestos aislados, por lo que las comparaciones con los extractos de nuestras cepas son difíciles de hacer.

La pigmentación desigual de la piel, asociada tanto con el envejecimiento como con la exposición a los rayos UV, sigue siendo una de las principales preocupaciones de las poblaciones que envejecen y de las industrias cosméticas. La mayoría de los estudios disponibles son insignificantes y utilizan la tirosinasa de hongo como modelo enzimático, lo que dificulta la traducción de los resultados al entorno humano, sin embargo, esta enzima tiene una gran similitud y homología con la tirosinasa humana[47]. Por lo tanto, el mismo modelo enzimático se usó aquí para explorar el potencial de los extractos de cianobacterias en la inhibición de la tirosinasa. En cuanto a la elastasa, solo los extractos de acetona fueron capaces de inhibir la tirosinasa. Nodosilinea nodulosa LEGE 06104 fue la más eficaz (Figura 2), siendo la única cepa que alcanzó la IC#N (989,26±4,3 ug/mL). Por debajo se encontraba Leptolyngbya boryana LEGE 15486, con IC25=784 78±4,33 ug/ mL, y por último Leptolyngbya cf.ectocarpi LEGE 11479, encontrándose los resultados más prometedores para las cepas marinas.
Morone y colaboradores [26] exploraron previamente la actividad de los extractos etanólicos de cianobacterias en el mismo modelo, pero no encontraron actividad. Un aspecto interesante de esto es que una de las cepas estudiadas fue Nodosilinea nodulosa LEGE 06102, que mostró los mejores resultados aquí, enfatizando una vez más la importancia de los solventes de extracción en la obtención de extractos bioactivos específicos. En cuanto a las otras enzimas exploradas, las encuestas centradas en las cianobacterias también son escasas para la tirosinasa. Ir trabajo realizado por Yabuta y su equipo [48], se informó que el extracto de agua caliente de Nostochopsis spp. inhibió significativamente la actividad tirosinasa (IC50=250 ug/mL). Este es un resultado muy interesante, considerando que proviene de un extracto acuoso, para el cual no se encontró actividad en el presente estudio. Los autores atribuyen el resultado a los compuestos de bajo peso molecular liberados de las PBP mediante el tratamiento térmico, a saber, una fracción bilina que actúa como un potente eliminador de radicales peroxilo. Otro estudio evaluó la actividad inhibitoria de los extractos de etanol (IC50=14,000 ug/mL) y agua (IC50 =72,000 ug/mL) de Arthrospira platensis, donde el los valores se atribuyeron a la presencia de compuestos fenólicos como los ácidos ferúlico y cafeico en el extracto de etanol [49].
2.3.3.Protección UV
A pesar de que un número creciente de empresas de cosméticos incorporan bloqueadores solares en sus productos, todavía es difícil convencer a los consumidores sobre los beneficios de su uso diario para frenar el envejecimiento prematuro de la piel. Si por un lado, la aplicación diaria de protectores solares es un hábito poco arraigado, por otro lado, existe cierto temor al uso de sustancias sintéticas, debido a los riesgos asociados no deseados[50]. A raíz de esto, la investigación sobre fotoprotección natural ha aumentado considerablemente en los últimos años, considerando su potencial de biodegradabilidad y menor toxicidad, haciéndolos más beneficiosos para el ser humano y el medio ambiente. Con el fin de explorar extractos de cianobacterias en este campo, se evaluó in vitro su capacidad de actuar como filtros solares para UVR-B, ya que es la radiación más dañina. Los resultados encontrados para los extractos acuosos y acetónicos de cianobacterias se presentan en la Tabla 7.

En cuanto a los extractos de acetona, el valor más prometedor (19,2) se encontró para Leptolyngbya boryana LEGE 15486, seguido de Leptolyngbya cf.ectocarpi LEGE 1479 (10,7), ambos a la concentración más baja probada, 200 ug/mL. Nodosilinea nodulosa LEGE 06104 fue el menos prometedor entre los extractos de acetona. En extractos acuosos, los resultados más prometedores se obtuvieron para la mayor concentración probada, destacándose Leptolyngbya boryana LEGE 15486 y Cephalothrix lacustris LEGE 15493 con valores SPF in vitro de 17,1 y 14,9, respectivamente (Cuadro 7).prolongación de la vida de la cistancheHablando de estudios previos en este campo, Hossain y su equipo [51] informaron que el valor SPF para el extracto de Cephalothrix komarekiana era 2.37. Otro grupo encontró que el SPF de un extracto de metanol de Aphanizomenon flos-aquae era 4 [52]. Sin embargo, la información sobre la concentración del extracto utilizada por los autores no estuvo disponible, lo que dificultó las posibles comparaciones.

El número de cepas de cianobacterias exploradas en el campo de la cosmética, especialmente en lo que respecta a SPF, es muy escaso, considerando las potencialidades de estos recursos. Los resultados aquí presentados demuestran que las especies en estudio pueden ser buenas opciones como fotoprotectores biológicos, y posiblemente actuar como potenciadores de otros fotoprotectores actualmente comercializados, permitiendo reducir la concentración de fotoprotectores sintéticos en las fórmulas. Por lo tanto, es crucial aumentar la investigación sobre estos organismos, especialmente sus extractos bioactivos, que, al ser de costo significativamente menor, mayor rendimiento y una obtención más rápida que los compuestos aislados, son más amigables con el medio ambiente y económicamente más atractivos.
2.4. Discriminación de extractos de cianobacterias mediante análisis PCA
La búsqueda de compuestos bioactivos de fuentes naturales, con potencial para su uso como ingredientes en el campo de la cosmética ha crecido en los últimos años. Además de ser potencialmente menos tóxicos y completamente biodegradables, los compuestos derivados de las cianobacterias están disponibles a partir de fuentes renovables y se pueden obtener a bajo costo en un ambiente controlado.cistanche nueva zelandaLa clasificación de extractos bioactivos según su composición química y actividades biológicas puede ser valiosa para señalar posibles relaciones. Al respecto, se aplicó el análisis de componentes principales (PCA), considerando la composición química de los extractos de cianobacterias y la bioactividad de la mayor concentración probada en cada ensayo (Figura 3). Como se puede observar, el 72,99 por ciento de la variabilidad podría explicarse por las dos primeras dimensiones: PCl representó el 50,41 por ciento de la varianza, mientras que PC2 fue responsable del 22,58 por ciento. Se distinguieron tres grupos (Figura 3A ): Gl, que implica el extracto acuoso de Leptolyngbya cf. exocarp LEGE 11479; G2, que involucra los extractos acuosos de Cephalothrix lacustris LEGE 15493, Leptolyngbya boryama LEGE 15486 y Nodosilinea nodulosa LEGE 06104; y G3, que involucra a todos los extractos de acetona. De acuerdo con la Figura 3B, Gl es químicamente distinta de las otras muestras debido al contenido de PE; Los extractos acuosos de Cephalothrix lacustris LEGE 15493, Leptolyngbya boryana LEGE 15486 y Nodosilinea nodulosa LEGE 06104 se agrupan según su contenido en PC, APC y proteínas totales (G2), mientras que todos los extractos de acetona se encuentran en el mismo grupo (G3) debido a su contenido en carotenoides, y clorofila a y sus derivados. Se muestran los compuestos más allá de las actividades enzimáticas, con los planos formados con el eje positivo de PCl (Figura 3B). Se puede observar que las muestras con mayor contenido en clorofila ay carotenoides están estrechamente relacionadas con la inhibición de elastasa ay tirosinasa. Esto se demuestra por la fuerte correlación positiva entre los carotenoides y la elastasa (0,725, p<0.01) and="" tyrosinase=""><0.01) inhibition,="" with="" similar="" observations="" between="" chlorophyll="" a="" and="" the="" same="" enzymes=""><0.01 and=""><0.05,respectively). on="" the="" other="" hand,="" hyaluronidase="" inhibition="" is="" more="" correlated="" vvith="" pe="" content="" (figure="" 3b),="" with="" a="" significant="" positive="" correlation="" between="" the="" values=""><0.01).the compounds="" responsible="" for="" the="" radical="" scavenging="" activity="" of="" the="" extracts="" are="" displayed,="" with="" the="" planes="" formed="" with="" the="" pcl="" negative="" axis.="" the="" closest="" correlation="" is="" observed="" for="" tpc=""><0.05); other="" compounds="" such="" as="" total="" proteins,="" pc,and="" apc="" also="" contribute="" to="" the="" activity,="" although="" to="" a="" lower="" extent="" (figure="" 3b).regarding="" the="" spf,="" there="" is="" a="" close="" correlation="" between="" the="" activity="" of="" the="" extracts="" and="" their="" pbp="" content,mainly="" apc=""><0.01)and pc="" (0.838,="" p="" <="" 0.01),="" which="" points="" to="" these="" compounds="" as="" predominantly="" responsible="" for="" blocking="" uv-b="" radiation.="" the="" total="" protein="" content="" also="" contributed="" to="" this="" biological="" activity="" (0.670,=""><0.01), with="" the="" lowest="" contribution="" being="" observed="" for="" pe="" (0.210,p="">0.05). En general, el análisis PCA permitió agrupar los extractos de acuerdo con las actividades biológicas desplegadas en el campo del envejecimiento de la piel, lo que llevó a la conclusión de que los extractos de acetona son más efectivos para inhibir las enzimas responsables de la degradación. de la matriz dérmica y la pérdida de estructura de la piel, mientras que los extractos acuosos son más efectivos para eliminar los radicales libres y proteger la piel de los efectos nocivos de la radiación UV.
Hasta donde sabemos, esta es la primera vez que se establece una relación entre la composición química y las actividades biológicas de los extractos de estas cepas de cianobacterias.
3.Materiales y Métodos
3.1. Producción de Biomasa de Cianobacterias
Cuatro cepas de cianobacterias filamentosas, Cephalothrix lacustris LEGE 15493 y Lep-tolyngbya boryana LEGE 15486, de ecosistemas de agua dulce de Brasil, y Leptolyngbya cf. En este estudio se utilizaron ectocarpi LEGE 11479 y Nodosilinea nodulosa LEGE 06104, de ecosistemas marinos portugueses. Las cepas se mantuvieron en la Colección de Cultivos de Biotecnología Azul y Ecotoxicología (CC LEGE) del Centro Interdisciplinario de Investigaciones Marinas y Ambientales (CIIMAR). Para la producción de biomasa, se estableció un esquema de cultivo a escala, comenzando con 40 mL en laboratorio. condiciones controladas, escaladas secuencialmente hasta 4 L. Las cepas se cultivaron en medio Z8 [53], complementado con 10 ug/L de vitamina B12 y 25 g/LNaCl para cepas marinas. Los cultivos se mantuvieron a 25 grados, con una intensidad de luz de 10 umol fotones m-2 s-4, y con un fotoperíodo de 14 h luz:10 h oscuridad. La biomasa fresca se recolectó después de 120 o 150 días de crecimiento (dependiendo de la cepa) mediante filtración, y se congeló, liofilizó y almacenó a -20 grados hasta la preparación del extracto.
3.2.Preparación de extractos
Se prepararon secuencialmente dos extractos diferentes de cada cepa: acetona y acuoso. Primero se preparó el extracto de acetona, utilizando 2g de biomasa seca. La biomasa se suspendió en acetona y se extrajo durante 10 min en un baño ultrasónico (Fisherbrand[FB15053, Loughborough, UK). Luego de la extracción con acetona, el sedimento resultante se dejó secar en la campana extractora y luego se extrajo con 70 mL de agua destilada, siguiendo el mismo procedimiento. Los restos celulares se eliminaron mediante centrifugación a 10,00×× g Gs durante 5 min a 4 grados, en una microcentrífuga HERAEUS MegafugeTM 16R (Thermo ScientificTM, Waltham, MA, EE. UU.). Los sobrenadantes de cada extracción se evaporaron a temperatura reducida. presión (Evaporador rotatorio BUCHIR-210) (extracto de acetona), o congelado y liofilizado (extracto acuoso). La extracción con el correspondiente sobrenadante se repitió 3 veces. Los extractos secos se mantuvieron a -20 grados hasta su posterior análisis químico y biológico.
3.3. Ensayos celulares
3.3.1.Cultivo celular
Se usaron queratinocitos humanos HaCAT (ATCC), fibroblastos de ratón 3L1 (ATCC) y células endoteliales humanas hCMEC (proporcionado por el Dr. POCouraud (INSERM)) para la evaluación de la citotoxicidad. Las líneas celulares se cultivaron en medio Eagle modificado de Dulbecco (DMEM GlutaMAXTM, Gibco, Glasgow, Reino Unido), complementado con 10 por ciento (v) de suero bovino fetal (Gibco), 1 por ciento de penicilina-estreptomicina (Pen-Strep 100 UI /ml y 10 mg/ml, respectivamente (Gibco) y anfotericina B al 0,1 por ciento (Gibco). El mantenimiento celular y los ensayos se realizaron a 37 grados en una atmósfera humidificada con CO2 al 5 por ciento, y el medio de cultivo se renovó cada dos días. Al 80-90 por ciento de confluencia celular, las células adherentes se lavaron con solución salina tamponada con fosfato (PBS, Gibco), se separaron con la enzima TrypLEX express (1x) (Gibco), se sometieron a mantenimiento y se sembraron para los ensayos planificados.
3.3.2.Citotoxicidad—Ensayo MTT
La viabilidad celular se evaluó mediante la reducción del {{0}}(4,5-dimetiltiazol-2-il)-2,5-bromuro de difeniltetrazolio (MTI, Sigma-Aldrich, Alemania), como se informó anteriormente [26]. Todas las líneas celulares (células endoteliales, fibroblastos y queratinocitos) se sembraron en 96-placas de pocillos, a una densidad de 1,0 × 10 células/mL, 3,3 × 104 células/mL y 2,5 × 104 células/mL, respectivamente.tamaño del pene cistancheDespués de 24 h de adhesión celular, se retiró el medio de cultivo y las células se expusieron durante 24 y 48 h a medio fresco que contenía los diferentes extractos de cianobacterias en cinco concentraciones seriadas, de 12,5 a 200 ug/mL. Para los extractos de acetona, se prepararon soluciones madre en dimetilsulfóxido (DMSO) (Gibco) y se diluyeron con DMEM antes de la exposición de las células para que la concentración máxima de DMSO no excediera el 1 por ciento. Se prepararon extractos acuosos en PBS y se diluyeron con DMEM antes de la exposición de las células. El control negativo fue PBS y el control para la muerte celular fue DMSO al 20 por ciento. Después de la incubación, se realizó el ensayo de citotoxicidad MIT. Brevemente, se agregaron 20 μL de solución de MTT a cada pocillo y se incubaron a 37 grados durante 3 h. Después de la incubación, se retiró cuidadosamente el medio y las sales de formazán de color púrpura se disolvieron en DMSO. La absorbancia se leyó a 550 nm con un lector de microplacas de detección múltiple Synergy HT (Biorek, Bad Friedrichshall, Alemania) operado por el software GEN51M. El ensayo se realizó por cuadruplicado y se promedió. Para la reproducibilidad, cada ensayo se repitió de forma independiente al menos tres veces. La citotoxicidad se expresó como el porcentaje de viabilidad celular, considerando 100 por ciento de viabilidad en el solvente control.
3.4. Perfil químico de extractos de cianobacterias
3.4.1.Contenido fenólico total (TPC)
Para determinar la TPC de los extractos se utilizó un ensayo colorimétrico, basado en la metodología de Folin-Ciocalteu [54] con ligeras modificaciones. Los extractos de acetona se solubilizaron en DMSO y los extractos acuosos en agua. Brevemente, se mezclaron completamente 25 μL de cada extracto (10mg/mL) con 25 μL de reactivo de Folin-Ciocalteu (Sigma-Aldrich)20{{20}} μL de solución de NagCO3 y 500 μL de agua desionizada. Para el blanco se reemplazó el reactivo de Folin-Ciocalteu por agua desionizada. La absorbancia del producto coloreado formado se midió a 725 nm, utilizando un lector de microplacas Synergy HT Multi-detection (Biotek, Bad Friedrichshall, Alemania) operado a través del software GEN51M. Las curvas estándar para la cuantificación de TPC se obtuvieron usando siete concentraciones de ácido gálico (GA) (0.025 a 0.5 mg/mL), preparadas en el mismo solvente que los extractos a ensayar (y=2.097x+0.01560 R²{{ 22}}.9989, para acetona, y y=2.204x+0.01401,R2=0.9982, para agua, donde "y" se refiere a la absorbancia y "x" se refiere a la concentración) . Se realizaron tres determinaciones independientes por duplicado. El contenido fenólico total se expresó como ug equivalentes de GA (GAE) por mg de extracto seco.
3.4.2.Proteínas totales
La concentración de proteína total se determinó utilizando el kit de ensayo de proteína BCA (n.º 23227, Thermo-Scientific). Los extractos acuosos se prepararon en agua, mientras que los extractos de acetona se prepararon en DMSO. Brevemente, en una 96-placa de pocillos, Se mezclaron 25 uL de cada extracto (1 mg/mL) con 200 μL del reactivo de trabajo. La absorbancia se midió a 562 nm, usando un lector de microplacas de detección múltiple Synergy HT (Biotek, Bad Friedrichshall, Alemania) operado a través del software GEN5IM. Una curva estándar (y=-126.87x3+547.73.353 -10.017; R2=0.999, y y=162.87x3-248.51x²+932.13x -11.715;R2=0.99, donde "y" se refiere a la absorbancia y "x" se refiere a la concentración) se obtuvo para cada extracto, utilizando nueve concentraciones de albúmina (BSA) (25 a 2000 ug/mL) para cuantificar las proteínas. Se llevaron a cabo tres experimentos independientes por triplicado. El contenido de proteína total se expresó como ug de equivalentes de albúmina de suero bovino (BSA) por mg de extracto seco.
3.4.3.Pigmentos
Los pigmentos presentes en los extractos acuoso y acetónico se cuantificaron espectrofotométricamente. La clorofila a y sus derivados se cuantificaron mediante una curva de calibración obtenida con el estándar comercial (Sigma-Aldrich): y=8.0791x-0.0{{19} }22 (R2=0.996), donde "y" se refiere a la absorbancia y "x" se refiere a la concentración. Los carotenoides totales se cuantificaron como -caroteno (Sigma-Aldrich), a través de su curva de calibración (y=17.133x+0.0099; R²=0.990, donde "y" se refiere a la absorbancia y "x" se refiere a la concentración). La concentración total de carotenoides se expresó como ug de -caroteno por mg de extracto seco. Las curvas de calibración para ambos estándares se obtuvieron usando cinco concentraciones diferentes (0.001 a 0.025 mg/mL). Las determinaciones espectrofotométricas se realizaron en 96-placas de pocillos, a 450 nm para -caroteno y 663 nm para clorofila a, usando un lector de microplacas de detección múltiple Synergy HT (Biotek, Bad Friedrichshall, Alemania) operado a través del software GEN5TM.
El contenido de PBP se determinó espectrofotométricamente midiendo las absorbancias de los extractos acuosos a diferentes longitudes de onda (562, 615 y 645 nm) y aplicando las fórmulas correspondientes, tal como lo describieron previamente Pagels et al. [34]: Los extractos acuosos se resuspendieron hasta una concentración final de 0,5 mg/mL. El experimento se realizó por triplicado y los resultados se expresaron en ug/mg de extracto seco. 3.5.Actividades biológicas
3.5.1. Eliminación de radicales aniónicos superóxido (O2*-)
El ensayo de captación de radicales libres de Oz*- se realizó para evaluar el potencial antioxidante de los extractos de cianobacterias, según Barbosa y colaboradores [55], con modificaciones menores. Los extractos acuosos se prepararon en agua, mientras que los extractos de acetona se prepararon en DMSO. Se prepararon cinco diluciones seriadas para cada extracto y se probaron para evaluar el comportamiento de los extractos y los valores de IC. Todos los reactivos se disolvieron en tampón de fosfato (19 uM, pH 7,4). Se mezcló un volumen de 50 μl de cada dilución con 50 ul de solución de forma reducida de dinucleótido de nicotinamida y adenina (NADH) 166 uM y 150 ul de cloruro de azul de nitrotetrazolio (NBT) 43 uM en una placa de pocillos 96-. Después de la adición de 50 μL de metosulfato de fenazina 2,7 μM (PMS), se controló la actividad de eliminación de radicales de las muestras con un lector de microplacas Synergy HT Multi-detection (Biotek, Bad Friedrichshall, Alemania) operado a través del software GEN51M, en función cinética, a temperatura ambiente durante 2 min a 562 nm. Se realizaron tres ensayos independientes por triplicado. Se utilizó GA como control positivo. Los resultados se expresaron como el porcentaje de captación de radicales en comparación con el control no tratado. Los resultados de los valores de IC calculados se expresaron como la media ± SD (ug/mL) de al menos tres ensayos independientes realizados por duplicado. Los valores de IC y las correspondientes curvas de dosis-respuesta se calcularon con el software Graphpad Prism@ (San Diego, CA, EE. UU.; versión 9, para MacOS).
3.5.2. Inhibición de hialuronidasa
El ensayo de inhibición de la hialuronidasa se modificó ligeramente del propuesto por Ferreres et al. 【56】. Brevemente, 25 μL de cada extracto (9 mg/mL), 175 μL de ácido hialurónico (HA) (0.7 mg/mL), y 25 μL de hialuronidasa (HAasa) (90{{ Se mezclaron 14}} U/ml en NaCl al 0,9 por ciento en un tubo de reacción. Los extractos acuosos se prepararon en agua y los extractos de acetona se prepararon en DMSO. Después de 30 min de incubación a 37 grados, la reacción se detuvo mediante la adición de 25 μL de tetraborato de disodio (0,8 M en agua), seguido de incubación durante 3 min a 90 grados en un baño de agua. Los tubos de reacción se enfriaron a temperatura ambiente antes de añadir 375 uL de solución de DMAB[4-(dimetilamino)benzaldehído]. Después de 20 min de incubación a 37 grados, se midió la absorbancia del producto coloreado formado a 560 nm, en un lector de microplacas Synergy, HT Multi-detection (Biotek, Bad Friedrichshall, Alemania) operado a través del software GEN5IM. El control negativo se realizó en ausencia de extracto. Se usó cromoglicato disódico (DSCG) como control positivo.
Se realizaron tres ensayos independientes por triplicado y los resultados se expresaron como el porcentaje de inhibición de la enzima en comparación con el control no tratado.
3.5.3.Inhibición de elastasa
El ensayo de inhibición de la elastasa pancreática porcina se realizó según Mota y colaboradores [57] con ligeras modificaciones. Los extractos acuosos se prepararon en agua, mientras que los extractos de acetona se prepararon en DMSO. Brevemente, en una 96-placa de pocillos, se mezclaron 50 μL del extracto con 90 μL de tampón HEPES (0,1 M), 10 uL de sustrato N-succinyl-Ala-Ala-Ala p-nitroanilida (100 uM), 70 uL de tampón de acetato (200 mM) y 30 uL de elastasa (1 U/mL). La placa se incubó a 37 grados durante 10 min, y la absorbancia del producto de reacción se midió a 405 nm, en un lector de microplacas Synergy HT Multi-detection (Biotek, Bad Friedrichshall, Alemania) operado a través de GEN51M. El control negativo se realizó en ausencia de extracto y como control positivo se utilizó ácido ascórbico.polvo de cistancheSe realizaron tres ensayos independientes por triplicado. Los resultados se expresaron como porcentaje de inhibición enzimática en comparación con el control no tratado.
3.5.4. Inhibición de tirosinasa
El ensayo de inhibición de tirosinasa se realizó de acuerdo con Adhikari et al.[58] con ligeras modificaciones. Brevemente, en una 96-placa de pocillos, se mezclaron 20 μL de cada extracto con 100 μL de tirosinasa (30 U/mL en tampón de fosfato). Los extractos acuosos se prepararon en agua, mientras que los extractos de acetona se prepararon en DMSO. La mezcla se incubó a 30 grados durante 8 min. Luego, se agregaron 80 μL de solución de L-DOPA (L-3,4-dihidroxifenilalanina) (2,5 mM en tampón fosfato) y se determinó inmediatamente la absorción (T0, absorbancia en un tiempo "cero"). medido con un lector de microplacas de detección múltiple Synergy HT (Biotek, Bad Friedrichshall, Alemania) operado a través del software GEN5TM, a 475 nm. La determinación de la absorbancia en T0 (antes de que se formara el producto de reacción) permitió eliminar posibles interferencias por el color natural de los extractos en estudio. Después de 8 min de incubación a 30 grados, se midió nuevamente la absorbancia (T8). Se calculó el porcentaje de inhibición de tirosinasa en presencia de extractos de cianobacterias en comparación con el control no tratado (negativo), donde la diferencia entre las absorbancias (T{ {21}}T0) corresponde al 100 por ciento de la actividad enzimática. El control negativo se realizó en ausencia de extracto y como control positivo se utilizó ácido kójico. Se realizaron tres ensayos independientes por triplicado. Los resultados se expresaron como porcentaje de inhibición enzimática en comparación con el control no tratado.
3.5.5.Factor de Protección Solar (FPS)
El factor de protección solar in vitro se determinó según Rohr y colaboradores[59] con ligeras modificaciones. Los extractos acuosos se prepararon en agua, mientras que los extractos de acetona se prepararon en acetona. Brevemente, se midió la absorbancia de 2mL de cada extracto (20 y 1000 ug/mL), en un espectrofotómetro (de 290 a 320 nm, 5 en 5 nm). El SPF se calculó utilizando la fórmula propuesta por Mansur [60]: donde EE(A) es el espectro de efecto eritematoso, I (A) es el espectro de intensidad solar, Abs(λ) es la absorbancia del extracto y CF es la corrección factor (28) determinado utilizando un protector solar comercial con un valor SFP conocido de 30.
3.6.Análisis estadístico
El análisis estadístico se realizó con el software de estadísticas IBM SPSS (versión 23.0 para macOS, IBM Corporation, Nueva York, NY, EE. UU., 2015). Los datos se analizaron para determinar la normalidad y la homogeneidad de las varianzas mediante Kolmogorov-Smirnov y Leven's pruebas, luego se someten a un ANOVA unidireccional usando HSD de Tukey (diferencia honestamente significativa) como una prueba postdoctoral, o a una prueba t no pareada. Se utilizó una prueba de correlación de Pearson para comparar los datos de expresión normalizados entre los perfiles químicos y las actividades biológicas de los extractos de cianobacterias.
3.7.Análisis de componentes principales (PCA)
PCA se utilizó para transformar una serie de variables potencialmente correlacionadas en una serie de variables relativamente independientes, capaces de clasificarse en función de su contribución para explicar la variación de todo el conjunto de datos[61]. Los componentes relativamente importantes de los patrones de alta dimensión se pueden identificar con éxito. Los datos originales de alta dimensión se pueden mapear en un espacio de menor dimensión y, por lo tanto, la complejidad de un problema de clasificación de patrones de alta dimensión se reduce considerablemente [62]. Para el presente estudio, el reconocimiento de patrones basado en PCA se realizó con el software estadístico IBM SPSS (versión 23.0 para macOS, IBM Corporation, Nueva York, NY, EE. UU., 2015). La matriz de datos consistió en los metabolitos presentes en los extractos acuoso y acetónico de las cuatro cepas de cianobacterias y su actividad a la concentración más alta probada.
4. Conclusiones
La actividad biológica mostrada por los extractos de cianobacterias analizados aquí demostró estar claramente correlacionada. De acuerdo con la presencia de PBP bioactivas, los extractos acuosos fueron los más efectivos para la protección UV, lo que, junto con su capacidad de eliminación de radicales, los sugiere como ingredientes prometedores para ser utilizados en formulaciones antienvejecimiento destinadas a prevenir el envejecimiento de la piel exacerbado por factores externos. Por otro lado, los extractos de acetona demostraron ser más efectivos para inhibir la actividad de las enzimas responsables de la degradación de la matriz dérmica y la pérdida de estructura de la piel, siendo así más adecuados para el envejecimiento de la piel relacionado con la edad.extracto de salsa cistancheEl esquema de extracción secuencial que proponemos podría resultar ventajoso, permitiendo la obtención de extractos bioactivos químicamente diferentes a través de la monetización de la biomasa de cianobacterias, haciendo el proceso más sostenible y económicamente atractivo. En conjunto, los extractos de cianobacterias demostraron ser dignos de una mayor explotación en el campo del envejecimiento de la piel, centrándose en la búsqueda de ingredientes naturales, seguros y sostenibles para formulaciones cosméticas.
Este artículo está extraído de Mar. Drugs 2022, 20, 183. https://doi.org/10.3390/md20030183 https://www.mdpi.com/journal/marinedrugs






