Detección y caracterización de nanopartículas mineralo-orgánicas en riñones humanos
Feb 22, 2022
Tsui Yin Wong1,2,*, Cheng-Yeu Wu1,2,3,* y otros
La calcificación ectópica está asociada con diversas enfermedades humanas, como la aterosclerosis, el cáncer,crónicoriñónenfermedad, ydiabetesmellitus. Aunque se han detectado nanopartículas minerales en vasos sanguíneos calcificados, la naturaleza y el papel de estas partículas en el cuerpo humano siguen sin estar claros. Aquí mostramos por primera vez que el ser humanoriñóntejidos obtenidos de etapa finalcrónicoriñónenfermedado los pacientes con cáncer renal contienen partículas minerales multilaminares redondas de 50 a 1.500 nm, mientras que en los controles sanos no se observan partículas. Las partículas minerales se encuentran principalmente en la matriz extracelular que rodea los túbulos contorneados, los conductos colectores y las asas de Henle, así como dentro del citoplasma de las células que delimitan los túbulos, y consisten en fosfato de calcio policristalino similar al mineral que se encuentra en los huesos y en las calcificaciones ectópicas. losriñónLas nanopartículas minerales contienen varias proteínas séricas que inhiben la calcificación ectópica en los fluidos corporales, incluidas la albúmina, la fetuina-A y la apolipoproteína A1. Dado que las nanopartículas minerales orgánicas se encuentran no solo en depósitos calcificados sino también en áreas desprovistas de calcificaciones microscópicas, nuestras observaciones indican que las nanopartículas pueden representar precursores de calcificación y cálculos renales en humanos.
Contacto:joanna.jia@wecistanche.com/ WhatsApp: 008618081934791

La calcificación ectópica se asocia con aterosclerosis, cáncer,crónicoriñónenfermedady diabetes mellitus1–3. Estudios recientes indican que la aterosclerosis ycrónicoriñónenfermedadlos pacientes con signos de calcificación vascular muestran mayores riesgos de morbilidad y mortalidad, lo que sugiere que la calcificación ectópica es perjudicial para la salud humana1,3. La calcificación no deseada también se observa en personas mayores y la mayoría de las personas mayores de 60 años muestran signos de calcificación vascular4. Por estas razones, descifrar los factores que inducen la calcificación ectópica y desarrollar un tratamiento efectivo representan metas importantes.
La calcificación ectópica se puede definir como un desequilibrio entre inhibidores e inductores de la calcificación en el organismo. Los inhibidores de la calcificación incluyen proteínas séricas como la albúmina, la fetuina-A, la osteopontina y la proteína GLA de la matriz, así como pequeños compuestos como el pirofosfato, mientras que la hiperfosfatemia y la inflamación representan los principales inductores de la calcificación5–7. Estudios recientes indican que los inductores de la calcificación activan un proceso celular similar a la formación de hueso durante la calcificación vascular7,8. En tejidos blandos calcificados también se han detectado vesículas de matriz similares a las que inducen la mineralización en huesos en desarrollo7–9. Estas vesículas de la matriz probablemente son liberadas por las células del músculo liso vascular que se diferencian en células similares a los osteoblastos, que inducen la calcificación7.
Se han detectado nanopartículas minerales (NP) en tejidos blandos que muestran signos de calcificación ectópica. Precio et al. encontraron que el suero de ratas tratadas con el bisfosfonato etidronato o con vitamina D albergaba complejos minerales-proteína que contenían los inhibidores de la calcificación fetuina-A y la proteína GLA de la matriz10,11. De manera similar, Jahnen-Dechent et al. observaron que en el líquido ascítico de pacientes con peritonitis calcificante podían detectarse complejos minerales que contenían fetuina-A, a los que denominaron partículas de calciproteína (CPP)12. Un estudio reciente de Bertazzo et al. demostraron la presencia de NP minerales en las válvulas aórticas y arterias coronarias de pacientes con fiebre aterosclerótica y reumática13. Si bien los estudios sobre la formación de partículas minerales generalmente se han centrado en el sistema cardiovascular humano, no está claro si las partículas se pueden encontrar en otros tejidos y si estas entidades juegan un papel en la salud o la enfermedad.
Anteriormente observamos que las NPS minerales orgánicas se forman espontáneamente en los fluidos corporales humanos y animales14–28. Estas NP minerales se describieron inicialmente como nanobacterias (NB) y se creía que no solo eran las células más pequeñas de la tierra29, sino también una posible causa transmisible de numerosas enfermedades, incluida la enfermedad de Alzheimer, la aterosclerosis, el cáncer,riñónpiedraformación, poliquísticoriñónenfermedady prostatitis30–32. Sin embargo, nuestros resultados han demostrado que las NB son, de hecho, NP minerales no vivas que imitan a las bacterias comunes en cuanto a su morfología, crecimiento, proliferación y subcultivo15,18,22. Queda por examinar la posibilidad de que se encuentren partículas minerales similares a los llamados NB en los tejidos humanos y si estas partículas desempeñan un papel en la enfermedad.
En el presente estudio, desarrollamos un enfoque de nanomateriales para detectar y analizar NP minerales-orgánicos en humanos enfermos.riñóntejidos. Mostramos que los tejidos renales de pacientes con enfermedad renal crónica en etapa terminal y cáncer renal contienen NP minerales multilaminares similares a las partículas minerales biomiméticas que precipitan espontáneamente en los fluidos corporales in vitro. Nuestros resultados revelan conocimientos críticos sobre la composición bioquímica, el mecanismo de formación y la función biológica de estas partículas minerales orgánicas y arrojan luz sobre los mecanismos de calcificación ectópica y el inicio de la enfermedad en el cuerpo humano.
Resultados
Examinamos tejidos renales extraídos quirúrgicamente de pacientes humanos con enfermedad renal crónica en etapa terminal (n=2) o cáncer renal (n=18; consulte la Tabla 1; para muestras de cáncer renal, nos enfocamos en las muestras no -parte cancerosa del tejido). Como controles sanos, estudiamos biopsias renales obtenidas de pacientes con trauma o hematoma pero que no tenían una función renal anormal previa (n=2; Tabla 1).
Los tejidos renales de individuos sanos mostraron características histológicas normales y no se observó calcificación ectópica después de la tinción de von Kossa (Fig. 1A, B). Por otro lado, los tejidos renales obtenidos de individuos enfermos y teñidos con hematoxilina y eosina (H&E) mostraron evidencia de daño tisular (Fig. 2A-C, indicado por flechas), y el 80 por ciento de los tejidos enfermos examinados mostraron depósitos mineralizados como se reveló. por tinción de von Kossa (Fig. 1C–T, Fig. 2E, F, la calcificación es visible como material negro indicado por flechas negras; consulte también la Tabla 1). Se observaron depósitos calcificados en la corteza y la médula, incluido el espacio extracelular que rodea los túbulos contorneados distales, los túbulos contorneados proximales, los conductos colectores y las asas de Henle, así como el citoplasma de las células que delimitan los túbulos y conductos (Fig. 1C-T y Fig. .2E, F). No se detectó calcificación en el corpúsculo renal (fig. 2D).

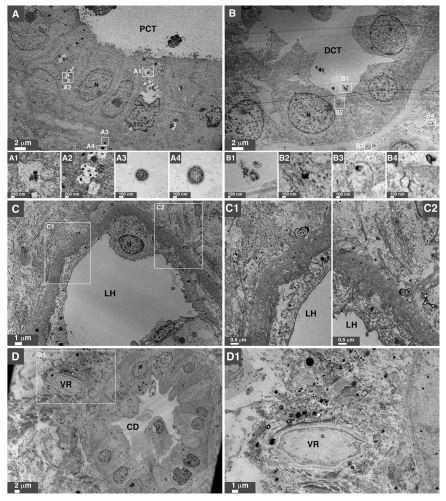
Para examinar la naturaleza de los precipitados minerales, preparamos secciones de riñón ultrafinas para su observación mediante microscopía electrónica de transmisión (TEM). En muestras que contenían depósitos minerales microscópicos, se detectaron partículas o gránulos minerales en el citoplasma de las células epiteliales renales, en la matriz extracelular debajo de la membrana basal y dentro de la luz de los túbulos contorneados proximales y distales (Fig. 3A, B, las partículas se agrandan en los paneles A1–A4 y B1–B4). También se observaron NP minerales dentro de las células que recubren las asas de Henle y los conductos colectores (Fig. 3C, D, ampliadas en los paneles C1, C2 y D1). Se encontraron algunas partículas dentro de vesículas intracelulares en células renales (Fig. 3A, paneles A1 y A2). El enfoque de microscopía electrónica utilizado aquí también nos permitió visualizar el interior de las partículas minerales; algunas partículas albergaban anillos densos en electrones que alternaban con capas livianas y transparentes para electrones (Fig. 3A, paneles A3 y A4, Fig. 3C, panel C1). Varios vasos sanguíneos, como los vasos rectos (las arterias rectas del riñón), están rodeados por una gran cantidad de NP minerales (Fig. 3D, panel D1). Por lo tanto, se encontraron NP minerales en varios lugares en todos los tejidos renales humanos que mostraban signos de calcificación ectópica, mientras que no se encontraron partículas en los controles sanos examinados.

Las partículas minerales que se encuentran en los tejidos renales parecen ser muy similares a las NP mineralo-orgánicas descritas que se forman espontáneamente en los fluidos corporales en nuestros estudios previos15,17 (y que hemos denominado bions24). Para verificar esta posibilidad, preparamos NP orgánicos minerales (o biones) usando un método de precipitación como describimos previamente15. Este método consiste en agregar iones precipitantes como calcio y fosfato en un medio de cultivo celular (medio de Eagle modificado por Dulbecco o DMEM) que contiene un fluido corporal como un suero humano (HS), seguido de incubación en condiciones de cultivo celular (ver Métodos). Las partículas producidas de esta manera (HS-NPS) eran esféricas o elipsoides y mostraban una superficie mineral lisa o cristalina (Fig. 4A-E), similar a las partículas descritas anteriormente en los fluidos corporales22,23, así como en la ascitis humana12 y arterias calcificadas13. Las partículas minerales eran muy similares a las NP o gránulos minerales observados en los tejidos renales en cuanto a su morfología general, estructura multicapa y características superficiales (Fig. 4F-J). El tamaño de las partículas derivadas de HS y los gránulos de riñón también fueron comparables, variando de 50 a 1500 nm de diámetro (Fig. 4A-E, F-J). Como se señaló anteriormente, algunos gránulos de riñón estaban rodeados por una membrana lipídica, lo que posiblemente representa vesículas de carga intracelular o vesículas de membrana extracelular (Fig. 4H, I, las membranas se indican con flechas); tales estructuras membranosas estaban ausentes en las muestras de HS-NP preparadas in vitro (Fig. 4A-E). Estas observaciones sugieren que los gránulos de riñón son similares a las NP mineralo-orgánicas ensambladas en el suero.

Usando el análisis de difracción de electrones de área seleccionada, observamos que la fase mineral de las HS-NP preparadas in vitro consistía en un nanomaterial policristalino (Fig. 4E, recuadro; observe los débiles anillos concéntricos). Se obtuvieron resultados similares para gránulos de riñón (Fig. 4J, recuadro) y para huesos y calcificaciones ectópicas como se describe en estudios previos33,35.
Estudiamos la composición química de HS-NP y gránulos de riñón mediante espectroscopia de rayos X de dispersión de energía (EDX). Los HS-NP mostraron picos importantes de carbono (C), calcio (Ca), oxígeno (O) y fósforo (P) (Fig. 4K), consistentes con la presencia de un mineral de fosfato de calcio. También se observó un pico bajo de silicio (Si) en HS-NP (Fig. 4K), lo que posiblemente represente un constituyente de partículas menor. Los gránulos de riñón también mostraron picos de carbono, calcio, oxígeno y fósforo, indicativos de un mineral de fosfato de calcio, junto con picos adicionales de silicio y hierro (Fe) (Fig. 4L). Los picos de uranio (U) se atribuyeron al acetato de uranilo utilizado como reactivo de contraste durante la preparación de la muestra (la presencia de uranio en algunas muestras de partículas minerales como gránulos de riñón y su ausencia en el tejido de control en la Fig. 4M puede atribuirse a la alta afinidad del uranio por el fosfato, como se informó previamente35). Los espectros EDX de control del tejido renal que rodea las partículas mostraron picos de carbono y oxígeno (Fig. 4M), lo que sugiere que el calcio y el fósforo se encontraron principalmente en las partículas minerales.
Las proporciones de calcio:fósforo (Ca:P) de HS-NP y gránulos de riñón variaron de 0.65 a 1.18. Estas proporciones difieren del valor teórico de 1,67 observado para la hidroxiapatita estequiométrica, pero todavía están dentro del rango visto anteriormente para los cristales de fosfato de calcio y apatita observados en varios grados de cristalización15. Juntos, estos hallazgos confirman que los gránulos renales consisten en NP de fosfato de calcio.
Se ha encontrado que varias proteínas inhiben la calcificación ectópica de manera sistémica en el cuerpo36,37. Además, se cree que la corona de proteínas que se encuentra en la superficie de las NP sintéticas determina la biodistribución y los efectos de las partículas en las células in vivo38,39. Por otro lado, la composición proteica de las NP mineralo-orgánicas que se encuentran en los tejidos renales humanos sigue sin comprenderse por completo. Encontramos previamente que la albúmina, la fetuina-A y la apolipoproteína-A1 (apo-A1) representan las principales proteínas que interactúan con las NP mineralo-orgánicas formadas en los fluidos corporales17,20. Aquí utilizamos el etiquetado de inmunooro para examinar la presencia y la ubicación ultraestructural de estas proteínas dentro de los gránulos de riñón.
Usamos anticuerpos policlonales contra albúmina sérica humana (HSA), fetuina-A sérica humana (HSF), apo-1A humana y HS completo para examinar la presencia de proteínas séricas en HS-NP y gránulos renales. La especificidad de los anticuerpos policlonales (preparados como se describió anteriormente25) se verificó mediante transferencia de Western (Fig. 5). Cada uno de los anticuerpos policlonales reaccionó positivamente con las HS-NP preparadas in vitro, así como con los gránulos minerales que se encuentran en los tejidos renales humanos (Fig. 6A,B, paneles A1-A3 y B1-B3; puntos negros). Los anticuerpos reaccionaron principalmente con las capas densas en electrones o el núcleo oscuro de las HS-NP y los gránulos renales (Fig. 6A, B), lo que indica que estas áreas oscuras pueden contener niveles más altos de proteínas en comparación con las áreas transparentes a los electrones. Los controles negativos realizados sin anticuerpo primario no produjeron reacción (Fig. 6A, B, paneles A4 y B4, control). Llegamos a la conclusión de que los gránulos de riñón representan NP mineralo-orgánicas similares a las HS-NP en función no solo de su morfología y composición mineral, sino también de su unión a los principales inhibidores de la calcificación presentes en el suero.
A continuación, se utilizó microscopía de inmunofluorescencia para confirmar la presencia de gránulos minerales que contenían HSA y HSF en riñones humanos enfermos. Usando esta técnica, los tejidos de riñón humano mostraron
tinción positiva para las dos proteínas en varias áreas, incluido el intersticio que rodea los túbulos renales, así como el citoplasma de las células que delimitan los túbulos (Fig. 7A, paneles A1 y A2). También se observaron agregados de proteínas que contenían albúmina y fetuina-A en estas áreas, aunque en cantidades más bajas en comparación con la tinción de las proteínas individuales (Fig. 7A y panel A3, tinción fusionada en amarillo). En particular, notamos que la tinción de proteínas detectada por inmunofluorescencia se superponía estrechamente con el patrón de calcificación ectópica observado mediante la tinción de von Kossa (Fig. 7A, B, la calcificación es visible como material negro indicado por flechas en B). Estos resultados proporcionan más apoyo a la presencia de partículas mineralo-orgánicas en los tejidos de riñón humano examinados.

Discusión
Si bien se han realizado avances en nuestra comprensión de las interacciones entre las NP sintéticas y las células humanas, sabemos mucho menos sobre los efectos de las NP mineralo-orgánicas que se forman espontáneamente en los fluidos corporales. Nuestros estudios previos han demostrado que estas partículas se forman en los fluidos biológicos cuando las concentraciones de calcio y fosfato superan la saturación15,16. También observamos que estas partículas son internalizadas por las células inmunitarias pero que solo las partículas grandes inducen reacciones inmunitarias proinflamatorias23. Sin embargo, hasta ahora no se había examinado la distribución de estas partículas en los tejidos humanos y si desempeñan algún papel fisiológico o patológico en el cuerpo.
En el presente estudio, detectamos por primera vez NP mineralo-orgánicas en riñones de pacientes humanos que padecían enfermedad renal en etapa terminal o cáncer renal. Las NP mineralo-orgánicas detectadas contienen fosfato cálcico pobremente cristalizado similar al mineral óseo, así como albúmina, fetuina-A y apo-A1 que actúan como inhibidores de la calcificación sistémica en los fluidos corporales. Nuestros resultados concuerdan con reportes previos que describieron la presencia de complejos mineral-proteicos en tejidos vasculares y fluidos corporales12,13,34,40. Dado que las partículas que observamos se encontraron en áreas que no contenían calcificaciones microscópicas, nuestras observaciones sugieren que las partículas pueden representar precursores de calcificación ectópica en tejidos humanos. Dada la posibilidad de que las NP mineralo-orgánicas puedan crecer gradualmente en tamaño y sufrir una conversión de partícula a película en condiciones favorables como se describe en nuestros estudios previos15,18, las observaciones presentadas aquí sugieren que los precursores minerales pueden conducir a la formación de partículas más grandes. depósitos minerales in vivo, como la placa de Randall y cálculos renales.
Nuestras observaciones de que se encuentran calcificaciones ectópicas minerales y NP mineralo-orgánicas en varias estructuras anatómicas de los riñones son consistentes con hallazgos previos de calcificaciones ectópicas en este órgano41. Las observaciones de Evan et al. indicaron que la mineralización en los riñones de pacientes con nefrolitiasis puede comenzar y ocurrir predominantemente en el tejido intersticial de las asas de Henle40,42. Estos autores observaron que los depósitos minerales que se forman en esta zona pueden sobresalir de la cara basal del urotelio y dar lugar a la formación de cálculos renales. Nuestras observaciones sugieren que, además de las asas de Henle, otras áreas renales pueden contener NP minerales que eventualmente pueden evolucionar para formar grandes depósitos minerales en los riñones humanos. También estamos investigando la posibilidad de que las NP minerales que se forman en la circulación sanguínea se transloquen a los tejidos renales e induzcan la calcificación ectópica y la formación de cálculos en los riñones.
Varios gránulos de riñón detectados en el presente estudio se encuentran dentro de vesículas intracelulares o extracelulares (Fig. 4H, I) y son similares a las vesículas de matriz que inducen la calcificación en huesos y dientes7,8. Recientemente observamos que las vesículas aisladas de suero humano y animal inducen la formación de NP minerales y precipitados microscópicos in vitro25. Schlieper et al.34 también observaron que las partículas minerales que se encuentran en las arterias están asociadas con estructuras de membrana y propusieron que las vesículas de matriz o cuerpos apoptóticos pueden representar nucleadores de partículas minerales en estos tejidos. Del mismo modo, Khan et al. informaron que los depósitos de fosfato de calcio que se encuentran en los riñones de pacientes humanos con cálculos renales idiopáticos están asociados con fibras de colágeno y vesículas de matriz9. Estos resultados sugieren que las NP mineralo-orgánicas detectadas en los tejidos renales pueden formarse a través de un mecanismo que involucra vesículas de membrana, una situación análoga a la que se observa en las arterias ateroscleróticas7,8. Por otro lado, un estudio reciente mostró que la calcificación ectópica encontrada en las arterias mamarias de mujeres no estaba asociada con marcadores celulares osteogénicos o apoptóticos43, lo que sugiere que el mecanismo de calcificación puede ser específico del órgano o contexto biológico involucrado. Además, las NP mineralo-orgánicas como las descritas aquí en los tejidos renales humanos también pueden formarse debido a la falta de mantenimiento de las concentraciones fisiológicas de iones (p. ej., calcio y fosfato) e inhibidores de la calcificación (p. ej., albúmina, fetuina-A y apo). -A1) en los fluidos corporales humanos.

Nuestros resultados sugieren que la capa densa en electrones y el núcleo de las NP minerales-orgánicas pueden contener niveles más altos de proteínas y moléculas orgánicas en comparación con las áreas lúcidas de electrones de las partículas (Fig. 6A, B). Estas capas densas en electrones parecen estar mineralizadas como se ve por la naturaleza cristalina de este material bajo TEM (ver Fig. 4A-J). Otros autores, incluidos Ryall41 y Evan et al.44, han propuesto que la capa electrolúcida puede representar minerales, mientras que las capas electrodensas pueden corresponder a moléculas orgánicas. Estas interpretaciones pueden deberse, al menos en parte, a la forma en que se procesaron y examinaron las muestras en cada estudio, así como a la naturaleza de los tejidos de partida utilizados.
Además de desempeñar un papel en la calcificación ectópica, las partículas orgánicas minerales pueden inducir inflamación en los tejidos renales. Hemos demostrado recientemente que, mientras que las NP mineralo-orgánicas no logran inducir la secreción de interleucina proinflamatoria-1 por parte de los macrófagos humanos, los agregados minerales de más de 1 μm pueden hacerlo23. Se ha demostrado que la liberación de interleucina-1 en respuesta a materiales cristalinos depende de la activación de complejos moleculares intracelulares denominados inflamasomas45–47. Además, las partículas minerales se detectaron en riñones que albergaban tumores y ahora se reconoce bien la asociación entre el cáncer y la inflamación48. Queda por investigar la posibilidad de que las partículas minerales agregadas puedan activar un inflamasoma y contribuir al desarrollo de inflamación y cáncer en los riñones u otros tejidos.
Además de la calcificación ectópica, los gránulos minerales descritos aquí pueden participar en otros procesos patológicos. Por ejemplo, hemos propuesto anteriormente que las NP minerales pueden unirse a varias proteínas en los fluidos corporales y agotar estas moléculas orgánicas de los fluidos corporales20,26. Por otro lado, el cuerpo humano puede prevenir la formación y acumulación de NP minerales en circunstancias normales al depender de la presencia de inhibidores de la calcificación y del sistema reticuloendotelial (es decir, macrófagos). Por lo tanto, las NP minerales pueden acumularse solo una vez que se perturba la homeostasis del calcio sistémica o local y cuando los mecanismos de protección han fallado en el cuerpo humano.
Proponemos que el enfoque de nanomateriales desarrollado aquí se puede utilizar para estudiar la formación de NP mineralo-orgánicas en tejidos animales y humanos. Por ejemplo, los anticuerpos generados contra las proteínas inhibidoras de la calcificación, como la albúmina, la fetuina-A y la apo-A1, pueden usarse en combinación con el análisis de minerales para detectar y caracterizar la formación de NP mineralo-orgánicas en los tejidos de modelos animales. Los resultados obtenidos con este enfoque pueden aplicarse a mediciones clínicas realizadas en fluidos corporales humanos para identificar parámetros biológicos que reflejen el estado de formación de partículas minerales y calcificación ectópica en el cuerpo. Esperamos que este conocimiento pueda conducir al desarrollo de nuevas estrategias terapéuticas para prevenir y tratar enfermedades humanas y afecciones asociadas con la calcificación ectópica.
Métodos
Tejidos renales.El uso de tejidos humanos y los experimentos realizados en este estudio fueron aprobados por la Junta de Revisión Institucional del Hospital Chang Gung Memorial; los métodos y experimentos se llevaron a cabo de acuerdo con las directrices aprobadas. Se obtuvo el consentimiento informado por escrito de los pacientes. Se obtuvieron tejidos renales sanos de control a partir de biopsias de pacientes con traumatismos y hematomas sin antecedentes de enfermedad renal (n=2); También se obtuvieron tejidos renales de pacientes con cáncer renal (n=20) y de pacientes con enfermedad renal en etapa terminal (n=2) cuyos riñones fueron extirpados o sometidos a biopsia durante la cirugía de trasplante (Tabla 1). Para los tejidos de cáncer renal, la parte no cancerosa del tejido se diseccionó y analizó en el presente estudio.

Análisis histológico.Los tejidos renales se montaron en bloques de parafina. Los bloques se seccionaron y los cortes de tejido se calentaron en una placa caliente a 70 grados durante 30 minutos para eliminar la parafina. Las secciones se sumergieron en una solución fresca de xileno tres veces durante 15 minutos para eliminar completamente la parafina restante. Las secciones se rehidrataron con etanol al 95 %, 80 % y 70 % durante 5 minutos cada vez. Las muestras rehidratadas se lavaron con agua bidestilada (ddH2O) durante 5 min. Los núcleos celulares se tiñeron con hematoxilina durante 8 min. El colorante se eliminó de las muestras con agua tibia durante 10 min. Las muestras de riñón se enjuagaron en ddH2O y se sumergieron 10 veces en etanol al 95 por ciento. Las muestras tratadas con etanol se contrateñeron con eosina Y durante 1 min. Los especímenes se deshidrataron con etanol al 95 por ciento y al 100 por ciento durante 10 minutos cada vez, seguido de un paso de deshidratación en xileno durante 10 minutos. Las muestras finales de riñón deshidratado se montaron en portaobjetos de vidrio con 50 por ciento de glicerol y se observaron bajo un microscopio óptico equipado con una cámara digital.

Las muestras desparafinadas y rehidratadas se prepararon como se describe para la tinción con H&E. Las secciones rehidratadas se tiñeron con nitrato de plata (5 por ciento), seguido de exposición a luz ultravioleta durante 20 min. La solución se lavó con ddH2O durante 15 min. Las secciones se tiñeron con tiosulfato de sodio (5 por ciento) durante 5 min, seguido de lavado con ddH2O durante 15 min. Las secciones se tiñeron con rojo sólido nuclear (Sigma-Aldrich, St. Louis, MI) durante 5 minutos. Las muestras teñidas se deshidrataron sucesivamente con etanol al 95 por ciento y al 100 por ciento durante 10 min cada una, antes de la deshidratación en xileno durante 10 min. Las muestras de riñón se montaron en portaobjetos de vidrio y se examinaron como se describe anteriormente.
Microscopía electrónica y análisis EDX.Las muestras de riñón se cortaron en pequeños trozos de menos de 1 mm de espesor utilizando un microscopio de disección LGPS (Olympus, Tokio, Japón). Los tejidos se fijaron con glutaraldehído al 2,5 por ciento y paraformaldehído al 1 por ciento en tampón de cacodilato 0, 1 M a 4 grados durante la noche. Las muestras fijadas se lavaron tres veces con tampón de cacodilato 0,1 M en sacarosa al 8 por ciento (pH 7,2) en hielo durante 10 min. Los tejidos lavados se incubaron en solución salina tamponada con fosfato (PBS; NaCl 137 mM, KCl 2,7 mM, Na2HPO4 10 mM) que contenía tetróxido de osmio al 1 por ciento y ferrocianuro de potasio al 1,5 por ciento durante 2 h en hielo. Los tejidos se lavaron con ddH2O en hielo 10 min tres veces. Los tejidos lavados se tiñeron en hielo con acetato de uranilo al 1 por ciento en ddH2O durante 1 hora, antes de lavarlos tres veces con ddH2O en hielo. Los tejidos renales se deshidrataron con etanol al 30, 50, 70, 80 y 90 por ciento durante 10 minutos cada vez, excepto cuando el etanol alcanzó el 70 por ciento, en cuyo caso las muestras se almacenaron a 4 grados durante la noche. Los tejidos se tiñeron con ácido fosfotúngstico al 1 por ciento en etanol al 95 por ciento durante 15 min, antes de la deshidratación con etanol al 95 por ciento durante 5 min. Las muestras se sumergieron en óxido de propileno al 40, 57, 67 y 100 por ciento en etanol durante 10 min cada vez, seguido de otra inmersión en óxido de propileno al 100 por ciento durante 5 min. Los tejidos renales se infiltraron con Eponate 812 al 50, 70 y 100 por ciento (Ted Pella, Redding, CA) durante 1 h cada vez. Se prepararon muestras de riñón incluidas en Eponate 812- incubando dos veces en Eponate al 100 por ciento. Las muestras incrustadas se incubaron en un horno a 60 grados durante la noche para permitir la polimerización de la resina.
Los gránulos de HS-NP lavados obtenidos como anteriormente se fijaron con glutaraldehído (2,5 por ciento) y paraformaldehído (1 por ciento) en ddH2O durante 4 horas a 4 grados. Los sedimentos fijos se lavaron con ddH2O tres veces durante 10 minutos cada vez. Los gránulos se deshidrataron con incubaciones sucesivas en etanol al 30, 50, 70, 80, 90, 95 y 100 por ciento, durante 10 minutos cada vez, excepto cuando el etanol alcanzó el 70 por ciento, en el que los gránulos se almacenaron a 4 grados durante la noche. Otras soluciones de etanol solo se pusieron en contacto con los gránulos durante 10 minutos. Los gránulos deshidratados se infiltraron con medio de inclusión blanco LR (Electron Microscopy Sciences, Hatfield, PA) utilizando diferentes proporciones de etanol y medio LR (3:1, 1:1 y 1:3) durante 30 minutos cada uno. Los sedimentos se infiltraron con medio LR fresco (100 por ciento) durante la noche antes de la polimerización. Los sedimentos infiltrados con medio LR se incubaron en un horno a 60 grados durante 2 días para permitir la polimerización de la resina. Se seccionaron bloques de riñón y HS-NP para producir rebanadas con un grosor de 70 a 100 nm utilizando un micrótomo Reichert Ultracut S (Leica, Wetzlar, Alemania). Las secciones de tejido se tiñeron con acetato de uranilo al 4 por ciento antes de la visualización en un microscopio electrónico de transmisión JEM 1230 (JEOL, Tokio, Japón) operado a 100 kV. Los patrones de difracción de electrones se obtuvieron usando el mismo sistema. Se utilizaron rejillas de níquel como soporte.
Para el análisis EDX, se tiñeron secciones delgadas de tejidos renales con acetato de uranilo y se lavaron con ddH2O como se indicó anteriormente, seguido de secado en un gabinete desecador electrónico. Los especímenes se observaron bajo un microscopio electrónico de transmisión (JEOL) JEM 2100 de alta resolución operado a 120 kV. Los espectros EDX se obtuvieron por triplicado utilizando un sistema INCA Energy EDS (Oxford Instruments, Abingdon, Reino Unido). Se observaron secciones delgadas de HS-NP sin tinción.
Preparación de NPs mineralo-orgánicas.Todas las soluciones iniciales se ajustaron a pH 7,4 y se esterilizaron mediante filtración a través de membranas de 0,2 μm antes de su uso. HS se obtuvo de voluntarios humanos sanos utilizando una técnica de venopunción convencional. El uso de fluidos biológicos humanos en este estudio fue aprobado por la Junta de Revisión Institucional del Hospital Conmemorativo Linko Chang Gung y se obtuvo el consentimiento informado por escrito de los voluntarios. Los HS-NP se prepararon agregando CaCl2 3 mM y Na2HPO4 cada uno en DMEM (Gibco, Carlsbad, CA) que contenía 10 por ciento de HS, seguido de incubación durante una semana en condiciones de cultivo celular (37 grados, 5 por ciento de CO2, aire humidificado). Las partículas se sedimentaron mediante centrifugación a 16,000 ×g durante 15 min a 4 grados y se lavaron dos veces con tampón HEPES (HEPES 20 mM, CaCl2 1 mM, Na2HPO4 2 mM, NaCl 150 mM) utilizando el mismo procedimiento de centrifugación.
SDS-PAGE y Western Blot.El análisis SDS-PAGE y Western blot se realizó esencialmente como antes15. Brevemente, 0.2 ug (Fig. 5A,D) o 1.2 ug (Fig. 5B,C) de proteínas HS, 47 ug (Fig. 5A,B,D) o 590ug de proteínas HS-NP (Fig. 5C), 0.1ug de HSA (Fig. 5A–D) y 0.6ug (Fig. 5A, C, D) o {{23} }.15 ug de HSF (Fig. 5B) se disolvieron en 5x "tampón de carga" (0.313 M Tris-HCl pH 6.8, 10 por ciento de SDS, 0.05 por ciento de azul de bromofenol, 50 por ciento de glicerol, 12.5 por ciento de - mercaptoetanol) hasta una concentración final de 1x, antes de calentar a 95 grados durante 5 minutos y separar en condiciones desnaturalizantes y reductoras en un SDS-PAGE al 10 por ciento usando un sistema de minigel (Hoefer, Holliston, MA). El control de NP (usado en el carril 1 de la Fig. 5A-D) consistió en NP minerales preparadas agregando CaCl2 3 mM y Na2HPO4 cada uno en DMEM (volumen final de 1 ml), seguido de incubación durante un día en condiciones de cultivo celular; las partículas se sedimentaron mediante centrifugación a 16,000 ×g durante 15 min, se lavaron dos veces con tampón HEPES y se resuspendieron en 50 ul de tampón HEPES. Se procesó una alícuota de 20 ul de partículas resuspendidas para SDS-PAGE como anteriormente. Las membranas de PVDF se bloquearon durante 1 h en leche desgrasada al 5 por ciento (p/v) a temperatura ambiente. Los anticuerpos primarios generados internamente como se describió antes25 se usaron a una dilución de 1:1,000 ( -apo-A1 y -HS-NP), 1:3,000 ( -HSF) , o 1:6,000 ( -HSA). El anticuerpo secundario conjugado con peroxidasa de rábano picante anti-conejo de cabra se usó según las instrucciones proporcionadas por el fabricante (Millipore, Billerica, MA). Las transferencias se revelaron usando quimioluminiscencia mejorada (Amersham Biosciences, Amersham, Reino Unido) y películas autorradiográficas.
Marcaje con inmunooro.Se prepararon muestras para observación TEM. Los bloques de HS-NP se seccionaron en rodajas de menos de 70 nm de espesor. Las secciones de muestra en las rejillas se bloquearon con gelatina de pescado al 1 por ciento (Sigma) en tampón HEPES 0, 1 M (pH 8,0) durante 25 minutos. Las rejillas se incubaron con los siguientes anticuerpos primarios: -HSA, 1:30; -HSF, 1:50; -apo-A1, 1:30; -HS-NP, 1:60. El control negativo no contenía anticuerpo primario (1 por ciento de gelatina de pescado en tampón HEPES). Las secciones incubadas se enjuagaron con tampón HEPES durante 15 min. Las secciones enjuagadas se bloquearon con gelatina de pescado al 1 por ciento en tampón HEPES durante 20 min. Los especímenes se trataron con IgG anti-conejo de cabra conjugada con oro 5-nm secundaria durante 1 h. Las muestras se lavaron con tampón HEPES durante 10 min, antes de lavarlas con ddH2O durante 10 min. Las observaciones TEM se realizaron como se indicó anteriormente.
Microscopio fluorescente.Los portaobjetos histológicos de tejido renal preparados como antes se bloquearon con albúmina de suero bovino al 1 por ciento durante 1 hora a temperatura ambiente. Los portaobjetos se incubaron con anticuerpos policlonales primarios a una dilución de 1:4,000. Después de los pasos de lavado, las muestras se incubaron con los anticuerpos secundarios cabra anti-conejo-FITC (492/520nm) y cabra anti-conejo-TRITC (550/570nm) (Jackson Immuno Research, West Grove, PA) a 1:100 durante 1 hora Los complejos se lavaron con PBST durante 15 min. La tinción fluorescente 4',6-diamidino-2-fenilindol (DAPI) se usó a 10 ug/ml durante 15 min. Los especímenes teñidos con DAPI se deshidrataron con etanol al 95 y al 100 por ciento durante 10 min cada uno, seguido de deshidratación en xileno durante otros 10 min. Las muestras de riñón deshidratadas se montaron con medio de montaje Vectashield fluorescence H-1000 (Vector Laboratories, Burlingame, CA) y se observaron con un microscopio confocal (LSM510 Meta; Zeiss, Oberkochen, Alemania) equipado con una cámara Spot Flex.

Cistanche tubulosa previene la enfermedad renal, haga clic aquí para obtener la muestra
Referencias
1. Giachelli, CM Calcificación ectópica: recopilación de datos concretos sobre la mineralización de tejidos blandos. Am J Pathol 154, 671–675 (1999).
2. Abedin, M., Tintut, Y. & Demer, LL Calcificación vascular: mecanismos y ramificaciones clínicas. Arterioscler Thromb Vasc Biol 24, 1161–1170 (2004).
3. Alexopoulos, N. & Raggi, P. Calcificación en la aterosclerosis. Nat Rev Cardiol 6, 681–688 (2009).
4. Allison, MA, Criqui, MH & Wright, CM Patrones y factores de riesgo para la aterosclerosis calcificada sistémica. Arterioscler Thromb Vasc Biol 24, 331–336 (2004).
5. Ketteler, M. et al. Deficiencias de proteínas reguladoras del calcio en pacientes en diálisis: un concepto novedoso de calcificación cardiovascular en la uremia. Kidney Int Suppl 84, S84–87 (2003).
6. Kapustin, A. & Shanahan, CM Apuntando a la calcificación vascular: ablandando un objetivo difícil. Curr Opin Pharmacol 9, 84–89 (2009).
7. Kapustin, AN & Shanahan, CM Regulación del calcio de vesículas de matriz derivadas de células de músculo liso vascular. Tendencias Cardiovasc Med 22, 133–137 (2012).
8. Doherty, TM et al. Calcificación en aterosclerosis: biología ósea e inflamación crónica en el cruce arterial. Proc Natl Acad Sci USA 100, 11201–11206 (2003).
9. Khan, SR, Rodriguez, DE, Gower, LB & Monga, M. Asociación de placas de Randall con fibras de colágeno y vesículas de membrana. JUrol 187, 1094–1100 (2012).
10. Price, PA, Nguyen, TM & Williamson, MK Caracterización bioquímica del complejo fetuína-mineral sérico. J Biol Chem 278, 22153–22160 (2003).
11. Price, PA, Williamson, MK, Nguyen, TM & Than, TN Los niveles séricos del complejo fetuin-mineral se correlacionan con la calcificación arterial en la rata. J Biol Chem 279, 1594-1600 (2004).
12. Heiss, A. et al. Papel jerárquico de fetuin-A y proteínas séricas ácidas en la formación y estabilización de partículas de fosfato de calcio. J Biol Chem 283, 14815–14825 (2008).
13. Bertazzo, S. et al. La microscopía electrónica nanoanalítica revela conocimientos fundamentales sobre la calcificación del tejido cardiovascular humano. Nat Mater 12, 576–583 (2013).
14. Martel, J. & Young, JD Supuestas nanobacterias en la sangre humana como nanopartículas de carbonato de calcio. Proc Natl Acad Sci USA 105, 5549–5554 (2008).
15. Young, JD et al. Las supuestas nanobacterias representan restos fisiológicos y subproductos de cultivo de la homeostasis normal del calcio. Plos One 4, e4417 (2009).
16. Young, JD et al. Caracterización de granulaciones de calcio y apatita en suero como complejos pleomórficos mineraloproteicos y como precursores de supuestas nanobacterias. Plos One 4, e5421 (2009).
17. Wu, CY, Martel, J., Young, D. & Young, JD Fetuin-A/albúmina-complejos minerales que se asemejan a gránulos de calcio sérico y supuestas nanobacterias: demostración de un concepto de siembra de inhibición dual. Plos One 4, e8058 (2009).
18. Young, JD & Martel, J. El ascenso y la caída de las nanobacterias. Sci Am 302, 52–59 (2010).
19. Martel, J., Wu, CY y Young, JD Evaluación crítica del suero irradiado con rayos gamma utilizado como alimentador en el cultivo y demostración de supuestas nanobacterias y nanopartículas calcificantes. Plos One 5, e10343 (2010).
20. Martel, J. et al. Análisis proteómico integral de nanopartículas minerales derivadas de fluidos corporales humanos y analizadas mediante cromatografía líquida-espectrometría de masas en tándem. Anal Biochem 418, 111–125 (2011).
