Ingredientes efectivos de Cistanche: método de separación y purificación de glucósidos feniletanoide
Mar 14, 2022
Contacto:joanna.jia@wecistanche.com
Aislamiento y purificación de glucósidos feniletanoide de Cistanche Deserticola por cromatografía a contracorriente de alta velocidad
Lia,b, Rong Tsaob,*, Raymond Yangb, Chunming Liua,
J. Christopher Youngb, Honghui Zhub
a Departamento de Química, Universidad Normal de Changchun, Changchun 130032, China
b Centro de Investigación Alimentaria de Guelph, Agricultura y Agroalimentación de Canadá, 93 Stone Road West, Guelph, Ontario, Canadá N1G 5C9
Recibido el 31 de mayo de 2007; recibido en forma revisada el 16 de octubre de 2007; aceptado el 29 de octubre de 2007
Resumen:
Cincoglucósidos de feniletanoide(PhG),echinacósido, cistanoside A, acteoside, isoacteoside y 20-acetylacteoside, fueron aislados y purificados deCistanche deserticapor primera vez por cromatografía en contracorriente de alta velocidad (HSCCC) utilizando dos sistemas bifásicos, uno compuesto por acetato de etilo-etanol-agua (5:0.5:4.5, v/v/v) y otro de acetato de etilo-n-butanol-etanol-agua ({{10}}.5:0.5:0.1:1, v/v/v/v). Un total de 28,5 mg de equinacósido, 18,4 mg decistanósido A, 14,6 mg deacteósido, se purificaron 30,1 mg de isoactósido y 25,2 mg de 20-acetilactósido a partir de 1412 mg del extracto de n-butanol deCistanche desertica, cada uno con más del 92,5 por ciento de pureza según lo determinado por HPLC. Las estructuras se identificaron por su tiempo de retención, UV, LC-ESI-MS en el modo de iones negativos y se confirmaron mediante experimentos de RMN. Se discute el patrón de fragmentación característico de LC-ESI-MSn de los cinco compuestos, y se encontró que es una herramienta muy específica y útil para la identificación estructural de PhG de esta importante planta medicinal.
Crown Copyright © 2007 Publicado por Elsevier Ltd. Todos los derechos reservados.
Palabras clave:Cistanche desertica; Feniletanoide;equinacósido; cistanósido A;Acteósido; isoactósido; 20-Acetilacteosido; HSCCC; LC-ESI-MS; RMN

1. Introducción
Cistanche deserticaYC Ma es una medicina herbaria china muy conocida y ha sido ampliamente utilizada en preparaciones tradicionales similares a los ingredientes de alimentos funcionales o complementos alimenticios actuales (Wong, Li, Cheng y Chen, 2006). Los principales constituyentes bioactivos de C. deserticola sonfeniletanoideglucósidos (PhG), incluidosechinacósido, acteósido, isoactósido, 20-acetilactósido ycistanósido A(Kobayashi, Karasawa y Miyase, 1984; Kobayashi et al., 1987). Las PhG están ampliamente distribuidas en el reino vegetal y han sido ampliamente estudiadas por sus diversas funciones biológicas, como hepatoprotección (Xiong et al., 1998), actividad antiinflamatoria, antinociceptiva (Schapoval et al., 1998) y actividad antioxidante (Cheng et al., 1998). , Wei, Guo, Ni y Liu, 2005; He, Lau, Xu, Li y But, 2000; Li, Wang y Wang, 1997; Li, Wang, Zheng, Liu y Jia, 1993; Wang, Jiang , Wu y Wang, 2001; Xiong, Kadota, Tani y Namba, 1996), mejora de la función sexual (Xie y Wu, 1993; Zong, He, Wu y Chen, 1996) y efecto sedante (Lu, 1998) .
Debido a las importantes bioactividades anteriores, se necesitan urgentemente grandes cantidades de compuestos puros como patrones de referencia y para varios estudios in vitro e in vivo relacionados con el uso de medicamentos tradicionales chinos. Por lo tanto, se hacen necesarios métodos efectivos para el aislamiento, la purificación y la caracterización estructural de las PhG. Sin embargo, dicho trabajo generalmente requiere el uso de múltiples pasos cromatográficos para la limpieza y el aislamiento de la muestra (Gross, Lahloub, Anklin, Schulten y Sticher, 1988; Nishimura, Sasaki, Inagaki, Chin y Mitsuhashi, 1991; Ravn, Nishibe , Sasahara, & Li, 1990; Shoyama, Matsumoto, & Nishioka, 1987), lo que generalmente resulta en bajas tasas de recuperación debido a la adsorción irreversible de PhG en el soporte sólido durante la separación (Lei et al., 2001). Por el contrario, la cromatografía en contracorriente de alta velocidad (HSCCC) se ha convertido en una alternativa eficaz a las técnicas cromatográficas convencionales para la separación de algunas PhG de extractos de plantas (Lei et al., 2001; Li et al., 2005). Ley et al. separados con éxitoacteósidoy 20-acetilacteoside de Cistanches salsa (CA Mey.) G. Beck usando HSCCC (Lei et al., 2001). Los autores de este artículo han informado previamente sobre la separación deacteósidoe isoactósido de Plantago psyllium L. por HSCCC (Li et al., 2005). Sin embargo, no se ha publicado ningún informe sobre la separación y purificación de múltiples PhG deCistanche deserticautilizando HSCCC. Debido a la falta de estándares, los métodos de LC-MS se han desarrollado y utilizado como una poderosa herramienta analítica para la caracterización e identificación rápidas de algunas PhG en extractos de plantas (Li et al., 2005; Wang et al., 2000).
En este artículo, presentamos un método HSCCC desarrollado para la preparación de echinacósido,cistanósido A, acteoside, isoacteoside y 20-acetylacteoside deCistanche desertica. La caracterización y el análisis de las cinco PhG separadas se realizaron mediante el uso de LC junto con experimentos de RMN y espectrometría de masas ESI en línea. En este artículo se presentan y analizan el tiempo de retención, el peso molecular y los iones de fragmentos característicos de las cinco PhG. Las estructuras de los cinco PhG identificados en esta investigación se muestran en la Fig. 1.

2. Experimental
2.1. Sustancias químicas y reactivos
Acteósidose adquirió de Sigma-Aldrich (Oak-Ville, ON), el equinacósido se adquirió de ChromaDex (Santa Ana, CA). El isoactósido se aisló de P. psyllium L. (Li et al., 2005).Cistanche deserticase compró en Beijing TongRenTang Medicinal Store (China). Todos los disolventes eran de grado HPLC y adquiridos de Caledon Laboratories Ltd. (Georgetown, ON).

2.2. preparación de la muestra
Cistanche desertica(20 g) se extrajo cinco veces a temperatura ambiente durante 12 h cada una con 100 ml de etanol acuoso al 80 por ciento. Cada vez, la mezcla de extracción se filtró a través de un papel de filtro Whatman No.1 (Whatman International Ltd., Maidstone, Inglaterra). El filtrado combinado se concentró a 100 ml al vacío a <40 grados.="" la="" solución="" acuosa="" resultante="" se="" desengrasó="" dos="" veces,="" cada="" una="" con="" 100="" ml="" de="" hexano,="" y="" luego="" se="" extrajo="" sucesivamente="" cinco="" veces,="" cada="" una="" con="" 100="" ml="" de="" n-butanol.="" las="" capas="" de="" n-butanol="" se="" combinaron="" y="" concentraron="" hasta="" sequedad="" al="" vacío="" a="">< 40="" grados,="" lo="" que="" produjo="" 2,2="" g="" de="" extracto="" de="" n-butanol.="" el="" extracto="" se="" almacenó="" a="" -20="" grados="" antes="" de="" la="" separación="">
2.3. Procedimiento de separación HSCCC
El HSCCC preparativo se llevó a cabo en una cromatografía en contracorriente de alta velocidad modelo CCC{{0}} (Pharma-Tech Research, Baltimore, Maryland, EE. UU.). Este aparato tenía tres bobinas preparativas, conectadas en serie (volumen total, 325 mL). La velocidad de revolución del aparato podría regularse entre 0 y 2000 rpm. El sistema HSCCC estaba equipado con una bomba HPLC (Pharma-Tech Research, Baltimore, Maryland, EE. UU.), un detector UV modelo 450 (Alltech, EE. UU.), un registrador de cama plana modelo L 120 E (Linseis Inc., Princeton Jct, EE. UU.), un colector de fracciones (Advantec MFS Inc., EE. UU.) y una válvula de inyección de muestra con un bucle de muestra de 10-mL.
Una mezcla de acetato de etilo-etanol-agua (5:0.5:4.5, v/v/v) se agitó vigorosamente en un embudo de decantación y se dejó reposar y separar a temperatura ambiente. Las dos fases se usaron en el HSCCC después de que alcanzaron el equilibrio. Toda la columna enrollada se llenó primero con la capa superior, que sirve como fase estacionaria. Luego, la capa inferior (fase móvil) se bombeó al extremo de cabeza de la columna a una velocidad de flujo de 1,5 ml/min. La velocidad de rotación se fijó en 1050 rpm. Una muestra (aprox. 230 mg cada vez) disuelta en 8 ml de la mezcla de acetato de etilo-etanol-agua (5:0,5:4,5, v/v/v) se cargó en la válvula de inyección después de que el sistema alcanzó la hidrodinámica. equilibrio. Este sistema solvente bifásico fue seleccionado en base al coeficiente de partición (K), que fue 0.87, 1.11 y 1.32 paraacteósido, isoactósido y 20 acetilactósido, respectivamente. El valor K fue la relación de las concentraciones en las capas superior e inferior del mismo compuesto determinado por HPLC (Fig. 2). El efluyente de la salida de la columna se monitoreó continuamente con un detector UV a 254 nm y se recolectó en tubos de ensayo con un colector de fracciones ajustado a 4 min para cada tubo.

2.4. Condiciones de CL
Para el análisis de PhGs en el extracto de n-butanol deCistanche deserticay fracciones recolectadas de la separación HSCCC. La separación se llevó a cabo en una columna Phenomenex ODS-C18 (250 × 4,6 mm, 5 lm) con una precolumna C18. La fase móvil binaria constaba de acetonitrilo (disolvente A) y agua que contenía ácido acético al 2 por ciento (disolvente B). Todos los solventes fueron filtrados a través de un
{{0}}.45 lm antes de usar. El caudal se mantuvo constante a 1,0 ml/min durante un tiempo de ejecución total de 25 min. El sistema se ejecutó con un programa de gradiente: 0–20 min: 90 por ciento B a 60 por ciento B; 20–22 min: 60 por ciento B a 0 por ciento B; y 22–25 min, 0 por ciento B a 90 por ciento B. El volumen de inyección de la muestra fue de 10 l. Los picos de interés se controlaron a 320 nm mediante un detector DAD.
2.5. Experimentos LC-ESI-MS
Los experimentos de LC-MS se llevaron a cabo utilizando un espectrómetro de masas con trampa de iones Finnigan LCQ DECA (Thermo Finnigan, San José, CA, EE. UU.) equipado con una fuente de ionización por electropulverización (ESI). Las muestras se analizaron en las mismas condiciones cromatográficas. Se utilizó un modelo negativo para la recolección de datos. Los caudales de gas envolvente y auxiliar se fijaron en 96 y 7 (unidad arbitraria), respectivamente. El voltaje del capilar se fijó en 29 V y su temperatura se controló a 350 grados. El voltaje de la lente de entrada se fijó en 40 V y la amplitud de RF multipolar se fijó en 540 V. El voltaje de la aguja ESI se controló en 4,5 kV. El desplazamiento de la lente del tubo fue de 16 V, el desplazamiento de la lente multipolar 1 fue de 8,20 V y el desplazamiento de la lente multipolar 2 fue de 10,5 V. El voltaje del multiplicador de electrones se fijó en 980 V para la detección de iones.
2.6. RMN para identificación
Los espectros de RMN se registraron en un espectrómetro Bruker Avance-600 (Bruker BioSpin Ltd., Milton, Canadá). Solo los compuestos 2 y 5 (sin estándares disponibles) se sometieron a experimentos de RMN. Las muestras se disolvieron en CD3OD.

3. Resultados y discusión
3.1. separación HSCCC
El extracto de n-butanol deCistanche deserticay las fracciones correspondientes a cada pico aislado por HSCCC se analizaron por HPLC, y los resultados se muestran en la Fig. 2. Se separaron y detectaron cinco compuestos principales (picos 1 a 5) con tiempos de retención de 9,2 min, 10,7 min, 12,3 min ,
13,3 min y 16,2 min, respectivamente.
Una separación exitosa de HSCCC depende en gran medida de un sistema de solvente de dos fases adecuado que proporcione un coeficiente de partición ideal (K) alrededor de 1 para el compuesto deseado. Dicho sistema bifásico también debería producir un tiempo de asentamiento razonablemente corto (Chen, Games y Jones, 2003; Foucault y Chevolot, 1998; Oka, Oka e Ito, 1991). En nuestro experimento, seleccionamos cuatro series de sistemas solventes de acuerdo con la solubilidad de los compuestos objetivo enCistanche desertica. Se usó HPLC para medir la concentración en cada fase, a partir de la cual se calcularon los valores de K de los compuestos objetivo. Dos sistemas, acetato de etilo-n-butanol-etanol-agua (4:0.6:0.6:5, v/v/v/v) y acetato de etilo-agua (1: 1, v/v), se han utilizado previamente en HSCCC para separaracteósidoy 20-acetillacteosido de C. salsa,acteósido, e isoactósido de P. Psyllium, respectivamente (Lei et al., 2001; Li et al., 2005). Aunque el primer sistema tuvo un tiempo de sedimentación relativamente corto, tuvo un rendimiento deficiente en la separación de las PhG deCistanche desertica, debido a los valores bajos de K para los compuestos 1 y 2, y los valores altos de K para los compuestos 3–5. Los valores de K fueron muy bajos para los compuestos 1–4 en el segundo sistema, pero muy altos para el compuesto 5 (Tabla 1). Un sistema modificado que contenía acetato de etilo-etanol-agua (5:{{10}}.5:4.5, v/v/v), dio un valor de K ideal para los compuestos 3–5 en 0.87, 1.11, y 1.32, respectivamente, y dieron como resultado una buena separación de estos tres compuestos (Fig. 3A y B). Este sistema, sin embargo, produjo
un valor de K demasiado pequeño para los compuestos 1 y 2, lo que hace que los dos compuestos coeluyan cerca del frente del disolvente (fracción 1 en la Fig. 3A). Una modificación adicional al sistema (acetato de etilo-n-butanol-etanol-agua (0.5:0.5:0.1:1, v/v/v/ v) elevó los valores de K para el compuesto 1 y 2 a 0.52 y 0.92, respectivamente, y condujo a una separación completa (Fig. 3C).La Fig. 3A muestra la separación HSCCC de un muestra que contiene 230 mg del extracto de n-butanol deCistanche deserticausando acetato de etilo-etanol-agua (5:0.5:4.5, v/v/v). Las fracciones que se confirmó por HPLC que contenían solo los compuestos 3, 4 o 5 se combinaron por separado, y las que contenían los compuestos 3 y 4 se agruparon, se liofilizaron y se volvieron a someter al HSCCC para una mayor separación (Fig. 3B). La separación de HSCCC en dos pasos descrita anteriormente produjo un total de 14,6 mg, 30,1 mg y 25,2 mg de los compuestos 3–5 a partir de 1412 mg de extracto de n-butanol. La Fig. 3C muestra la separación HSCCC de una muestra que contiene los compuestos 1 y 2 (fracción 1 en la primera separación) utilizando acetato de etilo-n-butanol-etanol-agua (0.5:0.5 :0.1:1, v/v/v/v). Se obtuvieron un total de 28,5 y 18,4 mg de los compuestos 1 y 2. Las purezas cromatográficas de los compuestos liofilizados 1–5 superaron el 92,5 % y se usaron directamente para análisis LC–ESI-MS y NMR.
3.2. Identificación estructural por LC-ESI-MS y NMR
La identificación tentativa de los compuestos 1, 3 y 4 se logró mediante tiempos de retención y datos espectrales UV congruentes con los del equinacósido auténtico.acteósido, e isoactósido (Fig. 2). Se desconocían los compuestos 2 y 5, sin embargo, los espectros UV de los cinco compuestos eran muy similares, lo que indica características estructurales similares.
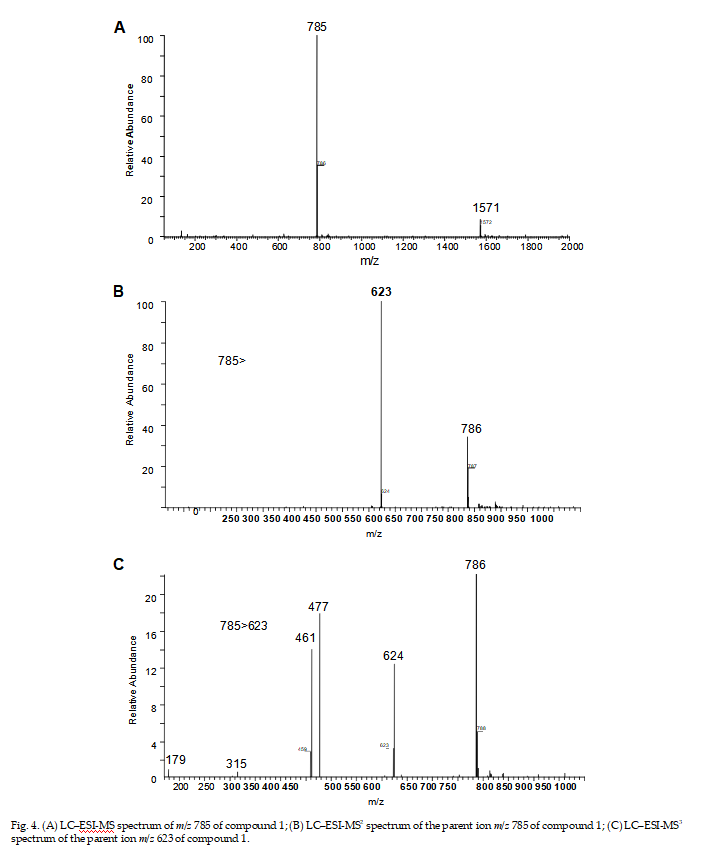
Para investigar más a fondo las estructuras de estos cinco compuestos, se intentaron experimentos LC-ESI-MSn y los resultados se muestran en la Fig. 4 y la Tabla 2. Los compuestos relacionados con los picos (1-5) en la Fig. 2 exhibieron iones moleculares desprotonados intensos. [MH]— en m/z 785, 799, 623, 623 y 665, respectivamente, en el modo negativo. También se observaron iones diméricos [2M H]— para los picos 1 a 4 en la Fig. 2. Estos confirmaron que los pesos moleculares de los picos 1 a 5 eran 786, 800, 624, 624 y 666, respectivamente. Los datos de LC-MSN (Tabla 2) proporcionaron información estructural muy útil para los cinco PhG, como la pérdida neutral de

Procedimiento experimental: se pesó aproximadamente 1 mg de cada muestra en un tubo de ensayo de 10 mL al que se agregó 1 mL de cada fase del sistema bifásico preequilibrado de disolventes. Se tapó el tubo de ensayo y se agitó vigorosamente durante 1 min, y se dejó reposar hasta que se separó por completo. Se tomó una alícuota de 100 l de cada capa y se evaporó por separado a sequedad al vacío a<40 °c.="" the="" residue="" was="" dissolved="" in="" 10="" ll="" methanol="" and="" analyzed="" by="" hplc="" for="" determining="" the="" partition="" coefficient="" (k)="" of="" compounds="" 1–5.="" the="" k="" value="" was="" expressed="" as="" the="" peak="" area="" of="" the="" target="" compound="" in="" the="" upper="" phase="" divided="" by="" that="" in="" the="" lower="">

el resto cafeoílo (162), el resto glucosa (162), el resto ramnosa (146), un radical CH2 (14) y el grupo COCH2 (42).
La LC-ESI-MS del pico 1 se muestra en la Fig. 4A. El ion molecular desprotonado [MH]— en m/z 785 con una alta abundancia y un ión molecular dimérico desprotonado

[2M H]— en m/z 1571 se observó en el modo negativo, lo que sugiere un peso molecular de 786, que era el mismo que el del equinacósido. La investigación adicional en el experimento LC-MS2 de los iones m/z 785 produjo un ion hijo principal en m/z 623 (Fig. 4B) producido directamente a partir de m/z 785 por pérdida de un resto cafeoílo o un resto hexosa como [M 162 H]—. El espectro LC-MS3 de m/z 623 exhibió dos iones principales en m/z 477 y 461, y dos iones menores en m/z 315 y 179 (Fig. 3C, Tabla 2). Las diferencias de masa entre m/z 623 y los iones del fragmento m/z 477 y 461 fueron 146 y 162, respectivamente, correspondientes a la pérdida de una unidad de ramnosa y una fracción de glucosa o una fracción de café [M 162 H]—. Los iones m/z 623 también perdieron un resto cafeoílo y un resto ramnosa para producir los iones m/z 315. El ion am/z 179 se produjo a partir de la escisión del resto cafeoílo, quedando la carga negativa en la parte del resto cafeoílo. El experimento LC-ESI-MSN en el echinacósido auténtico mostró el mismo patrón de fragmentación. Por lo tanto, se confirmó que el pico 1 era echinacósido.
Para el pico 2, la LC-ESI-MS mostró m/z 799 como el ion molecular desprotonado [MH] y m/z 1599 como su ion dimérico, lo que sugiere una masa molecular de 800. Durante los experimentos MS2, la m/z 799 iones formados tres hijas
iones en m/z 637, 623 y 475 (Tabla 1). El ion am/z 637 se produjo directamente a partir del ion original de m/z 799 nuevamente debido a la pérdida neutra del cafeoílo [M—162—H]—o un resto de glucosa [M—162—H]—. El ion am/z 623 resultó de la pérdida de un radical CH2. El ion am/z 475 se formó a partir de la pérdida neutra tanto del resto cafeoilo [M 162 H]- como del resto glucosa del ion original. El experimento MS3 en m/z 637 produjo tres iones en m/z 619, 491 y 475, correspondientes a las pérdidas de un agua, una unidad de ramnosa y un resto de glucosa, respectivamente. El ion hijo m/z 623 produjo m/z 461 y 315 en el estudio MS3, que siguió las mismas vías de fragmentación que el equinacósido, como se mencionó anteriormente. Los datos de LC–ESI-MSN apoyaron una identificación tentativa para el pico 2 comocistanósido A.
También se realizaron experimentos LC-ESI-MS para picos
3 y 4 (tR 12,49 y 13,46 min en la Fig. 2). Ambos picos mostraron el mismo ion [MH]— am/z 623 y dímero am/z 1247 en el modo negativo (Tabla 1), lo que indica que posiblemente son isómeros con el mismo peso molecular de
624, lo mismo queacteósidoe isoactósido. Los espectros de MS2 de los iones [MH]— también mostraron un mismo ión hijo de m/z 461, lo que indicaba la pérdida del resto cafeoílo del ión original m/z 623 (Tabla 1). Se obtuvieron espectros de MS3 similares para los dos compuestos. Para el pico 3, el espectro de MS3 del ion am/z 461 formó tres iones am/z 315, 161 y 135. El m/z 315 se forma después de perder la ramnosa como se discutió anteriormente. El ion m/z 161 se produjo a partir de la escisión del resto cafeoílo, seguido de una pérdida adicional de un agua; la carga permaneció por parte del resto cafeílo. El ion am/z 135 [aglicona 18 H]— surgió de la escisión del enlace glucosídico en la posición C1 con una pérdida adicional de agua, dejando la carga en la parte de la fracción aglicona. El espectro de MS3 del pico 4 siguió la misma ruta de fragmentación que el pico 3, excepto por el ion faltante am/z 135. El ion molecular y los patrones de fragmentación de estos dos compuestos son consistentes con los datos de la literatura sobreacteósidoe isoactósido (Wang et al., 2000), aunque se encontró un ion adicional m/z 153 y

asignado como [aglicona H]— por Wang et al. (Wang et al., 2000). Este ion puede haber sido inestable y haber perdido agua para dar m/z 135 en nuestro experimento. Según los datos de MS y los tiempos de retención congruentes de los picos 3 y 4 con los estándares, se identifican comoacteósidoe isoactósido, respectivamente.
Los datos de LC-ESI-MS del pico 5 se muestran en la Tabla 2. Un ion molecular desprotonado [MH]— (m/z 665) fue el único ion encontrado en el modo negativo, lo que implica una masa molecular de 666. Tres iones hijos se observaron en m/z 623, 503 y 461 en el experimento MS2 (Tabla 2). Los iones hijos am/z 623 y 503 se formaron directamente a partir del ion original por pérdida de un grupo COCH2 y un resto cafeoílo, respectivamente. El ion am/z 461 provino de la pérdida tanto del cafeoílo como del resto COCH2 [M 162 42 H] del ion original. En el experimento de MS, m/z 623 produjo m/z 461 y m/z 503 produjo tres iones en m/z 485, 461 y 315. El espectro de MS3 del ion hijo m/z 461 dio dos iones en 443 y 315. Al comparar el patrón de fragmentación LC-MSN del pico 5 con otros compuestos informados en este estudio y con otros informados (Li et al., 2005; Wang et al., 2000), concluimos que el pico 5 estaba estructuralmente muy relacionado a acteoside con la única diferencia de que la unidad COCH3 está en la posición R3. Por lo tanto, se dio una identidad tentativa al pico 5 como 20-acetilacteoside (Fig. 1).
Las estructuras de los dos compuestos identificados tentativamente, el pico 2 (como cistanosido A) y el pico 5 (como 20-acetil-acteosido) se confirmaron mediante 1H NMR. Los cambios químicos y las constantes de acoplamiento de todos los protones en los compuestos 2 y 5, como se muestra en la Tabla 3, coincidieron con los datos de RMN informados paracistanósido Ay 20-acetilacteoside, respectivamente (Kobayashi et al., 1984, 1987). Los experimentos de RMN 2D (correlación COSY, ROESY y CH de largo alcance) también se realizaron en el presente estudio y confirmaron aún más la identificación (datos no mostrados).

feniletanoideglucósidos en cistanche
4. Conclusiones
En el presente documento, HSCCC se utilizó con éxito para el aislamiento y purificación de echinacoside,cistanósido A, acteoside, isoacteoside y 20-acetylacteoside del extracto de n-butanol de C. deserticola. Por lo tanto, es un medio probado para la separación semipreparativa de bioactivos. Mientras tanto, las estructuras de los cinco PhG en Cistanche deserticola se han investigado mediante LC-ESI-MSN; se encontraron algunos rasgos característicos de las PhG, que nos permitieron determinar los grupos funcionales en las estructuras. Por lo tanto, el método LC-ESI-MSN es una poderosa herramienta para la identificación rápida defeniletanoidesy sus glucósidos enCistanche deserticaextractos, especialmente cuando se corroboran con datos de RMN.
Reconocimiento
Los autores desean agradecer a Jun Gu del Centro de Resonancia Magnética Nuclear de la Universidad de Guelph, Ontario, Canadá, por su ayuda en los experimentos de RMN. Este proyecto fue apoyado parcialmente por fondos de la Provincia de Jilin, China (No. 20060904).

Referencias
Chen, LJ, Juegos, DE y Jones, J. (2003). Aislamiento e identificación de cuatro constituyentes flavonoides de las semillas de Oroxylum Indicum por cromatografía a contracorriente de alta velocidad. Revista de cromatografía A, 988, 95–105.
Cheng, XY, Wei, T., Guo, B., Ni, W. y Liu, CZ (2005).Cistanche deserticacultivos en suspensión celular:Feniletanoidebiosíntesis de glucósidos y actividad antioxidante. Bioquímica de procesos, 40, 3119– 3124.
Foucault, AP y Chevolot, L. (1998). Cromatografía a contracorriente: instrumentación, selección de solventes y algunas aplicaciones recientes a la purificación de productos naturales. Revista de cromatografía A, 808, 3–22.
Gross, G.-A., Lahloub, MF, Anklin, C., Schulten, H.-R. y Sticher, O. (1988). Teucriósido, un glucósido fenilpropanoide de Teucrium Chamaedrys. Fitoquímica, 27, 1459–1463.
He, ZD, Lau, KM, Xu, HX, Li, PC y But, PPH (2000).
Actividad antioxidante defeniletanoideglucósidos de Brandisia chance. Diario de Etnofarmacología, 71, 483–486.
Kobayashi, H., Karasawa, H. y Miyase, T. (1984). Estudios sobre los constituyentes de Cistanchis Herba. tercero Aislamiento y estructuras de nuevos glicósidos fenilpropanoides,Cistanósido Ay B. Boletín químico y farmacéutico, 32, 3009–3014.
Kobayashi, H., Oguchi, H., Takizawa, N., Miyase, T., Ueno, A., Usmanghani, K., et al. (1987). Nuevofeniletanoideglucósidos deCistancheGancho tubulosa (Schrenk). Boletín químico y farmacéutico FI, 35, 3309–3314.
Lei, L., Yang, FQ, Zhang, TY, Tu, PF, Wu, LJ e Ito, Y. (2001).
Aislamiento preparativo y purificación deacteósidoy 2'-acetil acteósido de Cistanches salsa (CA Mey) G. Beck por cromatografía en contracorriente. Revista de cromatografía A, 912, 181–185.
Li, L., Tsao, R., Liu, ZQ, Liu, SY, Yang, R., Young, JC, et al. (2005). Aislamiento y purificación deacteósidoe isoactósido de Plantago psyllium L. por cromatografía en contracorriente de alta velocidad. Revista de cromatografía A, 1063, 161–169.
Li, LL, Wang, XW y Wang, XF (1997). Peroxidación antilipídica y acción antirradical de los glucósidos en herba Cistanches. China Journal of Chinese Materia Medica, 22, 364–367.
Li, J., Wang, PF, Zheng, RL, Liu, ZM y Jia, ZJ (1993). Protección de los glucósidos fenilpropanoides de Pedicularis contra la hemólisis oxidativa in vitro. Planta Médica, 59, 315–317.
Lu, MC (1998). Estudios sobre el efecto sedante deCistanche deserticaRevista de Etnofarmacología, 59, 161–165.
Nishimura, H., Sasaki, H., Inagaki, N., Chin, M. y Mitsuhashi, H. (1991). Nueve glucósidos de alcohol fenetílico de Stachys szeboldzz. Fitoquímica, 30, 965–969.
Oka, F., Oka, H. e Ito, Y. (1991). Una búsqueda sistemática de sistemas solventes bifásicos adecuados para la cromatografía en contracorriente de alta velocidad. Revista de cromatografía, 538, 99–108.
Ravn, H., Nishibe, S., Sasahara, M. y Li, X. (1990). Compuestos fenólicos de Plantago Asiatica. Fitoquímica, 29, 3627–3631.
Schapoval, EES, Winter de Vargas, MR, Chaves, CG, Bridi, R., Zuanazzi, JA y Henriques, AT (1998). Actividades antiinflamatorias y antinociceptivas de extractos y compuestos aislados de Stachytarpheta cayennensis. Diario de Etnofarmacología, 60, 53–59. Shoyama, Y., Matsumoto, M. y Nishioka, I. (1987). Glicósidos fenólicos de raíces enfermas de Rehmannia glutinosa Var. Purpúrea. Fitoquímica, 26, 983–986.
Wang, XW, Jiang, XY, Wu, LY y Wang, XF (2001). Efecto secuestrante de los glucósidos deCistanche deserticasobre los radicales libres y su protección contra el daño del ADN inducido por OH in vitro. Revista de Farmacología China, 36, 29–31.
Wang, YM, Zhang, SJ, Luo, GA, Hu, YN, Hu, JP, Liu, L., Zhu,
Y. y Wang, HJ (2000). Análisis defeniletanoideglucósidos en el extracto de hierbas Cistanchis por LC/ESI-MS/MS. Acta Pharmaceutica Sínica, 35, 839–842.
Wong, CC-C., Li, H.-B., Cheng, K.-W. y Chen, F. (2006). Un estudio sistemático de la actividad antioxidante de 30 plantas medicinales chinas utilizando el ensayo de poder antioxidante reductor férrico. Química de los alimentos, 97, 705–711. Xie, JH y Wu, CF (1993). Efecto del extracto etanólico deCistanche deserticasobre el contenido de neurotransmisores de monoamina en rata
cerebro. Drogas tradicionales y herbales chinas, 24, 417–419.
Xiong, Q., Hase, K., Tezuka, Y., Tani, T., Namba, T. y Kadota, S. (1998). Actividad hepatoprotectora defeniletanoidesdeCistanche desertica. Planta Médica, 64, 120–125.
Xiong, QB, Kadota, S., Tani, T. y Namba, T. (1996). Efectos antioxidantes de los feniletanoides deCistanche desertica. Boletín biológico y farmacéutico, 19, 1580–1585.
Zong, G., He, W., Wu, GL y Chen, LH (1996). Comparaciones entreCistanche deserticaYC Ma yCistanchetubular (Schenk) Wight en algunas actividades farmacológicas. Revista de Medicina Tradicional China, 21, 436–438.






