Efectos del extracto de Cistanche Tubulosa Wight en el síndrome de locomotora: un estudio controlado con placebo, aleatorizado, doble ciego
Mar 05, 2022
Yuna Inada, Chihiro Tohda * y Ximeng Yang
Sección de Ciencias Neuromédicas, Instituto de Medicina Natural, Universidad de Toyama, Toyama 930-0194, Japón; yuna@inm.u-toyama.ac.jp (YI.); ximeng@inm.u-toyama.ac.jp (X.Y)
* Correspondencia: chihiro@inm.u-toyama.ac.jp; Teléfono: +81-76-434-7646
Resumen: En una sociedad que envejece, la prevención de la disfunción y la restauración de la función de los órganos locomotores son necesarios para la calidad de vida a largo plazo. Pocos estudios de intervención han investigado la suplementación para el síndrome locomotor. Además, se han realizado muy pocos estudios clínicos de intervención sobre el síndrome locomotor como estudios controlados con placebo, aleatorizados y doble ciego. Anteriormente encontramos que la administración de extracto etanólico al 30% deCistanche tubulosamejora de la capacidad de caminar en un modelo de ratón con atrofia del músculo esquelético inmovilizado con yeso. Por lo tanto, se realizó un estudio clínico para evaluar los efectos deC. tubulosa(TC) extracto sobre el síndrome locomotor. Veintiséis sujetos con síndrome locomotor presintomático o leve completaron todas las pruebas y fueron analizados en el estudio. Los análisis de la masa muscular y la actividad física se realizaron en base al conjunto de análisis completo. La ingesta de extracto de TC durante 12 semanas aumentó el ancho de los pasos (prueba de dos pasos) y la velocidad de la marcha (prueba de caminata de 5 m) en pacientes mayores de 60 años en comparación con los de un control placebo (p = 0,046). Por el contrario, la masa muscular esquelética del tronco y las extremidades del cuerpo no se modificó después de la administración del extracto de TC. Los efectos adversos se evaluaron mediante análisis de sangre; no se observaron eventos adversos obvios después de la ingesta de extracto de TC. En conclusión, este estudio aleatorizado, doble ciego controlado con placebo demostró que el tratamiento con extracto de TC previno significativamente una disminución en la capacidad de caminar sin ningún efecto adverso notable en pacientes con el síndrome de la locomotora.
Palabras clave: síndrome locomotor;Cistanche tubulosa; capacidad para caminar; prueba de dos pasos; 5 m a pie
Para obtener más información, póngase en contacto con:Joanna.jia@wecistanche.com

Cistanche deserticola tiene muchos efectos, haga clic aquí para saber más
1. Introducción
En una sociedad que envejece, la prevención de la disfunción y la restauración de la función de los órganos locomotores son necesarias para la calidad de vida a largo plazo. El síndrome locomotor fue descrito por primera vez por la Asociación Ortopédica Japonesa (JOA) en 2007, y abarca una gama más amplia de discapacidades que los síntomas de discapacidad por deambulación musculoesquelética [1]. El sistema locomotor incluye músculos, articulaciones, cartílagos y huesos que se debilitan gradualmente con la edad o debido a otras enfermedades. Factores, como la falta de ejercicio, un estilo de vida sedentario y una nutrición inadecuada, también contribuyen a la progresión del síndrome locomotor. La prevención y la mejora del síndrome de la locomotora son necesarias para reducir la población que necesita atención. La mayoría de los estudios de intervención sobre el síndrome locomotor se han realizado para evaluar los efectos beneficiosos del ejercicio. Por ejemplo, el ejercicio durante 3 meses basado en el entrenamiento de locomotoras mejoró significativamente las pruebas de función física [2]. La longitud del paso, la longitud de la zancada y la velocidad de la caminata mejoraron en pacientes con síndrome locomotor después de 6 semanas de entrenamiento muscular flexor de cadera [3]. Sin embargo, la mayoría de los estudios de intervención sobre los efectos del ejercicio han comparado las respuestas antes y después del ejercicio en los mismos pacientes, sin la inclusión de un grupo de control. Además, pocos estudios de intervención han investigado la suplementación para el síndrome locomotor; la suplementación con vitamina D durante 24 semanas mejoró significativamente la fuerza de la extensión de la rodilla y la flexión de la cadera en comparación con los niveles previos al tratamiento [4]. Sin embargo, el estudio no incluyó un grupo placebo [4]. Hasta la fecha, se han realizado algunos ensayos clínicos de intervención sobre el síndrome locomotor como estudios controlados con placebo, aleatorizados y doble ciego [5].
Anteriormente, demostramos que la administración de extracto etanólico al 30% deCistanche tubulosamejoró la capacidad de caminar en un modelo de ratón con atrofia del músculo esquelético inmovilizado con yeso [6]. Aunque la administración oral del extracto no aumentó la masa muscular esquelética o el diámetro de la miofibra, la habilidad para caminar y la velocidad de la marcha mejoraron [6].Cistanchehierba se define en la Farmacopea Japonesa como tallos carnosos de Cistanche salsa G.Beck,C. deserticolaYC. Ma, oC. tubulosaWight. Acteoside (sinónimo: verbascoside), y echinacoside son reconocidos como los principales constituyentes activos de esta planta. Rico en acteoside y echinacosideC. deserticolaEl extracto ha demostrado actividad antifatiga en ratones [7]. El pretratamiento con acteosidos aumentó significativamente la contractilidad muscular en Bufo gastrocnemius, lo que indica un efecto anti-fatiga muscular de este compuesto [8]. En nuestro estudio anterior, el tratamiento con acteoside mejoró significativamente la función motora en ratones con lesiones de la médula espinal [9].Cistanchela hierba está clasificada como un agente no farmacéutico por la Oficina de Seguridad Farmacéutica y Alimentaria, Ministerio de Salud, Trabajo y Bienestar en Japón. La seguridad deC. tubulosaEl extracto (CT) en humanos se ha establecido en estudios clínicos de fase II y fase III realizados en China. Esos estudios no informaron efectos adversos a una dosis de 1800 mg de extracto por día durante 3 meses [10]. Por lo tanto, realizamos un estudio clínico para evaluar el efecto mejorador del extracto de TC sobre el síndrome locomotor en adultos humanos. Planteamos la hipótesis de que el extracto de TC podría proteger contra una disminución de la función motora.

echinacoside en cistanche puede estimular el sistema inmunológico
2. Materiales y métodos
2.1. Diseño del ensayo
Este fue un estudio doble ciego, aleatorizado y controlado con placebo en adultos sanos. Los sujetos solicitaron el estudio realizando su propio chequeo de locomotora después de ver un volante que los invitaba a participar en el estudio colocado en una instalación cercana. Después de aceptar participar en el estudio en la Universidad de Toyama, los sujetos se sometieron a pruebas de locomotoras en la línea de base. Los detalles del examen clínico de la locomotora se describirán más adelante. Luego, en la fase de intervención, los sujetos recibieron un medicamento aleatorizado (extracto de TC o placebo), y los sujetos un palo diario durante 12 semanas en casa. Después de la intervención de 12 semanas, los sujetos se sometieron nuevamente a pruebas de locomotoras.
1.2. Participantes
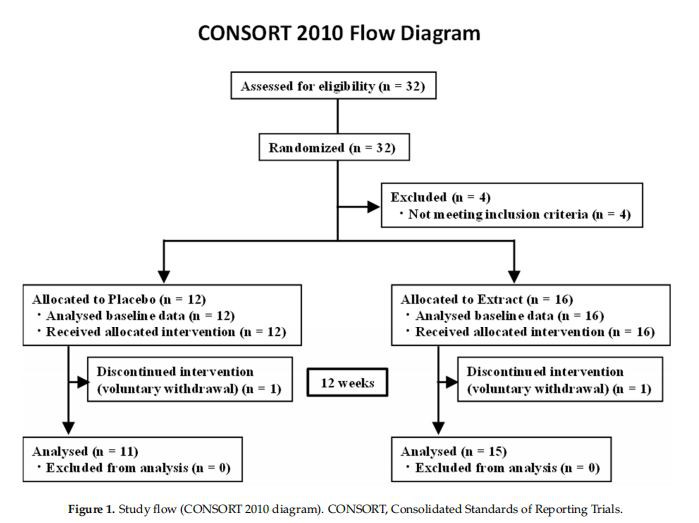
Se realizó el análisis de potencia previo. Calculado utilizando la prueba de rango firmado de pares emparejados de Wilcoxon con un tamaño de efecto de 0,5, un nivel de significancia de 0,05 y una potencia de 0,8, y luego el tamaño de muestra requerido fue 28. Treinta y dos sujetos fueron reclutados entre el 1 de diciembre de 2018 y el 31 de octubre de 2019. Los sujetos potenciales se asignaron en dos grupos; 28 cumplieron con los criterios de inclusión y se inscribieron. Dos sujetos se retiraron voluntariamente, por lo que 26 sujetos participaron en el estudio. Todos los sujetos visitaron la Universidad de Toyama dos veces para las evaluaciones. En la Figura 1 se muestra un diagrama de los Estándares Consolidados de Notificación de Ensayos (CONSORT) para el estudio. Los criterios de inclusión fueron los siguientes: sujetos (a) >40 años y<80 years;="" (b)="" able="" to="" complete="" this="" clinical="" study;="" and="" (c)="" checked="" at="" least="" one="" item="" on="" the="" “loco-check”="" questionnaire.="" the="" exclusion="" criteria="" were="" as="" follows:="" subjects="" (a)="" aged=""><39 years;="" (b)="" pregnant="" or="" lactating="" females;="" (c)="" on="" medication,="" such="" as="" muscle="" relaxants,="" osteoporosis,="" or="" rheumatoid="" arthritis="" drugs;="" (d)="" diagnosed="" with="" mental="" illnesses;="" or="" (e)="" judged="" ineligible="" for="" other="" reasons.="" subjects="" were="" followed="" up="" from="" 11="" may="" 2019="" to="" 29="" february="" 2020.="" this="" study="" was="" conducted="" with="" the="" approval="" of="" the="" ethics="" committee="" of="" the="" university="" of="" toyama="" (r2018090).="" each="" subject="" signed="" an="" informed="" consent="" form="" prior="" to="" study="">
2.3. Intervención
Se le dio un lugar o o C T a cada sujeto en un lugar de estudio el primer día del experimento. El extracto de CT fue preparado por Alps Pharmaceutical Ind. Co., Ltd. (Hida, Japón) de la siguiente manera:C. tubulosaLos tallos carnosos fueron recolectados de Shinjang Uyghur Aptonom Rayon, República Popular de China. Polvos mezclados (20 kg) deC. tubulosase sumergieron en etanol al 30%. La mezcla se refluyó durante 2 h a 55-64 °C. El rendimiento del extracto fue del 21,5% y contenía 5,41% de acteoside y 17,48% de equinacósido.
Evaluaciones de la seguridad en los otros lotes de extracto de CT (acteoside< 9.0%;="" echinacoside="">< 25.0%)="" were="" performed="" by="" oryza="" oil="" &="" fat="" chemical="" co.,="" ltd.="" the="" ct="" extract="" presented="" no="" acute="" toxicity="" in="" mice="" (ld50="">26.400 mg/kg), sin toxicidad crónica en ratas (a 1650 mg/kg después de 180 días de administración) y sin evidencia de mutagénesis genética. Las evaluaciones de seguridad clínica no revelaron efectos adversos durante la admiiaistración de 180 días a 1800 mg/sujeto/día [10].
Un palo contenía 1800 mg de extracto de TC, 72 mg de dióxido de silicio fino y 1782 mg de dextrina. Se tomó un palo, una vez al día, con gelatina de ayuda para tragar (Ryukakusan Co., Ltd., Tokio, Japón). El polvo de placebo contenía 48 mg de colorante cara mel, 72 mg de dióxido de silicio fino y 3480 mg de dextrina. Se tomó un palo una vez al día con gelatina de ayuda para tragar. Los polvos de mezcla y el embalaje fueron preparados por el fabricante (Sankyo Co., Ltd., Fuji, Japón) siguiendo los controles de Buenas Prácticas de Fabricación y la certificación ISO 22,000. La dosis de extracto de TC tomada cada día fue de 1800 mg.
2.4.Resultados y evaluaciones
Todos los participantes completaron un cuestionario sociodemográfico y de historia clínica básico e informaron cualquier medicamento utilizado al inicio del estudio. Los sujetos que verificaron al menos un elemento en el cuestionario Loco-check [11], que se indica a continuación, fueron reclutados y se consideró en riesgo del síndrome locomotor:
• No puede ponerse un par de calcetines mientras está de pie sobre una pierna.
• Tropiezas o resbalas en tu casa.
• Debe usar una barandilla al subir las escaleras.
• No se puede cruzar la carretera en un cruce antes de que cambie el semáforo.
• Tiene dificultad para caminar continuamente durante 15 minutos.
• Le resulta difícil caminar a casa con una bolsa de compras que pesa aproximadamente 2 kg.
• Le resulta difícil hacer las tareas domésticas que requieren fuerza física.
Las evaluaciones se realizaron en grupos de uno a diez participantes por día, dependiendo de la disponibilidad de los participantes. Todos los ítems se administraron en un día, y la participación fue de unos 30 min. El orden de las mediciones comenzó con la recolección de sangre, la medición de la altura y la medición de la fuerza de agarre, mientras que otros elementos se llevaron a cabo de forma individual y aleatoria. Durante la participación, a los sujetos se les permitió tomar un descanso cuando quisieran.
2.4.1. Medición de la masa muscular
La masa muscular de las extremidades superiores e inferiores y la masa muscular del tronco corporal se determinaron mediante análisis de impedancia bioeléctrica con un monitor de composición corporal (MC-780A, Tanita, Tokio, Japón).
2.4.2. Fuerza de agarre de la mano
La fuerza de la empuñadura se midió utilizando un dinamómetro de mano (T.K.K.5001, Takei, Niigata, Japón).
2.4.3. Velocidad de marcha de cinco metros
La "velocidad de caminata de cinco metros" mide el tiempo que pasa durante una sección de caminata de 5 m estableciendo secciones de aceleración de 1.0 m al comienzo de un total de 6 de longitud de caminata. Un punto de partida, 1,0 m, y puntos de llegada estaban marcados por líneas. Un recolector de fechas juzgó y midió el tiempo usando un cronómetro. Las mediciones se realizaron dos veces y se registró la velocidad de marcha más rápida, sin correr.
2.4.4. Prueba en dos pasos
La prueba de dos pasos evalúa la capacidad de caminar [12]. El sujeto parte de una postura de pie y se le pide que dé pasos hacia adelante con la máxima zancada sin perder el equilibrio. Se utilizó una estera específica con escamas para la prueba de dos pasos (JOA). La longitud de los dos pasos se midió de pies a cabeza. Antes de realizar la prueba, un instructor demostró el paso. La puntuación se calcula utilizando la longitud total de dos pasos (cm) dividida por la altura del sujeto (cm).
2.4.5. La prueba de pie
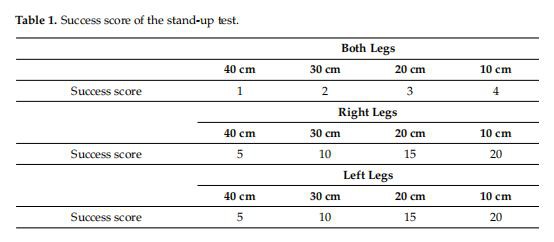
La prueba de pie se utiliza para medir la fuerza muscular de las extremidades inferiores. Evalúa la capacidad de un individuo para pararse usando ambas piernas, inicialmente, y luego en una pierna, desde una posición sentada en taburetes a alturas de 40, 30, 20 y 10 cm [13]. Los resultados se expresaron como puntuaciones sumadas, utilizando la Tabla de conversión 1.
2.4.6. GLFS-25
La Escala de Función Locomotora Geriátrica (GLFS-25) de 25 preguntas es un cuestionario autoevaluado utilizado para evaluar la función locomotora en individuos de edad avanzada [14]. Incluye 25 ítems con una puntuación de 0-4 para cada ítem: cuatro preguntas sobre el dolor, 16 preguntas sobre las actividades diarias, tres preguntas sobre la función social y dos preguntas sobre el estado de salud mental. La puntuación varía de 0 a 100, con puntuaciones más altas que indican una condición más pobre.
2.5. Evaluación de la seguridad
Las evaluaciones de seguridad incluyeron el registro de eventos adversos y análisis de sangre bioquímicos para evaluar la función hepática y renal, el azúcar en la sangre y los niveles de lípidos en cada visita.
2.6. Aleatorización
Los participantes fueron asignados al azar a uno de dos grupos: el grupo de extracto de TC o el grupo de placebo. La aleatorización se realizó mediante un método de aleatorización simple por un tercero que aseguró la lista de asignación de participantes y realizó una apertura de claves.
2.7. Análisis estadístico
Los resultados se expresaron como la media 土 desviación estándar (DE). Un intervalo de confianza (IC) del 95% denota el intervalo que es 95% seguro que contiene el verdadero valor de la población, ya que podría estimarse a partir de un estudio mucho más amplio. Los límites de IC del 95% se muestran en los rangos inferior y superior. Las comparaciones estadísticas se realizaron utilizando GraphPad Prism 6 (GraphPad Software, La Jolla, CA, USA) y SPSS (IBM, Chicago, IL, USA). Sobre la base de los resultados de las dos pruebas de normalidad (prueba de Kolmogorov-Smirnov y prueba de Shapiro-Wilk) y los valores de asimetría y curtosis, se decidió utilizar pruebas no paramétricas para todos los análisis estadísticos. Los datos se analizaron mediante la prueba de Mann-Whitney (para la comparación intergrupal), la prueba de rango firmado de pares emparejados de Wilcoxon (para la comparación intragrupal) o la prueba exacta de Fisher (para la comparación de varias personas). valores de p< 0.05="" were="" considered="">

cistanchetiene el efecto de antiinflamatorio
3. Resultados
3.1. Características basales de las Comisiones de Estudio
La población del estudio comprendió 32 hombres y mujeres. La Figura 1 presenta el diagrama de flujo CONSORT, la distribución de sujetos y los protocolos de estudio individuales. Treinta y dos sujetos fueron aleatorizados en dos grupos. Cuatro sujetos fueron excluidos porque no cumplían con los criterios de inclusión. Un grupo fue asignado para recibir un placebo durante 12 semanas, y el otro grupo fue asignado para recibir extracto de TC durante 12 semanas. Veintiséis sujetos completaron todas las pruebas y fueron incluidos en los análisis posteriores; las características basales se muestran en la Tabla 2. Las intervenciones se evaluaron en los sujetos con síndrome locomotor presintomático o leve. Los análisis de la masa muscular y la actividad física se realizaron en el conjunto de análisis completo. La edad de los sujetos en el grupo de extracto de TC fue significativamente mayor que la de los sujetos en el grupo de placebo. La altura, el peso corporal, el índice de masa corporal (IMC) inicial y las puntuaciones iniciales de Locomo 7 no fueron diferentes entre los grupos de placebo y extracto de TC (Tabla 2).

3.2. Masa muscular y actividades físicas
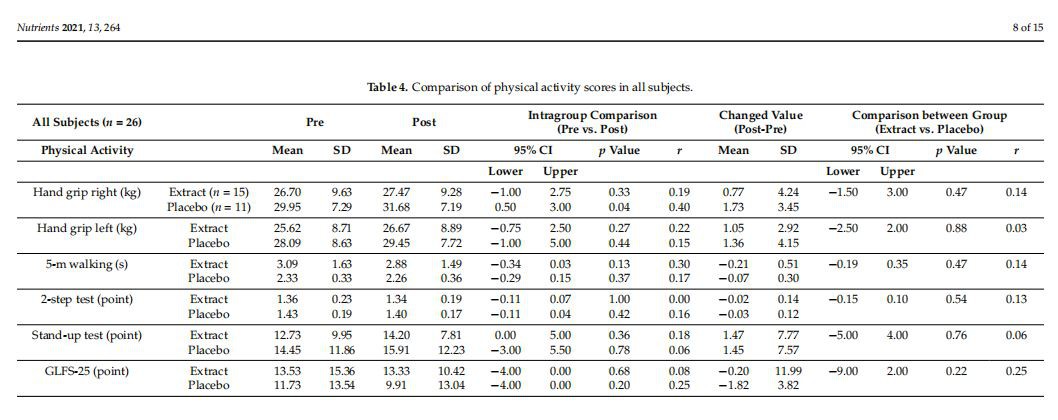
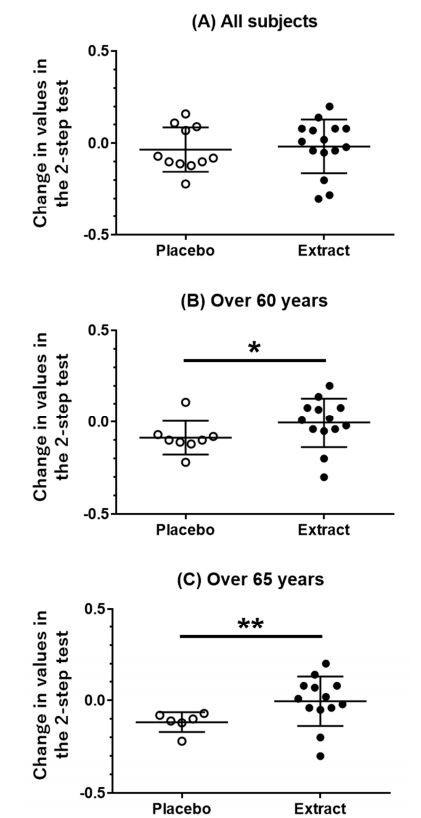
No hubo diferencias significativas en la masa muscular del tronco corporal, los brazos y las piernas, ni en el peso corporal entre los grupos de placebo y extracto de TC (Tabla 3). La comparación intragrupal antes y después del tratamiento con placebo o extracto de TC no reveló cambios significativos en ninguna de las variables anteriores (Tabla 3). Se evaluaron los puntajes de la empuñadura, la velocidad de caminata de 5 m, los puntajes de las pruebas de dos pasos y de pie, y el puntaje GLFS-25 para evaluar la actividad fisiológica. Las comparaciones intergrupales e intragrupales (Tabla 4, Figura 2A) no revelaron diferencias significativas en los resultados de ninguna prueba.
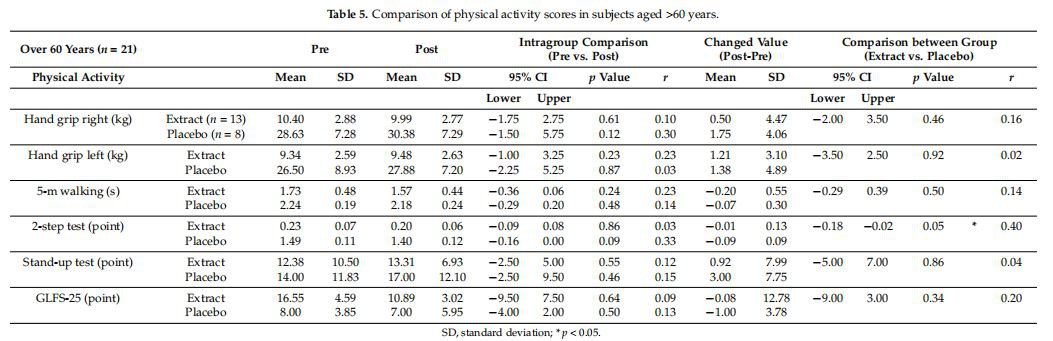
A continuación, se analizaron las actividades físicas por estratificación por edad (>60 o >65 años). La mejoría en la puntuación de la prueba de dos pasos en el grupo de extracto de TC fue significativamente mayor que en el grupo de placebo en sujetos de >60 años (Tabla 5, Figura 2B). Se observó un efecto positivo más evidente del extracto de TC en la puntuación de la prueba de dos pasos en sujetos de >65 años (Tabla 6, Figura 2C). Las comparaciones intragrupales indicaron que la puntuación de la prueba de dos pasos empeoró después del tratamiento en el grupo placebo, mientras que la del grupo de extracto de TC se mantuvo durante el período de prueba (Tabla 6). No se encontraron diferencias significativas en la masa muscular y el peso corporal, incluso cuando se estratificaron por edad.
Se comparó el número de sujetos de >60 años cuyas puntuaciones mejoraron tanto en la caminata de 5 m como en la prueba de dos pasos entre los grupos. La ingesta de extracto de TC mejoró significativamente las posibilidades de una respuesta positiva en los sujetos (Figura 3).
3.3. Seguridad
Treinta y un parámetros en sangre, así como los eventos adversos, se evaluaron después de la ingesta de extracto de TC y placebo. Los resultados de la evaluación de la seguridad se enumeran en la Tabla 7. Curiosamente, los niveles de iones de sodio leucina aminopeptidasa cambiaron significativamente entre los grupos de placebo y extracto de TC. Ningún otro parámetro difirió significativamente entre los grupos. Los datos de sodio bruto en el grupo placebo antes y después del tratamiento fueron de 140,8 y 142,0 mEq/L, respectivamente. Por el contrario, los datos de sodio bruto en el grupo de extracto de TC antes y después del tratamiento fueron de 141,7 y 141,7 mEq/L, respectivamente. Estos hallazgos indican que los niveles de iones de sodio no se vieron afectados por la ingesta de extracto de TC y que estuvieron dentro del rango normal en ambos grupos (más de 136 mEq / L). Los datos brutos de leucina aminopeptidasa en el grupo placebo antes y después del tratamiento fueron de 56,7 y 62,0 U/L, respectivamente. Por el contrario, los datos brutos de leucina aminopeptidasa en el grupo de extracto de TC antes y después del tratamiento fueron de 54,1 y 53,5 U/L, respectivamente. Estos valores indican que no hubo cambios en los niveles de leucina aminopeptidasa después de la ingesta de extracto de TC, y los niveles de leucina aminopeptidasa en ambos grupos estuvieron dentro del rango normal (37-81 U / L). En general, no se observaron efectos adversos después de la ingesta de extracto de TC.




4. Discusión
Este estudio es el primero en informar que una ingesta de 12 semanas de extracto de TC puede aumentar el ancho de los pasos (prueba de dos pasos) y la velocidad de la marcha (prueba de caminata de 5 m) en pacientes mayores de 60 años en comparación con el control con placebo. A pesar de que la edad del grupo de TC es mayor que la del grupo de placebo (Tabla 2), la ingesta de TC mejoró significativamente esas actividades físicas. Este resultado indica que el efecto del extracto de C T es probablemente confiable. En contraste, las masas musculares esqueléticas del tronco y las extremidades del cuerpo no cambiaron con la ingesta de extracto de TC. Utilizamos el mismo extracto de TC en un estudio previo en animales. La administración cisal del extracto de TC durante 13 días mejoró la capacidad de caminar en ratones con atrofia muscular inmovilizada con yeso, pero no aumentó la masa muscular esquelética [6]. Varios estudios en humanos han informado que la masa muscular y la calidad muscular, como la fuerza, no están necesariamente sincronizadas. Un gran estudio observacional, que incluyó a sujetos de 1880 años, mostró que la fuerza muscular disminuyó durante un seguimiento de 36 meses sin ninguna disminución en la masa muscular [15]. Otro estudio intervencionista controlado mostró que el entrenamiento de resistencia durante C meses aumentó significativamente la fuerza muscular de las extremidades inferiores; sin embargo, la masa muscular esquelética no cambió con la intervención [16].
Aunque el ancho del escalón en el grupo placebo disminuyó 12 semanas después en la Figura 2B, C, el ancho del paso en el grupo de extracto de TC se mantuvo. En otro estudio se observó una disminución natural en el ancho de los pasos durante unos pocos meses. Un estudio de adultos sanos (edad promedio: 57 años) indicó que el puntaje de la prueba de dos pasos disminuyó gradualmente dentro de las 8,12 y 16 semanas incluso en el grupo tratado con placebo [17]. Tomados en conjunto, los datos indican que el extracto de TC puede proteger contra la atenuación de la fuerza muscular. Se han investigado varias intervenciones en humanos para mejorar el rendimiento al caminar, incluidos los suplementos de vitamina D [4] y las proteínas de la leche, como la ricota [18], el suero de leche [19] y los aminoácidos [19-21]. Se demostró una mejora significativa en la velocidad de la marcha en un estudio [22], pero no en otros [4,18-21]. También en ratones, la suplementación con aminoácidos de cadena ramificada mejoró la actividad física [23]. Aunque se ha reportado un efecto positivo del ejercicio en el rendimiento de caminar, la mejoría aditiva con la suplementación con aminoácidos se evaluó negativamente [24]. Por lo tanto, el número de posibles candidatos a la suplementación que protegen contra el síndrome locomotor es limitado. Los resultados del presente estudio indicaron que el extracto de TC puede prevenir con seguridad una disminución en el rendimiento de la marcha, lo que sugiere que el extracto de TC podría ser un agente novedoso para el síndrome locomotor.
Con respecto al mecanismo subyacente al efecto del extracto de TC sobre la fuerza muscular, planteamos la hipótesis de que esto implica una mayor inervación axonal de las neuronas al músculo esquelético por acteoside, un componente activo en el extracto de TC. Previamente identificamos acteoside como el principal componente activo en el extracto de TC (datos no mostrados) y mostramos que puede activar la actividad de elongación axonal, lo que resulta en una regulación al alza de la función motora [9]. Sin embargo, el mecanismo molecular preciso que subyace al efecto del extracto de TC o acteoside sobre la fuerza muscular debe analizarse utilizando modelos animales apropiados en el futuro.
Cabe señalar varias limitaciones de esta investigación. Se inscribió una muestra de adultos asiáticos de 40 a 80 años; por lo tanto, nuestros resultados no pueden extenderse a otras poblaciones.
Además, no se evaluó la ingesta diaria de dieta ni el nivel de actividad física; por lo tanto, no está claro si estos afectaron los resultados del estudio. Se aconsejó a los participantes que no modificaran sus hábitos alimenticios o patrones de actividad durante la intervención. Finalmente, el estudio estuvo limitado por el pequeño tamaño de la muestra.

cistancheenlataranti-apopotosis
4. Conclusiones
En conclusión, este estudio doble ciego, aleatorizado y controlado con placebo reveló que el tratamiento con extracto de TC previno significativamente una disminución en la capacidad de caminar sin ningún efecto adverso. Sobre la base de la evidencia en este estudio, promoveremos el desarrollo del extracto de TC como alimento con declaraciones funcionales y medicina de venta libre en Japón.
Contribuciones del autor:C.T. diseñó todo el estudio; Y.I., C.T. y X.Y. realizaron investigaciones en humanos; Y.I. y C.T. analizaron datos; Y.I. y C.T. escribieron el artículo, y C.T. asume la responsabilidad principal del contenido final. Todos los autores han leído y aceptado la versión publicada del manuscrito.
Financiación:Este estudio fue apoyado por JSPS KAKENHI Grant (Número JP17H03558), fondos discrecionales del Presidente de la Universidad de Toyama, en 2017, 2018 y 2019, y 2020 Director de Gastos de Liderazgo, Instituto de Medicina Natural, Universidad de Toyama.
Declaración de la Junta de Revisión Institucional:El estudio se realizó según las directrices de la Declaración de Helsinki y fue aprobado por el Comité de Ética de la Universidad de Toyama (código de protocolo R2018090 y fecha de aprobación 2018.11.26).
Declaración de consentimiento informado:Se obtuvo el consentimiento informado de todos los sujetos involucrados en el estudio. Declaración de disponibilidad de datos: Los datos presentados en este estudio están disponibles a petición del autor correspondiente.
Reconocimientos:Agradecemos a Yoshiyuki Kimbara y Hidetoshi Watari por apoyar la recolección de muestras de sangre. Nuestro ensayo se registró en el Registro de Ensayos Clínicos de UMIN (ID: UMIN000036275).
Conflictos de intereses:Los autores declaran no tener conflicto de intereses. Los financiadores no tuvieron ningún papel en el diseño del estudio; en la recopilación, análisis o interpretación de datos; en la redacción del manuscrito, o en la decisión de publicar los resultados.
Referencias
1. Nakamura, K. Una sociedad "superenvejecida" y el "síndrome de la locomotora". J. Ortopédica. Sci. 2008,13,1-2.
2. Aoki, K.; Sakuma, M.; Ogisho, N.; Nakamura, K.; Chosa, E.; Endo, N. Los efectos del ejercicio domiciliario autodirigido con contactos telefónicos en serie sobre las funciones físicas y la calidad de vida en personas de edad avanzada con alto riesgo de disfunción locomotora. Acta. Med. Okayama 2015, 69, 245-253.
3. Sato, H.; Kondo, S.; Saito, M.; Saura, R. Efectos del fortalecimiento de los músculos flexores de la cadera en la capacidad de caminar y la prueba de rango del síndrome locomotor: un estudio de intervención. J. Ortopédica. Ciencia 2020,25, 892-896. [CrossRef] [PubMed]
4. Aoki, K.; Sakuma, M.; Endo, N. El impacto del ejercicio y la suplementación con vitamina D en la función física en personas mayores que viven en la comunidad: un ensayo aleatorizado. J. Ortopédica. Sci. 2018, 23, 682-687. [CrossRef] [PubMed]
5. Suzukamo, C.; Ishimaru, K.; Ochiai, R.; Osaki, N.; Kato, T. La membrana globular de grasa láctea más glucosamina mejora la función articular y el rendimiento físico: Un estudio aleatorizado, doble ciego, controlado con placebo y de grupos paralelos. J. Nutr. Sci. Vitaminol. 2019, 65, 242-250.
6. Kimbara, Y.; Shimada, Y.; Kuboyama, T.; Tohda, C. Cistanche tubulosa (Schenk) El extracto de Wight mejora el rendimiento de las extremidades posteriores y atenúa la expresión de IId/IIx de cadena pesada de miosina en ratones inmovilizados con yeso. Evid. Complemento basado. Alternar. Med. 2019, 2019, 9283171.
7. Cai, R.L.; Yang, M.H.; Shi, Y.; Chen, J.; Li, Y.C.; Qi, Y. Actividad antifatiga del extracto rico en feniletanoides de Cistanche deserticola. Phytother. 2010,24, 313-315.
8. Liao, F.; Zheng, R.L.; Gao, J.J.; Jia, ZJ. Retraso de la fatiga del músculo esquelético por los dos glucósidos fenilpropanoides: Verbascósido y martensita de Pedicularis plicata maxim. Phytother. 1999, 13, 621-623.
9. Kodani, A.; Kikuchi, T.; Tohda, C. Acteoside mejora la atrofia muscular y la función motora al inducir nueva secreción de miocina en la lesión crónica de la médula espinal. J. Neurotrauma 2019, 36, 1935-1948.
10. ACEITE DE ORYZA Y GRASA CHEMICAL CO., LTD. EXTRACTO DE CISTANCHE TUBULOSA. Catálogo Eléctrico ver. 2.0 JT. Disponible en línea: http://www.oryza.co.jP/pdf/japanese/cistanche%20tuburosa%20extract_j%202.0.pdf (consultado el 1 de octubre de 2020).
11. Nakamura, K. Guía sobre el síndrome de la locomotora; Bunkodo: Tokio, Japón, 2010.
12. Muranaga, S.; Hirano, K. Desarrollo de una forma conveniente de previsibilidad para caminar, utilizando una prueba de dos pasos. J. Showa Med. Assoc. 2003, 63, 301-303.
13. Ogata, T.; Morinaga, S.; Ishibashi, H.; Ohe, T.; Izumida, R.; Yoshimura, N.; Tsutomu Iwaya, T.; Nakamura, K. Desarrollo de un programa de detección para evaluar la función motora en la población adulta: un estudio observacional transversal. J. Ortopédica. Sci. 2015, 20, 888-895.
14. Seichi, A.; Hoshino, Y.; Doi, T.; Akai, M.; Tobimatsu, Y.; Iwaya, T. Desarrollo de una herramienta de detección del riesgo del síndrome locomotor en los ancianos: La escala de función locomotora geriátrica de 25 preguntas. J. Ortopédica. Ciencia 2012,17,163-172. [CrossRef] [PubMed]
15. Goodpaster, B.H.; Parque, S.W.; Harris, T.B.; Kritchevsky, S.B.; Nevitt, M.; Schwartz, A.V.; Simonsick, E.M.; Tylavsky, F.A.; Visser, M.; Newman, A.B. La pérdida de fuerza, masa y calidad del músculo esquelético en adultos mayores: El estudio de salud, envejecimiento y composición corporal. J. Gerontol. A Biol. Sci. Med. Sci. 2006, 61,1059-1064.
16. Strasser, E.M.; Hofmann, M.; Franzke, B.; Schober-Halper, B.; Olsen, S.; Jandrasits, W.; Graf, A.; Praschak, M.; Horvath-Mechtler, B.; Krammer, C.; et al. El entrenamiento de fuerza aumenta la calidad del músculo esquelético pero no la masa muscular en adultos mayores institucionalizados: un estudio de intervención aleatorizado, paralelo y controlado de múltiples brazos. Eur. J. Phys. Rehabil. Med. 2018, 54, 921-933.
17. Najima, M.; Shirakawa, T.; Ishii, I.; Okamoto, K. Un estudio para evaluar el efecto del suplemento que contiene glucosamina sobre el rendimiento articular y el rendimiento físico diario: Un estudio aleatorizado, doble ciego, controlado con placebo, evaluado principalmente por un cuestionario orientado a los sujetos. Jpn. Farmacol. Ther. 2017, 45, 939-955.
18. Alemán-Mateo, H.; Carreón, V.R.; Macías, L.; Astiazaran-García, H.; Gallegos-Aguilai; A.C.; Enriquez, J.R.R. Las proteínas lácteas ricas en nutrientes mejoran la masa muscular esquelética apendicular y el rendimiento físico, y atenúan la pérdida de fuerza muscular en hombres y mujeres mayores sujetos: un ensayo clínico aleatorizado simple ciego. Clin. Interv. Envejecimiento. 2014, 9,1517-1525.
19. Chanet, A.; Verlaan, S.; Salles, J.; Giraudet, C.; Patras, V.; Pidou, V.; Pouyet, C.; Hafnaoui, N.; Blot, A.; Cano, N.; et al. Complementar el desayuno con una bebida de nutrición médica de proteína de suero enriquecida con vitamina D y leucina mejora la síntesis de proteínas musculares postprandiales y la masa muscular en hombres mayores sanos. J. Nutr. 2017, 147, 2262-2271.
20. Ispoglou, T.; Blanco, H.; Preston, T.; McElhone, S.; McKenna, J.; Hind, K. Ensayo piloto doble ciego, controlado con placebo de mezclas de aminoácidos enriquecidos con L-leucina sobre la composición corporal y el rendimiento físico en hombres y mujeres de 65 a 75 años. Eur. J. Clin. Nutr. 2016, 70, 182-188.
21. Markovski, M.M.; Jennings, K.; Timmerman, K.L.; Dickinson, J.M.; Fry, C.S.; Borack, M.S.; Reidy, P.T.; Ciervo, R.R.; Randolph, A.; Rasmussen, B.B.; et al. Efecto del entrenamiento con ejercicios aeróbicos y la suplementación con aminoácidos esenciales durante 24 semanas sobre la función física, la composición corporal y el metabolismo muscular en adultos mayores sanos e independientes: un ensayo clínico aleatorizado. J. Gerontol. A Biol. Sci. Med. Sci. 2019, 74,1598-1604.
22. Scognamiglio, R.; Piccolotto, R.; Negus, C.; Tiengo, A.; Avogaro, A. Aminoácidos orales en sujetos de edad avanzada: Efecto sobre la función miocárdica y la capacidad de caminar. Gerontología. 2005, 51, 302-308.
23. Giuseppe, D.A.; Maurizio, R.; Annalisa, C.; Laura, T.; Marta, D.; Flavia, B.; Francesca, C.; Giovanni, C.; Roberto, B.; Michele, O.C.; et al. La suplementación con aminoácidos de cadena ramificada promueve la supervivencia y apoya la biogénesis mitocondrial cardíaca y del músculo esquelético en ratones de mediana edad. Celda Metab. 2010, 12, 362-372.
24. Kim, H.K.; Suzuki, T.; Saito, K.; Yoshida, H.; Kobayashi, H.; Kato, H.; Katayama, M. Efectos del ejercicio y la suplementación con aminoácidos en la composición corporal y la función física en mujeres sarcopénicas japonesas ancianas que viven en la comunidad: un ensayo controlado aleatorio. J. Am. Genial. Soc. 2012, 60, 16-23.






