Evaluación de las propiedades antioxidantes, blanqueadoras y antienvejecimiento de los hidrolizados de proteína de arroz
Mar 19, 2022
Contacto:joanna.jia@wecistanche.com/ WhatsApp: 008618081934791
Hui-Ju Chen 1,2, Fan-Jhen Dai 2, Cheng-You Chen 3, Siao-Ling Fan 2, Ji-Hong Zheng 4, Yu-Chun Huang 2, Chi-Fai Chau 1, Yung-Sheng Lin 3, 4,5,* y Chin-Shuh Chen 1,*
Resumen:Los hidrolizados de proteínas de origen vegetal tienen aplicaciones potenciales en nutrición. Los hidrolizados de proteína de arroz (RPH), una excelente fuente de proteínas, han llamado la atención para el desarrollo de cosmecéuticos. Sin embargo, pocos estudios han informado la aplicación potencial de RPH en el análisis, y este estudio examinó suantioxidanteactividades y las actividades inhibitorias de las enzimas del envejecimiento de la piel. Los resultados indicaron que las concentraciones totales de fenoles y flavonoides fueron de 2,06 ± 0,13 mg equivalentes de ácido gálico/g RPH y 25,96 ± 0,52 µg equivalentes de quercetina/g RPH, respectivamente. Los RPH demostraron una actividad dependiente de la dosis para eliminar los radicales libres de 1,1-difenil-2-picrilhidrazilo [la mitad de la concentración inhibitoria máxima (IC50)=42.58 ± 2,1 mg/g RPH] y 2 ,20-azino-bis (3-etilbenzotiazolina-6-ácido sulfónico) (IC50=2.11 ± 0,88 mg/g RPH), capacidad de reducción dependiente de la dosis (6,95 ± 1,40 mg de vitamina C equivalente/g RPH) y capacidad de absorción de radicales de oxígeno (473 µmol Trolox equivalente/g RPH). Las concentraciones de la solución de RPH requeridas para lograr una inhibición del 50 por ciento de hialuronidasa ytirosinasase determinó que las actividades eran 8,91 y 107,6 mg/ml, respectivamente. Este estudio demostró que los RPH tienenantioxidante, actividades antihialuronidasa y antitirosinasa para futuras aplicaciones cosméticas.
Palabras clave:hidrolizado de proteína de arroz;antioxidante; hialuronidasa;tirosinasa; cosmético

cistancheblanqueoefectoen la piel paraantioxidante
1. Introducción
La exposición a la radiación ultravioleta es responsable del fotoenvejecimiento (o envejecimiento extrínseco); por el contrario, las especies reactivas de oxígeno producidas en el metabolismo celular y el deterioro de las funciones biológicas son responsables del envejecimiento intrínseco [1,2]. Los alimentos procesados a menudo contienenantioxidantestales como catequinas, ácido ascórbico, tocoferoles, ácido rosmarínico y extractos fenólicos de varias plantas. La investigación realizada sobre antioxidantes naturales ahora considera procedencias no tradicionales. De origen naturalantioxidantesson más deseables que los producidos químicamenteantioxidantesya que se ha informado que algunos antioxidantes sintéticos son cancerígenos [3]. El arroz (Oryza sativa) es un alimento básico importante para las personas en todo el mundo, en particular las que viven en Asia. La producción anual de arroz en el mundo es de aproximadamente 741 millones de toneladas [4]. En los países asiáticos, se informa que el arroz es la fuente del 75 por ciento de la ingesta de energía de más de 2 mil millones de personas [5]. La producción extensiva de arroz da como resultado una cantidad correspondiente de producción de subproductos. El producto residual del proceso de producción de arroz contiene la mayor parte de la proteína del grano (~60–85 por ciento), pero se desecha o se usa para alimentar a los animales [6–8]. Los péptidos obtenidos de varios hidrolizados de proteínas supuestamente actúan como posiblesantioxidantes[9]. Por lo tanto, los antioxidantes naturales y no tóxicos pueden extraerse potencialmente de los hidrolizados de proteínas alimentarias. Numerosos académicos han empleado modelos ricos en lípidos y han informado que los hidrolizados de proteínas, así como la leche, la zeína y los péptidos de proteína de soya tienen características antioxidantes cruciales, que incluyen la eliminación de radicales libres, la inhibición de la peroxidación lipídica in vitro y de los alimentos, y la quelación de metales de transición [10– 12].
El ácido hialurónico (AH) ayuda a rejuvenecer la piel porque aumenta la viscosidad, contiene humedad y hace que los fluidos extracelulares sean menos permeables. Debido a su excelente capacidad de retención de agua, el AH aumenta la juventud, la hidratación y la tersura de la piel y reduce el grado de arrugas [13,14]. Desafortunadamente, el nivel de HA en la piel disminuye naturalmente con la edad. La hialuronidasa es una enzima que destruye el AH, lo que provoca la pérdida de fuerza, flexibilidad y humedad de la piel, lo que a su vez conduce al envejecimiento de la piel. Por lo tanto, las arrugas se pueden tratar inhibiendo la hialuronidasa y manteniendo el contenido de AH de la piel [15,16]. La enzima productora de melaninatirosinasacontribuye vitalmente al paso limitante de la velocidad del proceso a través del cual se produce la melanina. Por lo tanto, los trastornos de la pigmentación se tratan comúnmente y el brillo de la piel se logra al inhibir o regular a la bajatirosinasaactividad [17,18].
En varios estudios, se ha descubierto que los hidrolizados de proteínas de cereales y los péptidos que se pueden obtener de ellos tienen actividades antioxidantes, antihipertensivas y antitumorales [19,20]. Las contribuciones positivas a la salud humana de los péptidos y proteínas originarios de los alimentos se están reconociendo gradualmente [21]. Los consumidores demandan cada vez más que las industrias cosmética y de salud utilicen compuestos bioactivos naturales. Los hidrolizados de proteína de arroz (RPH) han llamado la atención como una excelente fuente de proteínas. Sin embargo, pocos estudios han informado sobre la caracterización y el análisis funcional de los RPH. Por lo tanto, este estudio evaluó la actividad antioxidante y la hialuronidasa ytirosinasa-Actividades inhibitorias de los RPH.
2. Resultados y Discusión
2.1. Concentración fenólica total (TPC) y contenido total de flavonoides (TFC)
El estándar en el ensayo TPC fue ácido gálico de varias concentraciones. Una absorbancia más alta indicó un TPC más alto. El TPC de las muestras de RPH se obtuvo ingresando los valores de absorbancia óptica de las muestras de RPH en la curva de calibración de ácido gálico. Al graficar la concentración de RPH contra la concentración fenólica (Figura 1a), se obtuvo un TPC promedio de 2.06 ± 0.13 mg GAE/g RPH. Se obtuvo una TFC de 25,96 ± 0,52 µg QE/gRPH siguiendo un procedimiento similar (Figura 1b). La Figura 1c relaciona además el TPC y el TFC de las muestras de RPH. Revela que la relación entre TPC y TFC se puede expresar como y=0.0121x más 0.0659, donde x e y son TPC y TFC, respectivamente.
El TPC de RPHs incluyó las concentraciones de aminoácidos fenólicos y compuestos fenólicos de los péptidos. La interacción proteína-compuesto fenólico generalmente involucra enlaces covalentes y no covalentes. Los compuestos fenólicos se liberan durante la hidrólisis enzimática. Las enzimas específicas pueden ser más capaces de destruir los complejos proteína-polifenol; esto da como resultado una mayor cantidad de compuestos fenólicos y péptidos con grupos fenólicos, como la tirosina, que se liberan [22]. Se ha informado una fuerte correlación entre el contenido total de polifenoles de los granos y su actividad biológica. Los polifenoles son bien conocidos por tener fuertes actividades antioxidantes [23]. Aunque se encuentran en menor cantidad, los terpenos [24] orsesquiterpenos [25] en el arroz también podrían contribuir a las actividades antioxidantes.
2.2. Actividad de los antioxidantes
2.2.1. Actividad de eliminación de radicales de los radicales libres DPPH
La figura 2 representa la actividad de captación de radicales libres de DPPH en la solución de RPH. Se descubrió que una mayor concentración de la solución daba como resultado una mayor actividad. La mitad de la concentración inhibitoria máxima (IC50), que es la concentración de extracto para la que se pueden eliminar la mitad de todos los radicales libres de DPPH, fue de 42,58 ± 2,1 mg/ml de péptidos de arroz.
2.2.2. Actividad de eliminación de radicales libres ABTS
La actividad de captación de radicales libres ABTS de RPH, ilustrada en la Figura 3, fue mayor cuando se empleó una mayor concentración de extracto. El IC50 fue de 2,11 ± 0,88 mg/mL de péptidos de arroz. Este resultado indicó que los RPH tenían una fuerte actividad de eliminación de radicales libres ABTS. Los aminoácidos que contienen azufre, incluidos Met y Cys, y los aminoácidos hidrofóbicos, incluidos Ala, Val, Ile, Leu, Met, Cys, Tyr, Phe, Try y Pro, podrían ser factores importantes con respecto al radical libre ABTS. actividad carroñera.
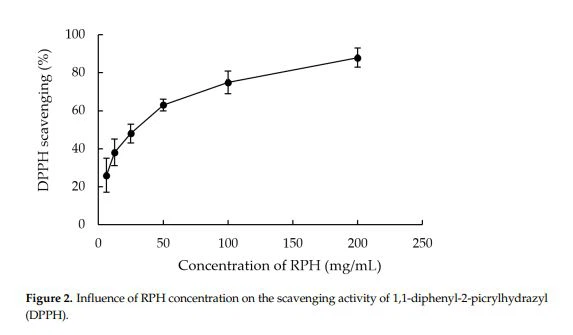
En este estudio, el valor IC50 de la actividad de eliminación de radicales libres de ABTS fue menor que la actividad de eliminación de radicales libres de DPPH, lo que concuerda con los resultados de la cáscara y el núcleo de la semilla de Jatropha curcas L. [28] y la pulpa de la cáscara y la semilla de la fruta de azufaifo [29]. Este hallazgo también corresponde al informe de hidrolizados de proteína de salvado de arroz con 43,98–66,25 µmol de Trolox equivalente/g de muestra y 403,28–430,12 µmol de Trolox equivalente/g de muestra para la actividad de eliminación de radicales libres de DPPH y la actividad de eliminación de radicales libres de ABTS, respectivamente [27].
Una posible razón es la diferencia en la solubilidad entre el radical libre DPPH (soluble en aceite) y el radical libre ABTS (soluble en aceite/agua) [30,31]. El potencial antioxidante de los hidrolizados de proteína de salvado de arroz estuvo influenciado por su perfil de peso molecular, composición de aminoácidos e hidrofobicidad [32].
2.2.3. Capacidad de reducción
Los hallazgos del ensayo de capacidad de reducción para RPH se presentan en la Figura 4. La capacidad de reducción aumentó con la concentración de RPH. La capacidad de reducción fue de 6,95 ± 1,40 mg VCE/g RPH, lo que indica que las RPH son un antioxidante eficaz.
2.2.4. Capacidad de absorción de radicales de oxígeno (ORAC)
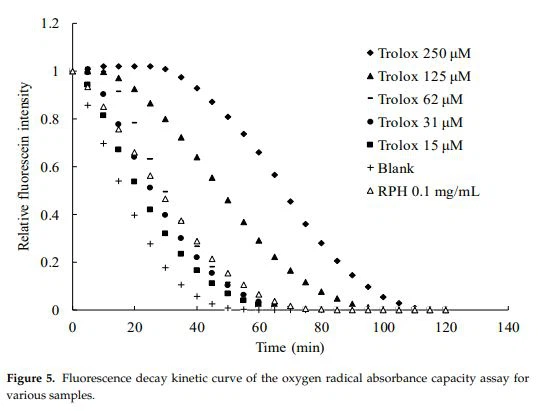
El ensayo ORAC tiene ventajas sobre otros enfoques para la determinación de la actividad antioxidante, incluidos los reactivos utilizados que son radicales peroxi con un mecanismo de reacción y un potencial redox similares a los oxidantes fisiológicos; la carga general y el estado de protonación con el queantioxidantesreaccionar se asemejan a los del cuerpo humano [33]. El método ORAC también tiene relevancia biológica para la eficacia de los antioxidantes en el cuerpo humano. La Figura 5 muestra los resultados del análisis ORAC de RPH y el estándar Trolox en varias concentraciones. El ORAC se derivó de la ecuación de regresión de la curva de calibración que relaciona el AUC neto con la concentración de Trolox. Los resultados indicaron que RPH tenía un ORAC de 473 µmol TE/g RPH.
Los péptidos o aminoácidos antioxidantes se pueden obtener por hidrólisis enzimática de proteínas, lo que resulta en una alta actividad contra los oxidantes [34]. La quelación de iones metálicos, la inhibición de la peroxidación de lípidos y la eliminación de radicales libres de péptidos biológicamente activos son responsables de su actividad antioxidante. Los radicales libres pueden apagarse y la expresión de proteínas y enzimas reductoras del estrés oxidativo puede regularse al alza mediante péptidos antioxidantes. Según se informa, la eficacia antioxidante de los hidrolizados de proteínas y los péptidos depende de la secuencia de aminoácidos y el tamaño del péptido, que se ven afectados por las condiciones de hidrólisis, la fuente de proteína y el tipo de proteasa [35]. Según Adebiyi et al. [36], la subtilisina puede dividir la proteína de salvado de arroz digerible más grande en pedazos más pequeños, lo que resulta en un mayor rendimiento y contenido de proteína. La actividad antioxidante y TPC de un hidrolizado puede verse afectada por la especificidad de las enzimas. Por lo tanto, la actividad antioxidante de un péptido podría estar influenciada por las características de la fuente de proteína, la especificidad de la enzima y el nivel de hidrólisis [37].
Hay muchos informes que utilizan proteasas (como Alcalasa, un nombre comercial de la subtilisina A de la especie Bacillus) para hidrolizar proteínas derivadas de plantas para obtener péptidos antioxidantes. En este sentido, la proteína de soya es una de las proteínas más reportadas [38]. Además, también se encuentra la hidrólisis de alcalasa de la proteína de salvado de arroz. En condiciones óptimas, la hidrólisis de alcalasa del salvado de arroz glutinoso produjo hidrolizados de proteínas con un valor IC50 de0.87 ± 0,02 mg/mL en la captación de radicales libres de DPPH [39]. En nuestro estudio, el valor de IC50 de RPHs fue de 42,58 ± 2,1 mg/mL. Aunque el valor de IC50 en la captación de radicales libres de DPPH en este estudio no fue tan eficaz como el de la proteína de salvado de arroz, la captación de radicales libres de ABTS (IC50=2.11 mg/mL) fue más eficaz que los hidrolizados de proteína de soja obtenidos por hidrólisis de Alcalase ( IC50=2.93 mg/mL) [40].
2.3. Actividad inhibidora de la hialuronidasa
Una enzima proteolítica, hialuronidasa, se encuentra en la dermis y cataliza la degradación de HA en la matriz extracelular [41]. Este estudio empleó ácido tánico como control positivo con fines de comparación. La Figura 6 revela que el ácido tánico tenía una mayor inhibición de la actividad hialuronidasa; el IC50 fue 0.14 mg/mL, valor similar al obtenido por Nishida et al. (0,121 mg/ml; 71,1 mM) [42]. Por el contrario, se calculó una IC50 de 8,91 mg/mL para la solución de RPH. Este resultado de la solución RPH correspondió a nuestro valor IC50 anterior, 7,61 mg/mL [43]. Las proteínas, los polisacáridos y los compuestos sintéticos y de origen vegetal se encuentran entre la gama de compuestos en los que están presentes los inhibidores de la hialuronidasa. Estos inhibidores ayudan a mantener el equilibrio entre la síntesis y la degradación de HA [44]. La baja concentración de HA en la piel produce sequedad y arrugas. Por lo tanto, la inhibición de la actividad hialuronidasa es una vía a través de la cual se puede mejorar la morfología de la piel y retrasar su envejecimiento.
2.4. Actividad inhibidora de la tirosinasa
Los hidrolizados de proteínas de fuentes naturales tienen el potencial de inhibiractividad de tirosinasa. La prueba de inhibición de la tirosinasa in vitro generalmente se usa para evaluar cómo los agentes blanqueadores de la piel afectan directamente la actividad de la tirosinasa [45]. Al participar en el paso limitante de la velocidad de síntesis de melanina, la tirosinasa cataliza la hidroxilación de L-tirosina en L-DOPA y luego la oxidación de esta última en o-dopaquinona. Cuando es deseable prevenir la biosíntesis de melanina, la inhibición de la actividad de la L-tirosinasa puede ser crucial. Aquí,tirosinasase usó para medir la actividad antitirosinasa RPH. Como se muestra en la Figura 7, la concentración107,6 mg/mL logró una inhibición del 50 por ciento de la actividad de tirosinasa. El ácido ascórbico exhibió una alta actividad inhibidora de la tirosinasa (IC50=0.098 mg/mL), que fue similar a los 0.102 mg/mL que Seo et al. reportado [46].
Los hidrolizados de proteína de salvado de arroz mostraron niveles significativamente altostirosinasa-actividad inhibidora [47,48]. La actividad inhibidora de la tirosinasa de la solución de RPH puede resultar de los perfiles de aminoácidos de los péptidos. Schurink et al. describió que efectivotirosinasaLos péptidos inhibidores consisten en residuos de arginina y fenilalanina [49]. La actividad inhibidora de la tirosinasa puede mejorarse mediante residuos de aminoácidos hidrófobos (p. ej., alanina) y la alanina puede interrumpir la producción de melanina [50]. Además, Zhang et al. también informaron que el hidrolizado de proteína de arroz podría reducir el contenido de melanina y la actividad de tirosinasa en el modelo celular inducido por UVB [51].

culturismo cistanche
2.5. Perfiles de aminoácidos y MW de RPH
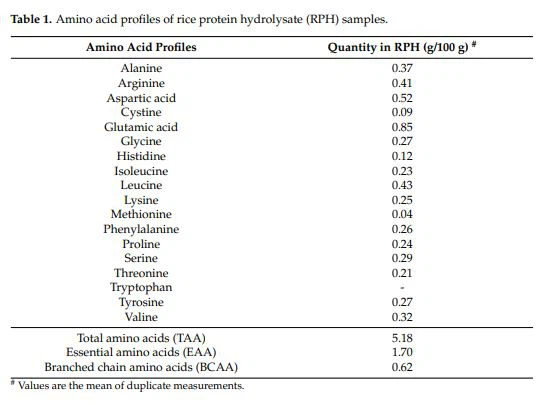
El contenido de proteína del arroz después de la eliminación del almidón en el presente estudio fue del 23,56 por ciento en peso, y el grado de hidrólisis de la muestra hidrolizada por proteasa fue del 9,36 por ciento. La Tabla 1 detalla la composición de aminoácidos en los RPH. En la muestra, cada 100 g contenía 5,18 g de aminoácidos. En cuanto a los componentes de aminoácidos, los RPH fueron ricos en alanina, leucina, arginina, ácido glutámico y ácido aspártico. Cada 100 g de la muestra contenían 1,73 g de aminoácidos hidrófobos (alanina, valina, leucina, isoleucina, prolina, fenilalanina y cisteína) en total. Este resultado fue completamente diferente de nuestro informe anterior [43] en la solución de amilasa y su temperatura de tratamiento para eliminar el almidón. El contenido de aminoácidos hidrófobos fue 1,90 veces mayor que nuestro informe anterior. La temperatura de tratamiento más baja (60 ◦C) en este estudio puede evitar la desnaturalización de las proteínas en grandes cantidades, por lo que se puede conservar mejor la actividad de los aminoácidos. Además, también se obtiene una conclusión similar a partir de otras amilasas y glucoamilasas fúngicas para sacarificar el almidón en el salvado de arroz blanco [52].
La investigación ha encontrado que los aminoácidos hidrofóbicos se asemejan aantioxidantesaumentando la solubilidad basada en lípidos en hidrolizados de proteínas y péptidos de diversas fuentes de proteínas, promoviendo así la interacción con los radicales libres [38,53]. Algunos aminoácidos fueron informados por Chen et al. [54] para ser generalmenteantioxidantes; los ácidos mencionados incluían triptófano, cisteína, metionina, tirosina e histidina. En el presente estudio, los aminoácidos aromáticos (fenilalanina, tirosina y triptófano) comprendían 0,53 g/100 g RPH. Por lo tanto, estos aminoácidos originadores de péptidos fueron probablemente los responsables de la actividad antioxidante de los RPH.
Además, las proteínas que se hidrolizan en péptidos más cortos tienen una distribución de PM diferente, y algunos grupos hidrófobos plegados en el interior de las moléculas de proteína natural completas suelen estar expuestos a la fase acuosa. Esto está relacionado con la reorganización estructural de las moléculas de proteína y, por lo tanto, con las propiedades funcionales de la proteína [55,56]. Los datos de tricine-SDS-PAGE indicaron que el MW de RPH estaba en el rango de 5 a 35 kDa (Figura 8a).
La Figura 8b representa el contenido relativo de varios MW en RPH. En general, el 45,24 por ciento de toda la proteína estaba en la banda principal (MW ≈ 2,4 kDa). Se obtuvieron resultados similares con respecto al péptido de los hidrolizados de proteína de salvado de arroz. La mayor actividad antioxidante obtenida por Thamnarathip et al. [37] fue el de los péptidos de PM=6–50 kDa. Además, existen relaciones entre la función de los hidrolizados de proteínas y la distribución de PM y la composición de aminoácidos [57]. Esto explica la actividad antioxidante de los RPH observada en el presente estudio.
2.6. Prueba de toxicidad celular
Se requiere una baja toxicidad celular para futuras aplicaciones. Para evaluar la citotoxicidad y la biocompatibilidad de las RPH, se midió la viabilidad celular de células 264.7 sin procesar en solución de RPH mediante el método MTT. Como se demuestra en la Figura 9, la viabilidad celular fue superior al 100 % cuando se trataron con 25–2000 µg/ml de RPH durante 24 h y 48 h. Los resultados indican la citotoxicidad notablemente baja de los RPH. Por lo tanto, los RPH pueden usarse potencialmente como aplicaciones cosméticas con una citotoxicidad muy baja.
3. Materiales y Métodos
3.1. reactivos
Cloruro de hierro(III), 2,20-azino-bis(3-etilbenzotiazolina-6-ácido sulfónico) (ABTS), Trolox(6-hidroxi-2,5 ,7,8-tetrametilcromano-2-ácido carboxílico), l-3,4-dihidroxifenilalanina (L-DOPA), 1,1-difenilo-2- el picrilhidrazilo (DPPH) y el ácido tricloroacético se adquirieron de Alfa Aesar (Tewksbury, MA, EE. UU.). 2,20-azobis(2-metilpropionamidina) diclorhidrato (AAPH), reactivo de fenol de Folin-Ciocalteu, ácido gálico, ácido ascórbico, hongotirosinasa, y la fluoresceína sódica se adquirieron de Sigma-Aldrich (St. Louis, MO, EE. UU.). El carbonato de sodio se obtuvo de Riedel-de Haën (Seelze, Alemania). Finalmente, se obtuvieron ferricianuro de potasio, hidrogenofosfato de sodio y dihidrogenofosfato de sodio de Showa Chemical (Tokio, Japón).
3.2. Preparación de RPH
Los RPH se prepararon como se describió anteriormente, excepto que se adoptó la amilasa fúngica para sacarificar el almidón en la harina de arroz, evitando el daño a los aminoácidos causado por la hidrólisis de la bacteriamilasa a altas temperaturas [43,58]. Cien gramos de harina de arroz se remojaron en 1000 mL de agua destilada que contenía 0,5 por ciento de amilasa fúngica (Genencor, NY, EE. UU.); la mezcla se calentó posteriormente durante 24 h a 60 ◦C ( pH 4,2), después de lo cual se dejó enfriar a temperatura ambiente. La centrifugación se realizó durante 10 min a 1968 × g para eliminar el sobrenadante restante. Después de añadir 20-veces de agua y 2 ml de proteasa hidrolítica al 0,1 por ciento (Healthmate, Changhua, Taiwán) a la porción insoluble, la solución se agitó y se incubó durante 4 horas a 55 °C. Se empleó el método pH-stat para mantener el pH de la solución en el nivel óptimo, y luego se realizó un calentamiento a 85 ◦C durante 10 min para la inactivación de la enzima. La fracción insoluble restante se eliminó mediante centrifugación durante 15 min a 3075 × g. Se realizó la liofilización del sobrenadante, que luego se almacenó a -20 ◦C antes de su uso.
3.3. Actividades antioxidantes de los RPH
3.3.1. Concentración fenólica total (TPC)
Se empleó el método de Folin-Ciocalteu para descubrir la TPC de los RPH [59]. En primer lugar, se mezclaron uniformemente 200 µL del reactivo de fenol de Folin-Ciocalteu (0,3 M) mediante agitación5-min con 200 µL de solución de RPH, ya esta mezcla se le añadieron 400 µL de agua desionizada (DI) y 200 µL de solución de carbonato de sodio al 10 por ciento (p/v). La solución mixta se sometió a 60 min de incubación en la oscuridad a temperatura ambiente. Luego se centrifugó por 15 min a 3000 rpm. La medición utilizó 100 µL de sobrenadante. Para determinar el TPC (unidad: mg) del equivalente de ácido gálico (GAE) por gramo de muestra RPH seca (unidad: mg GAE/g RPH), los datos de absorbancia óptica se ingresaron en una curva estándar que representa el ácido gálico. La absorbancia se obtuvo a 700 nm utilizando el espectrofotómetro EpochMicroplate (BioTek, VT, EE. UU.).
3.3.2. Contenido total de flavonoides (TFC)
El TFC se obtuvo siguiendo el enfoque de Wathoni et al. con modificaciones menores [60]. Primero, se mezclaron 500 µL de cada muestra y una solución de cloruro de aluminio al 2 por ciento (p/v). La solución de reacción se mezcló a fondo y se dejó durante 10 min, y se evaluó la absorbancia a 415 nm. El resultado se informa en microgramos de equivalente de quercetina (QE) por gramo de muestra RPH seca (µg QE/g RPH).

culturismo cistanche
3.3.3. Actividad de eliminación de radicales libres de DPPH
Primero, se mezclaron la solución de etanol DPPH 198 µM (50 µL) y la solución RPH o agua DI (0,5 µL; la muestra y el control, respectivamente) y luego se dejó reposar durante 30 min en la oscuridad a temperatura ambiente. Posteriormente se obtuvo la absorbancia de la solución a 517 nm. La actividad depuradora relativa se calculó determinando la diferencia de absorbancia entre la muestra y el control. La alta actividad eliminadora de radicales libres de DPPH se reflejó en una baja absorbancia óptica. En la evaluación de la actividad de eliminación de radicales libres de DPPH de la solución RPH, el estándar empleado fue la vitamina C [61–63].
3.3.4. Actividad de eliminación de radicales libres ABTS
El enfoque informado por Wu et al. se empleó para evaluar la actividad antioxidante de la solución RPH [64]. Primero, se hizo reaccionar una solución madre de ABTS 7 mM (250 µL) con persulfato de potasio 2,45 mM (250 µL) para producir el catión de radicales libres ABTS (ABTS• plus), y la mezcla se mantuvo durante 16 h a 4 ◦C en oscuridad antes de su empleo. Después del equilibrio en la oscuridad a temperatura ambiente, se empleó solución salina tamponada con fosfato 0,1 M (PBS; pH 7,4) para diluir la solución a 0,70 ± 0,02 de absorbancia a 734 nm. Luego, a 180 µL de solución ABTS diluida, se agregaron 20 µL de Trolox (control positivo) o la solución RPH (muestra). A continuación, la mezcla se sometió a 10 min de incubación a temperatura ambiente. Este estudio determinó la absorbancia óptica a 734 nm; una menor absorbancia correspondía a una mayor actividad de captación de radicales libres de ABTS. El estándar utilizado para evaluar la actividad eliminadora de radicales libres ABTS de RPHsolution fue el antioxidante Trolox.
3.3.5. Capacidad de reducción
Se empleó el ensayo de poder antioxidante reductor férrico para determinar la actividad antioxidante total de la solución RPH. Según lo informado por Lin et al. [29], la solución RPH (200 µL) se mezcló uniformemente con 1 por ciento (p/v) de K3Fe(CN)6 y tampón PBS 0,2 M (pH 6,6; 100 µL cada uno) .Durante 20 min se empleó un baño de agua a 50 ◦C para calentar la mezcla; después de retirar la mezcla del baño, se enfrió rápidamente durante 3 min. Posteriormente, se realizó una adición de ácido tricloroacético al 10 por ciento (p/v) (100 µL) y 10-min centrifugación a 3000 rpm. Esto fue seguido por la extracción del sobrenadante (400 µL) y su mezcla uniforme con O. 1 por ciento (p/v) de FeCl3 (100 µL) y agua DI (400 µL). El Fe4[Fe(CN)6]3 se obtuvo mediante la reacción10-min de esta mezcla en la oscuridad. Posteriormente, una mayor absorbancia óptica (medida a 700 nm) indicó una mayor capacidad de reducción. La vitamina C estándar se utilizó para determinar el contenido equivalente de vitamina C (VCE) por gramo de RPH.
3.3.6. Capacidad de absorción de radicales de oxígeno (ORAC)
Este estudio obtuvo el ORAC modificando un método previamente informado [65]. Después de la disolución de la muestra de RPH en agua destilada, la solución de RPH (50 µL) se mezcló con fluoresceína (10 µM) en una placa de microtitulación de 96-pocillos. La solución se sometió a una incubación de 15-min a 37 ◦C seguida de la adición de 50 µL de AAPH (500 mM). Cada 5 min y durante un total de 120 min, se registró la fluorescencia (λex y λem=485 y 528 nm, respectivamente). La capacidad antioxidante de los RPH se descubrió a partir de la cinética de decaimiento de la fluorescencia calculando el área bajo la curva (AUC ). Al calcular el RPH ORAC, el estándar fue Trolox de 15 a 250 µM. El ORAC se informa como micromoles de Trolox equivalente (TE) por gramo de muestra RPH seca (µmol TE/g RPH).
3.4. Actividad inhibidora de la hialuronidasa
La prueba de inhibición de la hialuronidasa se realizó utilizando una microplaca de {{0}}pocillos y un método previamente informado con ligeras modificaciones [40]. Se liberó N-acetilglucosamina al hacer reaccionar la hialuronidasa con el sustrato HA. En presencia de cualquier inhibidor, se redujo la liberación de N-acetilglucosamina, detectándose esta liberación obteniendo la absorbancia 600-nm. El HA se precipitó con una solución de albúmina ácida compuesta por tampón de acetato 0,1 M (pH 3,9) y albúmina de suero bovino (1 mg/ml). La solución de muestra y 5 mg/mL de hialuronidasa se incubaron 20-min a 37 ◦C. A la mezcla de incubación, se añadió posteriormente HA (1{{20}}0 µl; 5,0 mg/ml en tampón de acetato 0,1 M). Se realizó una incubación adicional a 37 ◦C durante 40 min. Se agregaron 0,1 ml de solución de borato alcalino 0,4 M para detener la reacción enzimática.
3.5. Actividad inhibidora de la tirosinasa
El presente estudio evaluó la actividad antitirosinasa de los RPH mediante el uso de un protocolo previamente informado con modificaciones [66]. Se preparó una solución enzimática (135 U/ml) disolviendo tirosinasa en tampón fosfato 20 mM (pH 6,8). Además, se empleó agua DI para la preparación de una solución de L-DOPA 1,25 mM. Luego, se mezclaron 40 µL de varias concentraciones de soluciones de muestra de RPH con 40 µL de solución de tirosinasa y 120 µL de solución de L-DOPA. Durante 30 min esta mezcla se mantuvo a 37 ◦C en el ensayo de inhibición de RPHstirosinasaactividad. Se empleó un espectrofotómetro (FLUOstar Omega MicroplateReader, BMG Labtech GmbH, Alemania) para obtener la absorbancia 475-nm. Todas las mediciones se realizaron tres veces. La absorbancia del grupo correspondiente cuandotirosinasano estaba presente se restó. La tasa de inhibición de la enzima se determinó como
3.6. Caracterización de RPH
3.6.1. Perfiles de aminoácidos
Este estudio descubrió la composición de aminoácidos de los RPH. En primer lugar, durante 24 hy a 115 ◦C, se empleó ácido metanosulfónico 4 M para hidrolizar las muestras en tubos sellados al vacío. Se emplearon dos sistemas de suministro de disolvente Waters 510 y un analizador de aminoácidos (L 8900; Hitachi, Tokio, Japón) para la separación de aminoácidos derivatizados en una columna Spherisorb ODS2 que mide 25 m × 64,6 mm. Este estudio empleó los siguientes solventes: (a) acetato de sodio (0.14 M) y trietilamina (850 µL/L; pH 5.6) y (b) 60 por ciento de acetonitrilo, para el cual el gradiente fue de 0 por ciento durante 2 min; 0–42 por ciento durante 15,5 min (curva convexa) y 100 por ciento durante 4 min. Se tomaron muestras por duplicado para medir los perfiles de aminoácidos a 254 nm [67,68].
3.6.2. Peso molecular (MW) de proteína
De acuerdo con el método de Schägger [69] y en condiciones reductoras, este estudio obtuvo la distribución de MW a través de electroforesis en gel de tricina-dodecilsulfato de sodio (SDS)-poliacrilamida (PAGE) con ligeras modificaciones. Un tampón de muestra (30 g/L SDS, 0.375 MTris-HCl, 0.125 g/L Coomassie Brilliant Blue G-250 y 75 g/ Se empleó L glicerol; pH 7) para dispersar la muestra liofilizada, realizándose entonces la centrifugación antes de la carga. Se añadió un total de 20 µl de 2-mercaptoetanol a 1 ml de la muestra de tricina-SDS-PAGE. La muestra se calentó a 100 ◦C durante 90 s. Se cargó un pocillo de muestra con cada muestra y el estándar de proteína sin teñir de amplio rango (Bio-Rad Laboratories, Alemania) utilizando una microjeringa. A continuación, se realizó la electroforesis, primero a 30 mV constantes hasta que la muestra completa quedó contenida dentro del gel de apilamiento y después hasta completarla a 100 mV constantes. Posteriormente, se aplicó una solución de Coomassie Brilliant Blue R-250 al 0,02 por ciento para la tinción del gel. Se realizó una decoloración de fondo absoluta de los geles agitando los geles en ácido acético al 10 por ciento durante la noche. Finalmente, se analizó la imagen del gel para identificar las bandas de proteína en los carriles; este análisis se realizó en ImageJ (Institutos Nacionales de Salud de EE. UU., Bethesda, MD, EE. UU.). Se emplearon marcadores estándar para obtener una curva de calibración a partir de la cual se estimó el PM. Brevemente, el primer paso fue determinar la longitud de migración (Rf) de cada banda desde la parte superior del gel de separación. El segundo paso fue el cálculo de la curva de calibración empleando Rf y log (MW) para un marcador estándar con un PM dado. La determinación del PM se realizó utilizando el Rf de las bandas de proteínas en los RPH.
3.7. Ensayo de citotoxicidad
Las células 264.7 sin procesar se cultivaron en medio Eagle modificado de Dulbecco (DMEM) con alto contenido de glucosa que contenía 10 por ciento de suero bovino fetal (FBS), 4,5 g/l de glucosa, solución antibiótica al 1 por ciento (100 unidades/ mL de penicilina y 100 µg/mL de Estreptomicina), L-Glutamina 4 mM y 1,5 g/L de bicarbonato de sodio a 37 ◦C y 5 por ciento de CO2. La toxicidad celular de células crudas 264.7 para RPH se midió mediante un método de ensayo de proliferación de 3-(4,5-dimetiltiazol-2-il)-2,5 bromuro de difeniltetrazolio (MTT) . Aproximadamente 1 × 104 células por pocillo se sembraron en 96-placas de pocillos. Después de 24 h, se añadieron a las células diversas concentraciones de RPH (0–2000 µg/ml). Después de 24 y 48 h de incubación, se añadieron 100 µL de solución de MTT (0,5 mg/mL). Se observaron cristales de formazan azul cuando se comprobaron bajo un microscopio. Se eliminó el DMEM y se añadieron 100 µl de dimetilsulfóxido (DMSO) por pocillo. La absorbancia se midió usando un lector de placas de microtitulación. Luego se calculó la viabilidad celular (porcentaje) como [A570 (células tratadas) - A570 (fondo)] / [A570 (células no tratadas) - A570 (fondo)] × 100 por ciento [70].
3.8. Análisis estadístico
El informe para cada muestra de hidrolizado fue el valor promedio de tres experimentos y determinaciones independientes repetidos. Los resultados expresados en media ± desviación estándar (SD) se analizaron mediante ANOVA unidireccional y la prueba post hoc de Duncan utilizando el StatisticalAnalysis System (versión 20.0; SPSS, Armonk, NY, EE. UU.). Se consideraron significativos valores de p <>
4. Conclusiones
Este estudio examinó las funciones de los RPH. Los resultados experimentales revelaron que los RPH contenían compuestos fenólicos y flavonoides y exhibieron una variedad de actividades antioxidantes, como actividades de eliminación de DPPH y ABTS, capacidad de reducción y ORAC. Además, los RPH inhibieron eficazmentetirosinasay actividades de hialuronidasa. La proteasa fue un factor crítico que afectó los patrones de PM de las RPH. El análisis de los RPH indica su potencial para su uso como ingrediente en cosméticos.

culturismo cistanche
Referencias
1. Ichihashi, M.; Ando, H.; Yoshida, M.; Niki, Y.; Matsui, M. Fotoenvejecimiento de la piel. Medicina antienvejecimiento. 2009, 6, 46–59. [Referencia cruzada]
2. Kim, J.-S.; Kim, D.; Kim, H.-J.; Jang, A. Efecto protector de los hidrolizados de gelatina de piel de burro sobre el fotoenvejecimiento inducido por UVB de los fibroblastos de piel humana. Proceso. Bioquímica 2018, 67, 118–126. [Referencia cruzada]
3. Carocho, M.; Ferreira, IC Una revisión sobre antioxidantes, prooxidantes y controversia relacionada: compuestos naturales y sintéticos, metodologías de detección y análisis y perspectivas futuras. Química alimentaria Toxicol. 2013, 51, 15–25. [Referencia cruzada]
4. Guo, X.; Zhang, J.; Mayo.; Tian, S. Optimización de la hidrólisis limitada de proteínas en residuos de arroz y caracterización de las propiedades funcionales de los productos. J. Proceso de alimentos. Preservar 2013, 37, 245–253. [Referencia cruzada]
5. Parque, H.-Y.; Lee, K.-W.; Choi, H.-D. Componentes del salvado de arroz: actividades inmunomoduladoras y terapéuticas. Función de alimentos. 2017, 8935–943. [Referencia cruzada] [PubMed]
6. Zhou, K.; Canning, C.; Sun, S. Efectos de los hidrolizados de proteína de arroz preparados por proteasas microbianas y ultrafiltración sobre los radicales libres y la oxidación de los lípidos de la carne. LWT 2013, 50, 331–335. [Referencia cruzada]
7. Piú', LD; Tassoni, A.; Serrazanetti, DI; Ferri, M.; Babini, E.; Tagliazucchi, D.; Gianotti, A. Explotación de subproductos líquidos de la industria del almidón para producir péptidos bioactivos a partir de proteínas hidrolizadas de arroz. Química alimentaria 2014, 155, 199–206. [Referencia cruzada]
8. Ferri, M.; Graen-Heedfeld, J.; Bretz, K.; Guillon, F.; Michelini, E.; Calabretta, MM; Lamborghini, M.; Gruarín, N.; Roda, A.; Kraft, A.; et al. Fracciones peptídicas obtenidas a partir de subproductos de arroz mediante un proceso respetuoso con el medio ambiente muestran bioactividades relacionadas con la salud in vitro. PLOS UNO 2017, 12, e0170954. [Referencia cruzada]
9. Wen, C.; Zhang, J.; Zhang, H.; Duan, Y.; Ma, H. Péptidos antioxidantes derivados de proteínas vegetales: aislamiento, identificación, mecanismo de acción y aplicación en sistemas alimentarios: una revisión. Tendencias Ciencias de la alimentación. Tecnología 2020, 105, 308–322. [Referencia cruzada]
10. Phelan, M.; Aherne, A.; FitzGerald, RJ; O'Brien, NM Péptidos bioactivos derivados de caseína: efectos biológicos, usos industriales, aspectos de seguridad y estado regulatorio. En t. Lechería J. 2009, 19, 643–654. [Referencia cruzada]
11. Udenigwe, CC; Aluko, RE Péptidos bioactivos derivados de proteínas alimentarias: producción, procesamiento y posibles beneficios para la salud. J. Food Sci. 2012, 77, 11–24. [Referencia cruzada] [PubMed]
12. Fardet, A.; Rock, E. Potencial antioxidante in vitro e in vivo de leches, yogures, leches fermentadas y quesos: una revisión narrativa de la evidencia. Nutrición Res. Rev. 2018, 31, 52–70. [Referencia cruzada]
13. Leach, JB; Katryn, AB; Charles, WPJ; Christine, ES Hidrogeles de ácido hialurónico fotorreticulados: andamios de ingeniería de tejidos biodegradables y naturales. Biotecnología. Bioing. 2003, 82, 578–589. [Referencia cruzada]
14. Jegasothy, SM; Zabolotniaia, V.; Bielfeldt, S. Eficacia de un nuevo ácido nanohialurónico tópico en humanos. J. Clin. Aesthet.Dermatol. 2014, 7, 27–29.
15. Ndlovu, G.; Fouché, G.; Tselanyan, M.; Cordier, W.; Steenkamp, V. Determinación in vitro del potencial antienvejecimiento de cuatro plantas medicinales del sur de África. Complemento BMC. Alterno Medicina. 2013, 13, 304. [Referencia cruzada]
16. Jiratchayamaethasakul, C.; Ding, Y.; Hwang, O.; Im, S.-T.; Jang, Y.; Myung, S.-O.; Lee, JM; Kim, H.-S.; Ko, SC-C.; Lee, S.-H.Evaluación in vitro de las actividades inhibidoras y antioxidantes de elastasa, colagenasa, hialuronidasa y tirosinasa de 22 extractos de plantas halófitas para nuevos cosmecéuticos. Pez. agua ciencia 2020, 23, 1–9. [Referencia cruzada]
17. Kang, M.; Park, S.-H.; Oh, SO; Lee, SE; Yoo, JA; Nho, YH; Lee, S.; Han, BS; Cho, JY; Lee, J. Los efectos antimelanogénicos del resorcinol están mediados por la supresión de la señalización de cAMP y la activación de la señalización de p38 MAPK. Biosci. Biotecnología. Biochem.2018, 82, 1188–1196. [Referencia cruzada]
18. Chatatikun, M.; Yamauchi, T.; Yamasaki, K.; Aiba, S.; Chiabchalard, A. Efecto antimelanogénico de las hojas de Croton roxburghii y Crotonsublyratus en células B16F10 estimuladas con -MSH. J. Tradición. Complementar. Medicina. 2019, 9, 66–72. [Referencia cruzada] [PubMed]
19. Rizzello, CG; Nionelli, L.; Coda, R.; Gobbetti, M. Síntesis del péptido preventivo del cáncer lunasina por bacterias de ácido láctico durante la fermentación de masa fermentada. Nutrición Cáncer 2012, 64, 111–120. [Referencia cruzada] [PubMed]
20. Rizzello, CG; Tagliazucchi, D.; Babini, E.; Rutella, GS; Saa, DLT; Gianotti, A. Péptidos bioactivos de matrices alimentarias vegetales: Tendencias de investigación y nuevas biotecnologías para síntesis y recuperación. Función J. Alimentos 2016, 27, 549–569. [Referencia cruzada]
21. Coscuetá, ER; Campos, DA; Osorio, H.; Nerli, BB; Pintado, M. Hidrólisis enzimática de proteína de soja: una herramienta para la producción de ingredientes alimentarios biofuncionales. Química alimentaria X 2019, 1, 100006. [Referencia cruzada]
22. Aydemir, LY; Yemenicioglu, A. ¿Los antioxidantes fenólicos unidos a proteínas en las legumbres no se ven como parte del iceberg? J. Planta. Biochem.Physiol. 2013, 1, 1–3. [Referencia cruzada]
23. Huang, SH; Ng, LT Cuantificación del contenido polifenólico y constituyentes bioactivos de algunas variedades comerciales de arroz en Taiwán. J. Alimentos Compos. Anal. 2012, 26, 122–127. [Referencia cruzada]
24. Yoshitomi, K.; Taniguchi, S.; Tanaka, K.; Uji, Y.; Akimitsu, K.; Gomi, K. La terpeno sintasa de arroz 24 (OsTPS24) codifica una monoterpeno sintasa sensible al jasmonato que produce un terpineno antibacteriano contra el patógeno del arroz. J. Planta. Fisiol. 2016, 191,120–126. [Referencia cruzada]
25. Kamolsukyeunyong, W.; Sukhaket, W.; Pitija, K.; Thorngkham, P.; Mahatheeranont, S.; Toojinda, T.; Vanavichit, A. Rice El sesquiterpeno juega un papel importante en la antixenosis contra el saltahojas marrón en el arroz. Plantas 2021, 10, 1049. [CrossRef][PubMed]
26. Liu, Y.; Wang, Z.; Li, H.; Liang, M.; Yang, L. Actividad antioxidante in vitro de la proteína de arroz afectada por el grado alcalino y la digestión con proteasa gastrointestinal. J. Ciencia. Alimentación Agrícola. 2016, 96, 4940–4950. [Referencia cruzada] [PubMed]
27. Phongthai, S.; D'Amico, S.; Schoenlechner, R.; Homthawornchoo, W.; Rawdkuen, S. Fraccionamiento y propiedades antioxidantes de hidrolizados de proteína de salvado de arroz estimulados por digestión gastrointestinal in vitro. Química alimentaria 2018, 240, 156–164. [Referencia cruzada][PubMed]
28. Huang, S.-L.; Wang, W.-H.; Zhong, X.-Y.; Lin, C.-T.; Lin, W.-S.; Chang, M.-Y.; Lin, Y.-S. Propiedades antioxidantes de Jatropha curcas L.Extractos de cáscara y grano de semilla. aplicación ciencia 2020, 10, 3279. [Referencia cruzada]
29. Lin, Y.-S.; Lin, W.-S.; Tung, J.-W.; Cheng, Y.-C.; Chang, M.-Y.; Chen, C.-Y.; Huang, S.-L. Capacidades antioxidantes de semillas de azufaifo y pulpa de cáscara. aplicación ciencia 2020, 10, 6007. [Referencia cruzada]
30. Shahi, Z.; Sayyed-Alangi, SZ; Najafian, L. Efectos del tipo de enzima y tiempo de proceso en el grado de hidrólisis, bandas de electroforesis y propiedades antioxidantes de proteínas hidrolizadas derivadas de Bunium persicum desgrasado Bioss. pastel de prensa. Heliyon 2020, 6,e03365. [Referencia cruzada] [PubMed]
31. Xie, H.; Huang, J.; Guau, MW; Hu, J.; Xiong, H.; Zhao, Q. Efecto de la desactivación de enzimas en frío y en caliente sobre las propiedades estructurales y funcionales de los hidrolizados de proteína de heces de arroz. Química alimentaria 2021, 345, 128784. [Referencia cruzada]
32. Rani, S.; Pooja, K.; Pal, GK Exploración de hidrolizados y péptidos de proteína de arroz con especial referencia al potencial antioxidante: enfoques derivados computacionales para la determinación de bioactividad. Tendencias Ciencias de la alimentación. Tecnología 2018, 80, 61–70. [Referencia cruzada]
33. Bisby, RH; Brooke, R.; Navaratnam, S. Efecto del potencial de oxidación antioxidante en el ensayo de capacidad de absorción de radicales de oxígeno (ORAC). Química alimentaria 2008, 108, 1002–1007. [Referencia cruzada]
34. Elías, RJ; Kellerby, SS; Decker, E. Actividad antioxidante de proteínas y péptidos. crítico Rev. ciencia de los alimentos. Nutrición 2008, 48, 430–441. [Referencia cruzada] [PubMed]
35. Mía, Y.; Li-Chan, E.; Jiang, B. (Eds.) Proteínas y péptidos bioactivos como alimentos funcionales y nutracéuticos; Wiley-Blackwell: Hoboken, Nueva Jersey, EE. UU., 2010; págs. 29–42.
36. Adebiyi, AP; Adebiyi, AO; Yamashita, J.; Ogawa, T.; Muramoto, K. Purificación y caracterización de péptidos antioxidantes derivados de hidrolizados de proteína de salvado de arroz. EUR. Alimentos Res. Tecnología 2008, 228, 553–563. [Referencia cruzada]
37. Thamnarathip, P.; Jangchud, K.; Nitisinprasert, S.; Vardhanabhuti, B. Identificación del peso molecular del péptido del hidrolizado de proteína de salvado de arroz con alta actividad antioxidante. J. Ciencias de los cereales. 2016, 69, 329–335. [Referencia cruzada]
38. Tacias-Pascacio, VG; Morellón-Sterling, R.; Siar, E.-H.; Tavano, O.; Berenguer-Murcia, Á.; Fernandez-Lafuente, R. Uso de Alcalasa en la producción de péptidos bioactivos: Una revisión. En t. J. Biol. macromol. 2020, 165, 2143–2196. [Referencia cruzada] [PubMed]
39. Sarringkarin, W.; Laokuldilok, T. Optimización de las condiciones de producción de hidrolizado de proteína de salvado de arroz glutinoso con propiedades antioxidantes. CMU J.Nat. ciencia 2017, 16, 1–18. [Referencia cruzada]
40. Zhang, Q.; Tong, X.; Qi, B.; Wang, Z.; Li, Y.; Sui, X.; Jiang, L. Cambios en la actividad antioxidante del hidrolizado de soja hidrolizada con Alcalasa bajo digestión gastrointestinal simulada y transporte transepitelial. Función J. Alimentos 2018, 42, 298–305. [Referencia cruzada]
41. Ma, PTB; Tawata, S. Propiedades antioxidantes, antienvejecimiento y antimelanogénicas de los aceites esenciales de dos variedades de Alpinia zerumbet. Moléculas 2015, 20, 16723–16740. [Referencia cruzada]
42. Nishida, Y.; Sugahara, S.; Wada, K.; Toyohisa, D.; Tanaka, T.; Ono, M.; Yasuda, S. Efectos inhibidores del extracto de acetato de etilo de los bulbos de Scilla scilloides sobre las actividades de la lipoxigenasa y la hialuronidasa. Farmacia Biol. 2014, 52, 1351–1357. [Referencia cruzada]
43. Chen, H.-J.; Dai, F.-J.; Ventilador, S.-L.; Huang, Y.-C.; Chau, C.-F.; Lin, Y.-S.; Chen, C.-S. Cinética de la inhibición de la hialuronidasa por hidrolizado de proteína de arroz (Oryza sativa L.). aplicación ciencia 2020, 10, 9087. [Referencia cruzada]
44. Girish, K.; Kemparaju, K. El pegamento mágico hialuronano y su borrador hialuronidasa: una descripción biológica. Ciencias de la vida 2007, 80, 1921–1943. [Referencia cruzada] [PubMed]
45. Zolghadri, S.; Bahrami, A.; Khan, MTH; Muñoz-Muñoz, J.; García-Molina, F.; García-Canovas, F.; Saboury, AA Una revisión exhaustiva sobre los inhibidores de la tirosinasa. J. enzima. inhibir Medicina. química 2019, 34, 279–309. [Referencia cruzada] [PubMed]
46. Seo, EJ; Hong, ES; Choi, MH; Kim, KS; Lee, SJ Efectos antioxidantes y blanqueadores de la piel de los extractos de Rhamnus yoshinoi. coreanoJ. ciencia de la comida Tecnología 2010, 42, 750–754.
47. Ochiai, A.; Tanaka, S.; Tanaka, T.; Taniguchi, M. Proteína de salvado de arroz como fuente potente de péptidos antimelanogénicos con actividad inhibidora de la tirosinasa. J.Nat. Pinchar. 2016, 79, 2545–2551. [Referencia cruzada] [PubMed]
48. Kubglomsong, S.; Theerakulkait, C.; Caña, RL; Yang, L.; Maier, CS; Stevens, JF Aislamiento e identificación de péptidos inhibidores de tirosinasa y quelantes de cobre a partir de albúmina hidrolizada derivada de salvado de arroz. J. Agric. Química alimentaria 2018, 66, 8346–8354.[Referencia cruzada]
49. Schurink, M.; van Berkel, WJ; Wichers, H.; Boeriu, CG Nuevos péptidos con actividad inhibidora de tirosinasa. Péptidos 2007, 28,485–495. [Referencia cruzada]
50. Ishikawa, M.; Kawase, I.; Ishii, F. La combinación de aminoácidos reduce la pigmentación en células de melanoma B16F0. Biol. Pharm.Bull. 2007, 30, 677–681. [Referencia cruzada] [PubMed]
51. Zhang, R.; Wei, Y.; Li, M.; Cai, M.; Gu, R.; Mayo.; Chen, L.; Wang, J. Efectos de la melanogénesis del hidrolizado de proteína de arroz y sus péptidos característicos Leu-Leu-Lys, Leu-Pro-Lys y pyroGlu-Lys en células de melanocitos epidérmicos humanos inducidas por UVB. FoodFunct. 2020, 11, 8757–8767. [Referencia cruzada]
52. Wang, Y.; Cai, D.; El, M.; Wang, Z.; Qin, P.; Tan, T. Producción fermentativa abierta de ácido l -láctico utilizando salvado de arroz blanco mediante sacarificación y fermentación simultáneas. Biorrecursos. Tecnología 2015, 198, 664–672. [Referencia cruzada] [PubMed]
53. Pan, M.; Jiang, TS; Pan, JL Actividades antioxidantes de los hidrolizados de proteína de colza. Bioprocesos alimentarios. Tecnología 2009, 4, 1144–1152. [Referencia cruzada]
54. Chen, HM; Muramoto, K.; Yamauchi, F.; Nokihara, K. Actividad antioxidante de péptidos diseñados basados en el péptido antioxidante aislado de la digestión de una proteína de soja. J. Agric. Química alimentaria 1996, 44, 2619–2623. [Referencia cruzada]
55. Liu, Q.; Kong, B.; Xiong, YL; Xia, X. Actividad antioxidante y propiedades funcionales del hidrolizado de proteína plasmática porcina influenciados por el grado de hidrólisis. Química alimentaria 2010, 118, 403–410. [Referencia cruzada]
56. Lemes, A.; Sala, L.; minerales, JDC; Braga, ARC; Egea, MB; Fernandes, KF Una revisión de los últimos avances en péptidos bioactivos cifrados a partir de desechos ricos en proteínas. En t. J. Mol. ciencia 2016, 17, 950. [Referencia cruzada] [PubMed]
57. Wang, J.-S.; Zhao, MM-M.; Zhao, Q.-Z.; Jiang, Y.-M. Propiedades antioxidantes de los hidrolizados de papaína del gluten de trigo en diferentes sistemas de oxidación. Química alimentaria 2007, 101, 1658–1663. [Referencia cruzada]
58. Gao, M.-T.; Kaneko, M.; Hirata, M.; Toorisaka, E.; Hano, T. Utilización de salvado de arroz como fuente de nutrientes para la producción de ácido láctico fermentativo. Biorrecursos. Tecnología 2008, 99, 3659–3664. [Referencia cruzada] [PubMed]
59. Huang, WY; Lin, YR; Ho, FR; Liu, HY; Lin, YS Efectos de las soluciones de agua en la extracción de hojas de té verde. ciencia World J. 2013,2013, 368350. [Referencia cruzada]
60. Wathoni, N.; Shan, CY; Shan, WY; Rostinawati, T.; Indradi, RB; Pratiwi, R.; Muchtaridi, M. Caracterización y actividad antioxidante de la pectina de la corteza del mangostán de Indonesia (Garcinia mangostana L.). Heliyon 2019, 5, e02299. [Referencia cruzada]
61. Tsai, C.-C.; Chan, C.-F.; Huang, W.-Y.; Lin, J.-S.; Chan, P.; Liu, H.-Y.; Lin, Y.-S. Aplicaciones del sobrenadante SpentCulture de Lactobacillus rhamnosus en aplicaciones cosméticas de antioxidación, blanqueamiento y retención de humedad. Moléculas 2013, 18, 14161–14171.[Referencia cruzada]
62. Huang, W.-Y.; Lee, PC-C.; Hsu, J.-C.; Lin, Y.-R.; Chen, H.-J.; Lin, Y.-S. Efectos de la Calidad del Agua en la Disolución de Polvos de Extracto de Yerba Mate. ciencia Mundo J. 2014, 2014, 1–6. [Referencia cruzada] [PubMed]
63. Chan, C.-F.; Wu, CT-T.; Huang, W.-Y.; Lin, W.-S.; Wu, H.-W.; Huang, T.-K.; Chang, M.-Y.; Lin, Y.-S. Antioxidación y melanogénesis Inhibición de varios extractos de Dendrobium tosaense. Moléculas 2018, 23, 1810. [CrossRef] [PubMed]64. Wu, CT-T.; Agrawal, DC; Huang, W.-Y.; Hsu, H.-C.; Yang, S.-J.; Huang, S.-L.; Lin, Y.-S. Análisis de Funcionalidad de Extractos de Café Molido Agotados Obtenidos por el Método Hidrotermal. J. Chem. 2019, 2019, 1–8. [Referencia cruzada]
65. Dorta, E.; Rodríguez-Rodríguez, EM; Jiménez-Quezada, A.; Fuentes-Lemus, E.; Speisky, H.; Lissi, E.; López-Alarcón, C. Uso del Ensayo de Capacidad de Absorción de Radicales de Oxígeno (ORAC) para Predecir la Capacidad de los Subproductos del Mango (Mangifera indica L.) para Inhibir la Oxidación de la Proteína de la Carne. comida anal. Métodos 2016, 10, 330–338. [Referencia cruzada]
66. Lin, Y.-S.; Chen, H.-J.; Huang, J.-P.; Lee, PC-C.; Tsai, C.-R.; Hsu, T.-F.; Huang, W.-Y. Cinética de la actividad inhibidora de tirosinasa usando extractos de hojas de Vitis vinifera. Res. biomédica. En t. 2017, 2017, 5232680. [Referencia cruzada] [PubMed]
67. Bidlingmeyer, BA; Cohen, SA; Tarvin, TL Análisis rápido de aminoácidos mediante derivatización precolumna. J. Chromatogr. Bbiomed. ciencia aplicación 1984, 336, 93–104. [Referencia cruzada]
68. Asai, TT; Oikawa, F.; Yoshikawa, K.; Inoué, N.; Sato, K. Los péptidos de colágeno derivados de los alimentos, la prolil-hidroxiprolina (Pro-Hyp) y la hidroxiprolil-glicina (Hyp-Gly) mejoran el crecimiento de fibroblastos de piel de ratón de cultivo primario utilizando suero bovino fetal libre de péptido de hidroxiprolilo. En t. J. Mol. ciencia 2019, 21, 229. [Referencia cruzada]
69. Schägger, H. Tricine–SDS–PAGE. Nat. Protocolo 2006, 1, 16–22. [Referencia cruzada]
70. Diao, J.; Chi, Z.; Guo, Z.; Zhang, L. El hidrolizado de proteína de frijol mungo modula la respuesta inmune a través de la vía NF-kB en macrófagos RAW 264.7 estimulados por lipopolisacáridos. J. ciencia de los alimentos. 2019, 84, 2652–2657.[Referencia cruzada]
