¿Cómo determinar la función renal en pacientes con cáncer?
Feb 24, 2022
Contacto: emily.li@wecistanche.com
Ben Sprangers y otros
Resumen
Un método preciso y eficiente para estimarriñónfunciónen pacientes con cáncer es importante para determinar su elegibilidad para ensayos clínicos y cirugía y para permitir el ajuste de dosis apropiado de medicamentos contra el cáncer, especialmente medicamentos tóxicos con un índice terapéutico estrecho. Dado que la medición directa de la tasa de filtración glomerular (TFG) es engorrosa, se han desarrollado varias fórmulas para estimarriñónfunción. La mayoría de estos se basan en la concentración de creatinina sérica. Aunque se reconoce que la fórmula CKD-EPI es la más precisa, existe un debate en curso sobre cuál es la fórmula óptima para los pacientes con cáncer. En esta revisión, proporcionamos una descripción general de diferentes ecuaciones de estimación de GFR parariñónfuncióny las ventajas y desventajas de cada método y comparar su desempeño en pacientes con cáncer. Discutimos la importancia de la indexación del área de superficie corporal y proponemos un marco para evaluarriñónfunciónen pacientes con cáncer.
PALABRAS CLAVE:Riñónfunción; Filtración glomerular; fórmula de TFG; indexación BSA

Haga clic aquí para obtener información detallada sobre Cistanche
1. Introducción
1.1. Importancia de evaluar la función renal en pacientes con cáncer
Estimación precisa deriñónfunciónes importante en hematología y oncología para determinar la elegibilidad para ensayos clínicos y cirugía y para facilitar los ajustes de dosis de quimioterapia, antibióticos, analgésicos opioides y otros medicamentos, especialmente para medicamentos tóxicos con un índice terapéutico estrecho. Dado que muchos medicamentos contra el cáncer se eliminan por vía renal, es necesario ajustar la dosis para los pacientes con función renal disminuida para evitar tanto la sobredosis como la infradosificación.Riñóndisfunciónes común entre los pacientes con cáncer y pérdidas significativas deriñónfuncióna menudo ocurren durante la terapia del cáncer [1]. Un estudio transversal que evaluó a pacientes con cáncer encontró una reducción en la tasa de filtración glomerular estimada (TFGe) de 13 ml/min/1,73 m2 después de 2 años, y el 17,7 % de los pacientes cambiaron de condición crónica.riñón enfermedad(CKD) Etapa 2 a CKD etapa 3 o 4 en el seguimiento [2]. Dado que no es práctico ni factible determinar las concentraciones séricas del fármaco o medir directamente la TFG repetidamente en la práctica clínica diaria, es importante determinar el método más preciso y factible para evaluar la función renal (p. ej., estimar la TFG).
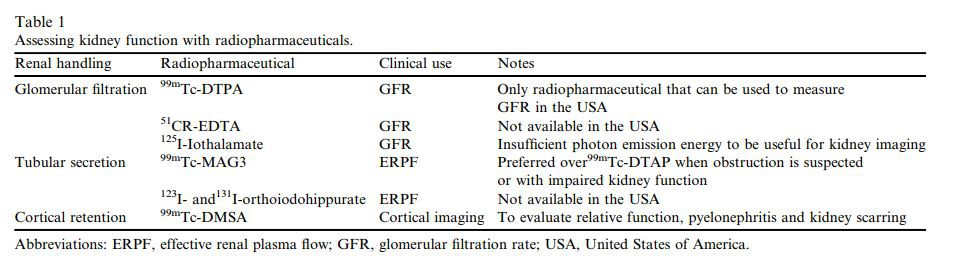
Hay varios métodos disponibles para medir directamente la TFG (Tabla 1). Sin embargo, todos estos métodos requieren mucho trabajo, son complejos y consumen mucho tiempo, lo que hace imposible realizar estos ensayos en todos los pacientes con cáncer de manera regular. La eliminación de inulina es el estándar de oro, pero rara vez se usa en la práctica clínica [3], y se han desarrollado métodos alternativos y más simples, como los métodos de eliminación del ácido etilendiaminotetraacético, iohexol, iotalamato y dietilentriaminopentaacetato [4,5]. El único método utilizado de forma rutinaria en la práctica clínica para medirriñónfunciónes el cálculo del aclaramiento de creatinina, que se basa en la creatinina sérica y la concentración de creatinina en orina en una colección de orina de 24- horas. Este método es problemático ya que la medición de la depuración de creatinina no ha sido validada en pacientes con cáncer [5] y se sabe que las recolecciones de orina son engorrosas y están sujetas a errores, especialmente en el ámbito ambulatorio. Actualmente no existen ensayos aleatorizados que apoyen la necesidad de realizar sistemáticamente la medición directa de la TFG en oncología. Sin embargo, se debe considerar la medición directa de la TFG para guiar el ajuste de la dosis del fármaco para los quimioterapéuticos con nefrotoxicidad potencialmente grave y con un índice terapéutico estrecho, como el cisplatino o el carboplatino, o en pacientes en los que las ecuaciones disponibles muestran poca precisión [6].
Actualmente, no hay consenso con respecto a los medios óptimos para estimar la TFG para permitir los ajustes de la quimioterapia (Tabla 2) y para definir la elegibilidad de un paciente para ensayos de nuevos fármacos contra el cáncer. Históricamente, los pacientes con deteriororiñónfunciónhan sido excluidos de los estudios de fase 1 de fármacos anticancerosos debido al mayor riesgo percibido de toxicidad importante limitante de la dosis. Un estudio reciente demostró que el 85 por ciento de los ensayos clínicos de medicamentos para las cinco neoplasias malignas más comunes publicados en revistas de factor de alto impacto excluyeron a la gran mayoría de los pacientes con ERC [7]. Un análisis retrospectivo de más de 10,000 pacientes de 373 ensayos clínicos de fase 1 de un solo agente no encontró un aumento clínicamente significativo en las toxicidades no hematológicas de grado 3 o 4, hematológicas de grado 4 o clínicamente relevantes en pacientes con insuficiencia renal leve. deterioro (definido según la FDA como CrCl 50-79 mL/min) en comparación con aquellos con normalriñón función[8]. En los últimos años, algunos han abogado por que los ensayos clínicos incluyan más pacientes con insuficiencia renal de leve a moderada [9].

1.2. Importancia del ensayo utilizado para estimar la función renal
RiñónfunciónEstá compuesto por funciones glomerulares y tubulares. Es importante darse cuenta de que todos los métodos comúnmente utilizados para estimar la función renal solo evalúan la TFG. El ensayo que se utiliza para estimar la TFG es importante ya que puede haber una importante variabilidad entre ensayos. Esta variabilidad se ejemplifica aplicando las diferentes fórmulas de estimación para determinar la elegibilidad de un paciente para recibir cisplatino. Cuando se comparó con eGFR usando la ecuación de la Colaboración Epidemiológica de Enfermedades Renales Crónicas (CKD-EPI), la fórmula de CockcrofteGault (CG) estimó que la depuración de creatinina (CrCl) da como resultado que un 20 por ciento más de pacientes sean excluidos de la elegibilidad para el cisplatino. Esta diferencia es aún más pronunciada entre los caucásicos, los ancianos y las mujeres [10e15]. Ya sea que se use la fórmula CG o CKD-EPI eGFR, cambiará la elegibilidad de un paciente para recibir cisplatino en aproximadamente el 15 por ciento de los casos [11,12,14]. Además, en un estudio realizado por Bennis et al., los ajustes de la dosis de cisplatino fueron necesarios para el 9,7 % que usaba la fórmula CG, pero solo en el 4,8 % que usaba la fórmula del estudio Modification of Diet in Renal Disease (MDRD) [16]. En comparación con la medición directa de CrCl basada en muestras de orina de 24-h, más pacientes se clasifican como no elegibles para cisplatino cuando se estima CrCl o GFR [15]. Este efecto es más pronunciado en pacientes mayores de 65 años, con un 24-53 por ciento de estos pacientes a los que se les niega el cisplatino cuando se compara el CrCl estimado o la TFG con el CrCl medido [10]. Estas diferencias son obviamente clínicamente importantes. Además, hay pruebas de que el CrCl medido se correlaciona con la capacidad del paciente para completar tres ciclos completos de quimioterapia, mientras que el CrCl y la TFG estimados no lo hacen [10]. Para carboplatino, el ensayo utilizado para determinarriñón funciónes también un determinante importante de la dosificación. La fórmula de Calvert se usa para determinar la dosis de carboplatino (Calvert: dosis total [mg] Z [área objetivo bajo la curva] [TFG + 25]). Corto et al. estudió retrospectivamente la dosis de carboplatino administrada a un paciente utilizando la fórmula CG [17]. Si se hubiera usado MDRD en su lugar, se habría producido una dosis discrepante de carboplatino (definida como una diferencia de más del 20 por ciento) en el 48 por ciento de los pacientes. Esto plantea la pregunta de si los umbrales utilizados para la selección de fármacos son adecuados y, lo que es más importante, cuál es el método más útil para estimar la función renal en pacientes con cáncer. Existen varios métodos para medir o estimar la TFG en la población general, y cada uno tiene sus limitaciones concomitantes. No existe consenso sobre cuál de los métodos disponibles es el ideal para la población general, y menos aún en pacientes oncológicos [6,18].
1.3. Estimación de la función renal a partir de la creatinina sérica
Por múltiples razones, la concentración de creatinina sérica es un sustituto imperfecto de la función renal. No obstante, es el método más utilizado para estimar el FG. La creatinina es producida por los músculos y eliminada del cuerpo a través de la filtración glomerular y la secreción tubular (Fig. 1). Es importante darse cuenta de que los pacientes con cáncer constituyen una población heterogénea y que el peso, el estado nutricional y la masa muscular pueden variar significativamente dentro de un solo paciente durante el curso de su tratamiento. El desgaste muscular es común entre los pacientes con cáncer y con frecuencia es progresivo durante la terapia del cáncer, especialmente entre aquellos con enfermedad avanzada que reciben quimioterapia [19]. Es importante señalar que la relación entre la creatinina sérica y la TFG no es lineal sino más bien hiperbólica, lo que significa que a concentraciones bajas de creatinina sérica, un pequeño cambio en la concentración de creatinina sérica corresponde a un gran cambio en la TFG. Por el contrario, a concentraciones altas de creatinina sérica, un gran cambio en la creatinina sérica corresponde a un cambio relativamente pequeño en la TFG.

También existen problemas analíticos asociados con las mediciones de creatinina sérica. Históricamente, se emplean dos técnicas para medir el suero: la reacción clásica de Jaffe y el método enzimático. En el método de Jaffe, una reacción entre el picrato y la creatinina en un medio alcalino produce un producto de color rojo anaranjado que se puede cuantificar. Los componentes endógenos (glucosa, proteínas, ácidos cetónicos, ácido ascórbico, acetoacetato y piruvato) también se recogen en este ensayo y estos pseudocromógenos representan del 15 al 20 por ciento de la reacción de Jaffe si la creatinina sérica está en el rango normal. Se han descrito diferentes métodos enzimáticos, pero todos tienen una mayor especificidad para la creatinina sérica que los ensayos de Jaffe y, por lo tanto, se consideran más exactos y precisos que el método de Jaffe. Hasta hace poco, había una heterogeneidad significativa entre los diferentes ensayos enzimáticos [20]. El método rastreable de espectrometría de masas por dilución de isótopos (IDMS) se introdujo para mejorar la estandarización [21]. Por todas las limitaciones antes mencionadas, las concentraciones de creatinina sérica por sí solas no deben usarse para monitorear la función renal en pacientes con cáncer. Cabe destacar que el estudio de Kithclu et al. demostró que de los ensayos clínicos de medicamentos que excluyeron a la gran mayoría de los pacientes con ERC, los valores umbral de creatinina sérica fueron el criterio de exclusión en el 62 por ciento de los pacientes [7].
1.4. Aclaramiento de creatinina estimado y eGFR
Las fórmulas más utilizadas para estimar la función renal utilizando la creatinina sérica son la ecuación CG, que estima el aclaramiento de creatinina, la fórmula MDRD y las ecuaciones CKD-EPI, que estiman la TFG [4]. Se han desarrollado varias fórmulas adicionales para estimar la TFG. En general, los resultados de estas fórmulas estarán dentro del 30 por ciento de los resultados de la TFG medida por un método de referencia (estudios de medicina nuclear) en el 85-90 por ciento de los sujetos [22]. Dado que todas estas fórmulas utilizan la creatinina sérica para estimar la TFG, en base a la discusión previa sobre las limitaciones de las mediciones de creatinina y el hecho de que la anorexia, la pérdida de peso y el desgaste muscular son hallazgos comunes en pacientes con cáncer, es posible que estas fórmulas no proporcionen estimaciones precisas de la función renal. función en esta población [23].
1.5. fórmula CG
La fórmula CG utiliza la creatinina sérica en combinación con la edad, el peso y el sexo para estimar el aclaramiento de creatinina. La fórmula no compensa los determinantes de la función renal de la creatinina sérica, como la raza, la dieta, la secreción tubular y la eliminación extrarrenal de creatinina. Además, la fórmula se desarrolló utilizando el aclaramiento de creatinina medido a partir de muestras de orina de 24-h como sustituto de la TFG verdadera y en un momento en que se empleaban ensayos no enzimáticos no estandarizados para la medición de la creatinina sérica. En consecuencia, la fórmula CG es una estimación imprecisa de la verdadera TFG. A pesar de estas importantes deficiencias, la fórmula CG se ha convertido en el ensayo más utilizado para la dosificación de fármacos basada en la función renal y para la determinación de la elegibilidad del fármaco desde su incorporación a las directrices de la Administración Federal de Medicamentos (FDA) de 1998 sobre farmacocinética para pacientes con insuficiencia renal.
1.6. MDRD y CKD-EPI
Tanto la ecuación MDRD como la CKD-EPI se desarrollaron utilizando la medición de iotalamato GFR, ensayos estandarizados de creatinina sérica enzimática, e incorporan determinantes de creatinina sérica no renales fácilmente disponibles, como la edad, el sexo y la raza. En comparación con la fórmula CG, las fórmulas MDRD y CKD EPI dan como resultado estimaciones de la TFG más cercanas a la verdadera TFG, especialmente entre los ancianos y en pacientes con una gran área de superficie corporal (ASC) [24]. Aunque tanto las guías Kidney Disease Improving Global Outcomes (KDIGO) como la National Kidney Foundation-Kidney Disease Outcomes Quality Initiative (NKF-KDOQI) recomiendan el uso de la fórmula CKD-EPI en la práctica clínica, esta recomendación aún no ha sido completamente adoptada por la comunidad médica [25]. No es sorprendente que los pacientes con cáncer no estuvieran bien representados en los estudios originales a partir de los cuales se desarrollaron las fórmulas MDRD y CKD-EPI. Hay pocos estudios que hayan comparado el rendimiento de las diferentes ecuaciones de estimación de la función renal entre pacientes con cáncer.
En un estudio de Redal-Baigorri et al. [26], se evaluó el rendimiento de MDRD y CKD-EPI en 185 pacientes con cáncer con una función renal relativamente bien conservada. Solo el 17 por ciento tenía una TFG medida por debajo de 60 ml/min/1,73 m2. Cuando se usó 51Cr-EDTA para medir la TFG y se obtuvieron mediciones de creatinina sérica trazable mediante IDMS, el MDRD y el CKD-EPI se comportaron de manera similar y aceptable, alrededor del 89 % para ambas ecuaciones [26]. En otro estudio, Lauritsen et al. [27] compararon el rendimiento de las fórmulas CG, MDRD y CKD-EPI en pacientes con cáncer de células germinales con función renal preservada que recibieron tratamiento con bleomicina, etopósido y cisplatino. Se usó 51Cr-EDTA para medir la TFG y se obtuvieron mediciones de creatinina sérica trazables mediante IDMS antes de la quimioterapia y en múltiples momentos durante el tratamiento. El desempeño de las ecuaciones CG, MDRD y CKD-EPI fue aceptable. Sin embargo, entre los pacientes con ciclos crecientes de quimioterapia, la precisión (definida como dentro del 30 por ciento de la TFG medida) disminuyó rápidamente del 85 al 90 por ciento al 76 por ciento para CG, 80 por ciento para MDRD y 50 por ciento para CKD-EPI [27]. Hallazgos similares fueron reportados por Funakoshi et al. [28] que informó una disminución de la precisión para todas las fórmulas después de la administración de cisplatino al 60 por ciento para CKD-EPI y al 56 por ciento para CG. Antes del tratamiento con cisplatino y en pacientes con una TFG medida (TFGm) superior a 50 ml/min, el rendimiento de CKD-EPI fue superior a la fórmula CG (precisión del 92 % frente al 78 %) [28]. Después de la quimioterapia, la precisión de la fórmula CKD-EPI disminuyó. Una cuarta parte de los pacientes con valores de CKD-EPI superiores a 60 ml/min en realidad tenían una TFGm inferior a 50 ml/min [28]. Hingorani et al. [29] compararon la TFGm (mediante la depuración plasmática de iohexol) con la CG (no indexada para BSA), MDRD y CKD-EPI (ambas indexadas para BSA) en 50 pacientes que se sometieron a un trasplante de células hematopoyéticas antes y 100 días después del trasplante [29]. Al inicio del estudio, CKD-EPI y MDRD subestimaron la TFG y CG la sobreestimó. Las precisiones fueron bajas para los pacientes con valores medios de TFG normales. De hecho, la precisión dentro del 30 % al inicio del estudio fue del 79 % para CKD-EPI, del 70 % para MDRD y del 57 % para CG. Después de 100 días, la precisión observada fue similar para CKD-EPI y MDRD y ligeramente mejor para CG [29].

1.7. Otras fórmulas
While several formulae specifific to cancer patients have been developed, these equations are not widely used because of the lack of any clear benefit over the more established MDRD and CKD-EPI formulae [30,31]. In an interesting recent report, Janowitz et al. assessed the most accurate and least biased method to estimate GFR in a population of 2,471 Caucasian adult cancer patients receiving carboplatin chemotherapy [32]. The authors compared 51Cr-EDTA GFR measurement with the eGFR determined by seven published formulae with their newly developed formula. They found that the BSA-adjusted CKD-EPI formula was the most accurate published model to estimate GFR in cancer patients. The author's newly developed model (including serum creatinine, age, gender, and BSA) improved the accuracy of eGFR estimation and carboplatin dosing. The new formula reduced the fraction of patients with a carboplatin dose with an absolute percentage error >20 por ciento (14.17 por ciento versus 18.62 por ciento para el CKD EPI ajustado por BSA y 25.51 por ciento para la fórmula CG). Es de destacar que este estudio tuvo algunas limitaciones importantes, incluido el uso de mediciones de creatinina estandarizadas no IDMS, la falta de mediciones reales de la dosis de carboplatino y una población caucásica casi exclusiva. Sugerimos que este nuevo modelo se examine más a fondo, junto con el CKD-EPI ajustado por BSA, en la práctica clínica con nefrología [33].
1.8. BSA o no BSA ajustado
Una cuestión que a menudo se pasa por alto pero que es importante es si se deben usar estimaciones de la función renal indexadas o no indexadas por BSA cuando se dosifican medicamentos de quimioterapia. Esta no es una discusión teórica o trivial ya que esta elección afectará significativamente la dosificación del fármaco y posiblemente los resultados clínicos [34,35]. El objetivo de la indexación de BSA es hacer que los resultados de GFR sean comparables entre sujetos con diferentes tamaños corporales. Por ejemplo, las diferencias en la dosificación de carboplatino dependen tanto del método utilizado para calcular la TFG como de si la TFG eGFR absoluta o indexada por BSA se incorporan a la fórmula de Calvert. Cuando la eGFR indexada para BSA se calcula mediante la ecuación CKD EPI, es menos probable que se asocie con una sobredosis de medicamentos, pero es más probable que se infradosifique un fármaco en pacientes en comparación con la eGFR no indexada por BSA calculada con el mismo método [35] . La indexación de BSA tendrá un impacto particular en la GFR en pacientes con cáncer con valores extremos de peso y/o altura. Se ha observado que los pacientes con cáncer con una BSA grande con frecuencia reciben tratamiento insuficiente porque los oncólogos a menudo reducen empíricamente la dosis de quimioterapia basándose en la creencia de que es preferible usar la masa corporal magra que la masa corporal total para el cálculo de la dosis [36]. Sin embargo, en el contexto de la adaptación de la dosis de un fármaco, el objetivo es obtener una estimación precisa de la capacidad del individuo para excretar un fármaco o metabolito de fármaco en particular.
La FDA y la Agencia Europea de Medicamentos (EMA) recomiendan que la adaptación de la dosis del fármaco se base en la TFG no indexada. Aunque muchos medicamentos contra el cáncer se dosifican de acuerdo con el BSA, el método más utilizado para estimar la TFG en oncología es la fórmula CG, que produce una métrica de función renal absoluta (mililitros por minuto) que no está indexada al BSA. El uso de una estimación absoluta de la función renal para prescribir medicamentos contra el cáncer que se dosifican de acuerdo con la BSA probablemente alterará la dosis en comparación con las decisiones de dosificación sobre la base de las estimaciones de la función renal indexadas por la BSA. Por lo tanto, en general, las estimaciones de GFR no indexadas deben usarse para calcular las dosis de medicamentos contra el cáncer. Sin embargo, cuando los medicamentos se dosifican de forma absoluta o en función de parámetros distintos del BSA, se deben utilizar estimaciones de la función renal en mililitros por minuto.
1.9. Otros métodos para evaluar la función renal
Amplios estudios en la población general han establecido que la medición de cistatina C en combinación con creatinina proporciona estimaciones de TFG más precisas [37]. Recientemente, Stabuc et al. demostraron que las estimaciones de GFR usando cistatina C con aclaramiento de creatinina de 24- h funcionaron mejor que las fórmulas de eGFR usando creatinina sérica en pacientes con tumores sólidos que recibieron quimioterapia basada en cisplatino [38]. Por el contrario, Hingorani et al. también evaluó fórmulas basadas en cistatina C y demostró que la ecuación combinada mostró una precisión ligeramente mejor dentro del 30 por ciento (al 89 por ciento) en comparación con las ecuaciones basadas en creatinina, solo al inicio, pero no en el día 100 después del trasplante [29]. Estos hallazgos contradictorios sugieren que es demasiado pronto para recomendar ensayos basados en cistatina C para estimar la función renal en pacientes con cáncer. Existen limitaciones potenciales adicionales para los ensayos basados en cistatina C. Primero, actualmente, los datos sobre pacientes con cáncer son limitados, carecen de un método de referencia para medir la TFG y/o incluyen muy pocos pacientes [39-41]. Además, en teoría, las células cancerosas también podrían producir cistatina C [42,43]. Finalmente, la producción de cistatina C también se ve afectada por otros factores independientes de la TFG que no son infrecuentes entre los pacientes con cáncer, como la exposición a corticoides, la disfunción tiroidea, la inflamación y la obesidad [44-46].
1.10. Directrices disponibles
Varias sociedades científicas, incluida la Sociedad Internacional de Oncología Geriátrica (SIOG) y la Red Nacional Integral del Cáncer (NCCN), recomiendan una evaluación de la función renal para permitir el ajuste de la dosis del medicamento contra el cáncer para reducir la toxicidad antes de la quimioterapia, incluso cuando la concentración de creatinina sérica está dentro de lo normal. rango. Por el contrario, existen pocas guías que proporcionen recomendaciones específicas sobre el método preferido para estimar la función renal en pacientes con cáncer. La SIOG sugiere usar la ecuación del estudio MDRD para pacientes con cáncer mayores de 65 años [6,47], mientras que la NCCN sugiere usar CrCl en pacientes de edad avanzada y "cálculos de TFG" en adolescentes y adultos jóvenes [48,49]. Las pautas actuales de la FDA recomiendan la fórmula CG para determinar la función renal. Sin embargo, una revisión preliminar de las pautas para evaluar la farmacocinética en la insuficiencia renal sugiere que la fórmula eGFR también debe usarse para estimar la función renal sin indicar una preferencia sobre qué fórmula usar.

2. Conclusión
Existe un debate en curso sobre si usar la fórmula CG o la fórmula CKD-EPI para guiar los ajustes de dosis de medicamentos para el cáncer en pacientes con ERC (Fig. 2). Los argumentos a favor del uso de la ecuación CKD-EPI son los siguientes. Primero, en la población general, el CKD-EPI es superior a la ecuación CG para estimar la TFG [50,51]. En segundo lugar, la fórmula CKD-EPI estima la TFG, mientras que la fórmula CG estima el CrCl, que es una estimación deficiente de la verdadera TFG. En tercer lugar, la ecuación de CG se desarrolló utilizando valores de creatinina sérica no calibrados y no rastreables por IDMS [21]. Por otro lado, históricamente, la fórmula CG se ha utilizado ampliamente para determinar los ajustes de dosis de la mayoría de los fármacos [52,53] y se ha demostrado que predice el riesgo de eventos adversos inducidos por fármacos [54]. Para el paciente con cáncer que está siendo evaluado para su inclusión en un ensayo clínico, el método elegido para estimar la función renal es de particular importancia. La clasificación actual de la FDA de insuficiencia renal leve es un CrCl de 50-79 ml/min, y la mayoría de los ensayos de fase 1 descalifican a los pacientes para que se inscriban con un CrCl < 60="" ml/min.="" dado="" que="" la="" fórmula="" cg="" subestima="" sistémicamente="" la="" función="" renal="" en="" un="" grado="" mayor="" que="" ckd-epi="" o="" mdrd,="" puede="" excluir="" innecesariamente="" a="" los="" pacientes="" con="" insuficiencia="" renal="" leve="" de="" los="" ensayos="">

Cualquier recomendación definitiva con respecto al mejor método para estimar la función renal en pacientes con cáncer requeriría realizar un ensayo prospectivo aleatorizado en el que la dosis de quimioterapia se calcule utilizando tanto mGFR como eGFR y luego recopilar datos sobre el cáncer posterior y los resultados adversos entre los diferentes grupos. Por muchas razones, existe una baja probabilidad de que se lleve a cabo un estudio de este tipo. Los datos disponibles generalmente muestran diferencias en las dosis de quimioterapia cuando se utilizan cálculos de mGFR y eGFR. De manera uniforme, estos estudios han demostrado diferencias en los cálculos de dosis cuando se utilizan estos dos métodos. No está firmemente establecido si estas diferencias de dosificación darían lugar a resultados diferentes. Solo hay datos limitados disponibles sobre el rendimiento de las fórmulas de estimación de GTR en pacientes con cáncer. A partir de esto, se puede concluir que las fórmulas son, en el mejor de los casos, subóptimas para estimar la TFG en pacientes con cáncer y su inexactitud se vuelve más pronunciada durante o después de los ciclos de quimioterapia.
Un enfoque incluye el uso de diferentes fórmulas de eGFR y el cálculo de la diferencia absoluta y relativa entre diferentes fórmulas. Si los resultados son concordantes (diferencia<10 ml/min="" of=""><10%), drug="" dosage="" recommendations="" available="" in="" the="" literature="" can="" be="" used.="" however,="" when="" signifificant="" discrepancies="" are="" noted,="" clinicians="" should="" consider="" the="" patient="" and="" their="" drug="" profile.="" for="" highly="" effective="" concentration-dependent="" drugs="" with="" a="" low="" risk="" of="" nephrotoxicity,="" the="" equation="" that="" gives="" the="" higher="" egfr="" results="" (and="" thus="" higher="" dosage="" of="" the="" chemotherapeutic)="" could="" be="" considered.="" conversely,="" for="" a="" drug="" with="" significant="" nephrotoxicity,="" a="" narrow="" therapeutic="" range,="" or="" invulnerable="" patient="" populations,="" it="" may="" be="" advisable="" to="" adjust="" the="" dosage="" based="" on="" a="" formula="" giving="" the="" loweregfr="" result.="" the="" cg="" formula="" is="" known="" to="" give="" systematically="" lower="" egfr="" values="" compared="" to="" ckd-epi,="" particularly="" in="" the="" elderly.="" as="" such,="" the="" use="" of="" the="" cgformula="" will="" thus="" result="" in="" a="" more="" protective="" behavior="" in="" terms="" of="" drug="">
En nuestra opinión, además de decidir qué fórmula usar, es importante considerar si se deben emplear estimaciones de la función renal indexadas por BSA versus no indexadas por BSA para determinar la dosificación y la elegibilidad para los medicamentos contra el cáncer. Es importante enfatizar que la suposición de que las estimaciones de la función renal son numéricamente equivalentes en unidades congruentes es incorrecta. En el futuro, se deben desarrollar pautas para mejorar la consistencia y abogar por el uso de la medida absoluta o indexada por BSA de la función renal (mililitros por minuto) para medicamentos dosificados de forma absoluta o sobre la base de cualquier parámetro que no sea BSA en comparación con la medida indexada por BSA. medida de la función renal (mililitros por minuto por 1,73 m2).
Declaración de conflicto de interésEl autor no tiene ningún conflicto de interés en relación con el manuscrito enviado.
Expresiones de gratitud
BS es investigador clínico sénior de The ResearchFoundation Flanders (FWO) (1842919N).
Referencias
[1] Launay-Vaccher V, Oudard S, Janus N, Gligorov J, Pourrat X, Rixe O, et al. Prevalencia de insuficiencia renal en pacientes con cáncer e implicaciones para el manejo de medicamentos contra el cáncer: el estudio de insuficiencia renal y medicamentos contra el cáncer (IRMA). Cáncer 2007;110:1376e84.
[2] Janus N, Oudard S, Beuzeboc P, Gligorov J, Ray-Coquard I, Morere JF, et al. Prevalencia de insuficiencia renal en pacientes con cáncer: datos del estudio IRMA-2 [Resumen]. J Clin Oncol 2009; 27:9559
[3] Rule AD, Bergstralh EJ, Slezak JM, Bergert J, Larson TS. Tasa de filtración glomerular estimada por cistatina C entre diferentes presentaciones clínicas. Riñón Int 2006;69:399e405.
[4] Levey AS, de Jong PE, Coresh J, El NM, Astor BC, Matsushita K, et al. La definición, clasificación y pronóstico de la enfermedad renal crónica: un informe de la Conferencia de Controversias KDIGO. Riñón Int 2011;80:17e28.
[5] Soveri I, Berg UB, Bjork J, Elinder CG, Grubb A, Mejare I, et al. Volver SE: medición de la TFG: una revisión sistemática. Am J Kidney Dis 2014;64:411e24.
[6] Launay-Vaccher V, Chatelut E, Lichtman SM, Wildiers H, Steer C, Aapro M. Insuficiencia renal en pacientes ancianos con cáncer: recomendaciones de práctica clínica de la Sociedad Internacional de Oncología Geriátrica. Ann Oncol 2007;18:1314e21.
[7] Kitchlu A, Shapiro J, Amir E, Garg AX, Kim SJ, Wald R, et al. Representación de pacientes con enfermedad renal crónica en ensayos de terapia contra el cáncer. J Am Med Assoc 2018;319:2437e9.
[8] Beumer JH, Ding F, Tawbi H, Lin Y, Viluh D, Chatterjee I, et al. Efecto de la disfunción renal sobre la toxicidad en tres décadas de estudios de fase I de un solo agente patrocinados por el programa de evaluación de la terapia del cáncer. J Clin Oncol 2016;34:110e6.
[9] Sprangers B, Jhaveri KD, Perazella MA. Mejorar la atención del cáncer para pacientes con enfermedad renal crónica. J Clin Oncol 2020;38(3): 188e92. epub antes de la impresión.
[10] Raj GV, Iasonos A, Herr H, Donat SM. Las fórmulas que calculan el aclaramiento de creatinina son inadecuadas para determinar la elegibilidad para la quimioterapia basada en cisplatino en el cáncer de vejiga. J Clin Oncol 2006;24:3095e100.
[11] Tsao CK, Moshier E, Seng SM, Godbold J, Grossman S, Winston J, et al. Impacto de la ecuación CKD-EPI para estimar la función renal en la elegibilidad para la quimioterapia basada en cisplatino en pacientes con cáncer urotelial. Clin Genitourin Canc 2012;10:15e20.
[12] Horn T, Ladwein B, Maurer T, Redlin J, Seitz AK, Gschwend JE, et al. El método de determinación de la TFG influye en la estimación de la elegibilidad para cisplatino en pacientes con cáncer urotelial avanzado. Mundo J Urol 2014;32:359e63.
[13] Dash A, Galsky MD, Vickers AJ, Serio AM, Koppie TM, Dalbagni G, et al. Impacto de la insuficiencia renal en la elegibilidad para la quimioterapia adyuvante basada en cisplatino en pacientes con carcinoma urotelial de vejiga. Cáncer 2006;107:506e13.
[14] Canter D, Viterbo R, Kutikov A, Wong YN, Plimack E, Zhu F, et al. El estado basal de la función renal limita la elegibilidad del paciente para recibir quimioterapia perioperatoria por cáncer de vejiga invasivo y se ve mínimamente afectado por la cistectomía radical. Urología 2011;77: 160e5.
[15] Niwa N, Kikuchi E, Masashi M, Tanaka N, Nishiyama T, Miyajima A, et al. ¿Las fórmulas utilizadas para estimar la función renal son adecuadas para los pacientes tratados con quimioterapia basada en cisplatino después de una nefroureterectomía por carcinoma urotelial del tracto superior? Clin Genitourin Canc 2016;14:e501e7.
[16] Bennis Y, Savry A, Rocca M, Gauthier-Villano L, Pisano P, Pourroy B. Ajuste de dosis de cisplatino en pacientes con insuficiencia renal, ¿qué recomendaciones debemos seguir? Int J Clin Pharm 2014;36:420e9.
[17] Shord SS, Bressler LR, Radhakrishnan L, Chen N, Villano JL. Evaluación de la dieta modificada en la ecuación de la enfermedad renal para el cálculo de la dosis de carboplatino. Ann Pharmacother 2009;43: 235e41.
[18] Matzke GR, Aronoff GR, Atkinson Jr AJ, Bennett WM, Decker BS, Eckardt KU, et al. Consideración de la dosificación de fármacos en pacientes con enfermedad renal aguda y crónica: una actualización clínica de Kidney Disease: Improving Global Outcomes (KDIGO). Riñón Int 2011;80:1122e37.
[19] Stene GB, Helbostad JL, Amundsen T, Sorhaug S, Hjelde H, Kaasa S, et al. Cambios en la masa muscular esquelética durante la quimioterapia paliativa en pacientes con cáncer de pulmón avanzado. Acta Oncol 2015;54:340e8.
[20] Delanaye P, Cavalier E, Pottel H. Creatinina sérica: ¡no es tan simple! Nephron 2017;136:302e8.
[21] Pieroni L, Delanaye P, Boutten A, Bargnoux AS, Rozet E, Delatour V, et al. Una evaluación multicéntrica de ensayos enzimáticos de creatinina rastreables por IDMS. Clin Chim Acta 2011;412:2070e5.
[22] Delanaye P, Potter H, Botev R, Inker LA, Levey AS. Con: ¿deberíamos abandonar el uso de la ecuación MDRD a favor de la ecuación CKD-EPI? Transplante Nephrol Dial 2013;28:1396e403.
[23] Delanaye P, Mariat C. La aplicabilidad de las ecuaciones de eGFR a diferentes poblaciones. Nat Rev Nephrol 2013;9:513e22.
[24] Kilbride HS, Stevens PE, Eaglestone G, Knight S, Carter JL, Delaney MP, et al. Precisión del estudio MDRD (modificación de la dieta en enfermedad renal) y las ecuaciones CKD-EPI (CKD Epidemiology Collaboration) para la estimación de la TFG en ancianos. Am J Kidney Dis 2013;61:57e66.
[25] Levey AS, Inker LA, Coresh J. GFR estimación: de la fisiología a la salud pública. Am J Kidney Dis 2014;63:820e34.
[26] Redal-Baigorri B, Stokholm KH, Rasmussen K, Jeppesen N. Estimación de la función renal en pacientes con cáncer. DanMed Bull 2011;58:A4236.
[27] Lauritsen J, Gundgaard MG, Mortensen MS, Oturai PS, Feldt-Rasmussen B, Daugaard G. Confiabilidad de la tasa de filtración glomerular estimada en pacientes tratados con terapia que contiene platino. Int J Canc 2014;135:1733e9.
[28] Funakoshi Y, Fujiwara Y, Kiyota N, Mukohara T, Shimada T, Toyoda M, et al. Validez de nuevos métodos para evaluar la función renal en pacientes oncológicos tratados con cisplatino. Canc Chemother Pharmacol 2016;77:281e8.
[29] Hingorani S, Pao E, Schoch G, Gooley T, Schwartz GJ. Estimación de la TFG en pacientes adultos con trasplante de células hematopoyéticas: comparación de ecuaciones de estimación con un patrón de referencia de iohexol. Clin J Am Soc Nephrol 2015;10:601e10.
[30] Wright JG, Boddy AV, Highley M, Fenwick J, McGill A, Calvert AH. Estimación de la tasa de filtración glomerular en pacientes con cáncer. Br J Canc 2001;84:452e9.
[31] Holweger K, Bokemeyer C, Lipp HP. Medición precisa de la tasa de filtración glomerular individual en pacientes con cáncer: un desafío continuo. J Canc Res Clin Oncol 2005;131:559e67.
[32] Janowitz T, Williams EH, Marshall A, Ainsworth N, Thomas PB, Sammut SJ, et al. Nuevo modelo para la estimación de la tasa de filtración glomerular en pacientes con cáncer. J Clin Oncol 2017;35:2798e805.
[33] Beumer JH, Inker LA, Levey AS. Mejora de la dosificación de carboplatino en función de la TFG estimada. Am J Kidney Dis 2018;71:163e5.
[34] Takimoto CH, Remick SC, Sharma S, Mani S, Ramanathan RK, Doroshow J, et al. Estudio farmacológico y de aumento de dosis de oxaliplatino en pacientes adultos con cáncer con insuficiencia renal: un estudio del grupo de trabajo sobre disfunción orgánica del Instituto Nacional del Cáncer. J Clin Oncol 2003;21:2664e72.
[35] Shepherd ST, Gillen G, Morrison P, Forte C, Macpherson IR, White JD, et al. Desempeño de estimaciones basadas en fórmulas de la tasa de filtración glomerular para la dosificación de carboplatino en el seminoma en estadio 1. Eur J Canc 2014;50:944e52.
[36] Lyman GH, Sparreboom A. Dosis de quimioterapia en pacientes con sobrepeso y obesos con cáncer. Nat Rev Clin Oncol 2013;10: 451e9.
[37] Inker LA, Schmid CH, Tighiouart H, Eckfeldt JH, Feldman HI, Greene T, et al. Estimación de la tasa de filtración glomerular a partir de la creatinina sérica y la cistatina C. N Engl J Med 2012;367:20e9.
[38] Stabuc B, Vrhovec L, Stabuc-Silih M, Cizej TE. Predicción mejorada de la disminución del aclaramiento de creatinina por la cistatina C sérica: uso en pacientes con cáncer antes y durante la quimioterapia. Clin Chem 2000;46:193e7.
[39] Bretagne M, Jouinot A, Durand JP, Huillard O, Boudou RP, Tlemsani C, et al. Estimación de la tasa de filtración glomerular en pacientes oncológicos con composición corporal anormal y relación con la toxicidad del carboplatino. Canc Chemother Pharmacol 2017;80:45e53.
[40] Cavalcanti E, Barchiesi V, Cerasuolo D, Di PF, Cantile M, Cecere SC, et al. Correlación de la cistatina C sérica con la tasa de filtración glomerular en pacientes que reciben quimioterapia basada en platino. Anal Cell Pathol 2016: 4918325. 2016.
[41] Schmitt A, Gladieff L, Lansiaux A, Bobin-Dubigeon C, EtienneGrimaldi MC, Boisdron-Celle M, et al. Fórmula universal a base de cistatina C para realizar la dosificación individual de carboplatino en pacientes con normopeso, bajo peso y obesidad. Clin Canc Res 2009;15:3633e9.
[42] Bodnar L, Wcislo GB, Smoter M, Gasowska-Bodnar A, Stec R, Synowiec A, et al. Cistatina C como parámetro de la tasa de filtración glomerular en pacientes con cáncer de ovario. Presión arterial renal Res 2010;33:360e7.
[43] Kos J, Werle B, Lah T, Brunner N. Cysteine proteinasas y sus inhibidores en fluidos extracelulares: marcadores para diagnóstico y pronóstico en cáncer. Int J Biol Markers 2000;15:84e9.
[44] Kimmel M, Braun N, Alscher MD. Influencia de la función tiroidea en diferentes pruebas de función renal. Res de prensa de sangre de riñón 2012; 35:9e17.
[45] Knight EL, Verhave JC, Spiegelman D, Hillege HL, De ZD, Curhan GC, et al. Factores que influyen en los niveles séricos de cistatina C distintos de la función renal y el impacto en la medición de la función renal. Riñón Int 2004;65:1416e21.
[46] Stevens LA, Schmid CH, Greene T, Li L, Beck GJ, Joffe MM, et al. Otros factores además de la tasa de filtración glomerular afectan los niveles de cistatina C sérica. Riñón Int 2009;75:652e60.
[47] Recomendaciones de Lichtman SM, Wildiers H, Launay-Vaccher V, Steer C, Chatelut E, Aapro M. International Society of Geriatric Oncology (SIOG) para el ajuste de la dosificación en pacientes ancianos con cáncer e insuficiencia renal. Eur J Canc 2007;43:14e34.
[48] NCCN NCCN. Pautas de práctica clínica en oncología: oncología de adultos mayores versión 1. 2018. [49] NCCN NCCN. Guías de Práctica Clínica en oncología: Adolescentes y adultos jóvenes versión 2. 2017.
[50] Froissart M, Rosset J, Jacquot C, Paillard M, Houllier P. Rendimiento predictivo de la modificación de la dieta en la enfermedad renal y ecuaciones de Cockcroft-Gault para estimar la función renal. J Am Soc Nephrol 2005;16:763e73.
[51] Levey AS, Stevens LA, Schmid CH, Zhang YL, Castro III AF, Feldman HI, et al. Una nueva ecuación para estimar la tasa de filtración glomerular. Ann Intern Med 2009;150:604e12.
[52] Ainsworth NL, Marshall A, Hatcher H, Whitehead L, Whitfield GA, Earl HM. Evaluación de la estimación de la tasa de filtración glomerular por Cockcroft-gault, Jelliffe, Wright y fórmulas de modificación de la dieta en la enfermedad renal (MDRD) en pacientes oncológicos. Ann Oncol 2012;23:1845e53.
[53] Nyman HA, Dowling TC, Hudson JQ, Peter WL, Joy MS, Nolin TD. Evaluación comparativa de la ecuación de Cockcroft-gault y la ecuación de estudio de modificación de la dieta en la enfermedad renal (MDRD) para la dosificación de fármacos: una opinión de la red de investigación y práctica de nefrología del colegio estadounidense de farmacia clínica. Farmacoterapia 2011;31:1130e44.
[54] Dufour B, Toussaint-Hacquard M, Kearney-Schwartz A, Manckoundia MD, Laurain MC, Joly L, et al. La tasa de filtración glomerular estimada por la fórmula de Cockcroft-Gault predice mejor los niveles de anti-Xa que la modificación de la dieta en la ecuación de enfermedad renal en pacientes mayores con enoxaparina profiláctica. J Nutr Salud Envejecimiento 2012;16:647e52.
