Impacto de la ingesta gestacional baja en proteínas en la expresión de microARN de riñón embrionario y en las células progenitoras de nefronas del feto masculino
Mar 08, 2022
Introducción
La falta de nutrientes puede provocar cambios de señalización en las vías fundamentales durante varias etapas del desarrollo fetal, lo que puede causar trastornos irreversibles de órganos y sistemas en la edad adulta [1]. La programación fetal se refiere a cualquier insulto durante el desarrollo, que causa efectos a largo plazo en la estructura o función de un organismo [2]. Las interrupciones en la programación fetal resultan en bajo peso al nacer, menos nefronas y mayor riesgo de enfermedades cardiovasculares yrenaltrastornos en la edad adulta [3-6]. Los estudios realizados por otros autores y por nosotros han demostrado un menor peso al nacer, un 28 por ciento menos de nefronas, una reducciónrenalexcreción de sal, crónicainsuficiencia renal, e hipertensión arterial en la ingesta gestacional baja en proteínas (LP) en comparación con la ingesta estándar de proteínas (NP) en la descendencia en la edad adulta [3-7]. La nefrogénesis implica un control estricto de la expresión génica, la síntesis de proteínas y la remodelación de tejidos. Los estudios han demostrado que el número de nefronas está determinado por las interacciones entre la yema del uréter (UB) y las células progenitoras del mesénquima metanefros (MM) [8-10]. Las señales de MM inducen el crecimiento y la ramificación del sistema de túbulos estimulados por UB. A su vez, la proliferación y diferenciación de MM, que constituye una tapa mesenquimatosa (CM), está mediada por los extremos de UB [11].

LA CITANCHE MEJORARÁ LA ENFERMEDAD RENAL/RENAL
Ha habido un gran interés en el papel de los cambios epigenéticos, en relación con los efectos a largo plazo del estrés prenatal, en el desarrollo fetal [12]. Los microARN (miARN) son pequeños ARN no codificantes codificados por el genoma de aproximadamente 22 nucleótidos de longitud y desempeñan un papel esencial en la regulación postranscripcional de la expresión del gen diana [13-16]. Los miARN controlan la expresión génica después de la transcripción al regular la traducción o la estabilidad del ARNm en el citoplasma [17, 18]. Los estudios funcionales indican que los miARN están involucrados en procesos biológicos críticos durante el desarrollo y en la fisiología celular [13, 16]. Se han observado cambios en su expresión en varias patologías [16, 19]. Por lo tanto, la caracterización de miARN ha ayudado a comprender la regulación génica y la proliferación, diferenciación y apoptosis celular y explicar los trastornos fisiopatológicos, que incluyenriñóntrastornos [20-22]. Los estudios han informado que duranteriñónLos miARN de ontogenia son indispensables para el desarrollo de las nefronas [23-26]. Además, la subexpresión de algunos miR NA en las células progenitoras de MM reduce la proliferación celular, lo que da como resultado una diferenciación temprana y, en consecuencia, una disminución del número de nefronas [27, 28]. Este fenómeno se caracteriza por un aumento de la apoptosis y una alta expresión de Bim en las células progenitoras [27]. Por lo tanto, los miARN modulan el equilibrio entre la apoptosis y la proliferación de estas células primarias metanéfricas [29].
Presumimos que los cambios epigenéticos desconocidos y el perfil de expresión de miARN están asociados conriñóntrastornos del desarrollo en la descendencia materna con restricción proteica. Por lo tanto, nuestro objetivo fue evaluar los patrones de miARN y la expresión génica predicha en el feto.riñóna los 17 días de gestación (17-DG) crías masculinas con restricción de proteínas para identificar vías moleculares y trastornos involucrados enrenalproliferación y diferenciación celular duranteriñóndesarrollo.
Palabras clave:insuficiencia renal; tubular renal; trastornos renales; desarrollo renal; riñón
Material y metodología
animales y dietasLos experimentos se realizaron como se describió en detalle anteriormente [5, 6] en ratas hembras y machos de la misma edad de ratas Wistar HanUnib apareadas con hermanos (250–300 g) originadas de un pie de cría suministrado por CEMIB/UNICAMP , Campinas, SP, Brasil. El ambiente y la vivienda presentaron las condiciones adecuadas para el manejo de su salud y bienestar durante el procedimiento experimental. Inmediatamente después del destete a las tres semanas de edad, los animales se mantuvieron a temperatura controlada (25 ˚C) y condiciones de iluminación (07:00–19:00 h) con libre acceso a agua del grifo y comida estándar para roedores de laboratorio (Purina Nuvital , Curitiba, PR, Brasil: contenido de Na más: 135 ± 3 μEq/g; contenido de K más: 293 ± 5 μEq/g), durante 12 semanas antes de la reproducción. El Comité Institucional de Ética en el Uso de Animales de la Universidad Estatal de São Paulo (#446-CEUA/UNESP) aprobó el protocolo experimental y durante toda la investigación se siguieron las directrices generales establecidas por el Colegio Brasileño de Experimentación Animal. Se designó el día 1 del embarazo como el día en que el frotis vaginal exhibió espermatozoides. Luego, las madres se mantuvieron ad libitum durante todo el embarazo con una comida isocalórica de laboratorio para roedores con contenido estándar de proteína [NP, n=36] (17 por ciento de proteína) o bajo contenido de proteína [LP, n=51 ] (6 por ciento de proteína). El consumo de alimento materno de NP y LP se determinó diariamente (posteriormente normalizado para el peso corporal), y el peso corporal de las madres se registró semanalmente en ambos grupos. A los 17 días de gestación (17-DG), las madres fueron anestesiadas con ketamina (75 mg/kg) y xilazina (10 mg/kg), y se expuso el útero. Los fetos fueron retirados e inmediatamente sacrificados por decapitación. Los fetos se pesaron y se recolectaron la cola y las extremidades para sexarlos. El metanefros se recolectó para análisis de secuenciación de próxima generación (NGS), RT-qPCR e inmunohistoquímica.

LA CITANCHE MEJORARÁ LA INSUFICIENCIA RENAL/RENAL
Determinación del sexadoEl presente estudio se realizó solo en crías macho 17-DG, y el sexado se determinó mediante análisis de secuencia de PCR (reacción en cadena de la polimerasa) convencional de Sry. El ADN se extrajo por lisis enzimática con proteinasa K y Fenol-Cloroformo. Para la reacción se utilizó Master Mix Colorless—Promega, con las condiciones de ciclado del fabricante. Integrated DNA Technologies (IDT) sintetizó el cebador siguiendo las siguientes secuencias: Directo: 5'-TACAGCCTGAGGACATATTA-3'Reverso: 5'-GCACTTTAACCCTTCGATTAG-3'.
Extracción de ARN totalEl ARN se extrajo de NP (n=4) y LP (n=4) enterosriñonesutilizando el reactivo Trizol (Invitrogen), de acuerdo con las instrucciones especificadas por el fabricante. La cantidad total de ARN se determinó mediante la absorbancia a 260 nm utilizando un espectrofotómetro nanoVue (GE Healthcare, EE. UU.). La integridad del ARN se aseguró mediante la obtención de un Número de integridad del ARN: RIN > 8 con el bioanalizador Agilent 2100 (Agilent Technologies, Alemania) [30].
miRNA-Seq y análisis de datosLa secuenciación se realizó en la plataforma MiSeq (Illumina). El protocolo siguió las instrucciones del fabricante disponibles enBrevemente, la secuenciación incluye la construcción de bibliotecas, y se utilizó 1 ug de ARN total. En este paso se conectan los adaptadores, el de 3' y el de 5'. Después de ligar los adaptadores, se realizó una reacción de transcripción inversa para crear ADNc. Luego se amplificó mediante una reacción de PCR estándar, que utiliza cebadores que contienen un índice de secuencia para la identificación de la muestra: esta biblioteca de ADNc se sometió a electroforesis en gel de agarosa para el aislamiento de miARN. Después de la cuantificación, la concentración de la biblioteca se normalizó a 2 nM usando Tris-HCl 10 nM, pH 8,5, y la secuenciación del transcriptoma se realizó con MiSeq Reagent Kit v2 (50 ciclos).
El análisis de datos se realizó en colaboración con Tao Chen, Ph.D. de la División de Genética y Toxicología Molecular, Centro Nacional de Investigación Toxicológica, Jefferson, AR, EE. UU. Los datos de Next Generation Sequencing (NGS) de miRNAs se generaron en formato FASTA y se importaron a BaseSpace.com (Illumina, EE. UU.). La calidad de los datos se evaluó utilizando el software CASAVA llamado base desarrollado por el fabricante (Illumina). Los análisis se realizaron mediante BaseSpace miRNA Analysis (de la Universidad de Torino, Canadá) y el mapeo de secuencias de diferentes miRNAs mediante Small RNA (Illumina, EE. UU.) para el genoma de rata. El estudio de miARN expresado diferencialmente se analizó utilizando el software Ingenuity Pathway Analysis (Ingenuity, EE. UU.).
validación de la expresión de miARNSe usaron cuatro crías macho de diferentes camadas en cada grupo para el miARN (miR{{0}}p, -144-3p, -298-5p, let-7a{{ 4}}p, -181a-5p, -181c-3p, y -199a-5p) análisis de expresiones. En resumen, 450 ng de ARN se transcribieron de forma inversa, sin amplificación previa, utilizando el kit de transcripción inversa de microARN TaqMan1, de acuerdo con las directrices del fabricante. El ADN complementario (ADNc) se amplificó utilizando TaqMan MicroRNA Assays (Life Technologies, EE. UU.) con TaqMan1 Universal PCR Master Mix, No AmpErase1 UNG (2x) en StepOnePlusTM Real-Time PCR System (Applied BiosystemsTM), según las instrucciones del fabricante. El análisis de datos se realizó utilizando la expresión génica relativa evaluada mediante el método de cuantificación comparativa (Pfaffl, 2001). Basado en el análisis de estabilidad, el snRNA U6 y el scaRNA U87 se usaron como gen de referencia. Todas las cuantificaciones relativas se evaluaron utilizando el software DataAssist, v 3.0, utilizando el método ΔΔCT. Los datos de miARN se han generado siguiendo las directrices de MIQE [31].

CISTANCHE MEJORARÁ LA FUNCIÓN RENAL/RENAL
RT-qPCR de genes diana predichosPara la síntesis de ADNc se utilizó el kit de transcripción inversa de ADNc de alta capacidad (Life Technologies, EE. UU.). Las reacciones de RT-qPCR para Bax, Bim, Caspase-3, Collagen 1, GDNF, PCNA, TGF -1, Bcl-2, Bcl-6, c-Myc, c -ret, ciclina A, Map2k2, PRDM1, Six-2, Ki-67, MTOR, -catenina, ZEB1, ZEB2, NOTCH1 e IGF1 fue realizado por SYBR Green Master Mix (Life Technologies, EE. UU. ) proporcionada por IDT1 Integrated DNA Technologies (Tabla 1). Las reacciones se realizaron en un volumen total de 20 μL utilizando 2 μL de ADNc (diluido 1:30), 10 μL de SYBER Green Master Mix (Life Technologies, EE. UU.) y 4 μL de cada cebador específico (5 nM). La amplificación y la detección se realizaron utilizando el sistema de PCR en tiempo real StepOnePlusTM (Applied BiosystemsTM). Los valores de Ct se convirtieron en valores de expresión relativa utilizando el método ΔΔCt con datos de metanefros descendientes normalizados con GAPDH como gen de referencia [32].
inmunohistoquímica,Se extrajo el feto (n {{0}} por grupo) y se fijó inmediatamente en paraformaldehído al 4 por ciento (fosfato 0,1 M, pH 7,4). Los materiales fueron deshidratados, diafanizados e incluidos en paraplast, y los bloques fueron cortados en secciones de 5-μm de espesor. Las secciones histológicas fueron desparafinadas y procesadas para inmunofluorescencia e inmunoperoxidasa. Las secciones fueron

incubados con una solución de bloqueo (8 por ciento de suero fetal bovino, 2,5 por ciento de albúmina bovina y 2 por ciento de leche desnatada en polvo en PBS). Posteriormente, fije con el anticuerpo primario (anti-Six-2) diluido en PBS que contiene leche descremada al 1 por ciento durante la noche en refrigeración. Después de lavar con PBS, las secciones se incubaron con un anticuerpo secundario específico, conjugado con el fluoróforo Alexa 488, diluido en el mismo tampón, que contenía leche al 1 por ciento durante 2 horas a temperatura ambiente. Después de lavados sucesivos con PBS, los portaobjetos se montaron con cubreobjetos utilizando el medio de montaje fluorescente Vectashield (Vector Laboratories, Inc. Burlingame). La fluorescencia en la muestra se detectó mediante microscopía confocal láser. Las imágenes se obtuvieron utilizando el sistema Focus Imagecorder Plus. Para las proteínas c-Myc, Ki-67, Bcl-2, TGF -1, -catenina, ZEB1, ZEB2, Caspasa 3 escindida, ciclina A y WT1, se realizó inmunohistoquímica. Los portaobjetos se hidrataron, y luego de ser lavados en PBS pH 7.2 por 5 minutos, se realizó la recuperación antigénica con tampón citrato pH 6.0 por 25 minutos en olla a presión. Los portaobjetos se lavaron en PBS. Posteriormente, se realizó bloqueo de peroxidasa endógena con peróxido de hidrógeno y metanol durante 10 minutos en la oscuridad. Las secciones se volvieron a lavar en PBS. Luego se siguió el bloqueo de la unión no específica y los portaobjetos se incubaron con una solución de bloqueo (5 por ciento de leche desnatada en polvo, en PBS) durante 1 hora. Las secciones se incubaron con el anticuerpo primario (Tabla 2), diluido en BSA al 1 por ciento durante la noche en el refrigerador. Después de lavar con PBS, las secciones se expusieron al anticuerpo secundario específico durante 2 horas a temperatura ambiente. Los portaobjetos se lavaron con PBS. Los cortes se revelaron con DAB (tetrahidrocloruro de 3,3'-diaminobencidina, Sigma-Aldrich CO1, EE. UU.). Después de sucesivos lavados con agua corriente, los portaobjetos fueron contrateñidos con hematoxilina, deshidratados y montados con cubreobjetos utilizando Entellan1. Las imágenes se obtuvieron usando el fotomicroscopio (Olympus BX51) o un Zeiss LSM 780-NLO confocal en un microscopio Axio Observer Z.1 (Carl Zeiss AG, Alemania) del Instituto Nacional de Ciencia y Tecnología en Fotónica Aplicada a la Célula. Biología (INFABIC) de la Universidad Estadual de Campinas.

Cuantificación de morfologíaParafina 5 μmriñónlas secciones se analizaron utilizando el software CellSens Dimension de un fotomicroscopio (Olympus BX51). losriñónSe accedió a cortes para determinar el área nefrogénica, la proteína CM y UB y el número de células, la hematoxilina-eosina teñida en 17-DG LP fetus (n=5) en comparación con la descendencia NP de la misma edad (n {{4 }}) de diferentes madres. Cuantificamos todos los CM y UB de cada metanefros analizados (4NP y 4LP de diferentes madres), y el análisis estadístico se realizó mediante la prueba t, y los valores se expresaron como media ± DE. Se consideró significativo el p�0.05. GraphPad Prism v01 Software, Inc., EE. UU., se utilizó para el análisis estadístico y la construcción de figuras.
análisis estadísticoSe utilizó la prueba t y los valores se expresaron como media ± desviación estándar (DE). P�0.05 se consideró significativo. Se utilizó el software GraphPad Prisma v. 01 (GraphPad Software, Inc., EE. UU.) para el análisis estadístico y la construcción de figuras.
Resultados
Expresión de miRNAs por miRNA-SeqComprender los cambios en el microARN asociados con el bajo contenido proteico maternorenalprogramación, realizamos la expresión de un análisis de perfil de miARN global. Se identificaron 44 miARN desregulados (p � 0.05), de los cuales 19 y 25 miARN, respectivamente, estaban regulados al alza o a la baja (Tabla 3). Los miARN expresados con más frecuencia y sus funciones, vías y redes se identificaron mediante el software Ingenuity (Tabla 4).
Validación de la expresión de miARNEn los animales del grupo LP, Let-7a-5p, miR-181a-5p, miR-181c-3p estaban regulados al alza, mientras que miR-127-3p, miR-144-3p y miR-199a-5p estaban regulados a la baja en relación con los animales NP. Los resultados no muestran ninguna diferencia en la expresión de miR-298, comparando ambos grupos (Fig. 1). La Tabla 5 reveló los valores obtenidos por la secuenciación de miRNAs con los datos de validación de RT-qPCR. Aunque se observó una diferencia significativa en la expresión de miARN en LP en relación con la descendencia de NP, el cambio de pliegue (FC) de los miARN validados fue similar a ambas técnicas.



dianas del gen miARN
Los genes de expresión de objetivos predichos de diferentes miARN como Six-2, Bcl-2, PRDM1, ciclina A, PCNA, GDNF, Colágeno 1, Caspasa 3 y Bim en LP no difirieron significativamente de NP feto. Sin embargo, Bax, TGF -1 Bcl-6, c-ret, Map2k2, Ki-67, mTOR, -catenina, ZEB1, ZEB2 y la expresión génica de IGF1 aumentaron en el {{15 }}Grupo DG LP en comparación con controles de la misma edad. Por el contrario, c-Myc y NOTHC1 se regularon a la baja en la descendencia materna con restricción de proteínas (Fig. 2).

Masa corporal del feto y morfometría metanefrosLa masa corporal 17-DG LP no difirió de la descendencia NP de la misma edad. Sin embargo, el mesénquima del metanefros de LP mostró un área reducida del 7,6 por ciento y una reducción del grosor de la corteza del 29 por ciento que el grupo NP (Fig. 3).inmunohistoquímicaEn el presente estudio, el feto LP mostró una reducción significativa (alrededor del 69 por ciento) de la fluorescencia Six-2 cap que la descendencia NP (Fig. 4).


El análisis de inmunoperoxidasa Six-2 demostró un número de células reducido (14 por ciento) en LP CM asociado con un 28 por ciento de células Six-2 plus reducidas en relación con el área de la tapa en comparación con la descendencia NP (Fig. 4). El presente estudio también mostró una reducción porcentual significativa de c-Myc CM y células inmunoteñidas UB (menos del 14 por ciento) en LP en relación con la descendencia NP (Fig. 4). Además, el porcentaje de área marcada con Ki-67 en CM fue un 48 % menor en fetos LP en comparación con NP, mientras que la inmunorreactividad de Bcl-2 y caspasa escindida-3 no fue diferente de ambos grupos (Figs. 5 y 6). El presente estudio también mostró una reducción porcentual significativa de c-Myc CM y células inmunoteñidas UB (menos del 14 por ciento) en LP en relación con la descendencia NP (Fig. 4). Además, el porcentaje de área marcada con Ki-67 en CM fue un 48 por ciento menor en LP en comparación con el feto NP, mientras que la inmunorreactividad de Bcl-2 y caspasa escindida-3 no fue diferente de ambos grupos (Figs. 5 y 6). Por otro lado, en LP, las áreas marcadas con catenina CM y UB aumentaron en un 154 y 85 por ciento, respectivamente, en comparación con las disponibles en la descendencia NP (Fig. 7). Al mismo tiempo, la distribución de inmunorreactividad de mTOR también ocupó un área significativamente más extensa en LP CM (139 por ciento) y UB (104 por ciento) que en el feto NP (Fig. 7). En la descendencia LP, el TGF -1 en la tinción de células UBS aumentó (alrededor del 30 por ciento), mientras que en el CM, las células inmunoteñidas no fueron diferentes en relación con el grupo NP (Fig. 8). El metanefros teñido ZEB1, ubicado en las células del núcleo CM, mejoró un 30 por ciento en LP en comparación con el feto NP (Fig. 8). Simultáneamente, la inmunofluorescencia de ZEB2, aunque presente en estructuras de metanefros completas, fue similar en ambos grupos experimentales (Fig. 8). El estudio actual, teniendo en cuenta la expresión de miARN y ARNm y las proteínas



Discusión
Ha aumentado el conocimiento sobre los mecanismos celulares y moleculares de la nefrogénesis [33-37]. Sin embargo, muchos factores reguladores y vías de señalización involucradas enrenalontogénesis siguen sin estar claros [38]. Los miARN juegan un papel crucial en la regulación de la expresión génica duranterenaldesarrollo [25, 39–41]. Hasta donde sabemos, no se han realizado análisis de expresión de miARN y ARNm en la ingesta de LP materna 17-DG células mesénquima masculinas. Proponemos un nuevo mecanismo molecular involucrado en la inhibición de la nefrogénesis temprana, lo que resulta en una reducción del número de nefronas. Usamos NGS para evaluar la expresión de miARN y descubrimos que 19 miARN estaban regulados hacia arriba y 25 hacia abajo en 17-DG LP en comparación con NP metanefros. Entre los 10 miARN desregulados principales, seleccionamos 7 miARN con objetivos biológicos involucrados en la proliferación, diferenciación y apoptosis celular. Tanto el análisis de datos de miRNA-Seq como el de TaqMan revelaron cambios consistentes y específicos en la expresión de miRNA en animales LP en relación con los animales control NP de la misma edad.
La familia miR-181 está compuesta por cuatro miembros muy conservados, a saber, miR-181a, miR-181b, miR-181c y miR-181d [ 42]. En las células neoplásicas, miR-181a actúa como un supresor de tumores, inhibiendo la proliferación y migración celular e induciendo la apoptosis celular [43]. Este estudio reveló una mayor expresión de miR-181a-5p en 17-DG LP en relación con la descendencia NP de la misma edad. Aunque la expresión de ARNm de caspasa no se alteró, un aumento del doble en la proporción de ARNm de Bax/Bcl-2 en LP en comparación con la descendencia NP sugiere un aumento de la apoptosis en el CM, lo que indica que la apoptosis se regula postranscripcionalmente. Los estudios han demostrado que la familia BCL promueve la liberación de citocromos de las mitocondrias y luego inhibe la activación de Casp3, lo que inhibe la apoptosis celular [44]. Li et al. usó un modelo de lesión pulmonar aguda para revelar que la sobreexpresión de miR-181a está relacionada con la disminución del nivel de proteína Bcl-2; por el contrario, la inhibición de miR-181a aumentó los niveles de Bcl-2 [45]. Este estudio confirmó los resultados de Lv et al., quienes demostraron que miR-181c regula negativamente la expresión de Six-2 y la proliferación celular, en paralelo a la pérdida del fenotipo de células mesenquimales duranteriñóndesarrollo en descendencia LP 17-DG [25].
Xiang et al. demostró que el aumento de la expresión de miR-144 suprimerenalproliferación del carcinoma, lo que resulta en una fase G2/M más corta. Además, Xiang et al. reveló que la sobreexpresión de miR-144 inhibe la expresión del gen y la proteína mTOR [46]. Nijland et al. demostraron que un aumento en la señalización de mTOR es crucial para determinar el número de nefronas en embriones cuyas madres fueron sometidas a restricción de nutrientes [47]. El objetivo de los mamíferos del complejo de rapamicina 1 (mTORC1) es esencial para el desarrollo del embrión; sin embargo, aún se desconoce cómo este complejo regula el equilibrio entre el crecimiento y la autofagia en condiciones fisiológicas y estrés ambiental [48]. Por lo tanto, la señalización de mTOR puede estar involucrada en las respuestas celulares en animales expuestos a la ingesta de LP durante la gestación; en la percepción, inducción y terminación de la autofagia; y en respuesta a la disponibilidad de nutrientes intracelulares [46]. Hipotéticamente, durante la restricción severa de proteínas, la expresión reducida de miR-144-3p puede estar asociada con una mayor expresión de mTOR, aproximadamente 139 por ciento y 104 por ciento en células CM y UB, respectivamente, para compensar la pérdida de nefronas en el {{ 11}}Descendencia de DG LP Chen et al. definió miR-127 como un nuevo regulador de la senescencia celular a través de Bcl-6 [49]. Pan et al. informó que la subexpresión de miR-127 se correlaciona con una mayor proliferación celular en las células hepáticas [50]. Este estudio mostró una disminución en la proliferación celular y una reducción significativa de células marcadas positivamente para Ki-67 en el CM de animales con restricción de proteínas. Además, se observó una reducción en el área nefrogénica y proliferación en la progenie de LP, lo cual fue consistente con los resultados de Menendez-Castro et al. en el 8,4 por ciento de la progenie con restricción de proteínas [51, 52]. Por lo tanto, el aumento de la expresión de ARNm de Ki-67 y Bcl-6, acompañado de una expresión reducida de miR-127-3p en la tapa 17-DG LP, podría estar asociado con mecanismos contrarreguladores para mantener proliferación.


sol et al. demostraron que la sobreexpresión de miR-199a-5p reduce la proliferación celular quística e induce la apoptosis, además de controlar el ciclo celular [53]. En este estudio, la expresión de miR-199a-5p se reduce en 17-DG LP se acompaña de una mayor transcripción de Ki-67, un marcador de proliferación celular, y Map2k2 se asocia con una menor reactividad de Ki-67 en metanefros LP 17-DG. Así, la desnutrición gestacional promueve la diferenciación a través de un mecanismo postranscripcional. En particular, nuestros resultados revelan un papel represor de la homeobox 1 (ZEB1) de unión a caja E con dedos de zinc, un inductor de EMT, que mantiene la pluripotencia de las células madre durante la diferenciación de células madre embrionarias. Se sabe que la -catenina activa la transcripción nuclear de ZEB1, lo que resulta en la expresión de ZEB1 [34]. La vía de señalización de TGF, una de las vías mejor estudiadas, puede inducir EMT durante el desarrollo embrionario. Se requieren varios ligandos similares a TGF para el desarrollo embrionario. Sin embargo, no todos los efectos mediados por TGF en EMT dependen de ZEB1/2, las células knockout pueden inducir la expresión de los genes mesenquimales fibronectina y N-cadherina. Sin embargo, la E-cadherina ya no está regulada a la baja y también se forman fibras de actina [54]. Karner et al. informó que duranterenaldesarrollo, el Wnt9b/ -catenina

La ruta de señalización, expresada tanto en UB como en CM, es necesaria tanto para la renovación como para la diferenciación de las células progenitoras de nefronas, siendo esencial para la formación de nefronas durante la embriogénesis [55]. La vía Wnt9b/ -catenina conservada evolutivamente desempeña un papel fundamental en el desarrollo de órganos, tejidos y reparación de lesiones en organismos pluricelulares. Un estudio demostró que c-Myc es un objetivo transcripcional de -catenina, que regula la proliferación y diferenciación derenalepitelio tubular [56]. La expresión de -catenina a nivel génico y proteico aumentó durante los periodos estudiados derenaldesarrollo en el feto 17-DG LP. Pan et al. informó que Myc coopera con -catenina para promover la renovación de las células progenitoras de nefronas [10]. Aquí, en comparación con la descendencia NP de la misma edad, LP mostró una menor expresión de c-Myc. Por lo tanto, estos animales pueden tener una menor reserva de células renovables necesarias para la proliferación y supervivencia y pueden reflejar el menor número de nefronas en el modelo LP. Es más,

Las vías de señales de Wnt/ -catenina y Notch pueden coordinar la regulación de la expresión de Six-2 y están involucradas en la regulación a la baja de la expresión de Six-2 en las células progenitoras de nefronas. Los estudios han demostrado que se pueden requerir niveles bajos de -catenina para mantener la expresión de Six-2 y las células progenitoras de CM en el estado indiferenciado; además, los niveles elevados de -catenina determinan el destino de las células progenitoras de la nefrona [57, 58]. Por lo tanto, planteamos la hipótesis de que la señalización reducida de cMyc y Notch, acompañada de una mayor expresión de -catenina, redujo la expresión de Six-2 en un 28 % en la descendencia de 17-DG LP y se correlacionó con la diferenciación temprana de células CM y la reducción de células madre y número de nefronas en la edad adulta. Además, nuestros datos pueden sostener que, en las células MM descendientes de LP, el aumento de la expresión Let-7a-5p y -catenina y la señal reducida de Notch pueden modular c-Myc, Six-2, y la expresión de Ki-67, lo que conduce a una reducción en la autorrenovación de las células progenitoras. El agotamiento de las células progenitoras restantes de CM conduce a una reducción en el número de nefronas y al desarrollo de hipertensión arterial yrenaltrastornos en la edad adulta (Fig. 10). De acuerdo con lo de Boivin et al., Nuestros resultados indican que el aumento de CM-catenina interrumpe el crecimiento y la nefrogénesis de UB [59]. Los estudios han demostrado que el factor de crecimiento neurotrófico derivado de la glía (GDNF), un regulador crucial del crecimiento de UB, emite señales a través del receptor de tirosina quinasa c-Ret y el correceptor Gfra1 [60, 61]. En la descendencia 17-DG LP, una cantidad significativa
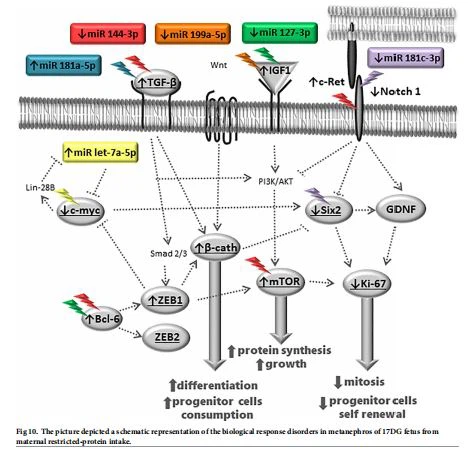
el aumento en el ARNm que codifica el receptor c-Ret conduciría teóricamente a un aumento en el crecimiento de UB. Sin embargo, en este estudio, la expresión de GDNF no cambió, lo que sugiere que, a pesar de un aumento en el ARNm de cRet, se redujo la ramificación de UB. Anteriormente, observamos una reducción del 28,3 % en las ramas de las yemas ureterales después de 14,5 días de restricción proteica gestacional [4], lo que podría estar asociado con una reducción del 28 % en el etiquetado Six-2 de las células MM, a pesar de que no hubo cambios en el GDNF transcripción. -catenina probablemente interactúa con el receptor c-ret y se transporta al núcleo de la célula UB, promoviendo la expresión de TGF -1 en las células epiteliales, inhibiendo la ramificación UB y provocando la diferenciación prematura de la célula progenitora CM, como se ve en {{11} Descendencia de }DG LP [62–64]. Por lo tanto, GDNF puede no ser esencial en la mediación de señales mesenquimatosas al brote ureteral; sin embargo, el mecanismo queda por dilucidar. De hecho, hemos demostrado que MM de la descendencia 17-DG LP mostró un aumento específico en la expresión de miARN Let-7, lo que resultó en una alteración significativariñóndesarrollo, lo que confirma el papel modulador de estos genes en el momento del desarrollo de la nefrogénesis [65].
En los estudios iniciales del factor de crecimiento similar a la insulina (IGF), las funciones predominantes de IGF-1 y -2 en el crecimiento fetal fueron aclaradas por evidencia abundante, pero en su mayoría indirecta. Se descubrió que los IGF actúan como factores de proliferación y diferenciación en células fetales cultivadas y embriones preimplantados. Además, se descubrió que los IGF son secretados por células fetales cultivadas y explantes in vitro [66]. Los factores de crecimiento, incluido el IGF, pueden provocar una transición epitelial-mesenquimatosa parcial o total. La activación de las vías de IGF da como resultado la regulación positiva de la EMT al inducir la expresión de ZEB1 [67]. Aunque varios factores de crecimiento candidatos están involucrados enriñóndesarrollo, se desconoce si están involucrados en la nefrogénesis. Es posible que se necesiten diferentes factores de crecimiento en diferentes momentos. Algunos factores de crecimiento pueden ser redundantes en este contexto. Durante el desarrollo embrionario, se necesitan rondas secuenciales de EMT y MET para diferenciar tipos de células especializadas y crear una estructura tridimensional. En este estudio, se encontró que la interconvertibilidad mesenquimatosa-epitelial mantiene la plasticidad celular, lo que sugiere la presencia de un sistema altamente inducible en condiciones de LP para el embrión. La expresión de la familia de miARN Let-7 se ha estudiado ampliamente en varios tejidos fetales. El aumento en la expresión de miARN Let-7 está relacionado con la reducción de la proliferación y el aumento temprano de la diferenciación de células MM y, en consecuencia, la disminución del número de nefronas [27, 15, 68–71]. Se ha demostrado una mayor expresión de Let-7 en organismos superiores durante la última fase de la embriogénesis cerebral en roedores [72, 73]. Nagalakshmi et al. reveló que la expresión de Let-7 miARN cambió el destino de las células epiteliales UB de precursor a estado diferenciado [71]. Por el contrario, Yermalovich et al. demostraron que la sobreexpresión de Lin28b, una proteína de unión a ARN, está asociada con los miARN Let-7 supresores. Aunque lin28 y Let-7 son reguladores conocidos del tiempo ontogénico en invertebrados, el papel de estos en el desarrollo de órganos de mamíferos no se comprende [65]. En este estudio, el aumento en la expresión de miARN Let-7a-5p en el feto LP podría estar asociado con una proliferación reducida de células CM, lo que compromete la nefrogénesis en relación con el grupo NP. Por lo tanto, planteamos la hipótesis de que la supresión de la proliferación de células CM y el cese temprano de la nefrogénesis causada por el aumento de miARN Let-7 pueden ocurrir directa o indirectamente a través de la expresión reducida transitoria de Lin28b en 17-DG LP. Este efecto puede perjudicar significativamenteriñóndesarrollo en 17-DG LP, lo que confirma que este gen regula el tiempo de desarrollo durante la nefrogénesis. En este estudio, el aumento de la expresión de miARN Let-7a-5p coincide con una disminución en la expresión de c-Myc. Myc participa en la proliferación, el crecimiento, la apoptosis y la diferenciación celular duranterenalorganogénesis [74-76]. En la descendencia LP 17-DG, la expresión del gen MM c-Myc se redujo, y el área de inmunorreactividad de CM c-Myc fue un 14 por ciento más pequeña en comparación con la descendencia NP. Simultáneamente, se observó una disminución del 14 por ciento en el número de células CM para disminuir el 48 por ciento de inmunorreactividad Ki-67 en LP en relación con la descendencia NP. Consistentemente, los estudios han demostrado que c-Myc juega un papel importante en la fase final de la ramificación de UB y en la estimulación de la proliferación de células progenitoras de CM [74].

LA CITANCHE MEJORARÁ LA INFECCIÓN RENAL/RENAL
nivel reducido en las células madre, manteniéndolas en un estado indiferenciado. Sin embargo, en este estudio, la fuerte expresión de Let-7a-5p miRNA en el CM reguló a la baja la expresión de c-Myc, lo que redujo la proliferación de células progenitoras y la diferenciación celular temprana en el LP 17-DG descendencia (Fig. 10). Estudios sobre elriñonesde ratones transgénicos c-Myc reveló una disminución simultánea de células CM inmunopositivas c-Myc y S-ix-2 asociada con una proliferación reducida de células madre [74]. Este estudio muestra una reducción significativa (28 por ciento) en seis-2 células positivas, unrenalmarcador de células madre, como la disminución observada en el número de nefronas, en el CM de la descendencia 17-DG LP en comparación con el de la descendencia NP. En 2009, Fogelgren et al. demostró que la expresión del gen Six-2 se reduce durante la ontogénesis fetal cuando se asocia con un número reducido de nefronas, hipertensión y enfermedad crónica.insuficiencia renal[77]. Por lo tanto, la expresión reducida del gen Six-2 en las células progenitoras de CM indica la supresión de la diferenciación inducida por señales duranterenaldesarrollo en la descendencia 17-DG LP. Sin embargo, la redundancia debe usarse con precaución: los defectos sutiles en la nefrogénesis pueden hacerse evidentes con un análisis más detallado o bajo diferentes condiciones. Los niveles de ARNm de IGF1 fueron más altos durante el período inicial del desarrollo metanéfrico, y se detectaron transcripciones en todo el MM, mientras que sus niveles disminuyeron durante el desarrollo posterior. Sin embargo, duranteriñónLa embriogénesis, un delicado equilibrio entre los factores de crecimiento facilitadores de nefronas (IGF1) y los factores de crecimiento inhibidores (TGF -1) regula la ramificación de UB.

Conclusión
Aunque varios autores han estudiado la nefrogénesis [34, 37, 78], se sabe poco sobre los mecanismos que determinan el número de nefronas. Este estudio demuestra que muchos miARN, ARNm y proteínas de células progenitoras de MM están alterados en la descendencia 17-DG LP, lo que conduce a una proliferación reducida y una diferenciación celular temprana (Fig. 11). Este delicado equilibrio entre la renovación y diferenciación de progenitores de nefronas es esencial parariñóndesarrollo debido a que la falta de lograr un número adecuado de nefronas es un factor de riesgo para la enfermedad crónicarenaltrastorno.
