Sensores de rejilla de fibra de larga duración para aplicaciones químicas y biomédicas
Oct 25, 2023
Abstracto: Los biosensores de fibra óptica (OFBS) se proponen cada vez más debido a sus ventajas intrínsecas sobre los sensores convencionales, incluida su compacidad, su potencial control remoto y su inmunidad a las interferencias electromagnéticas. Esta revisión presenta sistemáticamente los avances de OFBS basados en rejillas de fibra de período largo (LPFG) para aplicaciones químicas y biomédicas desde la perspectiva del diseño y la funcionalización. La sensibilidad de dicho sensor se puede mejorar diseñando el dispositivo para que funcione en el punto de inflexión de dispersión o cerca de él, evitando la transición de modo o su combinación. Además, se resumen en detalle varios métodos de funcionalización comunes, como la inmovilización covalente de silanización 3-aminopropiltrietoxisilano (APTES) y funcionalización de óxido de grafeno (GO), y la inmovilización no covalente del método de ensamblaje capa por capa. Además, también se han introducido sensores reflectantes basados en LPFG con diferentes configuraciones. Este trabajo tiene como objetivo proporcionar una comprensión integral de los biosensores basados en LPFG y sugerir algunas direcciones futuras para la exploración.

cistanche tubulosa-mejora el sistema inmunológico
Palabras clave: biosensores; sensor de fibra óptica; rejillas de fibra de larga duración; mejora de la sensibilidad; método de funcionalización
1. Introducción
Los biosensores desempeñan un papel crucial en el seguimiento de la salud humana y ambiental mediante la detección eficiente y precisa de la química y la biomasa. Un biosensor normalmente contiene dos componentes principales: un biorreceptor y un transductor [1]. Al diseñar un biosensor, un paso tecnológico clave es seleccionar el material sensible adecuado para el objetivo biológico. Teniendo en cuenta las propiedades de los compuestos resultantes, otro paso importante es seleccionar el transductor de acuerdo con los cambios químicos o físicos causados por la interacción molecular entre la diana biológica y el biorreceptor. La producción o consumo de luz, calor y sustancias químicas durante el proceso de reconocimiento se convierte en señales mensurables [2]. Según estos mecanismos, se puede seleccionar el transductor apropiado. La información que generan los procesos de reconocimiento es diversa; por ello, se han estudiado ampliamente los sensores basados en electroquímica, termótica y óptica. Los sensores ópticos, especialmente los basados en fibras ópticas, se proponen cada vez más en aplicaciones químicas y biomédicas debido a sus ventajas intrínsecas sobre los sensores convencionales. Los biosensores de fibra óptica (OFBS) suelen ser compactos y de tamaño pequeño [3] y, por tanto, pueden funcionar con volúmenes mínimos de muestra. Además, los OFBS son capaces de multiplexarse, son inmunes a las interferencias electromagnéticas [4] y son controlables de forma remota. El número de publicaciones sobre OFBS también ha aumentado constantemente durante las últimas dos décadas (como se muestra en la Figura 1). El principio de funcionamiento típico de OFBS se basa en monitorear el cambio del índice de refracción circundante (SRI), producido a partir de la unión del objetivo biológico en la superficie de la fibra, lo que conduce a la alteración del espectro detectable [5]. Para mejorar su sensibilidad al SRI, los OFBS generalmente se mecanizan en microestructuras y se modifican geométricamente para generar un fuerte campo evanescente en el área de detección.

Beneficios de la cistanche tubulosa-fortalecer el sistema inmunológico
Ejemplos de tales dispositivos incluyen fibras ópticas cónicas y en forma de U [6-10], fibras ópticas en forma de D [11,12], rejillas de Bragg (FBG) de fibra grabada o inclinada [13-15], rejillas de fibra de período largo ( LPFG) [16–20], resonancias en modo con pérdida (LMR) [21,22], resonancia de plasmón superficial (SPR) [23,24] interferómetros Mach-Zehnder (MZI) [25,26], fibra de cristal fotónico (PCF ) [27,28] y dispositivos Lab-on-Fiber [29–31]. Entre estas, algunas fibras geométricamente modificadas deben eliminar total o parcialmente el revestimiento, lo que afecta la robustez de las fibras ópticas, propiedad que debe considerarse en aplicaciones prácticas. Afortunadamente, una alternativa ideal para evitar esta dañina operación es la modulación del índice de refracción en el interior de la fibra óptica; la fibra basada en rejilla mantiene una estructura robusta y una alta sensibilidad, especialmente los LPFG, que se han utilizado ampliamente en la detección del índice de refracción, incluida la detección de moléculas bioquímicas [32,33], la detección de gases [34-36] y la detección de iones [37,38]. ].

Figura 1. El crecimiento de las publicaciones en función de los años para la OFBS. Datos de Web of Science
En esta revisión, centramos la atención en sensores basados en LPFG para aplicaciones químicas y biomédicas desde la perspectiva del diseño y la funcionalización. En primer lugar, se introduce sistemáticamente el principio de los biosensores basados en GLP. Luego, se resumen varios métodos para mejorar la sensibilidad de dicho sensor y se ilustran sus aplicaciones en el campo de la bioquímica. Además, describimos categóricamente en detalle las aplicaciones de biodetección de dicho sensor de acuerdo con varios métodos de funcionalización típicos. Finalmente, resumimos esta revisión y sugerimos algunas direcciones futuras para la exploración.
2. Principio de los biosensores basados en LPFG
Un LPFG es una modulación periódica (generalmente con un período Λ {{0}}–1000 µm) de RI en el núcleo de la fibra, como se muestra en la Figura 2; la modulación puede acoplar la luz desde el modo de núcleo fundamental (modo LP01) a los modos de revestimiento de propagación hacia adelante (modos LP0 m, donde m=2, 3, 4,...) y, por lo tanto, produce un conjunto de señales resonantes. bandas de atenuación centradas en longitudes de onda discretas en el espectro de transmisión LPFG [18]. Además, la condición de coincidencia de fase entre las constantes de propagación efectiva del modo LP01 y los modos LP0 m se puede expresar mediante [39]:
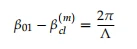
donde 01 y (m) cl son las constantes de propagación para los modos LP01 y LP0 m, respectivamente. Λ es el período de rejilla. Para el RI (neff) efectivo del modo LP01 y los modos LP0 m, se pueden expresar como ne ff ,co= 2 01 π λ y n (m) eff ,clad=(m) cl λ 2π, respectivamente. En este caso, las longitudes de onda resonantes (λres) están determinadas por el RI efectivo del modo LP01 y los modos LP0 m, y podemos obtener la siguiente expresión [40]:
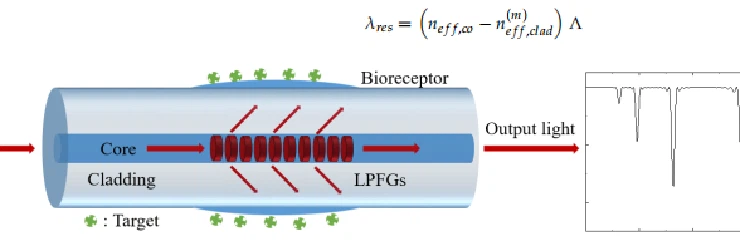
Figura 2. Ilustración esquemática de OFBS basado en un LPFG
Para un LPFG específico, Λ puede ser una constante, y ne ff, co está determinado por el RI del núcleo y el revestimiento, mientras que n (m) eff, clad depende de la diferencia entre el revestimiento RI y SRI del revestimiento. Por lo tanto, la característica de resonancia se ve afectada por el RI efectivo de la región de revestimiento, que es el principio básico de la detección biológica. De esta manera, un cambio en la longitud de onda de resonancia puede representarse mediante los cambios del SRI causados por la interacción molecular que ocurre en la superficie de la fibra. Naturalmente, se puede lograr un biosensor basado en LPFG equipando el sensor con recubrimientos químicamente sensibles para detectar selectivamente los objetivos biológicos.
3. Mejora de la sensibilidad RI del biosensor basado en LPFG
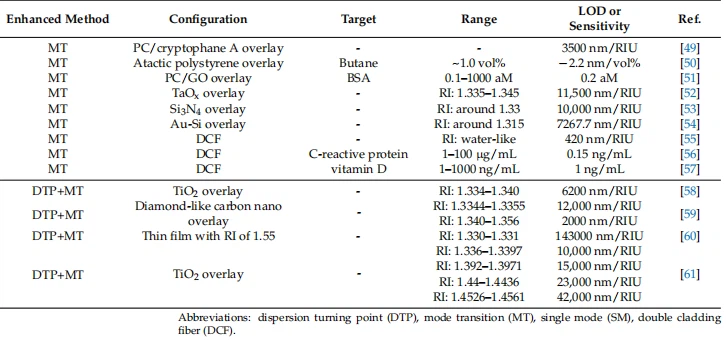
Para diseñar un biosensor basado en LPFG, el trabajo más importante debería centrarse en cómo mejorar la sensibilidad de dicho sensor. Además, una investigación detallada muestra que el mejor rendimiento de los sensores basados en la sensibilidad del RI se puede lograr cuando el SRI está cerca del RI del revestimiento (es decir, 1,44–1,46 RIU) [41]. Cabe señalar que la mayoría de los biosensores están diseñados para funcionar en soluciones acuosas (es decir, 1,33–1,34 RIU), que es muy diferente del RI del revestimiento de fibra, lo que hace que el dispositivo muestre una baja sensibilidad a las muestras acuosas. Para abordar este desafío, se han propuesto varios enfoques a lo largo de los años. El rendimiento de estos métodos para biosensores basados en LPFG se resume en la Tabla 1.
Tabla 1. Comparación de diferentes métodos para mejorar los biosensores basados en LPFG.

Tabla 1. Cont.
3.1. Punto de inflexión de la dispersión
La metodología más popular es diseñar un período y un modo de revestimiento en o cerca del punto de inflexión de dispersión (DTP) de acuerdo con su curva de coincidencia de fase (PMC), acoplando así el modo de núcleo de propagación hacia adelante con un modo de revestimiento de alto orden [62 ]. Como se muestra en la Figura 3, el PMC demuestra la relación entre el período de rejilla y la longitud de onda de resonancia, y el DTP se puede observar en el PMC para cada modo de revestimiento, donde la pendiente para el modo de orden superior cambia de positiva a negativa como la longitud de onda aumenta. Por lo tanto, para un período de rejilla determinado, dos longitudes de onda resonantes a cada lado del DTP se acoplan a un modo de revestimiento, formando resonancias de doble pico. La diferencia espectral entre los picos duales puede ser el parámetro de medición, debido a que su longitud de onda cambia con la respuesta de los LPFG al cambio del SRI. En nuestro trabajo anterior [18], verificamos teóricamente que la sensibilidad máxima de los LPFG al SRI se puede obtener en o cerca del DTP. Los sensores basados en LPFG diseñados cerca de su DTP se han utilizado ampliamente en el campo de la detección bioquímica a lo largo de los años, debido a su alta sensibilidad a muestras acuosas. Sin embargo, cabe señalar que el LPFG basado en un sensor DTP con banda ancha se divide en resonancias de doble pico cuando el dispositivo se sumerge en un entorno con un RI superior al del aire (es decir, agua). En este caso, el dispositivo puede tener un factor de sensibilidad bajo, debido a que la longitud de onda resonante está lejos del DTP. Para aliviar este problema, el grupo de P. Biswas ha demostrado teórica y experimentalmente que la sensibilidad se puede mejorar adaptando la fuerza de acoplamiento inicial del modo de revestimiento a un modo de revestimiento específico de orden superior en el DTP [63]. F. Chiavaioli et al. informaron sobre un biosensor basado en LPFG cerca de su DTP, con un período de rejilla de 165 µm, para la detección de anti-IgG [42]. La Figura 4a muestra el resultado de la simulación de la dependencia entre el PMC para el modo de revestimiento LP0,12 y el diámetro del revestimiento de fibra. La línea negra continua corresponde a la fibra no grabada; el diámetro del revestimiento se grabó con una solución de ácido fluorhídrico al 1%. La Figura 4b muestra la evolución espectral de un LPFG con dos bandas de resonancia durante el proceso de grabado. Los espectros de transmisión del LPFG con dos bandas de resonancia se pudieron obtener antes del proceso de grabado (dclad=125 µm) y durante el grabado con bandas más cercanas (dclad=124.6 µm y 124,2 µm). Al reducir aún más el diámetro del revestimiento a 123,8 µm, las bandas de resonancia duales se convirtieron en una banda de resonancia única y más amplia (es decir, hasta el DTP). Luego desaparecía si se reducía continuamente el diámetro del revestimiento. En la evaluación del rendimiento del biosensor, se adoptó el copolímero Eudragit L100 como capa químicamente modificada para proporcionar grupos funcionales carboxilo libres para inmovilizar la IgG. El sensor basado en LPFG obtenido se llevó a cabo en suero humano, donde se midió la detección de concentraciones de anti-IgG tan bajas como 70 µg/l (460 pM).
![Figure 3. Calculated variation of mode resonance wavelength with LPFG period. (a) Modes m = 1 to m = 10. (b) Modes m = 11 to m = 20. (c) Modes m = 21 to m = 30. The small circles locate the turning points of the slopes of the curves, and the LPFG exhibits the greatest sensitivity in the region between the two dotted lines. Adopted with from [18]. Under a Creative Commons license. Figure 3. Calculated variation of mode resonance wavelength with LPFG period. (a) Modes m = 1 to m = 10. (b) Modes m = 11 to m = 20. (c) Modes m = 21 to m = 30. The small circles locate the turning points of the slopes of the curves, and the LPFG exhibits the greatest sensitivity in the region between the two dotted lines. Adopted with from [18]. Under a Creative Commons license.](/Content/uploads/2023842169/202310241202439a04da7b955d4b4eb83686d74047ccbe.png)
Figura 3. Variación calculada de la longitud de onda de resonancia del modo con el período LPFG. (a) Modos m=1 a m=10. (b) Modos m=11 a m=20. (c) Modos m=21 a m=30. Los círculos pequeños localizan los puntos de inflexión de las pendientes de las curvas, y el LPFG muestra la mayor sensibilidad en la región entre las dos líneas de puntos. Adoptado con de [18]. Bajo licencia Creative Commons.
Además de ajustar el LPFG a un modo de revestimiento específico de orden superior en el DTP reduciendo el diámetro del revestimiento, también se ha adoptado la modulación del espesor de la capa funcional. El grupo de Korposh [43] propuso un biosensor basado en LPFG que utiliza biotina como biorreceptor para la detección de estreptavidina (SV). Como se muestra en la Figura 5, las nanopartículas de núcleo de sílice y cubierta de oro (SiO2:Au NP) se recubrieron sobre fibras utilizando el método capa por capa con la ayuda de una capa de policatión de poli (clorhidrato de alilamina) (PAH). Fue conveniente sintonizar el biosensor basado en LPFG que opera en el DTP mediante el método de deposición capa por capa. El diámetro de las NP de SiO2 también se controló para estudiar el efecto sobre la sensibilidad, y el resultado indica que las NP de SiO2 más grandes (es decir, 300 nm) exhibieron una mayor sensibilidad. Podría contribuir a la onda evanescente más eficiente en las NP de SiO2 de 300 nm de diámetro. Además, las NP de SiO2 más grandes eran más propicias para el depósito de biotina, mejorando así la capacidad de adsorción de SV. Finalmente, lograron la detección de SV con la concentración medida más baja de 2,5 nM, y este sensor propuesto podría aplicarse para apuntar a compuestos proteicos clínicamente relevantes, necesitando solo reemplazar el ligando.
![Figure 5. Schematic illustration of the layer-by-layer deposition of a (PAH/SiO2:Au)2 film onto an LPFG. Adopted from [43]. Under a Creative Commons license. Figure 5. Schematic illustration of the layer-by-layer deposition of a (PAH/SiO2:Au)2 film onto an LPFG. Adopted from [43]. Under a Creative Commons license.](/Content/uploads/2023842169/20231024120328a82c9ae5eb18424fbe913f41b84b0985.png)
Figura 5. Ilustración esquemática de la deposición capa por capa de una película (PAH/SiO2:Au)2 sobre un LPFG. Adoptado de [43]. Bajo licencia Creative Commons.
Por otro lado, se ha demostrado que puede ocurrir un modo de revestimiento de orden inferior cerca del DTP al reducir el diámetro del revestimiento, y luego se obtiene una capacidad más sensible debido a la mejora del campo evanescente [44]. Iluminado por esto, recientemente, ha habido una propuesta interesante para diseñar un modo de revestimiento de orden más bajo (modo de revestimiento LP0,2) de un LPFG cerca del DTP, para obtener un dispositivo de alta sensibilidad [47]. Se fabricó un LPFG cerca del DTP, seguido de grabar el diámetro del revestimiento hasta 20 µm, hasta la aparición del modo LP0,2 cerca del DTP. El dispositivo propuesto se integró en una celda de flujo cerrada dentro de un rango SRI de 1,333 a 1,3335 RIU para realizar pruebas, lo que generó una sensibilidad de 8751 nm/SRIU. Aunque mostró un excelente rendimiento como refractómetro, se deben considerar muchos factores relevantes en la biodetección real. Sobre la base de lo anterior, el mismo grupo desarrolló el dispositivo anterior utilizando IgG/antiIgG como un par de bioconjugados para una aplicación de biodetección, logrando un límite de detección (LOD) de 0,16 ng/ml (1,06 pM) [48]. En una palabra, los sensores basados en LPFG diseñados en o cerca de su DTP se han utilizado ampliamente en la detección de inmunoglobulinas [42,46,64], bacterias [16,45,65,66], ADN [67-69] y otros objetivos [70–74].

Beneficios del suplemento cistanche: aumentar la inmunidad.
3.2. Efecto de transición de modo
Como se mencionó en la introducción, la detección bioquímica se realiza detectando los cambios del SRI cuando las capas de biorreceptores depositadas en la región de la rejilla interactúan con el objetivo. Este principio se debe esencialmente al hecho de que una pequeña porción del campo del modo de revestimiento, el campo evanescente, se propaga hacia el exterior de la fibra e interactúa con el entorno externo, lo que resulta en n (m) eff, cambios de revestimiento, que dependen de el espesor de la región de interacción y la profundidad de penetración del campo evanescente [75]. El efecto de transición de modo (MT) se ha propuesto para optimizar la sensibilidad de los sensores basados en LPFG a los cambios del SRI. Puede ocurrir recubriendo la superficie del revestimiento de fibra con un espesor adecuado de materiales con alto RI (HRI). Del Villar et al. han creado una teoría integral y un método numérico en su literatura [76]. Demostró que los recubrimientos HRI podrían modificar uno de los modos de revestimiento, lo que resulta en la transición entre los modos guiados por revestimiento de orden inferior (es decir, con un índice de refracción efectivo más alto) a los modos guiados por revestimiento y, de ahora en adelante, cambia los valores de n (m) eff, clad, que podría aprovecharse para mejorar la sensibilidad de los sensores. El mismo año, Andrea Cusano et al. Confirmó experimentalmente una redistribución de los modos de revestimiento mediante el depósito uniforme de recubrimientos HRI a nanoescala a lo largo del LPFG y su efecto sobre la sensibilidad RI [77]. Iluminados por esto, Yang et al. [49] fabricaron un sensor de metano basado en LPFG, trabajando en MT con deposición superpuesta HRI de policarbonato (PC)/criptofano A. Utilizaron una técnica de recubrimiento por inmersión automática para ajustar el punto de trabajo del sensor en la región MT (RI a granel). la sensibilidad fue de 3,56 × 103 nm/RIU). La detección de metano se realizó con una alta sensibilidad de 2,5 nm/% y LOD de 0.2 % (v/v). El grupo de Esposito informó sobre un sensor basado en LPFG de un solo extremo para la detección de gas butano, modificado con una superposición HRI de poliestireno atáctico de tamaño nanométrico [50]. Mediante la optimización del rango de espesor de capa se pudo ajustar el punto de trabajo del dispositivo dentro de la región MT. La detección de vapor de butano se realizó con concentraciones de hasta 1,0 % en volumen, lo que da como resultado una sensibilidad de 2,2 nm/% en volumen y tiene la capacidad de detectar concentraciones tan bajas como una décima parte de butano por debajo del límite explosivo. El mismo grupo de investigación también fabricó un sensor basado en LPFG de estructura multicapa; El diagrama de estructura se muestra en la Figura 6a [51]. La capa consta de una película de PC y una capa mucho más delgada de óxido de grafeno (GO), donde el espesor nanométrico de la película de PC se controló de manera flexible mediante la técnica de recubrimiento por inmersión, a fin de ajustar el dispositivo para que funcione en la región MT. La Figura 6b muestra el cambio de longitud de onda de la banda de atenuación en función del espesor de la PC, el aire de funcionamiento y la solución de PBS como entorno. La segunda capa de GO fue aprovechada por sus propiedades de biocompatibilidad y abundantes grupos funcionales, lo que le dio al dispositivo la capacidad de unir moléculas biométricas; luego, se eligió el sistema de alta afinidad estreptavidina-biotina para evaluar el desempeño del dispositivo mediante la detección de BSA biotinilada, logrando un LOD de 0,2 aM.
![Figure 6. (a) The structure of multilayer fibers. (b) Numerical wavelength shift of the attenuation band versus PC overlay thickness. Reprinted with permission from [51]. Copyright © 2018 Elsevier B.V. Figure 6. (a) The structure of multilayer fibers. (b) Numerical wavelength shift of the attenuation band versus PC overlay thickness. Reprinted with permission from [51]. Copyright © 2018 Elsevier B.V.](/Content/uploads/2023842169/20231024120421a03f2093dc8340d4bd37e615143c47c4.png)
Figura 6. (a) La estructura de las fibras multicapa. (b) Cambio numérico de longitud de onda de la banda de atenuación versus el espesor de superposición de PC. Reimpreso con autorización de [51]. Copyright © 2018 Elsevier BV
Además de utilizar materiales orgánicos HRI como recubrimientos, también se han seleccionado muchos materiales inorgánicos para ajustar el punto de trabajo en la región MT. Las principales ventajas de los materiales de recubrimiento inorgánicos son que hay un mayor rango disponible de valores de RI y más técnicas de crecimiento y que es más fácil obtener un espesor uniforme en comparación con los materiales orgánicos. Piestrzy 'nska et al. informaron sobre un biosensor sin etiquetas basado en LPFG, depositado con una fina capa de óxido de tantalio (TaOx) para la sensibilidad RI. Dado que el RI de TaOx era tan alto como 2 en el rango espectral IR, el espesor de la superposición se controló con precisión en el subnanometro, utilizando la técnica de deposición de capas atómicas. La sensibilidad RI de los sensores basados en LPFG obtenidos fue de 11,500 nm/RIU en el rango RI de 1,335 a 1,345 RIU [52]. Continuamente, el grupo de Saha estudió teóricamente el fenómeno del revestimiento MT recubriéndolo con una capa HRI de Si3N4; el resultado mostró que la sensibilidad del RI era superior a 100 µm/RIU para la solución acuosa (es decir, RI= 1.33) [53]. Otra contribución reciente del grupo de Li., que utilizó un sensor basado en LPFG recubierto con películas delgadas de Au-Si para la detección de RI, fue el logro de una sensibilidad ultraalta de 7267,7 nm/RIU (es decir, alrededor de RI= 1. 315); atribuyeron este excelente rendimiento a la MT de los modos de revestimiento EH y a un fuerte campo evanescente que penetra los alrededores [54]. Aunque se han explotado varios tipos de materiales de recubrimiento, desde orgánicos hasta inorgánicos, todavía tienen un efecto negativo en el dispositivo obtenido, incluida su repetibilidad, estabilidad a largo plazo y pérdida de absorción [55]. Por lo tanto, se ha empleado una nueva estrategia mediante el uso de fibra de doble revestimiento (DCF) con un perfil RI en forma de W. El grupo Esposito se dio cuenta del efecto MT para la sensibilidad RI escribiendo por primera vez el LPFG fabricado en un DCF en forma de W. El revestimiento exterior RI del DCF era más alto que el revestimiento interior; por lo tanto, el revestimiento exterior del DCF actuó de manera similar al revestimiento HRI. Para ajustar el punto de trabajo a la región MT de este consejo, el revestimiento exterior fue grabado con un reactivo químico. Finalmente, la atención se centró en la sensibilidad SRI, logrando una sensibilidad de 420 nm/RIU en entornos similares al agua, lo que confirmó que este dispositivo podría usarse para detección bioquímica sin un recubrimiento HRI [55]. Posteriormente, desarrollaron y probaron este dispositivo de estructura especial, mediante el recubrimiento con una capa de GO a nanoescala para ofrecer grupos funcionales para unir covalentemente el anticuerpo. Se logró un rango de trabajo de 1 ng/ml a 100 µg/ml y un LOD de 0,15 ng/ml para la detección de proteína C reactiva en suero [56]. Recientemente, el mismo grupo informó sobre un biosensor DCF similar para la detección de vitamina D. Como se muestra en la Figura 7, también se seleccionó el GO nanométrico para proporcionar grupos funcionales carboxílicos para la inmovilización covalente de Anti-VitD3. Se obtuvo la detección selectiva con un rango de 1 a 1000 ng/ml en solución tampón, y estos dispositivos también funcionaron bien en un medio complejo con proteínas que interfieren [57].

Figura 7. Imagen esquemática para la detección de vitamina D basada en un LPFG en DCF con capa GO
3.3. La combinación de estos enfoques
Cuando los dispositivos LPFG se aplican a la detección bioquímica, se enfrentan a un rango de RI variable. Por ejemplo, para que el biorreceptor convencional (p. ej., proteína, ADN, anticuerpo) detecte un bioobjetivo (p. ej., proteína, antígeno), el SRI varía de 1,333 a 1,353 RIU [12,45]. Sin embargo, para el LPFG modificado con gelatina como sensor de humedad, el SRI varía desde 1.3408 RIU hasta el RI del revestimiento [78].
De manera similar, el efecto MT puede guiar uno de los modos de revestimiento a modos guiados por revestimiento, y se puede ajustar un rango de sensibilidad específico mediante el ajuste preciso del espesor y la reducción del diámetro del revestimiento [59,61]. Indica que la combinación del efecto DTP y MT puede mejorar las propiedades de detección de los LPFG, incluida la alta sensibilidad y el rango de trabajo SRI especificado. Por ejemplo, el grupo de Mateusz obtuvo una sensibilidad de RI de 2000 nm/RIU en un rango de RI más amplio (1,34–1,356 RIU) [59]. En este trabajo, el diámetro del revestimiento y el espesor del revestimiento se controlaron en un rango nanométrico para alcanzar los efectos DTP y MT, utilizando el método de grabado de iones reactivos (RIE) y deposición química de vapor mejorada con plasma de radiofrecuencia. Además, muchos trabajos publicados demostraron que la sensibilidad también podría mejorarse reduciendo el diámetro del sensor basado en LPFG [42,79]. Iluminado por esto, Del Villar combinó el diámetro del revestimiento con el efecto DTP y MT para optimizar la sensibilidad al SRI [60]. Se utilizó un método numérico basado en el cálculo exacto de los modos de núcleo y revestimiento y la teoría de modos acoplados para analizar la optimización de un LPFG basado en los tres factores anteriores. Finalmente, se obtuvo una sensibilidad considerable de 143 × 103 nm/RIU, que se esperaba que mejorara la resolución de los sensores químicos y biológicos basados en LPFG. Recientemente, Fang et al. también combinó adecuadamente los efectos DTP y MT utilizando TiO2 como nanopelícula de alto RI depositada mediante tecnología de deposición de capas atómicas [61]. Para mantener constante la diferencia espectral de los picos duales, se seleccionó el período de rejilla apropiado en diferentes LPFG y se investigaron diferentes espesores de TiO2 para optimizar la sensibilidad en un rango SRI específico. Como se muestra en la Figura 8, mostró una sensibilidad SRI de 10,000 nm/RIU en el rango de 1,336–1,3397 RIU, 42,000 nm/RIU en el rango de 1,4526–1,4561 RIU, 15 ,000 nm/RIU en el rango de 1,392 a 1,3971 RIU y 23 000 nm/RIU en el rango de 1,44 a 1,4436 RIU. De la Figura 8c,d, se indica que se podrían realizar dos rangos de alta sensibilidad en el mismo dispositivo LPFG.
![Figure 8. Transmission spectra and resonance wavelength shift in different ranges of SRI. (a) 65 nm TiO2 nanofilm, Λ = 230.5 µm. (b) 15 nm TiO2 nanofilm, Λ = 237 µm. (c,d) 50 nm TiO2 nanofilm, Λ = 230 µm. Adopted from [61]. Under a Creative Commons license. Figure 8. Transmission spectra and resonance wavelength shift in different ranges of SRI. (a) 65 nm TiO2 nanofilm, Λ = 230.5 µm. (b) 15 nm TiO2 nanofilm, Λ = 237 µm. (c,d) 50 nm TiO2 nanofilm, Λ = 230 µm. Adopted from [61]. Under a Creative Commons license.](/Content/uploads/2023842169/202310241208135e764e099e7045839ff3e06c3e3077df.png)
Figura 8. Espectros de transmisión y cambio de longitud de onda de resonancia en diferentes rangos de SRI. (a) Nanopelícula de TiO2 de 65 nm, Λ=230.5 µm. (b) Nanopelícula de TiO2 de 15 nm, Λ=237 µm. (c,d) Nanopelícula de TiO2 de 50 nm, Λ=230 µm. Adoptado de [61]. Bajo licencia Creative Commons.
4. La funcionalización de biosensores basados en LPFG
Es importante señalar que el biosensor basado en LPFG se aplica para medir el cambio de longitud de onda causado por el cambio de RI de la superficie del dispositivo debido a la adsorción selectiva de las moléculas objetivo en la superficie, en lugar de medir el cambio de longitud de onda causado por el cambio. del RI del medio circundante a granel. Por tanto, la funcionalización del biosensor basado en LPFG es un paso fundamental para realizar aplicaciones bioquímicas. Generalmente, se depositan capas funcionales de dos partes sobre la superficie del biosensor basado en LPFG: una parte es la capa portadora utilizada como inmovilización del biorreceptor y la otra es la capa de biorreceptor utilizada como elemento de reconocimiento (enzimas, proteínas, anticuerpos, etc.) para capturar selectivamente el objetivo. Por tanto, se han empleado diversos métodos para la inmovilización de la capa de biorreceptor sobre la fibra óptica. La comparación entre el biorreceptor, el objetivo y el rendimiento de los diferentes métodos de funcionalización de biosensores basados en LPFG se puede ver en la Tabla 2.
Tabla 2. Comparación de diferentes informes de la funcionalización de biosensores basados en LPFG

4.1. APTES Silanizati
El método más eficaz para la funcionalización de biosensores basados en LPFG se basa en la inmovilización covalente, debido a su unión permanente al biorreceptor. La silanización de 3- 3-aminopropiltrietoxisilano (APTES) es un método común e ideal utilizado en la mayoría de las modificaciones químicas de sustratos de sílice. Este método se realizó con éxito para la inmovilización covalente de la proteína [101,102], ADN [67,68], anticuerpos [17,82,103], etc. En este caso, la fibra óptica requiere un paso de pretratamiento para formar grupos silanol (Si-OH), mediante inmersión en KOH/NaOH, ácido o solución de piraña. De manera similar, los grupos etoxi (–OCH2CH3) existentes en la molécula APTES también pueden formar Si-OH a través de una reacción de hidrólisis en ambientes acuosos [104]. Luego, la condensación entre Si-OH conduce a la formación de un enlace siloxano (Si-O-Si), permitiendo que las moléculas APTES se inmovilicen en la superficie de la fibra. Además, las moléculas APTES adyacentes pueden formar una matriz polimérica mediante condensación, lo que da como resultado la formación de superficies aminofuncionales libres (–NH2) de sustratos de sílice [105]. Una vez lograda la silanización, existe un paso de activación de los grupos carboxilo en anticuerpos o enzimas, con la ayuda de clorhidrato de 1-etil-3-(3-dimetilaminopropil)carbodiimida (EDC) y N-hidroxisuccinimida (NHS). Luego, los anticuerpos o enzimas se pueden unir a los grupos –NH2 mediante la formación de enlaces amida, enlaces de hidrógeno o interacciones electrostáticas [106]. El grupo Anjli propuso un biosensor enzimático basado en LPFG mediante la unión covalente estable de la enzima lipasa para la detección de triacilglicéridos [80]. La Figura 9 muestra la etapa de inmovilización de la enzima lipasa; la enzima lipasa se unió a la superficie de la fibra formando enlaces amida entre los grupos –NH2 de la fibra y los grupos –COOH de la enzima. El cambio de longitud de onda se midió en asociación con la enzima que interactúa con el objetivo. Se midió la detección de concentraciones de triacilglicéridos tan bajas como 17,71 mg/dL; También se realizó una prueba específica en sangre humana y todo el experimento se realizó a una temperatura constante de 37 ◦C. Wu también realizó la silanización APTES para inmovilizar la glucosa oxidasa [81]. En este trabajo, la glucosa oxidasa se inmovilizó en el LPFG en forma de S mediante tecnología de silanización APTES y se utilizó como biorreceptor para la detección de glucosa. La variación de la pérdida de transmisión se utilizó como medida asociada con la glucosa oxidasa y la unión específica de la glucosa. Los resultados experimentales muestran que el sensor propuesto tuvo una sensibilidad de 6.229 dB/% en peso en un rango de 0∼ a 1% en peso. Más recientemente, Gan et al. [39] desarrollaron un sensor basado en LPFG basado en anticuerpos de yema de huevo (IgY) inmovilizados covalentemente mediante silanización APTES para la detección de Staphylococcus aureus. La prueba de detección se pudo completar en aproximadamente 20 minutos y la detección de Staphylococcus aureus se realizó hasta 33 UFC/mL. Por lo tanto, se esperaba que el dispositivo desarrollado para la detección de Staphylococcus aureus se aplicara al campo de la detección médica y alimentaria.
![Figure 9. Immobilization of enzymes to create the bio-recognition layer on the optical fiber probe. Reprinted with permission from [80]. Copyright © 2015 Elsevier B.V. Figure 9. Immobilization of enzymes to create the bio-recognition layer on the optical fiber probe. Reprinted with permission from [80]. Copyright © 2015 Elsevier B.V.](/Content/uploads/2023842169/20231024120933129fe213859f48b7bdc02daf9bce3114.png)
Figura 9. Inmovilización de enzimas para crear la capa de bioreconocimiento en la sonda de fibra óptica. Reimpreso con autorización de [80]. Copyright © 2015 Elsevier B.V.
4.2. Funcionalización GO
Aunque la fibra aminofuncionalizada se propone ampliamente, el grupo funcional único la hace incapaz de unirse a otros tipos de receptores biológicos, lo que limita su aplicación. Diferentes grupos de investigación han centrado su atención en GO; la superficie de la fibra se deposita química o físicamente con nanohojas GO después de la silanización. El GO es rico en grupos funcionales que contienen oxígeno, como epoxi, hidroxilo y carboxilo, que le proporcionan al GO la capacidad de unir covalentemente varias biomoléculas [107]. Además, el GO también está dotado de la capacidad de adsorber biomoléculas mediante inmovilización no covalente, como electrostática, interacción por enlaces de hidrógeno y apilamiento π – π [108,109]. Chen et al. [46] informaron sobre un LPFG de doble pico depositado con nanohojas de GO para inmovilizar la IgG y la IgG/anti-IgG como un par de bioconjugados para la inmunodetección. Adoptaron una nueva estrategia para depositar GO que se basaba en enlaces químicos seguidos de adsorción física. Se produjo un enlace químico entre la fibra silanizada APTES y GO. Mientras tanto, las nanohojas GO fueron adsorbidas físicamente en la superficie de la fibra, junto con la evaporación del agua. Finalmente, el sensor basado en LPFG depositado en GO se sumergió en una solución de IgG y se unió covalentemente mediante química de entrecruzamiento EDC/NHS. La detección de anti-IgG se obtuvo hasta una concentración de 7 ng/ml en tampón PBS. La reutilización del sensor también se llevó a cabo eliminando la anti-IgG unida. Sucesivamente, el mismo grupo desarrolló la detección de hemoglobina, basada en un sensor basado en LPFG funcionalizado con nanohojas GO [85]. Como se muestra en la Figura 10, el enlace químico seguido de una estrategia de adsorción física también se adoptó para depositar GO, y el principio de detección se basó en la medición de la variación en la intensidad de resonancia, causada por la interacción no covalente entre las moléculas de hemoglobina y GO. El espesor de GO deseable se controló a 501,8 nm, lo que proporcionó una interacción significativa entre la luz y la materia entre el campo evanescente y las moléculas objetivo. El sensor desarrollado se realizó con una sensibilidad de −77 dB/RIU y un LOD de 0,05 mg/ml para la detección de hemoglobina.
![Figure 10. Schematic of GO deposition on LPFG-based device. (a) The process of alkaline treatment, (b) APTES silanization, (c) the epoxy group of GO reacted with an amino group of APTES-silanized fiber surface, and (d) GO nanosheets were deposited onto the fiber surface. Reprinted with permission from [85]. Copyright © 2018 Elsevier B.V. Figure 10. Schematic of GO deposition on LPFG-based device. (a) The process of alkaline treatment, (b) APTES silanization, (c) the epoxy group of GO reacted with an amino group of APTES-silanized fiber surface, and (d) GO nanosheets were deposited onto the fiber surface. Reprinted with permission from [85]. Copyright © 2018 Elsevier B.V.](/Content/uploads/2023842169/20231024121022d5e75284481e411a8b0548de16a853e0.png)
Figura 10. Esquema de la deposición de GO en un dispositivo basado en LPFG. (a) El proceso de tratamiento alcalino, (b) silanización APTES, (c) el grupo epoxi de GO reaccionó con un grupo amino de la superficie de la fibra silanizada con APTES y (d) se depositaron nanohojas de GO sobre la superficie de la fibra. Reimpreso con autorización de [85]. Copyright © 2018 Elsevier BV
Recientemente, Wang et al. han mejorado aún más los límites de detección y el método de deposición. [{{0}}}]. En este trabajo, se depositó un LPFG microcónico con nanohojas GO para la detección de hemoglobina. Después de completar el enlace químico seguido de la adsorción física, aprovecharon el efecto de pinza óptica para mejorar aún más la interacción entre las nanohojas GO y la fibra. El espesor de GO de 2 0 3,6 nm se inmovilizó sobre el LPFG microcónico. Se obtuvo el LOD de {{10}}.02 mg/ml en diversos compuestos que interfieren. Más recientemente, el mismo grupo desarrolló un biosensor con la misma estructura para la detección de albúmina sérica bovina (BSA) [87]. El mecanismo de detección se basa en medir el cambio de longitud de onda causado por el enlace covalente entre GO y BSA. Se alcanzó un LOD de 0,043 mg/ml, 0,029 mg/ml y 0,032 mg/ml en agua desionizada, urea y glucosa, respectivamente. De manera similar, también propusieron un LPFG micro-cónico funcionalizado por nanocompuestos de GO/polidopamina para la detección de iones de cobalto [88]; Los nanocompuestos se depositaron sobre la superficie micro-cónica del LPFG debido a la silanización APTES seguida del efecto de pinzas ópticas. El sensor propuesto mostró una sensibilidad de 2,4 × 10−3 dB/ppb en el rango de concentración de iones cobalto de 1 ppb a 107 ppb, y se alcanzó un límite de detección de concentraciones tan bajas como 0,17 ppb. Los sensores micro-cónicos basados en LPFG funcionalizados por GO también se han implementado para la detección de iones Na+ y Mn2+ en [110] y la detección de iones Ni2+ en [89].

cistanche tubulosa-mejora el sistema inmunológico
Haga clic aquí para ver los productos Cistanche Enhance Immunity
【Pregunte por más】 Correo electrónico:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
4.3. Método de ensamblaje capa por capa
El método de modificación covalente de fibras presentado anteriormente tiene buena estabilidad; sin embargo, es más complicado controlar el espesor, como controlar la concentración y el tiempo de reacción. La realización de un recubrimiento funcional con un espesor controlable también es un factor a considerar al optimizar la sensibilidad de detección del dispositivo basado en LPFG. El ensamblaje capa por capa (LbL) proporciona una forma prometedora de depositar con precisión un recubrimiento funcional con un espesor de escala nanométrica [70,111], impulsado por interacciones electrostáticas entre polielectrolitos con carga opuesta [112,113]. El grupo de Tian [90] desarrolló un sensor de salinidad basado en LPFG recubierto con capacidad de respuesta de fuerza iónica de multicapas de polielectrolito de quitosano (CHI)/poli (ácido acrílico) (PAA) mediante el método de ensamblaje LbL. Todo el proceso de deposición se repitió 20 veces mediante la inmersión del dispositivo en un policatión CHI y un polianión PAA, respectivamente. Curiosamente, el cambio de longitud de onda de resonancia del LPFG cambió de rojo a azul al aumentar la concentración de sal. Podría explicarse por la hinchazón o deshinchamiento del recubrimiento en respuesta a un rango diferente de concentración de NaCl. La sensibilidad de 36 nm/M se obtuvo en el rango de 0.5 a 0,8 M. También se esperaba que esta investigación se aplicara a la biomedicina y la administración de fármacos. De manera similar, el mismo grupo también propuso un sensor de salinidad recubierto con hidrogel sensible a la fuerza iónica en el LPFG [91]. Los polielectrolitos de dos componentes depositados por el ensamblaje LbL podrían causar algunos problemas, es decir, sensibilidad cruzada del pH y relaciones no lineales entre el cambio de longitud de onda de resonancia y la concentración de salinidad. Como se muestra en la Figura 11, este trabajo fabricó un nuevo sensor recubierto con un hidrogel de poli (4-vinilpiridina) (qP4VP) cuaternizado mediante un ensamblaje LbL, seguido de reticulación química. Vale la pena señalar que el polianión PAA se liberó selectivamente del recubrimiento después de la reticulación química para obtener un hidrogel de un solo componente. El sensor desarrollado exhibió una sensibilidad de 7 nm/M y hubo una buena relación lineal entre el cambio de longitud de onda de resonancia y la concentración de salinidad en el rango de 0,4 a 0,8 M.
![Figure 11. Fabrication of a q37P4VP hydrogel coating. Adopted from [91]. Under a Creative Commons license Figure 11. Fabrication of a q37P4VP hydrogel coating. Adopted from [91]. Under a Creative Commons license](/Content/uploads/2023842169/202310241211208cda190a504a499a99d026f1495ce6c4.png)
Figura 11. Fabricación de un recubrimiento de hidrogel q37P4VP. Adoptado de [91]. Bajo una licencia Creative Commons
También se depositaron otros recubrimientos funcionales de polielectrolitos sobre un biosensor basado en LPFG mediante el método de ensamblaje LbL. Lee et al fabricaron un biosensor basado en LPFG recubierto con una película delgada nanoensamblada de poli (cloruro de dialil dimetilamonio) (PDDA) y tetrakis (4-sulfofenil) porfina (TSPP) mediante la técnica LbL para la detección de gas amoníaco. Alabama. [92]. El grupo de Abd-Rahman fabricó una capa de recubrimiento de nanopartículas de PDDA/poli (sulfonato de sodio-p-estireno) (PSS)-Au sobre una superficie de LPFG utilizando la técnica LbL para la detección de iones de mercurio (II) [93]. El sensor diseñado tuvo un rendimiento excelente en el rango de concentración de iones mercurio (II) de 0.5 ppm a 10 ppm. Liu y cols. [64] desarrollaron un biosensor basado en LPFG recubierto con poli (clorhidrato de alilamina) (PAH)/nanopartículas de sílice recubiertas de oro mediante el método LbL para la detección de estreptavidina e inmunoglobulina M (IgM). Ni et al. [94] investigaron un sensor basado en LPFG con un recubrimiento de poli (etilenimina) (PEI) y poli (ácido acrílico) (PAA) para la detección de pH; la capa de recubrimiento mejoró la dispersión y la capacidad de adhesión de los nanotubos de carbono de paredes múltiples. El grupo de Tian [95] consideró PAH/PAA como un recubrimiento funcional polielectrolítico depositado mediante ensamblaje LbL para unir anticuerpos específicos para la detección de Staphylococcus aureus. El recubrimiento funcional de polielectrolito podría facilitar la adhesión bacteriana y la detección con un LOD de 224 UFC/mL se demostró en PBS.
4.4. Otros metodos
El método de funcionalización de la fibra óptica depende hasta cierto punto del entorno de aplicación. El método de funcionalización de fibras ópticas aplicado en aire es más conciso y sencillo que el aplicado en soluciones acuosas. Por ejemplo, la técnica de recubrimiento por inmersión, que es sencilla de utilizar y facilita el control del espesor de la película sensible, se utiliza ampliamente en la detección de gases. El grupo de Feng [96] informó sobre las películas compuestas de sulfuro de molibdeno/ácido cítrico que se depositaron utilizando técnicas de sol-gel y recubrimiento por inmersión en un LPFG para medir trazas de gas de sulfuro de hidrógeno. La Figura 12 muestra las imágenes SEM de la superficie y la sección transversal del LPFG recubierto con películas compuestas de sulfuro de molibdeno/ácido cítrico. Se puede observar en la Figura 12b que el espesor de la película se controló uniformemente a 590 nm. El sensor propuesto exhibió una alta sensibilidad de 10.52 pm/ppm dentro de un rango de concentración de gas de sulfuro de hidrógeno de 0 a 70 ppm, y el gas de sulfuro de hidrógeno se detectó hasta una concentración de 0,5 ppm. . El mismo grupo también estudió el sensor cónico basado en LPFG funcionalizado con películas compuestas de sulfuro de molibdeno/ácido cítrico para la detección de gas de sulfuro de hidrógeno [114]. Se alcanzó una sensibilidad de 16,65 pm/ppm. Además, el grupo de Ding desarrolló un sensor basado en LPFG recubierto con GO para la detección de gas óxido nítrico (NO) [97]. Los recubrimientos se prepararon utilizando la técnica de recubrimiento por inmersión después de un tratamiento con una solución de HNO3 al 5 %. El sensor de NO exhibió excelentes características de detección en el rango de concentración de NO de 0 a 400 ppm. Xu et al. propusieron un sensor basado en LPFG depositado con compuestos de GO/acetato de celulosa para la detección de amoníaco [115]. Para depositar estos compuestos se utilizaron el método de reticulación química y la técnica de recubrimiento por inmersión. El sensor de amoníaco propuesto exhibió una sensibilidad excelente (98,32 pm/ppm).
![Figure 12. SEM images of (a) the side surface of the LPFG and (b) the cross section of the composite membrane-coated LPFG. Reprinted with permission from [96]. Figure 12. SEM images of (a) the side surface of the LPFG and (b) the cross section of the composite membrane-coated LPFG. Reprinted with permission from [96].](/Content/uploads/2023842169/202310241212254a1a407cc2e14a69a398363009e185e8.png)
Figura 12. Imágenes SEM de (a) la superficie lateral del LPFG y (b) la sección transversal del LPFG recubierto de membrana compuesta. Reimpreso con autorización de [96].
Además, las estructuras organometálicas (MOF), debido a sus excelentes propiedades de porosidad sintonizable, gran superficie interna y funcionalidad orgánica, se han aplicado ampliamente para funcionalizar sensores basados en LPFG para detección de gases y otros tipos de detección. Los MOF son nanomateriales cristalinos híbridos compuestos de cationes metálicos y ligandos orgánicos [116-118]. Los métodos de funcionalización de fibras ópticas con MOF se centran principalmente en la cristalización in situ [119,120]. El grupo de Korposh desarrolló un sensor de vapor orgánico basado en LPFG funcionalizado por películas de estructura de imidazol zeolítica-8 (ZIF-8) [121]. Como se muestra en la Figura 13a, las películas ZIF-8 se depositaron sobre la superficie de LPFG utilizando la técnica de cristalización in situ. El espectro de transmisión del LPFG fue monitoreado durante cada paso de modificación. El espesor uniforme del ZIF-8 se muestra en las imágenes SEM de la Figura 13b. Finalmente, este sensor propuesto se realizó con una sensibilidad de 0.015 ± {{20}}.001 y 0,018 ± 0,0015 nm/ppm y un LOD de 6,67 y 5,56. ppm para acetona y etanol, respectivamente, en [98]. El mismo grupo fabricó un sensor de dióxido de carbono (CO2) basado en LPFG modificado con una película delgada de HKUST-1 utilizando cristalización in situ y la técnica LbL [99]. La detección de CO2 se realizó con un LOD de 401 ppm. Además, los MOF también se pueden utilizar como matrices potenciales para la integración de enzimas [122]. Zhu et al. informaron que el ZIF-8 encapsulado en glucosa oxidasa (GOx) se recubría sobre el LPFG mediante cristalización in situ [100]. Se obtuvo una sensibilidad de 0,5 nm/mm en el rango de 1 a 8 mM para la detección de glucosa.
5. Sensores reflectantes basados en LPFG
Dado que un sensor basado en LPFG puede acoplar luz desde el modo de núcleo fundamental a los modos de revestimiento de propagación hacia adelante, produce un conjunto de bandas de atenuación resonantes centradas en longitudes de onda discretas en el espectro de transmisión. Una de las peculiaridades de los sensores basados en LPFG es su funcionamiento en modo de transmisión, lo que resulta inconveniente para algunas aplicaciones biológicas cuando es necesario introducirlos en viales/tubos de ensayo. Desde el punto de vista de la miniaturización, el puerto de emisión de luz y el puerto de recogida de señales deben desplegarse en la misma faceta. Además, la sensibilidad a la flexión puede interferir con la señal óptica transmitida [123]. Por lo tanto, existen algunos trabajos donde el funcionamiento en modo transmisión del LPFG se transforma en un funcionamiento en modo reflexión. Swart, PL propuso un interferómetro Michelson de sonda única basado en un LPFG donde el cambio de fase del interferómetro depende del RI del entorno [124]. Kim DW también desarrolló una sonda de fibra única basada en dos interferómetros, el LPFG en modo de reflexión para detección de RI y un interferómetro intrínseco de Fabry-Perot para medición de temperatura [125]. Aunque el sensor de interferómetro basado en LPFG funcionó en modo de reflexión, la longitud total del sensor podría ser de al menos 4 a 5 cm debido a la naturaleza del interferómetro [124,126], lo que resultaba inconveniente para la detección in vivo. Jiang et al. desarrolló un sensor LPFG reflectante compacto recubriendo solo la cara del extremo del revestimiento con una película de aluminio y luego reflejando solo los modos de revestimiento [127]. La longitud del dispositivo propuesto era normalmente de 0.5~3 cm de largo, que era la misma que la del sensor convencional basado en LPFG. Sin embargo, se utilizó el complejo proceso de recubrimiento. Rana S. et al. utilizó un método rentable de recubrimiento con brocha utilizando pasta de plata disponible para realizar un sensor LPFG reflectante. El dispositivo desarrollado se realizó con un coeficiente de sensibilidad a la temperatura de 0.046 nm/◦C en un rango entre 23 ◦C y 200 ◦C [128]. En [129], se fabricó un sensor reflectante basado en LPFG con un espejo de bucle de fibra Sagnac (SFLM) para medir el RI y la temperatura. Este dispositivo podría lograr la medición simultánea de RI y temperatura, debido a las diferentes sensibilidades a RI y temperatura del LPFG y SFLM. Otro problema inevitable de los sensores reflectantes basados en LPFG es la generación de bandas interferométricas no deseadas que se superponen a las bandas de atenuación de LPFG [130,131]. Algunos enfoques eficaces se centran en la escisión precisa al final del LPFG [123] o en el pulido después de la escisión [132] para obtener una banda de atenuación única. En [123], como se muestra en la Figura 14, el extremo de la rejilla se cortó con precisión y se cubrió con una capa reflectante. Para mejorar la sensibilidad SRI de este dispositivo, se modificó la superposición HRI del poliestireno atáctico en la superficie de la fibra. Luego, se recubrió la fibra con ácido poli (metacrilato de metilo) -com-metacrílico como una capa biofuncional para inmovilizar covalentemente el biorreceptor. La detección de lactamasas de clase C se obtuvo hasta una concentración del orden de unas pocas decenas de nM en tampón PBS.
![Figure 14. (a) Schematic view of the final reflective LPFG transducer; (b) the experimental and numerical SRI sensitivity; (c) a photograph showing the reflective LPFG biosensor probe developed in this work. Reprinted with permission from [123]. Copyright © 2016 Elsevier B.V Figure 14. (a) Schematic view of the final reflective LPFG transducer; (b) the experimental and numerical SRI sensitivity; (c) a photograph showing the reflective LPFG biosensor probe developed in this work. Reprinted with permission from [123]. Copyright © 2016 Elsevier B.V](/Content/uploads/2023842169/2023102412132225b02ba26f7f494e8334429e076bbc2c.png)
Figura 14. (a) Vista esquemática del transductor LPFG reflectante final; (b) la sensibilidad experimental y numérica del SRI; (c) una fotografía que muestra la sonda biosensora reflectante LPFG desarrollada en este trabajo. Reimpreso con autorización de [123]. Copyright © 2016 Elsevier BV
Villar ID et al. [133] propuso una forma más sencilla de obtener una única banda de atenuación; El extremo de la fibra estaba recubierto con un espejo plateado que podía absorber la energía transmitida a través de los modos de revestimiento. Más interesante aún, Dey TK et al. [101] eliminaron una porción del LPFG en una ubicación arbitraria, sin el requisito de escindir o pulir con precisión. Las bandas de resonancia no deseadas podrían eliminarse adaptando el PMC del modo de revestimiento; también se benefició al mejorar la sensibilidad RI de este dispositivo. Finalmente, se obtuvo una sensibilidad RI de ~1300 nm/RIU.
6. Conclusiones
Esta revisión destaca el principio operativo básico de los sensores basados en LPFG y sus mecanismos de sensibilización y mejora de la sensibilidad para aplicaciones químicas y biomédicas. El principio básico de los biosensores basados en LPFG es que los cambios del SRI se pueden convertir en la medición del cambio de longitud de onda de resonancia o la variación de la pérdida de transmisión. Para mejorar la sensibilidad de los biosensores basados en LPFG para aplicaciones químicas y biomédicas, se han adoptado dos metodologías principales en informes publicados recientemente. Una es diseñar un LPFG que funcione en o cerca de un DTP, lo que se puede lograr ajustando el período de la rejilla, el diámetro del revestimiento o el espesor de la capa funcional. Esta metodología tiene un buen desempeño para la detección de inmunoglobulinas, bacterias, ADN y otros objetivos. El otro es el efecto MT, que se puede lograr recubriendo la superficie del revestimiento de fibra con un espesor adecuado de materiales HRI. Se ha demostrado que esta metodología funciona bien en la detección de gases orgánicos (p. ej., metano y butano) y proteínas (p. ej., BSA biotinilada, proteína C reactiva). La combinación de estas estrategias también se revisa en este artículo. Por otro lado, la funcionalización de biosensores basados en LPFG es un paso indispensable para lograr una detección específica. Como se muestra en la Tabla 2, resumimos varios métodos de funcionalización comunes correspondientes a diferentes tipos de receptores. La silanización APTES generalmente se aplica para unir covalentemente anticuerpos o enzimas; una funcionalización adicional con GO puede ofrecer al dispositivo la capacidad de unir covalentemente más tipos de receptores debido a los abundantes grupos funcionales de GO. Además, en este artículo también se revisa el ensamblaje de LbL, el método de funcionalización no covalente. La ventaja de este método es que es más conveniente y permite controlar con precisión el espesor de la capa funcional. Este método se ha aplicado para depositar polielectrolitos para la detección de salinidad y pH, así como para la detección de iones, gases y bacterias. También se han revisado otros métodos de funcionalización (p. ej., técnicas de recubrimiento por inmersión y cristalización in situ). Además, también se han introducido sensores reflectantes basados en LPFG. Aunque los LPFG demostrados en configuraciones de reflexión exhiben menos sensibilidad, se pueden introducir en el vial/tubo de ensayo, lo cual es más conveniente y práctico para sus aplicaciones químicas o biomédicas. En esta revisión, se ha demostrado que el LPFG es una plataforma de detección prometedora para aplicaciones químicas y biomédicas. Una dirección futura significativa debería ser explotar materiales de recubrimiento innovadores y métodos de funcionalización para detectar más tipos de biomoléculas. Además, la capacidad de multiplexación inherente de OFBS debe utilizarse en sensores basados en LPFG para lograr mediciones de múltiples parámetros o múltiples objetivos escribiendo diferentes rejillas en el mismo dispositivo. En entornos de medición complejos, se deben centrar más esfuerzos en reducir o eliminar los efectos de sensibilidad cruzada (por ejemplo, temperatura, tensión) en los sensores basados en LPFG.

cistanche tubulosa-mejora el sistema inmunológico
Referencias
1. Mittal, S.; Kaur, H.; Gautama, N.; Mantha, AK Biosensores para el diagnóstico de cáncer de mama: una revisión de receptores, transductores y estrategias de amplificación de señales. Biosens. Bioelectrón. 2017, 88, 217–231. [Referencia cruzada] [PubMed]
2. Mehrotra, P. Biosensores y sus aplicaciones: una revisión. J. Oral Biol. Craneofac. Res. 2016, 6, 153–159. [Referencia cruzada]
3. Polley, N.; Basak, S.; Hass, R.; Pacholski, C. Sensores plasmónicos de fibra óptica: proporcionar plataformas de biosensores sensibles con un equipo de laboratorio mínimo. Biosens. Bioelectrón. 2019, 132, 368–374. [Referencia cruzada]
4. Roriz, P.; Silva, S.; Frazão, O.; Novais, S. Sensores de temperatura de fibra óptica y sus aplicaciones biomédicas. Sensores 2020, 20, 2113. [CrossRef]
5. Espósito, F.; Srivastava, A.; Sansone, L.; Giordano, M.; Campopiano, S.; Iadicicco, A. Biosensores sin etiquetas basados en rejillas de fibra de largo período: una revisión. IEEE Sens. J. 2021, 21, 12692–12705. [Referencia cruzada]
6. Wen, H.-Y.; Huang, C.-W.; Li, Y.-L.; Chen, J.-L.; Sí, Y.-T.; Chiang, C.-C. Un detector biosensor de fibra en forma de U para microARN. Sensores 2020, 20, 1509. [CrossRef]
7. Chen, K.-C.; Li, Y.-L.; Wu, C.-W.; Chiang, C.-C. Sensor de glucosa mediante sonda de fibra óptica en forma de U con nanopartículas de oro y glucosa oxidasa. Sensores 2018, 18, 1217. [CrossRef]
8. Liu, J.; Xing, Y.; Zhou, X.; Chen, GY; Shi, H. Sensor inmunológico fluorescente de fibra óptica en forma de U mejorado con rayos sesgados de lámina de luz para Microcystin-LR. Biosens. Bioelectrón. 2021, 176, 112902–112908. [Referencia cruzada]
9. Chen, L.; Leng, YK; Liu, B.; Liu, J.; Wan, SP; Wu, T.; Yuan, J.; Shao, L.; Gu, G.; Fu, YQJS; et al. Biosensor de fibra óptica sin etiquetas de sensibilidad ultraalta basado en un acoplador monomodo cónico, sin núcleo, para la detección de Staphylococcus aureus. Sens. Actuadores B Chem. 2020, 320, 128283. [Referencia cruzada]
10. Kumar, R.; Leng, Y.; Liu, B.; Zhou, J.; Shao, L.; Yuan, J.; Ventilador, X.; Wan, S.; Wu, T.; Liu, JJB Bioelectronics, Biosensor ultrasensible basado en microesferas magnéticas interferómetro de microfibra mejorado. Biosens. Bioelectrón. 2019, 145, 111563. [Referencia cruzada]
11. Quero, G.; Crescitelli, A.; Paladino, D.; Consales, M.; Buosciolo, A.; Giordano, M.; Cutolo, A.; Cusano, A. Rejilla de fibra de período largo de onda evanescente dentro de fibras ópticas en forma de D para la detección del índice de refracción de alta sensibilidad. Sens. Actuadores B Chem. 2011, 152, 196–205. [Referencia cruzada]
12. Jang, HS; Parque, KN; Kim, JP; Sim, SJ; Kwon, DO; Han, YG; Lee, KS Biosensor de ADN sensible basado en una rejilla de largo período formada en la superficie de la fibra pulida lateralmente. Optar. Expreso 2009, 17, 3855–3860. [Referencia cruzada] [PubMed]
13. Bekmurzayeva, A.; Dukenbayev, K.; Shaimerdenova, M.; Bekniyazov, I.; Ayupova, T.; Sypabekova, M.; Molardi, C.; Tosi, D. Biosensor de rejilla de Bragg de fibra grabada funcionalizado con aptámeros para la detección de trombina. Sensores 2018, 18, 4298. [CrossRef] [PubMed]
14. Sypabekova, M.; Korganbayev, S.; González-Vila, Á.; Caucheteur, C.; Shaimerdenova, M.; Ayupova, T.; Bekmurzayeva, A.; Vangelista, L.; Tosi, D. Aptasensor de rejilla de Bragg de fibra inclinada grabada funcionalizada para la detección de proteínas sin etiquetas. Biosens. Bioelectrón. 2019, 146, 111765. [Referencia cruzada]
15. Lobry, M.; Fasseaux, H.; Loyez, M.; Chah, K.; Goormagightigh, E.; Wattiez, R.; Chiavaioli, F.; Caucheteur, C. Biosensores de rejilla de fibra plasmónica demodulados a través de la intersección de envolturas espectrales. J. Luz. Tecnología. 2021, 39, 7288–7295. [Referencia cruzada]
16. Celebanska, A.; Chiniforooshan, Y.; Janik, M.; Mikulic, P.; Sellamuthu, B.; Perreault, J.; Bock, WJ Rejilla de fibra de larga duración decorada con carbohidratos bioinspirados para la detección de bacterias sin etiquetas. IEEE Sens. J. 2019, 19, 11965–11971. [Referencia cruzada]
17. Xiao, P.; Sol, Z.; Huang, Y.; Lin, W.; Ge, Y.; Xiao, R.; Li, K.; Li, Z.; Lu, H.; Yang, M.; et al. Desarrollo de un sensor inmunológico de microfibra óptica para el análisis del antígeno prostático específico utilizando una rejilla de difracción de alto orden y período largo. Optar. Expreso 2020, 28, 15783–15793. [Referencia cruzada]
18. Shu, X.; Zhang, L.; Bennion, I. Características de sensibilidad de las rejillas de fibra de larga duración. J. Luz. Tecnología. 2002, 20, 255–266.
19. Pilla, P.; Trono, C.; Baldini, F.; Chiavaioli, F.; Giordano, M.; Cusano, A. Sensibilidad gigante de rejillas de período largo en modo de transición cerca del punto de inflexión de dispersión: un enfoque de diseño integrado. Optar. Letón. 2012, 37, 4152–4154. [Referencia cruzada]
20. Zuppolini, S.; Quero, G.; Consales, M.; Diodato, L.; Vaiano, P.; Venturelli, A.; Santucci, M.; Spyrakis, F.; Costi, diputado; Giordano, M.; et al. Opción de fibra óptica sin etiquetas para la detección de lactamasas de clase C expresadas por bacterias resistentes a los medicamentos. Biomédica. Optar. Expreso 2017, 8, 5191–5205. [Referencia cruzada]
21. Chiavaioli, F.; Janner, D. Detección de fibra óptica con resonancias en modo con pérdida: aplicaciones y perspectivas. J. Luz. Tecnología. 2021, 39, 3855–3870. [Referencia cruzada]
22. Lin, Y.-C.; Chen, L.-Y. Aplicación sutil de resonancia en modo con pérdidas inducida por campo eléctrico para mejorar el rendimiento del biosensor óptico de guía de ondas planas. Biosensores 2021, 11, 86. [Referencia cruzada] [PubMed]
23. Wang, W.; Mai, Z.; Chen, Y.; Wang, J.; Pequeño.; Su, Q.; Li, X.; Hong, X. Un biosensor SPR de fibra óptica sin etiquetas para la detección específica de proteína C reactiva. Ciencia. Rep. 2017, 7, 16904. [CrossRef] [PubMed]
24. Huang, C.; Zhou, Y.; Yu, G.; Zeng, J.; Li, Q.; Shen, K.; Wu, X.; Guo, R.; Zhang, C.; Zheng, B. Sensor de rejillas de fibra de período largo funcionalizado con glutatión basado en resonancia de plasmón superficial para la detección de iones As3+. Nanotecnología 2021, 32, 485501. [CrossRef]
25. Chalyan, T.; Guía, R.; Pasquardini, L.; Zanetti, M.; Falke, F.; Schreuder, E.; Heideman, RG; Pederzolli, C.; Pavesi, L. Biosensores basados en interferómetro asimétrico de Mach-Zehnder para la detección de aflatoxina M1. Biosensores 2016, 6, 1. [CrossRef]
26. Janik, M.; Brzozowska, E.; Czyszczo 'n, P.; Celeba'nska, A.; Koba, M.; Gamian, A.; Bock, WJ; ´Smietana, M. Aptasensor de fibra óptica para la detección de bacterias sin etiquetas en pequeños volúmenes. Sens. Actuadores B Chem. 2021, 330, 129316. [Referencia cruzada]
27. Liu, Q.; Mamá, Z.; Wu, Q.; Wang, W. El sensor bioquímico se basa en una fibra de cristal fotónico de núcleo líquido llena de oro, plata y aluminio. Optar. Tecnología láser. 2020, 130, 106363. [Referencia cruzada]
28. Mahfuz, MA; Hossain, MA; Haque, E.; Hai, Nuevo Hampshire; Namihira, Y.; Ahmed, F. Un sensor de índice de refracción plasmónica basado en fibra de cristal fotónico, con baja pérdida de propagación y revestimiento bimetálico. Sensores 2019, 19, 3794. [CrossRef]
29. Consales, M.; Quero, G.; Spaziani, S.; Príncipe, M.; Micco, A.; Galdí, V.; Cutolo, A.; Cusano, A. Biosensores de laboratorio sobre fibra mejorados con metasuperficie. Fotónica láser Rev.2020, 14, 2000180. [CrossRef]
30. Managò, S.; Quero, G.; Zito, G.; Tullii, G.; Galeotti, F.; Pisco, M.; De Luca, AC; Cusano, A. Adaptación de optrodos SERS de laboratorio sobre fibra hacia objetivos biológicos de diferentes tamaños. Sens. Actuadores B Chem. 2021, 339, 129321. [Referencia cruzada]
31. Marco, P.; Francisco, G.; Giorgio, G.; Giuseppe, Q.; Andrea, C. Patrones periódicos autoensamblados en la punta de la fibra óptica mediante conjuntos de microesferas. En Actas de la 24ª Conferencia Internacional sobre Sensores de Fibra Óptica, Curitiba, Brasil, 28 de septiembre al 2 de octubre de 2015; pag. 96341N.
32. Badmos, AA; Sol, Q.; Sol, Z.; Zhang, J.; Yan, Z.; Lutsyk, P.; Rozhin, A.; Zhang, L. Rejilla de fibra de período largo con revestimiento delgado funcionalizada con enzimas en modo de transición en el punto de inflexión de dispersión para la detección del nivel de azúcar y glucosa. J. Biomed. Optar. 2017, 22, 027003. [Referencia cruzada]
33. Heidemann, BR; Chiamenti, I.; Oliveira, MM; Müller, M.; Fabris, JL Rejilla funcionalizada de largo período: sensor de fibra plasmónica aplicado a la detección de glifosato en agua. J. Luz. Tecnología. 2018, 36, 863–870. [Referencia cruzada]
34. Kanka, J. Diseño de rejillas de período largo con punto de inflexión en una fibra de cristal fotónico para refractometría de gases. Sens. Actuadores B Chem. 2013, 182, 16-24. [Referencia cruzada]
35. Gu, Z.; Xu, Y.; Gao, K. Rejilla de fibra óptica de larga duración con revestimiento de solgel para sensor de gas. Optar. Letón. 2006, 31, 2405–2407. [Referencia cruzada]
36. Wei, W.; Nong, J.; Zhang, G.; Tang, L.; Jiang, X.; Chen, N.; Luo, S.; Lan, G.; Zhu, Y. Sensor de resonancia de plasmón superficial de rejilla de fibra de larga duración basado en grafeno para detección de gases de alta sensibilidad. Sensores 2017, 17, 2. [CrossRef]
37. Tan, S.-Y.; Lee, SC; Kuramitz, H.; Abd-Rahman, F. Un nuevo sistema sensor híbrido de rejilla de fibra de largo período-gradiente difusivo en películas delgadas para la detección de iones de mercurio (II) en agua. Optik 2019, 194, 163040. [CrossRef]
38. Wang, J.-N. Una plataforma de sensor de rejilla de fibra de microfluidos de largo período para medir la concentración de iones cloruro. Sensores 2011, 11, 8550–8568. [Referencia cruzada]
39. Gan, W.; Xu, Z.; Li, Y.; Bi, W.; Chu, L.; Qi, Q.; Yang, Y.; Zhang, P.; Gan, N.; Dai, S.; et al. Detección rápida y sensible de Staphylococcus aureus mediante el uso de un inmunosensor de rejilla de fibra de largo período recubierto con anticuerpo de yema de huevo. Biosens. Bioelectrón. 2022, 199, 113860. [Referencia cruzada]
40. Vengsarkar, AM; Lemaire, PJ; Judkins, JB; Bhatia, V.; Erdogan, T.; Sipe, JE Rejillas de fibra de larga duración como filtros de rechazo de banda. J. Luz. Tecnología. 1996, 14, 58–65. [Referencia cruzada]
41. Patrick, HJ; Kersey, AD; Bucholtz, F. Análisis de la respuesta de rejillas de fibra de período largo al índice de refracción externo. J. Luz. Tecnología. 1998, 16, 1606–1612. [Referencia cruzada]
42. Chiavaioli, F.; Biswas, P.; Trono, C.; Bandyopadhyay, S.; Giannetti, A.; Tombelli, S.; Basumallick, N.; Dasgupta, K.; Baldini, F. Hacia una inmunodetección sensible sin etiquetas mediante rejillas de fibra de largo período con punto de inflexión. Biosens. Bioelectrón. 2014, 60, 305–310. [Referencia cruzada] [PubMed]
43. Marqués, L.; Hernández, FU; James, SO; Morgan, SP; Clark, M.; Tatam, RP; Korposh, S. Biosensor de rejilla de largo período de fibra óptica altamente sensible anclado con nanopartículas de capa de oro con núcleo de sílice. Biosens. Bioelectrón. 2016, 75, 222–231. [Referencia cruzada] [PubMed]
44. Del Villar, I.; Cruz, JL; Socorro, AB; Corres, JM; Matias, Optimización de la sensibilidad IR con rejillas de fibra de larga duración grabadas en revestimiento en el punto de inflexión de la dispersión. Optar. Expreso 2016, 24, 17680–17685. [Referencia cruzada]
45. Dandapat, K.; Tripathi, SM; Chinifooroshan, Y.; Bock, WJ; Mikulic, P. Biosensor compacto y rentable insensible a la temperatura basado en rejillas de fibra de largo período para la detección precisa de bacterias E. coli en agua. Optar. Letón. 2016, 41, 4198–4201. [Referencia cruzada]
46. Liu, C.; Cai, Q.; Xu, B.; Zhu, W.; Zhang, L.; Zhao, J.; Chen, X. Rejilla de largo período funcionalizada con óxido de grafeno para inmunodetección ultrasensible sin etiquetas. Biosens. Bioelectrón. 2017, 94, 200–206. [Referencia cruzada]
47. Dey, conocimientos tradicionales; Tombelli, S.; Biswas, P.; Giannetti, A.; Basumallick, N.; Baldini, F.; Bandyopadhyay, S.; Trono, C. Análisis del modo de revestimiento de orden más bajo de rejillas de fibra de período largo cerca del punto de inflexión. J. Luz. Tecnología. 2021, 39, 4006–4012. [Referencia cruzada]
48. Dey, conocimientos tradicionales; Tombelli, S.; Biswas, P.; Giannetti, A.; Basumallick, N.; Baldini, F.; Bandyopadhyay, S.; Trono, C. Inmunodetección sin etiquetas mediante rejillas de fibra de período largo en el modo de revestimiento de orden más bajo y cerca del punto de inflexión. Optar. Tecnología láser. 2021, 142, 107194. [Referencia cruzada]
49. Yang, J.; Zhou, L.; Huang, J.; Tao, C.; Li, X.; Chen, W. Mejora de la sensibilidad de la rejilla de fibra de período largo en modo de transición como sensor de metano utilizando una deposición superpuesta de policarbonato/criptofano de alto índice de refracción. Sens. Actuadores B Chem. 2015, 207, 477–480. [Referencia cruzada]
50. Espósito, F.; Zotti, A.; Ranjan, R.; Zuppolini, S.; Borriello, A.; Campopiano, S.; Zarrelli, M.; Iadicicco, A. Rejilla de fibra de un solo extremo de larga duración recubierta con una película delgada de poliestireno para detección de gas butano. J. Luz. Tecnología. 2018, 36, 825–832. [Referencia cruzada]
51. Espósito, F.; Sansone, L.; Taddei, C.; Campopiano, S.; Giordano, M.; Iadicicco, A. Biosensor ultrasensible basado en rejilla de largo período recubierta con multicapa de policarbonato-óxido de grafeno. Sens. Actuadores B Chem. 2018, 274, 517–526. [Referencia cruzada]
52. Piestrzy ´ska, M.; Dominik, M.; Kosiel, K.; Janczuk-Richter, M.; Szot-Karpi´ska, K.; Brzozowska, E.; Shao, L.; Niedziółka-Jonsson, J.; Bock, WJ; ´Smietana, M. Rejillas ultrasensibles de período largo nanorrecubiertas de óxido de tantalio para la detección de diversos objetivos biológicos. Biosens. Bioelectrón. 2019, 133, 8-15. [Referencia cruzada]
53. Saha, N.; Kumar, A. Sensor de índice de refracción altamente sensible basado en la transición de modo en una guía de ondas de cresta inscrita de rejilla de período largo de resonancia dual. J. Luz. Tecnología. 2019, 37, 5576–5582. [Referencia cruzada]
54. Li, Z.; Zhu, H. Rendimiento de detección de modos de guía de ondas de superficie excitados en rejillas de fibra de período largo con nanorrevestimientos de oro y silicio. Optar. Letón. 2021, 46, 266–269. [Referencia cruzada] [PubMed]
55. Espósito, F.; Srivastava, A.; Sansone, L.; Giordano, M.; Campopiano, S.; Iadicicco, A. Mejora de la sensibilidad en rejillas de largo período mediante transición de modo en fibras de doble revestimiento sin recubrimiento. IEEE Sens. J. 2020, 20, 234–241. [Referencia cruzada]
56. Espósito, F.; Sansone, L.; Srivastava, A.; Baldini, F.; Campopiano, S.; Chiavaioli, F.; Giordano, M.; Giannetti, A.; Iadicicco, A. Rejilla de largo período en fibra de doble revestimiento recubierta con óxido de grafeno como plataforma óptica de alto rendimiento para biodetección. Biosens. Bioelectrón. 2021, 172, 112747. [CrossRef] [PubMed]
57. Espósito, F.; Sansone, L.; Srivastava, A.; Cusano, AM; Campopiano, S.; Giordano, M.; Iadicicco, A. Detección sin etiquetas de vitamina D mediante biodetección óptica basada en rejillas de fibra de período largo. Sens. Actuadores B Chem. 2021, 347, 130637. [Referencia cruzada]
58. Smietana, M.; Koba, M.; Brzozowska, E.; Krogulski, K.; Nakonieczny, J.; Wachnicki, L.; Mikulic, P.; Godlewski, M.; Bock, WJ Sensibilidad sin etiquetas de rejillas de período largo mejorada por nanosuperposiciones de TiO2 depositadas en capas atómicas. Optar. Expreso 2015, 23, 8441–8453. [Referencia cruzada]
59. ´Smietana, M.; Koba, M.; Mikulic, P.; Bock, WJ combinó el grabado de fibra a base de plasma y la deposición de nanosuperposición de carbono similar al diamante para mejorar la sensibilidad de las rejillas de período prolongado. J. Luz. Tecnología. 2016, 34, 4615–4619. [Referencia cruzada]
60. Del Villar, I. Sensores de ultra alta sensibilidad basados en rejillas de período largo recubiertas con una película delgada y diámetro reducido, en modo de transición y cerca del punto de inflexión de dispersión. Optar. Expreso 2015, 23, 8389–8398. [Referencia cruzada]
61. Zou, F.; Liu, Y.; Mou, C.; Zhu, S. Optimización de la sensibilidad del índice de refracción en rejillas de fibra de período largo recubiertas con nanopelículas cerca del punto de inflexión de la dispersión. J. Luz. Tecnología. 2020, 38, 889–897. [Referencia cruzada]
62. Shu, X.; Zhu, X.; Wang, Q.; Jiang, S.; Shi, W.; Huang, Z.; Huang, DJEL Picos resonantes duales del modo de revestimiento LP015 en rejillas de período largo. Electrón. Lett 1999, 35, 649–651. [Referencia cruzada]
63. Biswas, P.; Basumallick, N.; Bandyopadhyay, S.; Dasgupta, K.; Ghosh, A.; Bandyopadhyay, S. Mejora de la sensibilidad de las rejillas de período largo de punto de inflexión mediante el ajuste de la condición de acoplamiento inicial. IEEE Sens. J. 2015, 15, 1240–1245. [Referencia cruzada]
