Nuevos ingredientes antioxidantes de subproductos cerveceros para formulaciones cosméticas
Jul 06, 2022
Por favor contactaroscar.xiao@wecistanche.compara más información
Resumen:El propósito de este trabajo fue evaluar el contenido de fenoles totales y la actividad antioxidante de diferentes tipos de cervezas artesanales (Ego, Alter, IFiat Lux, Triplo Malto, Ubi y Maior), así como los materiales de partida (maltas, lúpulos y levadura), los productos intermedios y los productos de desecho (maltas usadas, lúpulo y levadura), con vistas a su uso en formulaciones cosméticas innovadoras. Las extracciones de muestras iniciales y gastadas se tomaron de agua o alcohol de 70 grados. El contenido total de fenoles (ensayo de Folin Ciocalteau) de todos los productos cerveceros dependía del producto específico bajo investigación. Los valores más altos se encontraron en los lúpulos de partida (que van desde aproximadamente 93 a 155 mg GAE/g, según el solvente de extracción), los intermedios en la malta de partida y la levadura de partida, y los valores más bajos en el mosto. El contenido total de fenoles en las cervezas finales se origina a partir de los fenoles que se extrajeron de los diferentes ingredientes, a saber, las maltas de partida, el lúpulo y la levadura, pero aún se observaron valores no despreciables en los productos agotados. El método utilizado para la evaluación de la actividad antioxidante, la capacidad antioxidante equivalente de Trolox (LPPH), el parámetro antioxidante reductor de iones férricos (FRAP) y la actividad de eliminación de cationes radicales y el poder reductor (ABTS) influyeron fuertemente en los resultados. En general, los resultados reflejaron la tendencia observada para el contenido total de fenoles: que las cervezas se enriquecen progresivamente con fenoles provenientes de todos los ingredientes de partida, y que los productos agotados aún poseen una actividad antioxidante no despreciable.colesterol cistancheEs interesante notar que la levadura de desecho frecuentemente mostró valores más altos que los del material de partida; se puede inferir que la levadura es capaz de absorber los fenoles de la cerveza durante la elaboración. Teniendo en cuenta el interés en el aprovechamiento de los residuos derivados del procesamiento de alimentos, se ha evaluado la actividad biológica de los residuos de productos cerveceros de Alter en cultivos celulares de queratinocitos (productos gastados de malta, lúpulo y levadura). Se llevaron a cabo ensayos in vitro preliminares en células HaCaT de queratinocitos para evaluar la bioactividad potencial de los extractos gastados. Entre los extractos agotados, los extractos agotados de lúpulo y levadura mostraron la capacidad de mejorar la actividad mitocondrial y prevenir el estrés oxidativo en las células HaCaT, dos características del envejecimiento de la piel. En conclusión, este estudio ofrece evidencia de que los desechos de las cervezas artesanales pueden ser una fuente interesante de fenoles para la preparación de cosméticos antienvejecimiento para la piel.
Palabras clave:cerveza artesanal; productos cerveceros; contenido de fenoles totales; actividad antioxidante; citotoxicidad;antienvejecimiento
1. Introducción
La cerveza artesanal se ha vuelto cada vez más popular en los EE. UU. y Europa [1,2], con importantes repercusiones para la economía [3]. Este éxito ha sido impulsado por el interés de los consumidores en probar nuevas cervezas con diferentes sabores y aromas [2] y la atención a los beneficios para la salud del consumo moderado de cerveza [4].

Por favor haga clic aquí para saber más
A diferencia de las cervezas comerciales, las cervezas artesanales no están filtradas ni pasteurizadas, por lo que sus características sensoriales permanecen inalteradas por el proceso de elaboración. Además, también se pueden ahorrar sustancias beneficiosas para la salud, como los antioxidantes.
Las cervezas comerciales y sus productos de desecho ya han sido evaluados por sus propiedades antioxidantes. Zhao et al. [5] determinaron los perfiles de fenoles y las actividades antioxidantes correspondientes de 34 cervezas comerciales y encontraron diferencias notables en el contenido fenólico total e individual y la actividad antioxidante. Los compuestos fenólicos más abundantes fueron los ácidos gálico y ferúlico. En el mismo período, Ribeiro Tafulo et al. [6] determinaron la actividad antioxidante de otras 27 cervezas comerciales, usando varios métodos espectrofotométricos. Ese mismo año, Piazzon et al., 2010 [7] evaluaron la actividad antioxidante y el contenido fenólico de diferentes tipos de cervezas comerciales (abadía, ale, bock, trigo, lager, pilsner y desalcoholizadas), y encontraron gran variedad entre ellas. En un estudio sobre cervezas caseras, Farcas et al. [8] determinaron el contenido de polifenoles totales y la actividad antioxidante durante todo el proceso de producción, partiendo de las materias primas (malta y lúpulo) y finalizando con los residuos recuperados. Demostraron que un mayor contenido inicial de polifenoles totales y actividad antioxidante en las materias primas se debió a la presencia de malta y que el contenido de polifenoles totales disminuyó considerablemente al pasar a la cerveza y la malta gastada en el producto final de cerveza y en la malta gastada. No se analizó la levadura.

Cistanche puede antienvejecimiento
El hecho de que los compuestos antioxidantes derivados de la malta fueran probados por Zhao y colaboradores [9], quienes demostraron la actividad antioxidante y el contenido total de fenoles de varias variedades de cebada cervecera. Otros autores identificaron cuarenta y siete compuestos fenólicos de cuatro tipos de cerveza comercial, utilizando cromatografía líquida junto con una técnica híbrida de espectrometría de masas Orbitrap de ionización por electropulverización de cuadrupolo lineal con trampa de iones [10]. Recientemente, la identificación de compuestos fenólicos y nitrogenados de bajo peso molecular en cervezas artesanales se logró mediante análisis HPLC-ESI-MS/MS [11]. Los autores intentaron diferenciar los tipos de cervezas, como IPA, Lager y Weiss, según los compuestos fenólicos y nitrogenados, pero no encontraron diferencias significativas en estos compuestos entre los distintos tipos de cerveza.
Más recientemente [12], se seleccionaron y cuantificaron 20 compuestos fenólicos, por ejemplo, ácido gálico, catequina, ácido cafeico, quercetina, xantohumol y humulona, en diferentes cervezas artesanales, mostos, ingredientes de partida para la elaboración de cerveza (malta de cebada, lúpulo y levadura). ) y subproductos (cáscara de cebada, lúpulo gastado y levadura gastada). A partir de este estudio, se encontró que existían diferencias significativas entre todas las muestras y que la composición de la cerveza depende del proceso de recepción y elaboración. Los compuestos fenólicos de las cervezas se originaron principalmente a partir de la malta de cebada y, curiosamente, la levadura pudo absorber compuestos fenólicos de otras fuentes.
Por lo tanto, la evaluación de antioxidantes en los productos de desecho de la producción de cerveza puede ser de gran importancia si se considera el rápido crecimiento del mercado de la cerveza artesanal a nivel mundial.
La explotación de los subproductos de la cervecería para desarrollar productos para la salud como cosméticos y/o suplementos ayudaría a aumentar la sostenibilidad de la producción de cerveza. Este estudio tiene múltiples objetivos: evaluar el contenido de fenoles totales y la actividad antioxidante de diferentes tipos de cervezas artesanales italianas (lager, ámbar, triple malta, roja y negra), y evaluar sus intermedios de producción, así como sus productos de desecho. Así se evaluó la actividad biológica de los extractos de desecho de la cervecería Alter en queratinocitos humanos. Esto abre nuevas e interesantes oportunidades para explotar nuevos ingredientes a partir de subproductos cerveceros para formulaciones cosméticas.
2. Experimental
2.1. Materiales
11-Diphenyl-2-picrylhydrazyl (DPPH),2,4,6-Tris(2-pyridyl)-s-triazine (TPTZ), (±)-6-Hydroxy-2,5,7,8-tetramethylchromane-2-carboxylic acid (TROLOX), 2,2'-Azino-bis(3-ethylbenzothiazoline-6-sulfonic acid) diammonium salt(98%TLC)(ABTS), gallic acid, sodium carbonate monohydrate ACS reagent, sodium acetate and ethanol(ethanol absolute grade) were purchased from Sigma-Aldrich(Steinheim, Germany). Manganese (IV)oxidize activated(>90 por ciento) y el reactivo de fenol de Folin-Ciocalteu se adquirió de Fluka (Buchs, Suiza). El acetato de sodio anhidro y el cloruro de hierro (III) anhidro se adquirieron de JT Baker (Center Valley, PA, EE. UU.) y el carbonato de sodio anhidro se adquirió de Carlo Erba (Milán, Italia). Todos los solventes y reactivos fueron de grado analítico. El agua ultrapura fue producida por Gradient Milli-Q (Millipore, Molsheim, Francia). Las materias primas, las cervezas artesanales, los mostos y sus productos de desecho fueron amablemente proporcionados por Birrificio Collesi (Apecchio, Italia).
Las características detalladas de las cervezas investigadas en el presente estudio se proporcionan en la Tabla 1. El tipo de malta de partida y el lúpulo determinaron las principales diferencias entre todas las cervezas. Se pueden utilizar cinco maltas de partida diferentes, frecuentemente en mezclas y en diferentes proporciones. Los lúpulos Perle y Saaz se utilizan en diferentes proporciones por sus diferentes aromas. La misma levadura, Saccharomyces Cerevisiae, se usó para todas las cervezas, que eran todas de fermentación alta. Las diversas combinaciones producen diferentes tipos de cervezas (lager, ámbar, triple malta, roja y negra) con contenidos de alcohol que van desde el 6,0 hasta el 9,0 por ciento V/V.

2.2. Preparación de la muestra
Previo a los análisis, los materiales de partida (malta, lúpulo y levadura), cervezas, mostos y desechos (malta gastada, lúpulo y levadura) fueron sometidos a diferentes procesos de acuerdo a su estado físico, los cuales podían ser secados sólidos, húmedos sólido o líquido turbio (Cuadro 2).
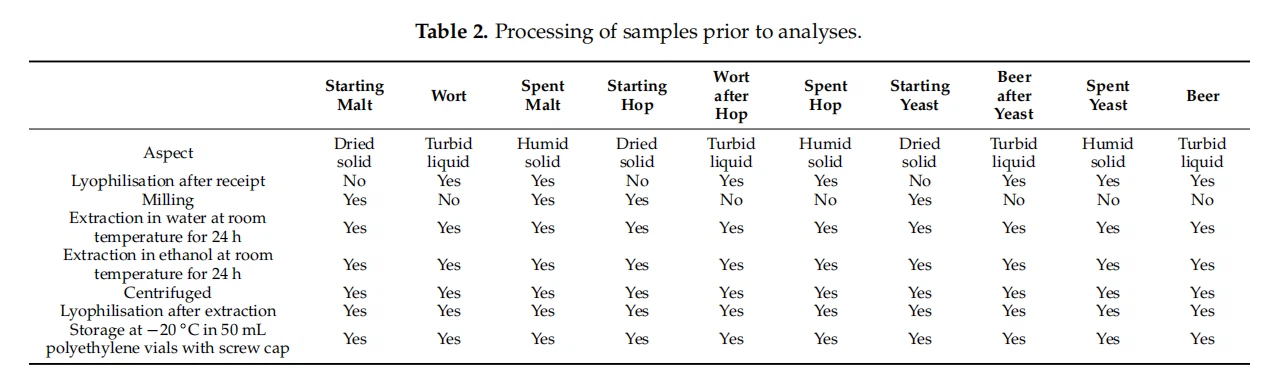
Los sólidos y líquidos húmedos se sometieron primero a liofilización a una temperatura de {{0}} grados y una presión de 0,03 bares (FreeZone 1 Litro Benchtop Series77400 liofilizador, LABCONCO, Kansas City, MO, EE. UU.). Los sólidos secos se sometieron a molienda en un molino cortador. A continuación, todas las muestras fueron sometidas a extracciones. Se pesó cuidadosamente una cantidad de muestra y se dispersó en 100 mL de solvente (agua o etanol de 70 grados). El líquido resultante se colocó en el matraz Erlenmeyer, que luego se cerró con cuidado. Las muestras se agitaron magnéticamente durante 24 h a temperatura ambiente, luego se centrifugaron a 12,000 rpm a 20 grados durante 10 min para eliminar las partículas no disueltas (Zetalab CNZ-140HE, Padua, Italia). Las muestras se liofilizaron y almacenaron a -20 grados en viales de polietileno de 50 ml con tapa roscada (BD Falcon TM, BD Biosciences, Bedford, MA, EE. UU.) para garantizar las condiciones óptimas de almacenamiento.
2.3. Determinación del contenido total de fenol
El Contenido de Fenol Total (TPC) de las muestras se determinó según el método espectrofotométrico de Folin-Ciocalteu [13] con algunas modificaciones [14]. En resumen, todos los productos liofilizados se utilizaron para preparar soluciones límpidas a una concentración de 10 mg mL-1. Una alícuota de 50 μL de esta solución se añadió a 150 μL de reactivo fenol de Folin-Ciocalteu, diluido 1:4 con agua. Luego se agregaron 50 uL de solución saturada de Na,CO3. Después de incubar a temperatura ambiente durante 10 min, se determinó la absorbancia de cada pocillo a 765 nm utilizando un lector de microplacas (FLUOstar Omega, BMG Labtech GmbH, Ortenberg, Alemania). La medición se comparó con una solución estándar de calibración de ácido gálico (GA), y los resultados se expresaron como miligramos de equivalentes de ácido gálico (GAE) por gramos de subproducto (mg GAE/g).
2.4. Evaluación de la Actividad Antioxidante
La actividad antioxidante de la cerveza artesanal y los subproductos se evaluó midiendo la actividad de captación de radicales 11-Difenil-2-picrilhidrazilo (DPPH"), 2,2'-Azino-bis(3- etilbenzotiazolina-6-ácido sulfónico)(ABTS*) capacidad de captación de cationes radicales y capacidad antioxidante reductora de hierro (FRAP).dosis de cistanche redditTrolox (6-Hidroxi-2,5,7,8-tetrametilcromano-2-ácido carboxílico) se usó como estándar de calibración. Los valores se expresaron como equivalentes de mmol Trolox/g de la muestra en función de la IC50, definida como la concentración del material analizado requerida para causar una disminución del 50 por ciento en la concentración inicial de DPPH, ABTS o hierro.
2.5. Evaluación de la Capacidad Antioxidante Equivalente de Trolox (DPPH)
La actividad de eliminación de radicales libres de DPPH se evaluó a través de un ensayo analítico en microplaca de acuerdo con los métodos publicados previamente [15] con algunas modificaciones [16]. En resumen, una alícuota de 50 μL de la muestra (concentración de 10 mg mL-') y el estándar se agregaron a 150 μL de DPPH en etanol absoluto en una placa de microtitulación de 96-pocillos (BD FalconTM) después de la incubación a 37ºC. grado durante 20 min, la absorbancia de cada pocillo se determinó a 517 nm utilizando un lector de microplacas. La actividad antioxidante se calculó y expresó frente a la cantidad de Trolox según la Ecuación (1)[17] donde Ag y A son las absorbancias de la solución radical DPPH● a 517 nm en presencia de la muestra de control y las muestras de extracto, respectivamente.
2.6. Actividad de eliminación de cationes radicales y poder reductor (ABTS)
El ensayo ABTS se realizó siguiendo los procedimientos anteriores [18] y se aplicó a un ensayo de placa de microlitro de 96-pocillos. La solución ABTS* plus (5 mM) se preparó oxidando ABTS con MnO en agua durante 30 min en la oscuridad. Se añadió una alícuota de 50 μL de las diferentes concentraciones de muestra y estándar (Trolox) a 150 μL de solución ABTS* en una placa de microtitulación de 96-pocillos (BD FalconTM).beneficios del extracto de cistancheDespués de la incubación a temperatura ambiente durante 10 min, se determinó la absorbancia de cada pocillo a 734 nm utilizando un lector de microplacas. Los valores se calcularon y expresaron frente a la cantidad de Trolox de acuerdo con la Ecuación (2) [17] donde Ag y A son las absorbancias de la solución de radical OHe a 734 nm en presencia de la muestra de control y las muestras de extracto, respectivamente.

2.7. Parámetro antioxidante de reducción larga férrica (FRAP)
Los valores FRAP de cerveza artesanal/subproductos se determinaron de acuerdo con un método publicado previamente [19], con algunas modificaciones [20]. El reactivo FRAP se preparó mezclando las siguientes tres soluciones:
1. 50mL0.3M tampón de acetato pH 3.6(1.23g de acetato de sodio en 50 mL de agua acidificante
con ácido acético);
2. 5 ml de solución madre de 5 mMTPTZ(2,4,6-Tripiridil-s-triazina)(15,6 mg) en HCl 40 mM;3. 5 ml de FeCl3:6 H2O 5 mM (16,2 mg) en HCl 40 mM.
El reactivo FRAP se calentó a 37 grados C antes de su uso. Se agregaron alícuotas de una muestra de 25 μL (soluciones a una concentración de 10 mg mL-1) por triplicado en pocillos de una 96-placa de pocillos (BD Falcone). El ensayo se inició agregando 175 μL de reactivo FRAP a cada pocillo. La placa se agitó inmediatamente en un lector de placas FLUOstar Omega durante 30 s y se permitió que la reacción transcurriera durante 10 min, después de lo cual se leyó la placa en un lector de placas (593 nm). Se corrió una solución de referencia de Trolox simultáneamente y se usó para generar la curva de calibración por regresión lineal. La curva estándar fue lineal entre 25 y 800 μM de Trolox (TE). Los resultados se expresaron en μM Trolox equivalente (TE) muestra gI.

2.8. Culturas celulares
La línea celular de queratinocitos humanos, HaCaT, se cultivó de forma rutinaria en medio de Eagle modificado por Dulbecco (DMEM), complementado con suero fetal bovino (FBS) al 10 por ciento, L-glutamina 2 mM, penicilina 50 U/ml y estreptomicina 50 ug/ml a 37 grados centígrados. una incubadora humidificada con 5 por ciento de CO. Para evaluar la citotoxicidad, la actividad mitocondrial y la formación de ROS intracelular, se sembraron células HaCaT en 96-placas de pocillos a 2 × 10* células/pocillo. Todos los experimentos se realizaron después de 24 h de incubación a 37 grados en CO2 al 5 por ciento. Para los experimentos con células HaCaT, se prepararon soluciones madre de extractos gastados en agua a 60 mg/mL. A continuación, las soluciones madre se diluyeron en un medio completo para obtener las concentraciones deseadas de extractos agotados.
2.9. Citotoxicidad y actividad mitocondrial
La viabilidad celular se evaluó mediante la reducción de {{{{10}}}}(4,5-dimetil-2-tiazolil)-2,5-difenilo -2bromuro de H-tetrazolio (MTT) a su formazán insoluble, como se describió previamente 21]. En resumen, las células HaCaT se trataron durante 24 h con diferentes concentraciones de extracto (0,003-3 mg/mL) a 37 grados en 5 % de CO. Posteriormente, el medio de tratamiento se reemplazó con MTT en solución salina equilibrada de Hank ( HBSS (0,5 mg/ml) durante 2 horas a 37 grados en 5 por ciento de CO. Después de lavar con HBSS, los cristales de formazán se disolvieron en isopropanol. Los niveles de formazán se midieron (570 nm, filtro de referencia 690 nm) utilizando el lector de placas multimarca VICTORTM X3 (PerkinElmer, Waltham, MA, EE. UU.). La viabilidad celular se expresó como porcentaje de las células de control.
La actividad mitocondrial fue determinada por MTT, como se describió anteriormente, con ligeras modificaciones [22].efectos secundarios de la cistanche deserticolaEn resumen, las células HaCaT se trataron durante 4 h con DMEM al 10 por ciento de FBS (medio nutritivo) o solución salina tamponada con fosfato de Dulbecco (solución salina sin nutrientes) en presencia de 0,03 mg/ml de extracto a 37 grados en 5 por ciento de CO. Posteriormente, el tratamiento se reemplazó con MTT durante 2 h a 37 grados en 5 por ciento de CO2. Después de lavar con HBSS, los cristales de formazán se disolvieron en isopropanol. Se midieron los niveles de formazán que se correlacionaron con la actividad mitocondrial (570 nm, filtro de referencia 690 nm) utilizando el lector de placas multimarca VICTORTM X3 (PerkinElmer). La actividad mitocondrial se expresó como porcentaje de las células de control.
2.10. Formación intracelular de ROS
La formación de especies reactivas de oxígeno (ROS) se evaluó mediante una sonda fluorescente de diacetato de diclorodihidrofluoresceína 2'-7' (H2DCF-DA), como se describió anteriormente [23] (las células HaCaT se trataron durante 2 h con 0).{ {23}}3 mg/mL de extracto a 37Cin 5 por ciento de CO2. Posteriormente, se eliminó el medio de tratamiento y se agregaron 100 μL de H2DCF-DA (10 ug/mL) a cada pocillo. Después de 30 min de incubación a temperatura ambiente, el La solución de H2DCF-DA se reemplazó con una solución de H2O2 (100 μM) durante 30 min. Se trató un conjunto paralelo de células HaCaT con H2O y 0,03 mg/mL de extracto durante 30 min.cistanche genghis khanLa formación de ROS se midió en términos de Unidades Arbitrarias de Fluorescencia, AUF (excitación a 485 nm y emisión a 535 nm), utilizando el lector de placas multimarca VICTORTM X3 (PerkinElmer). Los datos se expresan como veces de aumento en la formación de ROS frente a células no tratadas (es decir, AUF de células tratadas con H, O/AUF de células no tratadas).
Este artículo está extraído de Cosmetics 2021, 8, 96. https://doi.org/10.3390/cosmetics8040096 https://www.mdpi.com/journal/cosmetics
