Parte 2: El oligosacárido 2/-fucosilactosa de la leche humana induce la neuroprotección del accidente cerebrovascular por hemorragia intracerebral
Mar 23, 2022
Contacto: Audrey Hu Whatsapp/hp: 0086 13880143964 Correo electrónico:audrey.hu@wecistanche.com
Por favor haga clic aquí para la Parte 1
3. Discusión
En este estudio, 2FL redujo la activación de microglía inducida por hemina yneurodegeneraciónen una cortical primarianeuronay cocultivo de microglía BV2. 2FL mejoró la actividad locomotora en ratas ICH. Usando análisis inmunohistoquímicos y qPCR, demostramos que 2FL inhibía la activación de la microglía, la infiltración de linfocitos CD4(plus) y la expresión de marcadores de estrés inflamatorio y ER en el cerebro ICH. El principal hallazgo de este estudio es que 2FL esneuroprotectorcontra la lesión ICH.
La HIC causa daño cerebral agudo e irreversible. Después del insulto agudo, se activa una serie de reacciones en cascada, que dan como resultado una degeneración secundaria crónica. La hemoglobina y sus productos de degradación están estrechamente relacionados con la lesión secundaria. La hemina es citotóxica y contribuye al daño cerebral, acompañado de accidente cerebrovascular hemorrágico [21,22]. El exceso de hemina cataliza reacciones en cadena de radicales libres [23] y facilita la apoptosis y la fisión mitocondrial [24]. La hemina también potencia la activación microglial y agrava la lesión inflamatoria después de una hemorragia intracerebral [25,26]. En este estudio, se usó hemina para simular ICH en unneuronay cocultivo de microglía BV2. Demostramos que la hemina eraneurotóxicoy microglía activada. El tratamiento con 2FL redujo la activación de IBA1 mediada por hemina y restauró la inmunorreactividad de MAP2. Nuestros datos sugieren que 2FL es antiinflamatorio yneuroprotectoren un modelo celular de HIC.
Previamente, demostramos que la infusión de colagenasa local resultó en HIC y bradicinesia en ratas [13]. En este estudio, se utilizó un modelo animal similar para examinar el efecto protector de 2FL in vivo. Demostramos que la aplicación sistémica de 2FL durante 5 días mejoró los movimientos locomotores en ratas ICH. Dado que la inflamación desempeña un papel fundamental en la progresión de la HIC [7,8,27], también encontramos activación de la microglía en el cerebro con HIC. 2FL redujo IBA1-ir y restauró parcialmente la ramificación de microglia en el cerebro ICH lesionado. Además, encontramos que 2FL regula al alza la expresión de M2 (antiinflamatorio) microglía / macrófagos fabricantes inflamatorios en el cerebro de rata ICH. Estos datos sugieren que 2FL suprimió la activación de la microglía mediada por ICH en el cerebro lesionado.
La HIC promueve la migración de células inmunitarias periféricas, como las células T CD4 plus y CD8 plus, al cerebro lesionado [28,29]. Anteriormente informamos sobre la expresión de marcadores de células T citotóxicas en el cerebro ICH [13]. Además, la infiltración máxima de células T CD4 se produjo entre los días 3 y 4 después de la lesión isquémica en los ratones [30]. En este estudio, demostramos que la HIC aumentó la infiltración de linfocitos CD4 más en el cuerpo estriado lesionado el día 5 en ratas; La infiltración de células CD4 se mitigó significativamente con 2FL. Estos datos respaldan la idea de que 2FL inhibe la migración de células T desde la periferia al cerebro ICH.

Cistanche tiene efecto neuroprotector
Estudios previos han indicado que 2FL tiene efectos protectores en la periferia. En enterocitos humanos, 2FL atenuó la inducción de CD14 [18] y la expresión de IL-8, IL-1b y MIP-2 [31]. 2FL también atenúa la gravedad de la enterocolitis necrotizante en los intestinos neonatales de ratón [32]. En este estudio, demostramos que 2FL tiene propiedades antiinflamatorias yneuroprotectorefectos en el cerebro ICH. Otros estudios también respaldan que 2FL mejoró el aprendizaje y la potenciación del hipocampo a largo plazo en roedores [17], así como evitó la muerte celular en el cerebro isquémico [19]. Estos datos sugieren que 2FL tiene efectos benéficos multifacéticos contra el SNC y la inflamación y degeneración periférica.
ICH puede inducir secundarianeurodegeneracióna través del estrés ER [33]. Por ejemplo, la vía PERK se activó en el cerebro ICH, como lo demuestra la regulación al alza de p-eIF2& y ATF4 [34]. El estrés ER resultante indujo aún másneuronalesapoptosis y muerte celular. También informamos que la expresión de PERK, IRE1, CHOP, SigmaR1 y caspasa-3 mejoró en el cerebro ICH. 2FL inhibió significativamente estas respuestas. Los mecanismos detallados que subyacen a la regulación del estrés ER por 2FL justifican una investigación.
Hay algunas limitaciones en este estudio. No usamos el tamaño del hematoma para evaluar el resultado después de la terapia 2FL. Como se indicó anteriormente, la cuantificación del área del hematoma en cortes histológicos suele ser laboriosa y, a veces, subjetiva [35]. Recientemente se ha desarrollado un nuevo método para permitir mediciones precisas y eficaces del volumen del hematoma cerebral [35]. Será de interés determinar la asociación del volumen del hematoma con mejoras en la actividad locomotora después del tratamiento con 2FL utilizando este nuevo enfoque. Nuestro estudio se realizó en modelos celulares y animales de HIC. Se requieren estudios adicionales con primates no humanos y ensayos aleatorios prospectivos del tratamiento con 2FL en sujetos humanos antes de su uso clínico.
La leche humana se considera la mejor fuente de nutrición para los recién nacidos y los lactantes en desarrollo. Más allá de su nutrición, la leche humana también contiene compuestos beneficiosos [36], como 2FL. En este estudio, demostramos que 2FL, un componente bioactivo en la leche humana, tiene efectos protectores contra la ICH. 2FL puede tener implicaciones clínicas para el tratamiento de la HIC.

beneficio del extracto de cistanche
4. Materiales y Métodos
4.1. animales
Se compraron ratas Sprague-Dawley macho adultas y preñadas en BioLASCO, Taipei, Taiwán. El uso de animales fue aprobado por el Comité de Investigación Animal de los Institutos Nacionales de Investigación en Salud de Taiwán (NHRI-IACUC106101-A). Todos los experimentos con animales se llevaron a cabo de acuerdo con la Guía para el cuidado y uso de animales de laboratorio de los Institutos Nacionales de Salud (NIH Publicaciones No. 8023, revisada en 1978).
4.2. Materiales
La 2′-fucosilactosa fue proporcionada por Advanced Protein Technologies Corp. (Suwon-si, provincia de Gyeonggi-do, Corea). Se adquirieron albúmina sérica bovina, hidrato de cloral, suero bovino fetal, L-glutamato, paraformaldehído, poli-D-lisina, hemina y Triton X-100 de Sigma (St. Louis, MO, EE. UU.). Alexa Fluor 488 (anticuerpo secundario), suplemento B27, medio de Eagle modificado por Dulbecco,neurobasalEl medio y la tripsina se adquirieron de Invitrogen (Carlsbad, CA, EE. UU.). El anticuerpo anti-CD4 se adquirió de Proteintech (Rosemont, IL, EE. UU.). Anti-MAP2 se adquirió de Millipore (Burlington, VT, EE. UU.). El anticuerpo anti-IBA1 se adquirió de Wako (Richmond, VA, EE. UU.).
4.3. Neurona cortical primaria de rata (PCN) y cocultivo de microglía
cortical primarianeurona(PCN) se prepararon cultivos a partir de tejidos de la corteza embrionaria (E14-15) obtenidos de los fetos de ratas Sprague-Dawley embarazadas a término. Después de eliminar los vasos sanguíneos y las meninges, las cortezas agrupadas se tripsinizaron (0,05 por ciento; Invitrogen, Carlsbad, CA, EE. UU.) durante 20 minutos a temperatura ambiente. Después de enjuagar la tripsina con medio de Eagle modificado por Dulbecco precalentado (Invitrogen, Carlsbad, CA, EE. UU.), las células se disociaron por trituración, se contaron y se sembraron en 96-pocillos (5,0 × 104/pocillo) placas de cultivo celular recubiertas previamente con poli-D-lisina (Sigma-Aldrich, St. Louis, MO, EE. UU.). El medio de cultivo en placas consistió enneurobasalsuplementado con 2 por ciento de FBS inactivado por calor, 0.5 mmol/L L-glutamina, 0.025 mM L-glutamato y 2 por ciento de B27 (Invitrogen, Carlsbad, CA, EE. UU.). Los cultivos se mantuvieron a 37 О C en una atmósfera humidificada de 5 por ciento de CO2 y 95 por ciento de aire. Los cultivos se alimentaron intercambiando el 50 por ciento del medio con medio de alimentación (medio neurobasal), 0,5 mmol/L L-glutamina y el 2 por ciento de B27 con un suplemento antioxidante en días in vitro ( DIVs) 3 y 5. La microglía BV2 se cultivó por separado, se separó con ácido tripsina-etilendiaminotetraacético al 0,05 % (EDTA, Invitrogen) y se centrifugó a 100 × g durante 5 min. Las células BV2 se resuspendieron en el medio de alimentación que contenía el suplemento B27 sin antioxidantes (一AO, de Invitrogen, Carlsbad, CA, EE. UU.). La densidad de las células supervivientes se contó utilizando un ensayo de azul tripán; las células se sembraron en pocillos sembrados con PCN a una concentración de 3,0 × 103/pocillo en DIV 7, como se describió anteriormente [37]. Los cocultivos se alimentaron con medio 一AO en DIV 7 y 10. En DIV 10, los cultivos se trataron con glutamato con 2FL o vehículo. A las 48 h después del tratamiento farmacológico, las células se fijaron con paraformaldehído al 4 por ciento (PFA, Sigma-Aldrich, St. Louis, MO, EE. UU.) durante 1 hora a temperatura ambiente.

efectos neuroprotectores de la cistanche: tratar la enfermedad de Parkinson
4.4. Inmunocitoquímica
Después de eliminar la solución de PFA al 4 por ciento, las células se lavaron con PBS. Las células fijadas se trataron con una solución de bloqueo (5 por ciento de BSA y 0,1 por ciento de Triton X-100 en PBS) durante 1 h. Las células se incubaron durante 1 día a 4 ºC con un anticuerpo monoclonal de ratón contra MAP2 (1:500; Millipore, Billerica, MA, EE. UU.) y un anticuerpo policlonal de conejo contra IBA1 (1:500; Wako, Richmond, VA, EE. UU.) , antes de enjuagar tres veces en PBS. El anticuerpo primario unido se visualizó utilizando el anticuerpo secundario anti-ratón de cabra AlexaFluor 488 o el anticuerpo secundario anti-conejo de cabra AlexFluoro 568 (Invitrogen, Carlsbad, CA, EE. UU.). Las imágenes fueron adquiridas usando una cámara DS-Qi2 (Nikon, Tokio, Japón) conectada a un microscopio invertido NIKON ECLIPSE Ti2 (Nikon, Tokio, Japón) por observadores cegados. La densidad de píxeles de MAP2-ir o IBA1-ir se analizó con el software NIS Elements AR 5.11 (Nikon).
4.5. Cirugía
Las ratas se alojaron en un ciclo de 12 h de oscuridad (7 pm a 7 am) y 12 h de luz (7 am a 7 pm). Los animales fueron anestesiados y colocados en un marco estereotáxico. Se inyectó estereotácticamente colagenasa tipo VII (0.5 U/uL × 1.0 uL, C{{10}}, Sigma Aldrich, St. Louis, MO, EE. UU. en el cuerpo estriado derecho (coordenadas: 0.0 mm rostral y 3.0 mm lateral al bregma, 5,5 mm por debajo del cráneo) a 0,4 uL/min durante 5 min el día 0. Luego, se administró ip 2FL (400 mg/kg/día × 5 días) o vehículo desde el día 1 al día 5. Los animales se sacrificaron el día 5 para análisis histológico y PCR.
4.6. Medición del comportamiento locomotor
La locomoción se midió el día 5 utilizando un monitor de actividad infrarrojo (Accuscan, Columbus, OH, EE. UU.). Las ratas se colocaron individualmente en una cámara de comportamiento infrarrojo 3D (42 × 42 × 21 cm) durante 120 min. Se midieron seis variables: (i) actividad vertical (VACTV, el número total de interrupciones de haz que ocurrieron en los sensores verticales), (ii) distancia total recorrida (TOTDIST, la distancia, en centímetros, recorrida por los animales), (iii) ) tiempo de movimiento vertical (VTIME), (iv) actividad horizontal (HACTV, el número total de interrupciones de haz que ocurrieron en los sensores horizontales), (v) tiempo de movimiento horizontal (MOV-TIME), y (vi) número de movimientos verticales (VMOVNO).
4.7. inmunohistoquímica
Los animales fueron anestesiados y perfundidos transcardiacamente con solución salina seguido de PFA al 4 por ciento en tampón de fosfato (PB; 0.1 mol/L; pH 7.2); se fijaron posteriormente durante 18-20 h y luego se transfirieron a sacarosa al 20 por ciento en PB 0,1 M durante al menos 16 h. Secciones seriadas de cerebros
se cortaron a un espesor de 30 um utilizando un criostato (modelo: CM 3050 S; Leica, Heidelberg, Alemania). Se enjuagaron secciones de cerebro en PB y se bloquearon con albúmina de suero bovino al 4 por ciento (Sigma-Aldrich) con Triton X-100 al 0,3 por ciento (Sigma-Aldrich) en PB 0,1 mM. Luego, los cortes de cerebro se incubaron con anticuerpos primarios contra CD4 (policlonal 1:100, protein tech, Rosemont, EE. UU.) o IBA1 (monoclonal 1:100, Wako, Richmond, VA, EE. UU.) a 4 °C durante la noche. Las secciones se enjuagaron en PB 0,1 mM y se incubaron en solución de anticuerpo secundario Alexa Fluor 488 (1:500; Molecular Probes, Eugene, OR, EE. UU.). Las secciones de control se incubaron sin el anticuerpo primario. Las secciones de cerebro se montaron en portaobjetos y se cubrieron con cubreobjetos. El análisis confocal se realizó con un microscopio Nikon D-ECLIPSE 80i (Nikon Instruments, Inc., Tokio, Japón) y el software EZ-C1 3.90 (Nikon, Tokio, Japón). La densidad óptica de la inmunorreactividad de IBA1 o CD8 se cuantificó en dos secciones cerebrales consecutivas con una comisura anterior visualizada en cada animal. Se tomaron dos microfotografías a lo largo de la región perilesionada por corte de cerebro; La densidad óptica de IBA1 o CD4 se analizó utilizando el software NIS Elements AR 3.2 (Nikon) y se promedió en cada cerebro para el análisis estadístico. Todas las mediciones inmunohistoquímicas fueron realizadas por observadores ciegos.

efectos neuroprotectores de la cistanche: enfermedad antiparkinsoniana
4.8. PCR de transcripción inversa cuantitativa (RT-PCR)
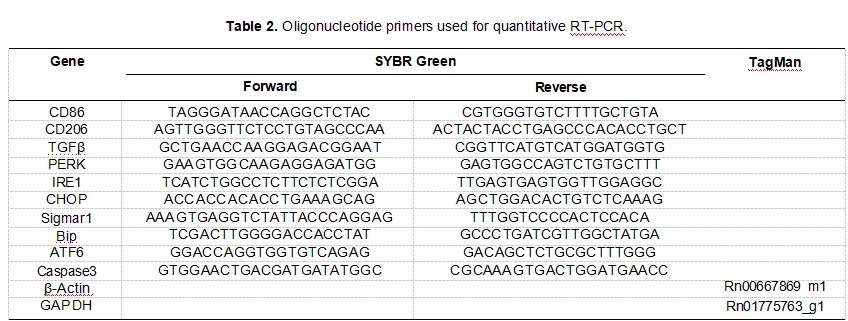
Se recogieron tejidos estriatales de los hemisferios lesionados y no lesionados. Los ARN totales se aislaron utilizando el reactivo TRIzol (ThermoFisher, #15596-018, Waltham, MA, EE. UU.) y los ADNc se sintetizaron a partir de 1 ug de ARN total mediante el uso de un kit de síntesis de ADNc de primera cadena RevertAid H Minus (Thermo Scientific , #K1631, Waltham, MA, EE. UU.). Los niveles de ADNc para CD86, CD206, TGF, PERK, IRE1, CHOP, Sigmar1, BIP, ATF6, caspasa3, actina y GAPDH se determinaron utilizando conjuntos de cebador-sonda de la biblioteca universal de sondas específicas o cebadores específicos de genes (Tabla 2). Las muestras se mezclaron con TaqMan Fast Advanced Master Mix (Life Technologies, #4444557, Carlsbad, CA, EE. UU.) o SYBR (Luminaris Color HiGreen Low ROX qPCR Master Mix; ThermoScientific, Waltham, MA, EE. UU.). La PCR cuantitativa en tiempo real (qRT-PCR) se llevó a cabo utilizando el sistema de PCR en tiempo real QuantStudio™ 3 (ThermoScientific, Waltham, MA, EE. UU.). La expresión de los genes objetivo se normalizó en relación con los genes de referencia endógenos (promedios de beta-actina y GAPDH) utilizando un algoritmo delta-delta-Ct modificado. Todos los experimentos se llevaron a cabo por duplicado.
4.9. Estadísticas
Los datos se presentan como la media 士 SEM. Se utilizó una prueba t no pareada o ANOVA de una o dos vías para las comparaciones estadísticas, con un nivel de significancia de p < 0.05.="" en="" caso="" de="" múltiples="" comparaciones,="" se="" realizó="" una="" prueba="" post="" hoc="" de="">
Contribuciones de los autores: T.-WH, redacción de manuscritos, cirugía animal y recopilación y/o ensamblaje de datos; K.-JW, cirugía animal y recogida y/o montaje de datos; Y.-SW, PCR, recolección y/o ensamblaje de datos; E.-KB, cultivo celular, inmunocitoquímica y análisis de datos; YS y JY, síntesis de 2′-FL, análisis e interpretación de datos y provisión de materiales de estudio; S.-JY, conceptualización y diseño, redacción del manuscrito, apoyo administrativo y aprobación final del manuscrito. Todos los autores han leído y aceptado la versión publicada del manuscrito.
Financiamiento: Este estudio fue financiado en parte por los Institutos Nacionales de Investigación en Salud de Taiwán (NP-109-PP-02) y el Ministerio de Ciencia y Tecnología de Taiwán (MOST 106-2320-B{{3 }}MY2; MAYORÍA 108-2320-B-400-023).
Declaración de la Junta de Revisión Institucional: El estudio se realizó de acuerdo con las pautas de la Declaración de Helsinki y fue aprobado por el Comité de Investigación Animal de la National Health
Institutos de Investigación de Taiwán (NHRI-IACUC106101-A).
Declaración de consentimiento informado: No aplicable.
Declaración de disponibilidad de datos: Los datos que respaldan los hallazgos de este estudio están disponibles a través del autor correspondiente previa solicitud razonable.
Agradecimientos: Los autores agradecen a Yun Wang por sus comentarios críticos. Conflictos de interés: YS y JY son empleados de Advanced Protein Technologies.

beneficio de la cistanche: neuroprotección
Referencias
1. Goulart, AC; Benseñor, IM; Fernández, TG; Aléncar, AP; Fedeli, LM; Lotufo, PA Mortalidad temprana y de un año por accidente cerebrovascular en Sao Paulo, Brasil: aplicación de los PASOS para accidentes cerebrovasculares de la Organización Mundial de la Salud. J. Stroke Cerebrovasc. Dis. 2012, 21, 832–838. [Referencia cruzada]
2. Kojic, B.; Buriña, A.; Hodzic, R.; Pasic, Z.; Sinanovic, O. Los factores de riesgo impactan en la supervivencia a largo plazo después de un accidente cerebrovascular hemorrágico. Medicina. Arco. 2009, 63, 203–206.
3. Feigin, VL; Lawes, CM; Bennett, DA; Barker-Collo, SL; Parag, V. Incidencia mundial de accidentes cerebrovasculares y letalidad temprana informada en 56 estudios basados en la población: una revisión sistemática. LancetaNeurol. 2009, 8, 355–369. [Referencia cruzada]
4. De Miguel-Yanes, JM; López-de-Andrés, A.; Jiménez-García, R.; Hernández-Barrera, V.; de Miguel-Diez, J.; Méndez-Bailón, M.; Pérez-Farinos, N.; Muñoz-Rivas, N.; Carabantes-Alarcón, D.; Lopez-Herranz, M. Incidencia y resultados del ictus hemorrágico
entre adultos en España (2016-2018) según sexo: Estudio retrospectivo, observacional, de cohortes, emparejado por puntaje de propensión.
J. Clin. Medicina. 2021, 10, 3753. [Referencia cruzada]
5. Marrugat, J.; Arboix, A.; García-Eroles, L.; Salas, T.; Vila, J.; Castell, C.; Tresserras, R.; Elosua, R. La incidencia estimada y la tasa de letalidad de la enfermedad cerebrovascular isquémica y hemorrágica en el año 2002 en Cataluña. Rev. Esp. Cardiol. 2007, 60, 573–580. [Referencia cruzada] [PubMed]
6. Arboix, A.; García-Eroles, L.; Masones, J.; Oliveres, M.; Targa, C. Accidente cerebrovascular lacunar hemorrágico. Cerebrovasc. Dis. 2000, 10, 229–234. [Referencia cruzada]
7. Mantener, RF; Hua, Y.; Xi, G. Hemorragia intracerebral: mecanismos de lesión y dianas terapéuticas. LancetaNeurol. 2012, 11, 720–731. [Referencia cruzada]
8. Shet, KN; Rosand, J. Orientación del sistema inmunológico en la hemorragia intracerebral. JAMANeurol. 2014, 71, 1083–1084. [Referencia cruzada] [PubMed]
9. Chu, X.; Wu, X.; Feng, H.; Zhao, H.; Tan, Y.; Wang, L.; corrió, H.; Yi, L.; Peng, Y.; Tong, H.; et al. El acoplamiento entre la interleucina-1R1 y el complejo necrosómico implica la inducción de hemina.neuronalesNecroptosis tras hemorragia intracraneal. Carrera 2018, 49, 2473–2482. [Referencia cruzada]
10. Gramo, M.; Sveinsdottir, S.; Ruscher, K.; Hansson, SR; Cintio, M.; Akerstrom, B.; Ley, D. La hemoglobina induce la inflamación después de una hemorragia intraventricular prematura mediante la formación de metahemoglobina. jneuroinflamación. 2013, 10, 100. [Referencia cruzada]
11. Tschoe, C.; Bushnell, CD; Duncan, PW; Alexander-Miller, MA; Wolfe, SQneuroinflamacióndespués de una hemorragia intracerebral y posibles dianas terapéuticas. J. Stroke 2020, 22, 29–46. [Referencia cruzada]
12. Wang, J. Investigación preclínica y clínica sobre la inflamación después de una hemorragia intracerebral. prog.Neurobiol. 2010, 92, 463–477. [Referencia cruzada]
13. Yu, S.-J.; Wu, K.-J.; Wang, Y.-S.; Song, J.-S.; Wu, C.-H.; Jan, J.-J.; Bae, E.; Chen, H.; Shia, K.-S.; Wang, Y. Efecto protector del antagonista CXCR4 CX807 en un modelo de rata de accidente cerebrovascular hemorrágico. En t. J. Mol. ciencia 2020, 21, 7085. [Referencia cruzada]
14. Mosca, F.; Gianni, ML Leche humana: composición y beneficios para la salud. pediatra Medicina. Chir. 2017, 39, 155. [Referencia cruzada]
15. Donovan, SM; Comstock, SS Los oligosacáridos de la leche humana influyen en la inmunidad sistémica y de la mucosa neonatal. Ana. Nutrición metab. 2016, 69, S42–S51. [Referencia cruzada]
16. Oliveros, E.; Ramírez, M.; Vázquez, E.; Barranco, A.; Subvención, A.; Delgado-García, JM; Buck, R.; Rueda, R.; Martin, MJ La suplementación oral de 2 -fucosilactosa durante la lactancia mejora la memoria y el aprendizaje en ratas.′ J. Nutr. Bioquímica 2016, 31, 20–27. [Referencia cruzada]
17. Vázquez, E.; Barranco, A.; Ramírez, M.; Subvención, A.; Delgado-García, JM; Martínez-Lara, E.; Blanco, S.; Martín, MJ; Castanys, E.; Buck, R.; et al. Efectos de un oligosacárido de la leche humana, 2'-fucosilactosa, sobre la potenciación a largo plazo del hipocampo y las capacidades de aprendizaje en roedores. J. Nutr. Bioquímica 2015, 26, 455–465. [Referencia cruzada] [PubMed]
18. Él, Y.; Liu, S.; Kling, DE; Leona, S.; Lawlor, NT; Huang, Y.; Feinberg, SB; Colina, RD; Newburg, DS El oligosacárido de la leche humana 2'-fucosilactosa modula la expresión de CD14 en enterocitos humanos, atenuando así la inflamación inducida por LPS. Tripa 2016, 65, 33–46. [Referencia cruzada] [PubMed]
19. Wu, K.-J.; Chen, Y.-H.; Bae, E.-K.; Canción, Y.; Min, W.; Yu, S.-J. El oligosacárido 2′ -fucosilactosa de la leche humana reduceneurodegeneraciónen accidente cerebrovascular. Traducir Carrera Res. 2020, 11, 1001–1011. [Referencia cruzada] [PubMed]
20. Wang, T.; Lu, H.; Li, D.; Huang, W. La activación de SERPINE1 mediada por TGF-beta1-está involucrada en la lesión apoptótica e inflamatoria inducida por hemina en las células HT22.neuropsiquiatra. Dis. Tratar. 2021, 17, 423–433. [Referencia cruzada]
21. Dang, Tennessee; obispo, GM; Dringen, R.; Robinson, SR El metabolismo y la toxicidad de la hemina en astrocitos. Glia 2011, 59, 1540–1550. [Referencia cruzada]
22. Robinson, SR; Dang, TN; Dringen, R.; Bishop, toxicidad de GM Hemin: una fuente prevenible de daño cerebral después de un accidente cerebrovascular hemorrágico. Redox Rep. 2009, 14, 228–235. [Referencia cruzada]
23. Gutteridge, JM; Smith, A. Protección antioxidante por hemopexina de peroxidación lipídica estimulada por hemo. Bioquímica J. 1988, 256, 861–865. [Referencia cruzada]
24. Dai, J.; Wu, P.; Xu, S.; Li, Y.; Zhu, Y.; Wang, L.; Wang, C.; Zhou, P.; Shi, H. Cambios en la ultraestructura mitocondrial en células SH-SY5Y durante la apoptosis inducida por hemina.Neuroinforme2017, 28, 551–554. [Referencia cruzada]
25. Lin, S.; Yin, Q.; Zhong, Q.; Lv, F.-L.; Zhou, Y.; Li, J.-Q.; Wang, J.-Z.; Su, B.-Y.; Yang, Q.-W. El hemo activa la lesión inflamatoria mediada por TLR4- a través de la vía de señalización MyD88/TRIF en la hemorragia intracerebral. J. Neuroinflamm. 2012, 9, 46. [Referencia cruzada]
26. Wang, Y.-C.; Zhou, Y.; Colmillo, H.; Lin, S.; Wang, P.-F.; Xiong, R.-P.; Chen, J.; Xiong, X.-Y.; Lv, F.-L.; Liang, Q.-L.; et al. El heterodímero del receptor tipo Toll 2/4 media la lesión inflamatoria en la hemorragia intracerebral. Ana. Neurol. 2014, 75, 876–889. [Referencia cruzada] [PubMed]
27. Kuramatsu, JB; Hüttner, HB; Schwab, S. Avances en el manejo de la hemorragia intracerebral. J. Neural. Transm. 2013, 120, S35–S41. [Referencia cruzada]
28. Suzuki, S.; Kelley, RE; Dandapani, BK; Reyes-Iglesias, Y.; Dietrich, WD; Duncan, RC Respuesta aguda de leucocitos y temperatura en la hemorragia intracerebral hipertensiva. Carrera 1995, 26, 1020–1023. [Referencia cruzada] [PubMed]
29. Wang, J.; Dore, S. Inflammation after intracerebral hemorrhage. J. Cereb. Metab. del flujo sanguíneo. 2007, 27, 894–908. [Referencia cruzada]
30. Stevens, SL; Bao, J.; Hollis, J.; Lesov, NS; Clark, WM; Stenzel-Poore, MP El uso de la citometría de flujo para evaluar los cambios temporales en las células inflamatorias después de la isquemia cerebral focal en ratones. Res. cerebral. 2002, 932, 110–119. [Referencia cruzada]
31. Yu, ZT; Nanthakumar, NN; Newburg, DS El oligosacárido de la leche humana 2' -fucosilactosa apaga la inflamación inducida por Campylobacter jejuni en las células epiteliales humanas HEp-2 y HT-29 y en la mucosa intestinal del ratón. J. Nutr. 2016, 146, 1980–1990. [Referencia cruzada] [PubMed]
32. Bien, M.; Sodhi, CP; Yamaguchi, Y.; Jia, H.; Lu, P.; Fulton, WB; Martín, LY; Prindle, T.; Niño, DF; Zhou, Q.; et al. El oligosacárido 2'-fucosilactosa de la leche humana atenúa la gravedad de la enterocolitis necrosante experimental al mejorar la perfusión mesentérica en el intestino neonatal. Hermano J. Nutr. 2016, 116, 1175–1187. [Referencia cruzada] [PubMed]
33. Thangameeran, SIM; Tsai, S.-T.; Hung, H.-Y.; Hu, W.-F.; Pang, C.-Y.; Chen, S.-Y.; Liew, H.-K. Un papel para el estrés del retículo endoplásmico en la hemorragia intracerebral. Celdas 2020, 9, 750. [CrossRef] [PubMed]
34. Huang, Q.; Lan, T.; Lu, J.; Zhang, H.; Zhang, D.; Lou, T.; Xu, P.; Ren, J.; Zhao, D.; Sol, L.; et al. DiDang tang inhibe la apoptosis mediada por el estrés del retículo endoplásmico inducida por la privación de oxígeno-glucosa y la hemorragia intracerebral mediante el bloqueo de las vías GRP78-IRE1/PERK. Frente. Farmacol. 2018, 9, 1423. [Referencia cruzada]
35. Zhang, Z.; Cho, S.; Rehni, AK; Quero, HN; Dave, KR; Zhao, W. Evaluación automatizada del volumen de hematoma de roedores sometidos a accidente cerebrovascular hemorrágico intracerebral experimental mediante el enfoque de segmentación de Bayes. Traducir Carrera Res. 2020, 11, 789–798. [Referencia cruzada]
36. Bode, L. Oligosacáridos de la leche humana: prebióticos y más allá. Nutrición Rev. 2009, 67, S183–S191. [Referencia cruzada]
37. Yu, S.-J.; Wu, K.-J.; Bae, E.; Wang, Y.-S.; Chiang, C.-W.; Kuo, L.-W.; Harvey, BK; Greig, Nueva Hampshire; Wang, Y. El tratamiento posterior con posición reduce el estrés del retículo endoplásmico y la neurodegeneración en el cerebro con accidente cerebrovascular. iScience 2020, 23, 100866. [Referencia cruzada]
