Primera parte Disfunción de las células endoteliales y aumento del riesgo cardiovascular en pacientes con enfermedad renal crónica
Jun 07, 2023
Abstracto
Se considera que el endotelio es el guardián de la pared del vaso, que mantiene y regula la integridad vascular. En pacientes con enfermedad renal crónica, las funciones protectoras de las células endoteliales se ven afectadas debido al entorno proinflamatorio, protrombótico y urémico causado por la disminución de la función renal, lo que se suma al aumento de las complicaciones cardiovasculares en esta población vulnerable de pacientes. En esta revisión, discutimos el funcionamiento de las células endoteliales en condiciones saludables y la contribución de la disfunción de las células endoteliales a la enfermedad cardiovascular. Además, resumimos los cambios fenotípicos del endotelio en pacientes con enfermedad renal crónica y la relación de la disfunción de las células endoteliales con el riesgo cardiovascular en la enfermedad renal crónica. También revisamos los mecanismos que subyacen a los cambios endoteliales en la enfermedad renal crónica y consideramos posibles intervenciones farmacológicas que pueden mejorar la salud endotelial.
Palabras clave
aterosclerosis, enfermedades cardiovasculares, enfermedades renales crónicas, células endoteliales, rigidez vascular.

Haga clic aquí para comprar el suplemento Cistanche
AUMENTO DEL RIESGO CARDIOVASCULAR EN LA ENFERMEDAD RENAL CRÓNICA
La enfermedad renal crónica (ERC) se define por daño renal o una función de filtración renal reducida (tasa de filtración glomerular<60 mL/minute per 1.73 m²) for a period beyond 3 months that affects health.1 With a global prevalence of ≈13.4%,2 CKD imposes a serious burden on our socioeconomic and healthcare system. CKD is a progressive disease, classified into stages 1 to 5 based on the reduction in kidney function (Figure 1A).1 In end-stage kidney disease (CKD stage 5: glomerular filtration rate <15 mL/minute per 1.73 m²), patients require kidney support therapy as dialysis or kidney transplantation to replace the failing kidney function.

Cabe destacar que los pacientes con ERC de moderada a avanzada tienen un mayor riesgo cardiovascular en comparación con la población general y los pacientes con ERC leve, con una tasa de filtración glomerular estimada más baja y una albuminuria más alta identificadas como factores de riesgo de mortalidad cardiovascular y por todas las causas, independientemente de los tratamientos cardiovasculares tradicionales. factores de riesgo.5,6 En general, del 33,3 % al 37,1 % de los pacientes con CKD3(a/b) y el 39,9 % de los pacientes con CKD4 mueren a causa de enfermedades cardiovasculares (ECV) en comparación con el 21,7 % al 26 % de la población general (Figura 1B). 3 Para los pacientes con enfermedad renal en etapa terminal de 25 a 34 años, la mortalidad anual incluso aumenta de 500 a 1000 veces en comparación con los controles de edad similar con función renal saludable y es comparable a los 85-años de edad en la población general, lo que subraya la alta carga cardiovascular en la ERC6.
En la población general, el infarto de miocardio y los eventos cerebrovasculares son las causas cardiovasculares más importantes de muerte, y subyacen a ≈75 por ciento de todas las muertes relacionadas con ECV (Figura 1C).4 Además, en pacientes con CKD5 en diálisis (CKD5D), estos tipos de ECV siguen siendo importantes ya que representan el 45 por ciento (infarto de miocardio) y el 13 por ciento (eventos cerebrovasculares) de las muertes por causas cardiovasculares, aunque con una responsabilidad conjunta de ≈58 por ciento de todas las muertes asociadas a ECV, tienen una importancia relativa reducida en comparación con el general población. En cambio, los pacientes con CKD5D muestran un aumento relativo de muerte cardíaca súbita e insuficiencia cardíaca, siendo responsables del 28 % y el 9 % de todas las muertes asociadas a ECV en comparación con el 2 % y el 7 % observados en la población general (Figura 1C).4 Esto revela un elevado incremento, especialmente en el riesgo de muerte súbita cardiaca en la ERC avanzada4.
1. Aterosclerosis e infarto de miocardio
La principal causa subyacente tanto del infarto de miocardio como del accidente cerebrovascular es la aterosclerosis, una enfermedad inflamatoria impulsada por los lípidos de las arterias de tamaño mediano a grande que desencadena el desarrollo de lesiones ateroscleróticas.7 Estas lesiones crecen gradualmente con el tiempo y, en última instancia, pueden restringir el flujo sanguíneo o desencadenar trombosis a través de ruptura o erosión de la placa.7,8 Los pacientes con ERC3-5D muestran una mayor prevalencia de lesiones ateroscleróticas subclínicas en comparación con la población general, con un mayor aumento en los estadios más avanzados de la ERC después del ajuste por sexo, edad y diabetes. 9,10 Además, en comparación con los pacientes sin progresión de la ERC, los pacientes con progresión de la ERC durante 24 meses también mostraron con mayor frecuencia una progresión de las lesiones ateroscleróticas detectadas por ecografía.10,11 Después de un infarto agudo de miocardio, los pacientes con ERC muestran una supervivencia reducida en el tiempo. en comparación con los pacientes sin ERC, con un mayor riesgo de muerte, así como de eventos cardíacos no fatales con el aumento del estadio de la ERC.12
2. Muerte súbita cardíaca y miocardiopatía urémica
En la población general, la cardiopatía coronaria es responsable del 80 por ciento de las muertes cardíacas súbitas.13 El aumento desproporcionado de muerte cardíaca súbita en pacientes con ERC avanzada sugiere diferencias en su fisiopatología y causas a medida que disminuye la función renal. La hipertrofia ventricular izquierda se asocia significativamente con un mayor riesgo de muerte súbita cardíaca en la población general14 y puede ser causada por precarga cardíaca (sobrecarga de volumen intravascular), poscarga cardíaca (sobrecarga de presión) o factores independientes de poscarga/precarga.15 Pacientes con ERC se presentan más frecuentemente con hipertrofia ventricular izquierda, con una prevalencia de hasta el 40 por ciento e incluso el 75 por ciento en pacientes con ERC5D.16 Junto con la fibrosis cardíaca, la hipertrofia ventricular izquierda es una de las características de la miocardiopatía urémica y puede desencadenar alteraciones eléctricas cardíacas y lesiones letales. arritmias.15

Cistanche tubulosa
3. La disfunción endotelial (celular) como contribuyente al riesgo cardiovascular
Un contribuyente principal al aumento del riesgo cardiovascular es la disfunción de las células endoteliales, que abarca toda una serie de alteraciones desadaptativas en el fenotipo funcional de las células endoteliales asociadas con un mayor riesgo cardiovascular. Este término fue sugerido en una excelente revisión de Gimbrone et al17 para brindar una distinción del término más restringido "disfunción endotelial", que generalmente se ha utilizado para referirse a anomalías endoteliales que provocan una reducción en la biodisponibilidad del óxido nítrico y la relajación vascular asociada. Existe una heterogeneidad endotelial significativa en todo el árbol vascular, por ejemplo, cuando se comparan las arterias con las venas, así como la microvasculatura (incluidas las grandes arterias de conductos elásticos y musculares) frente a la microvasculatura (incluidos los capilares, las arteriolas y las vénulas) y ambas. La disfunción de las células endoteliales a nivel macro y microvascular contribuye a un mayor riesgo cardiovascular. En esta revisión, discutimos la contribución de la disfunción de las células endoteliales a la ECV con un enfoque especial en pacientes con ERC. Revisamos los hallazgos sobre los mecanismos moleculares que subyacen a la disfunción de las células endoteliales en la ERC y discutimos el impacto de las intervenciones farmacológicas.
LA DISFUNCIÓN DE LAS CÉLULAS ENDOTELIALES COMO CONTRIBUYENTE AL RIESGO CARDIOVASCULAR
1. Disfunción de las células endoteliales y riesgo aterosclerótico
La capa de células endoteliales de la vasculatura proporciona una barrera semipermeable que permite un intercambio regulado de fluidos, moléculas y células y desempeña un papel importante en el mantenimiento de la salud vascular (Figura 2). La disfunción de las células endoteliales macrovasculares es un evento temprano en el desarrollo de lesiones ateroscleróticas. Por un lado, está influenciado por factores hemodinámicos: en áreas de las arterias resistentes a la aterosclerosis, un flujo sanguíneo laminar contribuye a un fenotipo protector de células endoteliales. Sin embargo, las regiones propensas a la aterosclerosis de la vasculatura arterial están expuestas a un flujo sanguíneo oscilatorio perturbado y a un estrés de cizallamiento promediado en el tiempo bajo asociado, que induce estrés oxidativo, cambios fenotípicos endoteliales y alteraciones de la unión celular, así como renovación de células endoteliales (como se discutió). con más detalle en la revisión de Gimbrone et al17). Además, los factores desencadenantes de la inflamación, como las citocinas proinflamatorias, la oxLDL (proteína oxidada de baja densidad), así como diferentes factores de riesgo cardiovascular, como las alteraciones metabólicas y el tabaquismo, contribuyen a la disfunción de las células endoteliales. Además, el estiramiento excesivo de los vasos sanguíneos puede desencadenar la permeabilidad endotelial, las respuestas inflamatorias y el estrés oxidativo.18 Combinado, esto desencadena la señalización proinflamatoria en las células endoteliales con una regulación al alza de las citocinas proinflamatorias (p. ej., IL [interleucina]-1, IL{ {8}}), quimiocinas (p. ej., ligando de quimiocina con motivo CC 2) y moléculas de adhesión de leucocitos endoteliales (VCAM-1 [molécula de adhesión de células vasculares 1], ICAM-1 [molécula de adhesión intercelular 1] , P-selectina), reduce la producción endotelial de óxido nítrico ateroprotector y aumenta la permeabilidad endotelial. Como resultado, se reclutan leucocitos inflamatorios, se adhieren al endotelio inflamado y se infiltran en la pared vascular, donde junto con los lípidos acumulados contribuyen al desarrollo y progresión de las lesiones ateroscleróticas7. El fenotipo ateroprotector del endotelio está regulado por factores de transcripción maestros. como KLF (factor similar a Krupel)-2, KLF-4 y NRF (factor nuclear eritroide 2-factor relacionado)-2, mientras que NF-κB (factor nuclear-κB ) es un factor de transcripción clave que impulsa la inflamación endotelial.17 Además, las células endoteliales muestran una desdiferenciación y una mayor heterogeneidad durante la progresión de la aterosclerosis, con también signos de transición endotelial a mesenquimatosa. La transición de endotelio a mesénquima se caracteriza por la adquisición de funciones de células mesenquimales como la producción de ECM (matriz extracelular) y está impulsada principalmente por los factores de transcripción Snail, Slug y Twist1. Su extensión se ha asociado con la gravedad de las placas de aterosclerosis en las arterias humanas,19,20 y los estudios en animales que investigan los reguladores clave de la transición del endotelio al mesénquima sugirieron un papel importante en la progresión de la placa20 y la calcificación,21 como se analiza en detalle en una excelente revisión por Souilhol et al.22

Cabe señalar que la disfunción de las células endoteliales no solo contribuye al inicio, la progresión y la desestabilización de la placa con la posterior ruptura de la placa, sino también a la erosión de la placa aterosclerótica, que se espera que sea responsable de un tercio de los síndromes coronarios agudos. En este caso, la activación endotelial crónica de bajo grado por, por ejemplo, los ligandos TLR (receptor tipo toll)-2 combinado con la apoptosis de las células endoteliales y el catabolismo de los componentes de la membrana basal puede desencadenar el desprendimiento de las células endoteliales con la posterior formación de trombos en el área denudada.8
2. Disfunción de las células endoteliales y riesgo trombótico
Una capa endotelial sana y funcional a nivel macro y microvascular es crucial en la regulación de la hemostasia e interfiere tanto a nivel de la hemostasia primaria como secundaria para evitar la coagulación y la activación plaquetaria no deseadas (Figura 2). A nivel de la hemostasia primaria, el endotelio provoca una fuerte inhibición plaquetaria por la secreción continua de óxido nítrico (NO) y prostaciclina provocando un aumento de los niveles intraplaquetarios de GMPc (monofosfato de guanosina cíclica) y AMPc (monofosfato de adenosina cíclica), respectivamente23. activación plaquetaria por ATP extracelular y ADP, la capa endotelial expresa CD39 y CD73, exonucleasas que convierten ATP y ADP en adenosina, un inhibidor de plaquetas que al aumentar los niveles de AMPc plaquetario eleva el umbral de activación de plaquetas.24 Además, el glucocáliz endotelial repele las plaquetas al su carga negativa y, como tal, ayuda en la prevención de la adhesión plaquetaria.25,26 A nivel de la hemostasia secundaria, dentro del glucocáliz, los proteoglucanos de sulfato de heparán se unen y promueven la actividad de ATIII (antitrombina III), un potente inhibidor de múltiples factores de coagulación incluyendo trombina, FIXa, FXa, FXIa y FXIIa.26,27 Además, las células endoteliales expresan TFPI (inhibidor de la vía del factor tisular), una serina proteasa que, como su nombre sugiere, interfiere con la coagulación inducida por TF (factor tisular) y, por lo tanto, limita la actividad de la vía extrínseca.27 Junto al TFPI, las células endoteliales expresan constitutivamente trombomodulina, una proteína unida a la membrana que captura la trombina de la circulación y al unirse aumenta la afinidad de la trombina por la proteína C anticoagulante. Junto con la proteína S, activa la proteína C desactiva FVa y FVIIIa.27
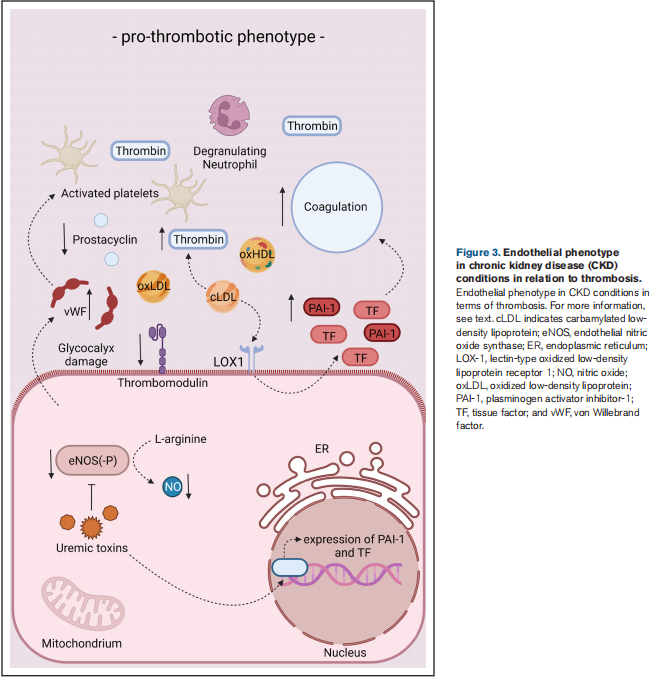
Tras las alteraciones en el metabolismo de los lípidos, la inflamación, el estrés oxidativo y el estrés de cizallamiento fisiopatológico, se desarrolla una disfunción de las células endoteliales, caracterizada por una disminución de las propiedades antitrombóticas y antiinflamatorias y la degradación del glucocáliz. Concomitantemente, el endotelio disfuncional adquiere características proinflamatorias y protrombóticas (Figuras 3 y 4)27. Como resultado, la producción de NO y prostaciclina disminuye, mientras que la secreción de moléculas protrombóticas y proinflamatorias como el vWF (factor de von Willebrand) y la quimiocina CC motivo aumenta el ligando 2.27 Además, la expresión de trombomodulina se regula fuertemente a la baja con la disfunción de las células endoteliales, lo que resulta en una regulación a la baja de la activación de la proteína C, mientras que la expresión de TF se regula al alza favoreciendo la activación de la coagulación.27 Ya durante las primeras etapas de la aterogénesis, los neutrófilos las trampas extracelulares están implicadas en la disfunción de las células endoteliales y alimentan la respuesta tromboinflamatoria.28

En general, estas respuestas protrombóticas y proinflamatorias del endotelio disfuncional se salen de control, creando un círculo vicioso en el que progresa la disfunción de las células endoteliales y se pierde la integridad vascular, lo que resulta en un fuerte aumento del riesgo trombótico.
3. Disfunción endotelial, reducción de la vasorrelajación, aumento de la rigidez vascular y riesgo cardiovascular
El envejecimiento, así como la remodelación fisiopatológica de la pared vascular por factores de riesgo cardiovascular (p. ej., hipertensión, diabetes, enfermedad renal) inducen rigidez arterial, lo que reduce la distensibilidad arterial y aumenta el cizallamiento pulsátil y la presión sobre la vasculatura. A nivel estructural, la rigidez arterial se caracteriza por el depósito de colágeno y la degradación de elastina en la MEC29. Además, el tono de las células musculares lisas vasculares (VSMC) y la disfunción endotelial impactan en la reactividad vascular, con una capacidad de relajación alterada de las VSMC, así como un endotelio reducido. - vasorrelajación dependiente que contribuye a la rigidez arterial. Las células endoteliales juegan un papel importante en la vasorrelajación a través de la producción de NO por eNOS (NO sintasa endotelial; Figura 2), con producción reducida y/o biodisponibilidad de NO u otras sustancias vasodilatadoras que reducen la capacidad de relajación vascular (Figura 5).

El estándar de oro para cuantificar la rigidez arterial es el análisis de la tasa de flujo sanguíneo, medida como velocidad de onda del pulso (PWV, analizada como PWV carótido-femoral o PWV braquial-tobillo). Como alternativa, la forma de la onda de la presión arterial (análisis de la onda del pulso) proporciona información sobre la rigidez arterial mediante la cuantificación del índice de aumento. La función endotelial en términos de respuestas vasodilatadoras se puede medir de forma invasiva o no invasiva dentro de las arterias coronarias epicárdicas, las arterias de conducto periféricas (analizando la dilatación mediada por flujo [FMD] de la arteria braquial como estándar de oro), o dentro de la microvasculatura coronaria o periférica ( Figura 6). Se ha informado que la disfunción endotelial periférica y coronaria se correlaciona entre sí,30,32 aunque otros han informado correlaciones bastante modestas entre la disfunción endotelial periférica y coronaria y sugirieron un posible reflejo de diferentes patologías o lechos vasculares.33 Además, mientras que PWV y el aumento mostraron una buena correlación, este no fue siempre el caso para el índice de aumento y el "índice de hiperemia reactiva" como lectura funcional endotelial no invasiva en la periferia, posiblemente debido al impacto de otros factores además de la función endotelial en la rigidez vascular.34

La rigidez vascular es un marcador de pronóstico temprano de enfermedad coronaria.35 La rigidez vascular aumenta la carga sobre el corazón; insta a una mayor demanda de energía para la eyección cardíaca y desencadena hipertrofia cardíaca.29 Dado que el aumento de la rigidez arterial se asocia con una reducción de la función de Windkessel (es decir, una reducción en la capacidad amortiguadora elástica necesaria para amortiguar las fluctuaciones de la presión arterial), la rigidez arterial también impone un aumento pulsatilidad en la microcirculación y mayor estiramiento cíclico en las células endoteliales. Recientemente, se demostró que este último desencadena la secreción de la proteína GAS6 (growth arrest-specific 6) por parte de las células endoteliales con la posterior señalización proinflamatoria de GAS6/Axl en los monocitos y su transformación en macrófagos y células dendríticas. Como se muestra en un modelo de ratón de remodelación aórtica crónica inducida por angiotensina II, esto contribuyó a la inflamación vascular y renal,36,37 vinculando la rigidez arterial con un mayor daño en los órganos diana.
Dado que la disfunción endotelial es un evento temprano en la ECV que precede a las complicaciones macrovasculares, también se han estudiado intensamente los análisis funcionales endoteliales en términos de regulación del tono vascular para una capacidad predictiva del riesgo cardiovascular más allá de los factores de riesgo cardiovascular tradicionales. En múltiples estudios, la disfunción endotelial macro y microvascular podría predecir de forma independiente eventos cardiovasculares en pacientes con riesgo de enfermedad arterial coronaria. se asoció con un mayor riesgo de eventos cardíacos en pacientes con arteriopatía periférica sometidos a cirugía vascular.38 También en pacientes con insuficiencia cardíaca crónica, la disfunción endotelial analizada por FMD braquial y radial se asoció con futuros eventos cardíacos o mortalidad.39–41 Otros mostraron función endotelial saludable registrada por FMD braquial en individuos aparentemente sanos para dar como resultado una supervivencia significativamente mayor durante un seguimiento de 5-años, incluso después de ajustar los factores de riesgo tradicionales.42,43 Por lo tanto, la disfunción de las células endoteliales puede agregar información importante sobre el riesgo cardiovascular más allá de los factores de riesgo tradicionales.30 Cabe destacar que este valor del análisis de la disfunción endotelial para la predicción del riesgo cardiovascular parece estar influenciado por la cohorte de pacientes analizada, ya que otros no pudieron confirmar un valor de predicción del riesgo cardiovascular para el análisis de la disfunción endotelial basado en la FMD. en una cohorte de ancianos, posiblemente debido a la distensibilidad arterial reducida (es decir, la capacidad vascular para expandirse cuando aumenta la presión) en sujetos de edad avanzada.44 No obstante, este estudio informó una asociación de disfunción endotelial microvascular periférica con un mayor riesgo cardiovascular, como se analiza párrafo con más detalle.

Cistanche en polvo
4. Disfunción microvascular y riesgo cardiovascular
Mientras que las arterias más grandes se ven afectadas predominantemente por cambios ateroscleróticos, la disfunción de la microvasculatura (la red de arteriolas, capilares y vénulas que permiten la perfusión tisular) es diferente. La disfunción microvascular (MVD) puede desarrollarse a nivel de la microcirculación coronaria, así como en la periferia en ausencia o presencia de enfermedad arterial obstructiva de los vasos más grandes. El desarrollo de MVD es multifactorial y puede ser el resultado de cambios funcionales o estructurales o una combinación de ambos, dependiendo de la enfermedad subyacente. En términos de cambios funcionales, las respuestas vasodilatadoras alteradas, al menos parcialmente dependientes del endotelio, subyacen a la MVD. Además, los aumentos en los niveles de sustancias vasoconstrictoras en combinación con una mayor capacidad de respuesta a estos estímulos se han implicado en la MVD, lo que contribuye a la aparición de espasmos vasculares. Los cambios estructurales asociados con la MVD abarcan el estrechamiento luminal de la microvasculatura debido a la remodelación vascular adversa y la fibrosis perivascular; compresión microvascular; rarefacción microvascular que resulta en una pérdida de árboles microvasculares coherentes (capilares, arteriolas pequeñas y vénulas); y microembolización de material aterosclerótico y trombótico.45–48
En cuanto a la disfunción endotelial macrovascular, también la disfunción endotelial microvascular se ha asociado con el riesgo cardiovascular.49 Este fue, por ejemplo, el caso en un estudio prospectivo basado en la población, en el que la disfunción endotelial microvascular periférica, pero no el análisis de la función endotelial mediada por FMD de las arterias de conducto —correlacionada con eventos cardiovasculares (infarto de miocardio, accidente cerebrovascular o muerte) en pacientes de edad avanzada durante 5 años de seguimiento, incluso más allá de los principales factores de riesgo cardiovascular de la escala de riesgo de Framingham44. En la misma línea, la disfunción endotelial microvascular periférica e incluso se desempeñó mejor en la predicción del riesgo cardiovascular futuro en la enfermedad arterial coronaria no obstructiva en comparación con otras puntuaciones de riesgo.50 Además, la disfunción del endotelio arteriolar retiniano predijo de forma independiente MACE en pacientes con enfermedad arterial coronaria o con alto riesgo de enfermedad coronaria.51
También sobre la insuficiencia cardiaca, tanto los pacientes con insuficiencia cardiaca con fracción de eyección del ventrículo izquierdo reducida como los pacientes con insuficiencia cardiaca con fracción de eyección conservada presentan disfunción microvascular. En la insuficiencia con fracción de eyección del ventrículo izquierdo reducida, el análisis de la función endotelial microvascular periférica se asoció con una mayor tasa de eventos relacionados con la IC.52 Los pacientes con insuficiencia cardíaca con fracción de eyección conservada presentan disfunción tanto de los grandes vasos como microvascular.53 Además, muestran una reducción en la densidad microvascular cardíaca54, así como un aumento en los marcadores de disfunción de las células endoteliales en las biopsias de miocardio, incluida la regulación al alza de las moléculas de adhesión endotelial (E-selectina, ICAM-1), reguladores prooxidativos (NOX{{ 7}}) y desacoplamiento de eNOS.55 Se ha propuesto que la disfunción microvascular coronaria contribuye al endurecimiento de la pared cardíaca y la disfunción diastólica en pacientes con insuficiencia cardíaca con fracción de eyección conservada. Sin embargo, sigue debatiéndose si esto implica una relación causal real o más bien una asociación no causal entre la disfunción microvascular coronaria y la insuficiencia cardíaca con fracción de eyección conservada56,57. Cabe señalar que la disfunción microvascular coronaria también puede tener un papel fisiopatológico y pronóstico en otros tipos de ECV, para lo cual nos remitimos a una excelente revisión reciente de Del Buono et al.46

Extracto de Herba Cistanche y Cistanche
5. Disfunción de las células endoteliales y envejecimiento vascular
La disfunción de las células endoteliales con capacidad reducida de vasodilatación endotelial, aumento de la inflamación y la permeabilidad y propiedades protrombóticas mejoradas, todas descritas anteriormente, es una característica importante del envejecimiento vascular. La disfunción de las células endoteliales no solo se observa en la macrocirculación, sino que también contribuye a la disfunción microvascular con el envejecimiento. El envejecimiento vascular se caracteriza además por cambios funcionales y estructurales de la pared vascular y la adventicia por procesos de, por ejemplo, inflamación, calcificación vascular y remodelación de la MEC, que contribuyen aún más a aumentar la rigidez vascular y el riesgo cardiovascular.58
REFERENCIAS
1. Inker LA, Astor BC, Fox CH, Isakova T, Lash JP, Peralta CA, Kurella Tamura M, Feldman HI. Comentario de KDOQI EE. UU. sobre la guía de práctica clínica KDIGO de 2012 para la evaluación y el manejo de la ERC. Am J enfermedad renal. 2014;63:713–735. doi: 10.1053/j.ajkd.2014.01.416
2. Hill NR, Fatoba ST, Oke JL, Hirst JA, O-Callaghan CA, Lasserson DS, Hobbs FDR. La prevalencia mundial de la enfermedad renal crónica: una revisión sistemática y un metanálisis. Más uno. 2016;11:e0158765. doi: 10.1371/journal.pone.0158765
3. Thompson S, James M, Wiebe N, Hemmelgarn B, Manns B, Klarenbach S, Tonelli M; Red de enfermedades renales de Alberta. Causa de muerte en pacientes con función renal reducida. J Am Soc Nephrol. 2015;26:2504–2511. doi: 10.1681/ASN.2014070714
4. Roberts MA, Polkinghorne KR, McDonald SP, Ierino FL. Tendencias seculares en las tasas de mortalidad cardiovascular de pacientes que reciben diálisis en comparación con la población general. Am J enfermedad renal. 2011;58:64–72. doi: 10.1053/j.ajkd.2011.01.024
5. van der Velde M, Matsushita K, Coresh J, Astor BC, Woodward M, Levey A, de Jong P, Gansevoort RT, Matsushita K, Coresh J, et al; Consorcio de Pronóstico de la Enfermedad Renal Crónica. La tasa de filtración glomerular estimada más baja y la albuminuria más alta se asocian con mortalidad cardiovascular y por todas las causas. Un metanálisis colaborativo de cohortes de población de alto riesgo. Riñón Int. 2011;79:1341–1352. doi 10.1038/ki.2010.536
6. Jankowski J, Floege J, Fliser D, Bohm M, Marx N. Enfermedad cardiovascular en la enfermedad renal crónica: conocimientos fisiopatológicos y opciones terapéuticas. Circulación. 2021;143:1157–1172. doi: 10.1161/CIRCULACIÓNAHA.120.050686
7. Weber C, Noels H. Aterosclerosis: patogenia actual y opciones terapéuticas. Nat Med. 2011;17:1410–1422. doi: 10.1038/nm.2538
8. Quillard T, Franck G, Mawson T, Folco E, Libby P. Mecanismos de erosión de las placas ateroscleróticas. Curr Opin Lipidol. 2017;28:434–441. doi: 10.1097/MOL.0000000000000440
9. Betrui A, Martinez-Alonso M, Arcidiacono MV, Cannata-Andia J, Pascual J, Valdivielso JM, Fernández E; Investigadores del Estudio NEFRONA. Prevalencia de ateromatosis subclínica y factores de riesgo asociados en la enfermedad renal crónica: el estudio NEFRONA. Trasplante de Nephrol Dial. 2014;29:1415–1422. doi 10.1093/ndt/gfu038
10. Valdivielso JM, Rodríguez-Puyol D, Pascual J, Barrios C, BermúdezLópez M, Sánchez-Niño MD, Pérez-Fernández M, Ortiz A. Aterosclerosis en la enfermedad renal crónica: ¿más, menos o simplemente diferente?. Arterioscler Thromb Vasc Biol. 2019;39:1938–1966. doi: 10.1161/ATVBAHA.119.312705
11. Gracia M, Betrui A, Martinez-Alonso M, Arroyo D, Abajo M, Fernández E, Valdivielso JM; Investigadores NEFRONA. Predictores de progresión de ateromatosis subclínica a lo largo de 2 años en pacientes con diferentes estadios de ERC. Clin J Am Soc Nephrol. 2016;11:287–296. doi: 10.2215/CJN.01240215
12. Anavekar NS, McMurray JJV, Velazquez EJ, Solomon SD, Kober L, Rouleau JL, White HD, Nordlander R, Maggioni A, Dickstein K, et al. Relación entre la disfunción renal y los resultados cardiovasculares después del infarto de miocardio. N Engl J Med. 2004;351:1285–1295. doi: 10.1056/NEJMoa041365
13. Myerburg RJ, Junttila MJ. Muerte súbita cardiaca causada por enfermedad coronaria. Circulación. 2012;125:1043–1052. doi: 10.1161/CIRCULACIÓNAHA.111.023846
14. Haider AW, Larson MG, Benjamin EJ, Levy D. El aumento de la masa ventricular izquierda y la hipertrofia se asocian con un mayor riesgo de muerte súbita. J Am Coll Cardiol. 1998;32:1454–1459. doi: 10.1016/s0735-1097(98)00407-0
15. Glassock RJ, Pecoits-Filho R, Barberato SH. Masa ventricular izquierda en enfermedad renal crónica y ESRD. Clin J Am Soc Nephrol. 2009;4:S79–S91. doi: 10.2215/CJN.04860709
16. Middleton R, Parfrey PS, Foley RN. Hipertrofia ventricular izquierda en el paciente renal. J Am Soc Nephrol. 2001;12:1079–1084. doi 10.1681/ASN.V1251079
17. Gimbrone MA Jr, García-Cardena G. Disfunción de las células endoteliales y patobiología de la aterosclerosis. Circo Res. 2016;118:620–636. doi: 10.1161/CIRCRESAHA.115.306301
18. Meza D, Musmacker B, Steadman E, Stransky T, Rubenstein DA, Yin W. Las respuestas biomecánicas de las células endoteliales dependen tanto de la tensión de cizallamiento del fluido como de la tensión de tracción. Cell Mol Bioeng. 2019;12:311–325. doi 10.1007/s12195-019-00585-0
19. Evrard SM, Lecce L, Michelis KC, Nomura-Kitabayashi A, Pandey G, Purushothaman KR, d'Escamard V, Li JR, Hadri L, Fujitani K, et al. La transición endotelial a mesenquimatosa es común en las lesiones ateroscleróticas y se asocia con inestabilidad de la placa. Nat Comun. 2016;7:11853. doi: 10.1038/ncomms11853
20. Chen PY, Qin L, Baeyens N, Li G, Afolabi T, Budatha M, Tellides G, Schwartz MA, Simons M. La transición endotelial a mesenquimal impulsa la progresión de la aterosclerosis. J Clin Invest. 2015;125:4514–4528. doi: 10.1172/JCI82719
21. Bostrom KI, Yao J, Guihard PJ, Blazquez-Medela AM, Yao Y. Endothelialmesenchymal Transition in Atherosclerotic lesion calcification. Aterosclerosis. 2016;253:124–127. doi 10.1016/j.aterosclerosis.2016.08.046
22. Souilhol C, Harmsen MC, Evans PC, Krenning G. Transición endotelial-mesenquimal en la aterosclerosis. Cardiovascular Res. 2018;114:565–577. doi: 10.1093/cvr/cvx253
23. Mitchell JA, Ali F, Bailey L, Moreno L, Harrington LS. Papel del óxido nítrico y la prostaciclina como hormonas vasoactivas liberadas por el endotelio. Exp fisiol. 2008;93:141–147. doi: 10.1113/expfisiol.2007.038588
24. Johnston-Cox HA, Ravid K. Adenosina y plaquetas sanguíneas. Señal Purinérgica. 2011;7:357–365. doi: 10.1007/s11302-011-9220-4
25. Born GV, Palinski W. Concentraciones inusualmente altas de ácidos siálicos en la superficie del endotelio vascular. Br J Exp Pathol. 1985;66:543–549.
26. Reitsma S, Slaaf DW, Vink H, van Zandvoort MAMJ, oude Egbrink MGA. El glucocáliz endotelial: composición, funciones y visualización. Arco de Pfugers. 2007;454:345–359. doi 10.1007/s00424-007-0212-8
27. Yau JW, Teoh H, Verma S. Control de trombosis de células endoteliales. Trastorno cardiovascular BMC. 2015;15:130. doi: 10,1186/s12872-015-0124-z
28. Döring Y, Soehnlein O, Weber C. Trampas extracelulares de neutrófilos en la aterosclerosis y la aterotrombosis. Circo Res. 2017;120:736–743. doi: 10.1161/CIRCRESAHA.116.309692
29. Zieman SJ, Melenovsky V, Kass DA. Mecanismos, fisiopatología y terapia de la rigidez arterial. Arterioscler Thromb Vasc Biol. 2005;25:932– 943. doi 10.1161/01.ATV.0000160548.78317.29
30. Flammer AJ, Anderson T, Celermajer DS, Creager MA, Deanfield J, Ganz P, Hamburg NM, Lüscher TF, Shechter M, Taddei S, et al. La evaluación de la función endotelial: de la investigación a la práctica clínica. Circulación. 2012;126:753–767. doi: 10.1161/CIRCULACIÓNAHA.112.093245
31. Alexander Y, Osto E, Schmidt-Trucksass A, Shechter M, Trifunovic D, Duncker DJ, Aboyans V, Back M, Badimon L, Cosentino F, et al. Función endotelial en medicina cardiovascular: un documento de consenso de los Grupos de Trabajo de la Sociedad Europea de Cardiología sobre Aterosclerosis y Biología Vascular, Aorta y Enfermedades Vasculares Periféricas, Fisiopatología Coronaria y Microcirculación, y Trombosis. Cardiovascular Res. 2021;117:29–42. doi: 10.1093/cvr/cvaa085
32. Lerman A, Zeiher AM. Función endotelial: eventos cardíacos. Circulación. 2005; 111: 363–368. doi 10.1161/01.CIR.0000153339.27064.14
33. Schnabel RB, Schulz A, Wild PS, Sinning CR, Wilde S, Eleftheriadis M, Herkenhoff S, Zeller T, Lubos E, Lackner KJ, et al. Medición de la función vascular no invasiva en la comunidad: relaciones transversales y comparación de métodos. Circ Cardiovascular Imaging. 2011;4:371–380. doi: 10.1161/CIRCUITO.110.961557
34. Perrault R, Omelchenko A, Taylor CG, Zahradka P. Estableciendo la intercambiabilidad de la rigidez arterial pero no los parámetros de función endotelial en individuos sanos. Trastorno cardiovascular BMC. 2019;19:190. doi: 10,1186/s12872-019-1167-3
35. Bonarjee VVS. Rigidez arterial: un marcador pronóstico en la enfermedad coronaria. Métodos disponibles y aplicación clínica. Delantero Cardiovasc Med. 2018;5:64. doi: 10.3389/fcvm.2018.00064
36. Van Beusecum JP, Barbaro NR, Smart CD, Patrick DM, Loperena R, Zhao S, de la Visitacion N, Ao M, Xiao L, Shibao CA, et al. Específico de la detención del crecimiento-6 y Axl coordinan la inflamación y la hipertensión. Circo Res. 2021;129:975–991. doi: 10.1161/CIRCRESAHA.121.319643
37. Chen W, Van Beusecum JP, Xiao L, Patrick DM, Ao M, Zhao S, Lopez MG, Billings FT, Cavinato C, Caulk AW, et al. Papel de Axl en la inflamación y el daño de órganos diana debido a la remodelación aórtica hipertensiva. Soy J Physiol Corazón Circ Physiol. 2022;323:H917–H933. doi: 10.1152/ajpheart.00253.2022
38. Huang AL, Silver AE, Shvenke E, Schopfer DW, Jahangir E, Titas MA, Shpilman A, Menzoian JO, Watkins MT, Raffetto JD, et al. Valor predictivo de la hiperemia reactiva para eventos cardiovasculares en pacientes con enfermedad arterial periférica sometidos a cirugía vascular. Arterioscler Thromb Vasc Biol. 2007;27:2113–2119. doi: 10.1161/ATVBAHA.107.147322
39. Fischer D, Rossa S, Landmesser U, Spiekermann S, Engberding N, Hornig B, Drexler H. La disfunción endotelial en pacientes con insuficiencia cardíaca crónica se asocia de forma independiente con una mayor incidencia de hospitalización, trasplante cardíaco o muerte. Eur Heart J. 2005;26:65–69. doi: 10.1093/eurheartj/ehi001
40. Meyer B, Mörtl D, Strecker K, Hülsmann M, Kulemann V, Neunteufl T, Pacher R, Berger R. La vasodilatación mediada por flujo predice el resultado en pacientes con insuficiencia cardíaca crónica: comparación con el péptido natriurético tipo B. J Am Coll Cardiol. 2005;46:1011–1018. doi 10.1016/j.jacc.2005.04.060
41. Katz SD, Hryniewicz K, Hriljac I, Balidemaj K, Dimayuga C, Hudaihed A, Yasskiy A. Disfunción endotelial vascular y riesgo de mortalidad en un paciente con insuficiencia cardíaca crónica. Circulación. 2005; 111: 310–314. doi 10.1161/01.CIR.0000153349.77489.CF
42. Yeboah J, Crouse JR, Hsu FC, Burke GL, Herrington DM. La dilatación mediada por flujo braquial predice eventos cardiovasculares incidentes en adultos mayores: el Estudio de Salud Cardiovascular. Circulación. 2007;115:2390–2397. doi: 10.1161/CIRCULACIÓNAHA.106.678276
43. Yeboah J, Folsom AR, Burke GL, Johnson C, Polak JF, Post W, Lima JA, Crouse JR, Herrington DM. Valor predictivo de la dilatación mediada por flujo braquial para eventos cardiovasculares incidentes en un estudio basado en la población: el estudio multiétnico de aterosclerosis. Circulación. 2009;120:502–509. doi: 10.1161/CIRCULACIÓN AHA.109.864801
44. Lind L, Berglund L, Larsson A, Sundström J. Función endotelial en las arterias de resistencia y conducto y 5-año de riesgo de enfermedad cardiovascular. Circulación. 2011; 123: 1545–1551. doi: 10.1161/CIRCULACIÓNAHA.110.984047
45. Vancheri F, Longo G, Vancheri S, Henein M. Disfunción microvascular coronaria. J Clin Med. 2020;9:2880. doi: 10.3390/jcm9092880
46. Del Buono MG, Montone RA, Camili M, Carbone S, Narula J, Lavie CJ, Niccoli G, Crea F. Disfunción microvascular coronaria en todo el espectro de enfermedades cardiovasculares: revisión JACC State-of-the-Art. J Am Coll Cardiol. 2021;78:1352–1371. doi 10.1016/j.jacc.2021.07.042
47. Ehling J, Babickova J, Gremse F, Klinkhammer BM, Baetke S, Knuechel R, Kiessling F, Floege J, Lammers T, Boor P. Microtomografía computarizada cuantitativa de la disfunción vascular en enfermedades renales progresivas. J Am Soc Nephrol. 2016;27:520–532. doi 10.1681/ASN.2015020204
48. Prommer HU, Maurer J, von Websky K, Freise C, Sommer K, Nasser H, Samapati R, Reglin B, Guimaraes P, Pries AR, et al. La enfermedad renal crónica induce microangiopatía sistémica, hipoxia tisular y angiogénesis disfuncional. Sci Rep. 2018;8:5317. doi: 10.1038/s41598-018-23663-1
49. Querfeld U, Mak RH, Pries AR. Enfermedad microvascular en la enfermedad renal crónica: la base del iceberg en la comorbilidad cardiovascular. Clin Sci (Londres). 2020;134:1333–1356. doi 10.1042/CS20200279
50. Matsuzawa Y, Sugiyama S, Sugamura K, Nozaki T, Ohba K, Konishi M, Matsubara J, Sumida H, Kaikita K, Kojima S, et al. Evaluación digital de la función endotelial y cardiopatía isquémica en mujeres. J Am Coll Cardiol. 2010;55:1688–1696. doi 10.1016/j.jacc.2009.10.073
51. There JD, Al-Fiadh AH, Amirul Islam FM, Patel SK, Burrell LM, Wong TY, Farouque O. Impaired retinal microvascular function predice eventos adversos a largo plazo en pacientes con enfermedad cardiovascular. Cardiovascular Res. 2021;117:1949–1957. doi: 10.1093/cvr/cvaa245
52. Fujisue K, Sugiyama S, Matsuzawa Y, Akiyama E, Sugamura K, Matsubara J, Kurokawa H, Maeda H, Hirata Y, Kusaka H, et al. Importancia pronóstica de la disfunción endotelial microvascular periférica en la insuficiencia cardíaca con fracción de eyección del ventrículo izquierdo reducida. Circ J. 2015;79:2623–2631. doi: 10.1253/circa.CJ-15-0671
53. Maréchaux S, Samson R, van Belle E, Breyne J, de Monte J, Dédrie C, Chebai N, Menet A, Banfi C, Bouabdallaoui N, et al. Función endotelial vascular y microvascular en insuficiencia cardiaca con fracción de eyección preservada. Fallo de la tarjeta J. 2016;22:3–11. doi: 10.1016/j.cardfail.2015.09.003
54. Mohammed SF, Hussain S, Mirzoyev SA, Edwards WD, Maleszewski JJ, Redfield MM. Rarefacción microvascular coronaria y fibrosis miocárdica en insuficiencia cardíaca con fracción de eyección conservada. Circulación. 2015;131:550– 559. doi: 10.1161/CIRCULATIONAHA.114.009625
55. Franssen C, Chen S, Unger A, Korkmaz HI, De Keulenaer GW, Tschöpe C, Leite-Moreira AF, Musters R, Niessen HWM, Linke WA, et al. Activación endotelial inflamatoria microvascular miocárdica en insuficiencia cardíaca con fracción de eyección conservada. Fallo cardíaco JACC. 2016;4:312–324. doi: 10.1016/j.jchf.2015.10.007
56. D'Amario D, Migliaro S, Borovac JA, Restivo A, Vergallo R, Galli M, Leone AM, Montone RA, Niccoli G, Aspromonte N, et al. Disfunción microvascular en insuficiencia cardiaca con fracción de eyección conservada. Fisiol delantero. 2019;10:1347. doi: 10.3389/Phys.2019.01347
57. Cornuault L, Rouault P, Duplàa C, Couffinhal T, Renault MA. Disfunción endotelial en insuficiencia cardiaca con fracción de eyección conservada: ¿cuáles son las pruebas experimentales? Fisiol delantero. 2022;13:906272. doi: 10.3389/Phys.2022.906272
58. Harvey A, Montezano AC, Alves Lopes R, Rios F, Touyz RM. Fibrosis vascular en el envejecimiento y la hipertensión: mecanismos moleculares e implicaciones clínicas. Can J Cardiol. 2016;32:659–668. doi 10.1016/j.cjca.2016.02.070
Constance CFMJ Baaten, Sonja Vondenhoff, Heidi Noels






