Enfermedad pulmonar intersticial pos-COVID y otras secuelas pulmonares, parte 2
Aug 28, 2023
Pacientes hospitalizados
PASC afecta a personas a lo largo de todo el espectro de la enfermedad, desde síntomas mínimos/leves hasta enfermedades críticas. Entre los pacientes hospitalizados, una entrevista telefónica de 488 supervivientes, 60 días después del inicio de los síntomas, encontró que el 32% tenía síntomas persistentes definidos como un conglomerado de dificultad para respirar, tos, opresión en el pecho, sibilancias, dificultad para caminar, dificultad para respirar al subir escaleras, uso de oxígeno, y uso de presión positiva continua en las vías respiratorias (CPAP), y solo el 16 % pudo regresar al trabajo.67 Otra encuesta de 143 pacientes hospitalizados realizada 60 días después del diagnóstico inicial encontró que el 87 % tenía al menos un síntoma persistente y el 55 % tenía tres. o más; sólo el 12% afirmó estar completamente libre de síntomas.68 Halpin y colegas69 realizaron una evaluación transversal de 100 pacientes hospitalizados entre 4 y 8 semanas después de la aparición de los síntomas; El 70% continuó presentando fatiga y el 50% refirió disnea. Huang y sus colegas realizaron un análisis de 17 síntomas diferentes en 1733 pacientes hospitalizados 6 meses después del ingreso, dividiendo la cohorte en escalas de gravedad; El 76% de la cohorte total tuvo al menos un síntoma y la carga de síntomas aumentó con la gravedad de la enfermedad. Los síntomas más comunes fueron debilidad muscular (63%), dificultades para dormir (26%) y ansiedad o depresión (23%). Es de destacar que el 23% de los pacientes tenía una disminución de la 6MWD ajustada por edad y defectos de difusión que se correlacionaban con la gravedad de la enfermedad.
Cistanche puede actuar como antifatiga y potenciador de la resistencia, y estudios experimentales han demostrado que la decocción de Cistanche tubulosa podría proteger eficazmente los hepatocitos hepáticos y las células endoteliales dañadas en ratones nadadores que soportan peso, regular positivamente la expresión de NOS3 y promover el glucógeno hepático. síntesis, ejerciendo así eficacia antifatiga. El extracto de Cistanche tubulosa rico en glucósidos feniletanoides podría reducir significativamente los niveles séricos de creatina quinasa, lactato deshidrogenasa y lactato, y aumentar los niveles de hemoglobina (HB) y glucosa en ratones ICR, y esto podría desempeñar un papel antifatiga al disminuir el daño muscular. y retrasar el enriquecimiento de ácido láctico para el almacenamiento de energía en ratones. Las tabletas compuestas de Cistanche Tubulosa prolongaron significativamente el tiempo de natación con carga de peso, aumentaron la reserva de glucógeno hepático y disminuyeron el nivel de urea sérica después del ejercicio en ratones, mostrando su efecto antifatiga. La decocción de Cistanchis puede mejorar la resistencia y acelerar la eliminación de la fatiga en ratones que hacen ejercicio, y también puede reducir la elevación de la creatina quinasa sérica después del ejercicio de carga y mantener normal la ultraestructura del músculo esquelético de los ratones después del ejercicio, lo que indica que tiene los efectos. de potenciación de la fuerza física y antifatiga. Cistanchis también prolongó significativamente el tiempo de supervivencia de los ratones envenenados con nitritos y mejoró la tolerancia contra la hipoxia y la fatiga.

Haga clic en Fatiga de Covid
【Para más información:george.deng@wecistanche.com / WhatApp:8613632399501】
Pacientes no hospitalizados
Se han hecho observaciones similares en pacientes no hospitalizados. Jacobsen y sus colegas encontraron que en una encuesta de 118 pacientes (96 pacientes ambulatorios), la carga de síntomas fue estadísticamente similar entre el estado hospitalario y el ambulatorio y el 67% de los pacientes continuaron experimentando síntomas, incluida una 6MWD media del 59% de lo esperado. Del mismo modo, en una mediana de seguimiento de 169 días, Logue y colegas72 encontraron una carga similar de persistencia de al menos un síntoma (33 versus 31%) en pacientes ambulatorios versus hospitalizados, respectivamente. También es más probable que los pacientes utilicen los recursos del sistema de salud, incluida la atención primaria ambulatoria y las visitas hospitalarias ambulatorias.73
Factores de riesgo
Los factores de riesgo de PASC siguen siendo desconocidos y los datos siguen siendo discordantes. Wynberg y colegas74 encontraron que el sexo femenino (índice de riesgo ajustado [aHR] 0.65, IC 0.47–0.92) y el índice de masa corporal (IMC) superior a 3{ {8}} (aHR {{10}}.62 IC 0,39–0,97) se asociaron con una recuperación más lenta y los síntomas más allá de los 6 meses se correlacionaron con una menor probabilidad de resolución. Un gran estudio de 2149 profesionales de la salud identificó a 323 participantes que no tenían síntomas o tenían síntomas leves y que resultaron ser seropositivos; El 83 % eran mujeres y el 15 % informó al menos un síntoma persistente a los 8 meses, en comparación con los participantes seronegativos (riesgo relativo [RR] 4,4 [IC 95, 2,9–6,7]), lo que provocó una interrupción significativa en la vida laboral, familiar y en cualquier categoría de la Escala de Discapacidad de Sheehan.75 Entre los pacientes que sobrevivieron a la hospitalización, la presencia de ingreso en la UCI, la necesidad de asistencia respiratoria, problemas pulmonares premórbidos, mayor edad, mayor IMC y BAME (negros, asiáticos y minorías étnicas) predijeron la dificultad para respirar después de la hospitalización. alta.69 Otro estudio sugirió que las mujeres tenían más probabilidades de desarrollar fatiga y ansiedad/depresión y presentar síntomas de palpitaciones, rinitis, disgeusia, insomnio, hiperhidrosis, ansiedad, dolor de garganta y dolor de cabeza predijeron PASC.76 Sudre77 y colegas encontraron que PASC era más probable con el aumento de la edad, el género femenino, un IMC más alto y tener cinco o más síntomas dentro de la primera semana de la aparición. Un estudio de cohorte de 189 personas encontró de manera similar que solo el género femenino y el trastorno de ansiedad preexistente predijeron el PASC en comparación con los controles; en este grupo de pacientes con infección inicial predominantemente leve/moderada, no hubo asociación entre el desarrollo de PASC y cualquier modalidad de prueba de diagnóstico (PFT, ecocardiograma, pruebas serológicas/marcadores inflamatorios y pruebas cognitivas), aunque los participantes con PASC tuvieron puntuaciones significativamente más bajas. en la Encuesta de Salud de SF-36. No hubo evidencia de activación inmune sistémica anormal, enfermedad autoinmune o infección viral persistente.78
Secuelas posagudas de los fenotipos del SARS-CoV-2
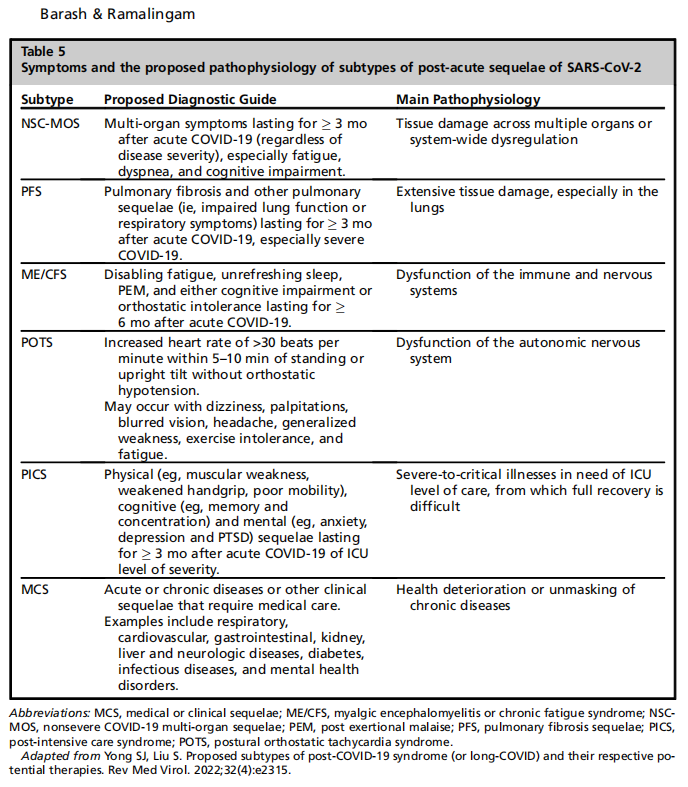
Pueden existir varios fenotipos de PASC. Definirlos es complejo debido a la naturaleza dinámica tanto de la enfermedad inicial como de las secuelas posteriores según la gravedad de la enfermedad. Por ejemplo, un superviviente de SDRA y de un ingreso en la UCI puede desarrollar disnea y PFP anormales que se correlacionan con fibrosis posinfecciosa residual y se superponen con el síndrome post-cuidados intensivos (PICS). Un paciente con una enfermedad leve sin antecedentes conocidos de neumonía u hospitalización también puede desarrollar disnea desproporcionada con las anomalías de las imágenes y los trastornos de la PFT. Como anécdota, este último es un hallazgo notablemente común observado en nuestra clínica PASC, donde la mayoría de las derivaciones son pacientes sin antecedentes de hospitalización y, en general, sin antecedentes conocidos de neumonía previa. Se han propuesto varios sistemas de clasificación. Becker propuso un sistema basado en la gravedad y la evolución de los síntomas a lo largo del tiempo.79 Yong propuso subtipos basados en secuelas clínicas y fisiológicas a largo plazo.80 Las tablas 4 y 5 resumen estos dos esquemas diferentes de subtipificación de fenotipos PASC. Es probable que estas descripciones cambien con el tiempo y probablemente surja otro esquema que ilustre la naturaleza compleja de PASC que, sin duda, continuará evolucionando junto con nuestra comprensión. Lo ideal sería que un esquema más nuevo agrupara a los pacientes en fenotipos que también se correlacionen con resultados clínicamente relevantes. Actualmente no existen pautas formales para definir los fenotipos PASC.

Mecanismo(s) de secuelas posagudas del SARS-CoV-2
Sigue siendo difícil encontrar un mecanismo unificador para la variedad y variabilidad de los síntomas de PASC. Varios estudios han tratado de aclarar las causas de la intolerancia al ejercicio, ya que es un síntoma común y debilitante. Los estudios que utilizaron pruebas de ejercicio cardiopulmonar (CPET) en diversos momentos desde la enfermedad y la recuperación han demostrado limitaciones predominantemente de los umbrales circulatorios y anaeróbicos en comparación con controles emparejados81–83; sin embargo, también se ha sugerido ineficiencia ventilatoria.82 Cassar y colegas 83 realizaron una evaluación longitudinal de 58 sobrevivientes y 30 controles emparejados mediante cuestionarios de síntomas, imágenes por resonancia magnética (RMC) cardíaca y pulmonar y CPET a los 3 y 6 meses. A los 6 meses, los supervivientes demostraron la normalización de las anomalías cardíacas observadas en imágenes de RMC anteriores, aunque las anomalías persistentes (y mejoradas) de bajo grado de las anomalías parenquimatosas y el VO2 máximo persistieron en el 52% de los participantes; Lo más importante (y congruente con nuestra experiencia en el mundo real) es que estas anomalías no se correlacionaron con los síntomas cardiopulmonares. Estos deterioros podrían estar relacionados con daño directo al tejido muscular, deterioro de la extracción/utilización de oxígeno o simple falta de condición física debido a una estadía hospitalaria prolongada y una enfermedad crítica. Con este fin, es probable que la gran variedad de síntomas físicos, neuropáticos y neuropsiquiátricos no se explique únicamente por estos mecanismos, y ciertamente no todos los pacientes experimentarán disnea o intolerancia al ejercicio.
Otros mecanismos propuestos incluyen la regulación negativa de los receptores ACE-2/Ang 1 a 7 con efectos nocivos en sentido ascendente,84 la producción de autoanticuerpos dirigidos a citocinas, quimiocinas, sistema del complemento o proteínas de la superficie celular85, y citocinas proinflamatorias.86,87 La naturaleza de la respuesta inmunitaria inicial también puede influir tanto en el curso clínico de la enfermedad como en las secuelas duraderas.88
Clasificación, evaluación y tratamiento
Debido a la afluencia masiva de pacientes con multitud de síntomas, muchos centros en los Estados Unidos y en el extranjero han iniciado clínicas de COVID de múltiples especialidades para ayudar a clasificar, tratar y abordar la escasez de conocimientos y experiencia en el proceso de esta enfermedad. Las clínicas pueden tener proveedores que representen diversas especialidades médicas, incluidas neurología, neuropsiquiatría y psicología, otorrinolaringología, cardiología, neumología, medicina física y rehabilitación, y terapia física y ocupacional, entre muchas otras. Aún no se ha validado ningún enfoque estandarizado, pero en general se recomienda abordar a los pacientes de manera integral en función de la gravedad de la enfermedad y la carga de síntomas. 55,89,90 Es probable que sean razonables las pruebas de laboratorio básicas, como el hemograma completo, los paneles metabólicos básicos, la función hepática y la función tiroidea. Las pruebas más especializadas, por ejemplo, en busca de evidencia de deficiencias vitamínicas, marcadores inflamatorios, afecciones reumatológicas, lesión miocárdica, etc., deben guiarse por los síntomas y la gestalt clínica. Las pruebas avanzadas pueden incluir imágenes cardíacas y de tórax, electrocardiogramas y pruebas invasivas como cateterismo cardíaco o CPET si existe una alta sospecha clínica. Cabe señalar que no se recomienda un enfoque "rápido" para las pruebas dada la dudosa utilidad clínica, el aumento del costo y la carga emocional para el paciente.

Según la experiencia del autor (MB), los pacientes a menudo tienen problemas para afrontar sus nuevos síntomas y encontrar comprensión por parte de sus familias, compañeros e incluso otros proveedores de atención médica. Una encuesta de 114 profesionales médicos, en su mayoría mujeres (80/114) (51/114) con PASC en el Reino Unido, describió una fuerte sensación de pérdida y estigma, problemas para acceder y navegar por los servicios, y dificultad para ser tomado en serio.91 El médico debe considerar luego, la carga adicional que supone para sus pacientes no médicos. Reconocer los síntomas es muy importante, al igual que validar afirmaciones como "lo que estás pasando es muy real" y "hay muchos otros como tú, que están aprendiendo a afrontar esta nueva enfermedad"; por ejemplo, después de una anamnesis y un examen exhaustivos, nos centramos principalmente en establecer expectativas de que se desconoce el curso temporal de la enfermedad y la recuperación. Una vez que tanto el paciente como el proveedor están listos para seguir adelante, se solicitan las pruebas adecuadas para diagnosticar afecciones nuevas y preexistentes. Se debe hacer hincapié en la terapia sintomática y de apoyo.60 Nuestra práctica se inclina en gran medida hacia la terapia física y ocupacional, ya que la fatiga y la sensación de disnea son a menudo bastante prevalentes y debilitantes. Se debe aconsejar a los pacientes que presten especial atención al "malestar post-esfuerzo", un estado debilitante de aparición de fatiga debido a un sobreesfuerzo físico y/o mental que ha sido bien caracterizado en el contexto del SFC/EM.92 Hábitos alimentarios saludables, higiene del sueño y se fomenta la modificación de las rutinas diarias para priorizar determinadas actividades sobre otras. Los protocolos de reacondicionamiento individualizados deben ser implementados por fisioterapeutas y terapeutas ocupacionales experimentados con experiencia en el tratamiento de pacientes con PASC.55 La clasificación, la evaluación y el tratamiento de los pacientes que padecen PASC siguen siendo dinámicos y un enfoque holístico es primordial.60,93–96
RESUMEN
Las secuelas posteriores a la COVID, incluidas la lesión pulmonar y las PASC, son complejas y poco conocidas y representan manifestaciones, mecanismos y resultados heterogéneos a corto y largo plazo. La base de la terapia sigue siendo principalmente de apoyo, aunque se están realizando investigaciones sólidas para comprender y caracterizar mejor las vías de intervención. La visión histórica sigue siendo importante para aclarar si las observaciones actuales son verdaderamente novedosas o representativas de síndromes previamente ignorados o mal entendidos.
CLÍNICAS PUNTOS DE ATENCIÓN


DIVULGACIÓN
Los autores no tienen nada que revelar.
REFERENCIAS
1. Entonces M, Kabata H, Fukunaga K, et al. Secuelas pulmonares radiológicas y funcionales de COVID-19: una revisión sistemática y metanálisis. BMC Pulm Med 2021;21(1):97.
2. Herridge MS, Tansey CM, Matte A, et al. Incapacidad funcional 5 años después del síndrome de dificultad respiratoria aguda. N Engl J Med 2011;364(14):1293–304.
3. Ahmed H, Patel K, Greenwood DC, et al. Resultados clínicos a largo plazo en sobrevivientes de brotes de coronavirus del síndrome respiratorio agudo severo y del síndrome respiratorio de Oriente Medio después de la hospitalización o el ingreso a la UCI: una revisión sistemática y un metanálisis. J Rehabil Med 2020;52(5): jrm00063.
4. Chen Y, Ding C, Yu L, et al. Seguimiento de un año de los hallazgos de la TC de tórax en pacientes después de una infección por SARS-CoV-2. BMC Med 2021;19(1):191.
5. Bellan M, Soddu D, Balbo PE, et al. Secuelas respiratorias y psicofísicas entre pacientes con COVID-19 cuatro meses después del alta hospitalaria. JAMA Netw Open 2021;4(1):e2036142.
6. Lerum TV, Aalokken TM, Bronstad E, et al. Disnea, función pulmonar y hallazgos de TC 3 meses después del ingreso hospitalario por COVID-19. Eur Respir J 2021;57(4).
7. van den Borst B, Peters JB, Brink M, et al. Evaluación integral de salud a 3 meses de la recuperación de la enfermedad aguda por coronavirus 2019 (COVID-19). Clin Infect Dis 2021;73(5):e1089–98.
8. González J, Benítez ID, Carmona P, et al. Función pulmonar y características radiológicas en sobrevivientes de COVID crítico-19: una cohorte prospectiva de 3-meses. Pecho 2021;160(1):187–98.
9. Liang L, Yang B, Jiang N, et al. Estudio de seguimiento de tres meses de supervivientes de la enfermedad por coronavirus 2019 después del alta. J Korean Med Sci 2020;35(47): e418.
10. van Gassel RJJ, Bels JLM, Raafs A, et al. Alta prevalencia de secuelas pulmonares a los 3 meses del alta hospitalaria en supervivientes de COVID con ventilación mecánica-19. Am J Respir Crit Care Med 2021;203(3):371–4.
11. Guler SA, Ebner L, Aubry-Beigelman C, et al. Función pulmonar y características radiológicas 4 meses después de COVID-19: primeros resultados del estudio nacional prospectivo observacional suizo de pulmón COVID-19. Eur Respir J 2021;57(4):2003690.
12. Zhao YM, Shang YM, Song WB y col. Estudio de seguimiento de la función pulmonar y las características fisiológicas relacionadas de los sobrevivientes de COVID-19 tres meses después de la recuperación. EClinicalMedicine 2020;25:100463.
13. Huang L, Li X, Gu X, et al. Resultados de salud en personas 2 años después de sobrevivir a la hospitalización con COVID-19: un estudio de cohorte longitudinal. Lancet Respir Med 2022;10(9):863–76.
14. Ambardar SR, Hightower SL, Huprikar NA, et al. Fibrosis pulmonar post-COVID-19: nuevas secuelas de la pandemia actual. J Clin Med 2021;10(11): 2452.
15. Han X, Fan Y, Alwalid O, et al. Hallazgos de la TC de tórax de seguimiento a los seis meses después de una neumonía grave por COVID-19. Radiología 2021;299(1): E177–e186.
16. Wang Y, Dong C, Hu Y, et al. Cambios temporales de los hallazgos de la TC en 90 pacientes con neumonía por COVID-19: un estudio longitudinal. Radiología 2020; 296(2):E55-e64.
17. Han X, Fan Y, Alwalid O, et al. Anomalías pulmonares intersticiales fibróticas en la TC de seguimiento de 1-años después de COVID grave-19. Radiología 2021;301(3): E438– e440.

18. Antonio GE, Wong KT, Hui DS, et al. TC de sección delgada en pacientes con síndrome respiratorio agudo severo después del alta hospitalaria: experiencia preliminar. Radiología 2003;228(3):810–5.
19. Das KM, Lee EY, Singh R, et al. Seguimiento de los hallazgos radiológicos de tórax en pacientes con MERS-CoV después de la recuperación. Imágenes de Indian J Radiol 2017; 27(3):342–9.
20. Albert RK, Smith B, Perlman CE, et al. ¿La progresión de la fibrosis pulmonar se debe a una lesión pulmonar inducida por la ventilación? Am J Respir Crit Care Med 2019;200(2):140–51.
21. Cabrera-Benítez NE, Laffey JG, Parotto M, et al. Fibrosis pulmonar asociada a ventilación mecánica en el síndrome de dificultad respiratoria aguda: un factor que contribuye significativamente al mal resultado. Anestesiología 2014;121(1):189–98.
22. Cabrera-Benı´tez NE, Parotto M, Post M, et al. El estrés mecánico induce fibrosis pulmonar por transición epitelial-mesenquimatosa. Cuidado Crítico Med 2012; 40(2):510–7.
23. Tzouvelekis A, Harokopos V, Paparountas T, et al. El perfil de expresión comparativo en la fibrosis pulmonar sugiere un papel del factor alfa inducible por hipoxia en la patogénesis de la enfermedad. Am J Respir Crit Care Med 2007;176(11):1108–19.
24. Higgins DF, Kimura K, Bernhardt WM, et al. La hipoxia promueve la fibrogénesis in vivo mediante la estimulación HIF-1 de la transición epitelial a mesenquimatosa. J Clin Invest 2007;117(12):3810–20.
25. Manresa MC, Ahijado C, Taylor CT. Vías sensibles a la hipoxia en la fibrosis provocada por inflamación. Am J Physiol Regul Integr Comp Physiol 2014;307(12): R1369–80.
26. Myall KJ, Mukherjee B, Castanheira AM, et al. Enfermedad pulmonar intersticial persistente post-COVID-19. Un estudio observacional del tratamiento con corticosteroides. Ann Am Thorac Soc 2021;18(5):799–806.
27. Doglioni C, Ravaglia C, Chilosi M, et al. Neumonía intersticial COVID-19: características histológicas e inmunohistoquímicas en criobiopsias. Respiración 2021;100(6):488–98.
28. Menter T, Haslbauer JD, Nienhold R, et al. El examen postmortem de pacientes con COVID-19 revela daño alveolar difuso con congestión capilar grave y hallazgos variados en los pulmones y otros órganos que sugieren disfunción vascular. Histopatología 2020;77(2):198–209.
29. Barisione E, Grillo F, Ball L, et al. Progresión fibrótica y correlación radiológica en muestras de pulmón coincidentes de autopsias de COVID-19. Arco de Virchows 2021;478(3):471–85.
30. Li Y, Wu J, Wang S, et al. Progresión a daño alveolar difuso fibrosante en una serie de 30 autopsias mínimamente invasivas con neumonía por COVID-19 en Wuhan, China. Histopatología 2021;78(4):542–55.
31. Bharat A, Querrey M, Markov NS, et al. Trasplante de pulmón para pacientes con COVID grave-19. Sci Transl Med 2020;12(574):eabe4282.
32. Aesif SW, Bribriesco AC, Yadav R, et al. Patología pulmonar de COVID-19 después de 8 semanas a 4 meses de enfermedad grave: informe de tres casos, incluido uno con trasplante de pulmón bilateral. Soy J Clin Pathol 2021;155(4):506–14.
33. Bharat A, Machuca TN, Querrey M, et al. Resultados tempranos después del trasplante de pulmón por COVID grave-19: una serie de los primeros casos consecutivos de cuatro países. Lancet Respir Med 2021;9(5):487–97.
34. Culebras M, Loor K, Sansano I, et al. Hallazgos histológicos en criobiopsias transbronquiales obtenidas de pacientes después de COVID-19. Pecho 2022;161(3): 647–50.
35. Konopka KE, Perry W, Huang T, et al. La neumonía intersticial habitual es el hallazgo más común en las biopsias pulmonares quirúrgicas de pacientes con enfermedad pulmonar intersticial persistente después de una infección por SARS-CoV-2. EClinicalMedicine 2021;42:101209.
36. Funke-Chambour M, Bridevaux PO, Clarenbach CF, et al. Recomendaciones suizas para el seguimiento y tratamiento del COVID pulmonar prolongado. Respiración 2021;100(8):826–41.
37. Kostorz-Nosal S, Jastrze˛bski D, Chyra M, et al. Una terapia prolongada con esteroides puede ser beneficiosa en algunos pacientes después de la neumonía por COVID-19. Eur Clin Respir J 2021;8(1):1945186.
38. Zhang P, Li J, Liu H, et al. Consecuencias óseas y pulmonares a largo plazo asociadas con el síndrome respiratorio agudo grave adquirido en el hospital: un seguimiento de 15-años de un estudio de cohorte prospectivo. Bone Res 2020;8:8.
39. Ogata H, Nakagawa T, Sakoda S, et al. Tratamiento con nintedanib para la fibrosis pulmonar después de la enfermedad por coronavirus 2019. Respirol Case Rep 2021;9(5): e00744.
40. Bussolari C, Palumbo D, Fominsky E, et al. Informe de caso: Nintedaninb puede acelerar la recuperación pulmonar en la enfermedad crítica por coronavirus 2019. Front Med (Lausana) 2021;8:766486.
41. Zhang F, Wei Y, He L, et al. Un ensayo de pirfenidona en pacientes adultos hospitalizados con enfermedad grave por coronavirus 2019. Chin Med J (Engl) 2021;135(3): 368–70.
42. Umemura Y, Mitsuyama Y, Minami K, et al. Eficacia y seguridad de nintedanib para la fibrosis pulmonar en la neumonía grave inducida por COVID-19: un estudio intervencionista. Int J Infect Dis 2021;108:454–60.
43. Reina-Gutiérrez S, Torres-Costoso A, Martínez Vizcaíno V, et al. Efectividad de la rehabilitación pulmonar en la enfermedad pulmonar intersticial, incluidas las enfermedades por coronavirus: una revisión sistemática y un metanálisis. Arch Phys Med Rehabil 2021;102(10): 1989–97. e1983.
44. Goodwin VA, Allan L, Bethel A, et al. Rehabilitación para permitir la recuperación de COVID-19: una revisión sistemática rápida. Fisioterapia 2021;111:4–22.
45. Condiciones posteriores a COVID: una descripción general para los proveedores de atención médica. 2022. Un
46. López-León S, Wegman-Ostrosky T, Perelman C, et al. Más de 50 efectos a largo plazo de la COVID-19: una revisión sistemática y un metanálisis. Representante de ciencia ficción 2021;11(1):16144.
47. Assaf GDH, McCorkell L., Louise T., et al., ¿Cómo es la recuperación de COVID-19? Un análisis de la encuesta prolongada sobre síntomas de COVID-19 realizada por un equipo de investigación dirigido por pacientes.
48. Honigsbaum M, Krishnan L. Tomar en serio las secuelas de la pandemia: desde la influenza rusa hasta los transportistas de larga distancia de COVID-19. Lanceta 2020;396(10260): 1389–91.
49. Reid AH, McCall S, Henry JM, et al. Experimentando con el pasado: el enigma de la encefalitis letárgica de von Economo. J Neuropathol Exp Neurol 2001; 60(7):663–70.
50. Comidas RW, Hauser VF, Bower AG. Epidemia de poliomielitis en Los Ángeles de 1934: Parte I. Cal West Med 1935;43(2):123–5.
51. Acheson ED. El síndrome clínico recibe diversos nombres: encefalomielitis miálgica benigna, enfermedad de Islandia y neurastenia epidémica. Am J Med 1959;26(4):569–95.
52. Holmes GP, Kaplan JE, Gantz NM, et al. Síndrome de fatiga crónica: una definición de caso práctico. Ann Intern Med 1988;108(3):387–9.
53. Brurberg KG, Fønhus MS, Larun L, et al. Definiciones de casos de síndrome de fatiga crónica/encefalomielitis miálgica (SFC/EM): una revisión sistemática. Abierto BMJ 2014;4(2):e003973.
54. Fukuda K, Straus SE, Hickie I, et al. El síndrome de fatiga crónica: una aproximación integral a su definición y estudio. Grupo de estudio internacional sobre el síndrome de fatiga crónica. Ann Intern Med 1994; 121(12):953–9.
55. Herrera JE, Niehaus WN, Whiteson J, et al. Declaración de orientación de consenso colaborativo multidisciplinario sobre la evaluación y el tratamiento de la fatiga en pacientes con secuelas posagudas de la infección por SARS-CoV-2 (PASC). Pm r 2021;13(9): 1027–43.

56. Tansey CM, Louie M, Loeb M, et al. Resultados de un año y utilización de la atención médica en sobrevivientes del síndrome respiratorio agudo severo. Arch Intern Med 2007;167(12):1312–20.
57. Lam MH-B, Wing YK, Yu MW-M, et al. Morbilidades mentales y fatiga crónica en supervivientes del síndrome respiratorio agudo severo: seguimiento a largo plazo. Arch Intern Med 2009;169(22):2142–7.
58. Batawi S, Tarazan N, Al-Raddadi R, et al. Calidad de vida informada por los sobrevivientes después de la hospitalización por el síndrome respiratorio de Oriente Medio (MERS). Resultados de calidad de vida en salud 2019; 17(1):101.
59. Lee SH, Shin HS, Park HY, et al. La depresión como mediador de la fatiga crónica y los síntomas de estrés postraumático en supervivientes del síndrome respiratorio de Oriente Medio. Psychiatry Investig 2019;16(1): 59–64.
60. Greenhalgh T, Knight M, A'Court C, et al. Manejo del covid-19 posagudo en atención primaria. Bmj 2020;370:m3026.
61. Tenforde MW, Kim SS, Lindsell CJ, et al. Duración de los síntomas y factores de riesgo para el retraso en el retorno a la salud habitual entre pacientes ambulatorios con COVID-19 en una red de sistemas de atención médica multiestatales - Estados Unidos, marzo-junio de 2020. MMWR Morb Mortal Wkly Rep 2020;69(30):993– 8.
62. Orientación sobre el "COVID prolongado" como discapacidad según la ADA, sección 504 y sección 1557. 2022.
63. Prevalencia de síntomas continuos después de la infección por coronavirus (COVID-19) en el Reino Unido. 2022.
64. Antonelli M, Pujol JC, Spector TD, et al. Riesgo de COVID prolongado asociado con variantes delta versus omicrón del SARS-CoV-2. Lanceta 2022;399(10343): 2263–4.
65. COVID prolongado autoinformado después de la infección con la variante Omicron en el Reino Unido: 6 de mayo de 2022.
66. Ayoubkhani D, Bermingham C, Pouwels KB, et al. Trayectoria de síntomas prolongados de COVID después de la vacunación contra COVID-19: estudio de cohorte comunitario. Bmj 2022;377:e069676.
67. Chopra V, Flanders SA, O'Malley M, et al. Resultados a sesenta días entre pacientes hospitalizados con COVID-19. Ann Intern Med 2021;174(4): 576–8.
68. Carfi A, Bernabei R, Landi F. Síntomas persistentes en pacientes después de COVID agudo-19. JAMÁ 2020; 324(6):603–5.
69. Halpin SJ, McIvor C, Whyatt G, et al. Síntomas posteriores al alta y necesidades de rehabilitación en sobrevivientes de infección por COVID-19: una evaluación transversal. J Med Virol 2021;93(2):1013–22.
70. Huang C, Huang L, Wang Y, et al. 6-consecuencias mensuales de COVID-19 en pacientes dados de alta del hospital: un estudio de cohorte. Lanceta 2021;397(10270): 220–32.
71. Jacobson KB, Rao M, Bonilla H, et al. Los pacientes con enfermedad por coronavirus 2019 (COVID-19) no complicada tienen síntomas persistentes a largo plazo y deterioro funcional similar a los pacientes con COVID grave-19: una advertencia durante una pandemia global. Clin Infect Dis 2021;73(3):e826–9.
72. Logue JK, Franko NM, McCulloch DJ y col. Secuelas en adultos a los 6 meses de la infección por COVID-19. JAMA Netw Open 2021;4(2):e210830.
73. Lund LC, Hallas J, Nielsen H, et al. Efectos posagudos de la infección por SARS-CoV-2 en personas que no requieren ingreso hospitalario: un estudio de cohorte poblacional danés. Lancet Infect Dis 2021;21(10):1373–82.
74. Wynberg E, van Willigen HDG, Dijkstra M, et al. Evolución de los síntomas de COVID-19 durante los primeros 12 meses desde el inicio de la enfermedad. Clin Infect Dis 2021;75(1):e482–90.
75. Havervall S, Rosell A, Phillipson M, et al. Síntomas y deterioro funcional evaluados 8 meses después de COVID leve-19 entre trabajadores de la salud. JAMA 2021;325(19):2015–6.
76. Huang Y, Pinto MD, Borelli JL, et al. Síntomas de COVID, grupos de síntomas y predictores para convertirse en un viajero de larga distancia: buscando claridad en la bruma de la pandemia. medRxiv 2021;03(03): 21252086.
77. Sudre CH, Murray B, Varsavsky T, et al. Atributos y predictores de COVID prolongado. Nat Med 2021; 27(4):626–31.
78. Sneller MC, Liang CJ, Marques AR, et al. Un estudio longitudinal de las secuelas e inmunidad de COVID-19: hallazgos iniciales. Ann Intern Med 2022; 175(7):969–79.
79. Becker RC. COVID-19 y sus secuelas: una plataforma para la atención, el descubrimiento y la formación óptimos del paciente. J Tromb Thrombolysis 2021;51(3):587–94.
80. Yong SJ, Liu S. Subtipos propuestos de síndrome post-COVID- 19 (o COVID prolongado) y sus respectivas terapias potenciales. Rev Med Virol 2022;32(4): e2315.
81. Rinaldo RF, Mondoni M, Parazzini EM, et al. El descondicionamiento como principal mecanismo de alteración de la respuesta al ejercicio en supervivientes de COVID-19. Eur Respir J 2021;58(2):2100870.
82. Singh I, Joseph P, Heerdt PM, et al. Intolerancia persistente al esfuerzo después de COVID-19: conocimientos de las pruebas de ejercicio cardiopulmonar invasivas. Pecho 2022;161(1):54–63.
83. Cassar MP, Tunnicliffe EM, Petousi N, et al. Persistencia de los síntomas a pesar de la mejora en la salud cardiopulmonar: conocimientos de la RMC longitudinal, la CPET y las pruebas de función pulmonar posteriores a la COVID-19. EClinicalMedicine 2021;41:101159.
84. Bolay H, Gul A, Baykan B. COVID-19 es un verdadero dolor de cabeza. Dolor de cabeza 2020;60(7):1415–21.
85. Wang EY, Mao T, Klein J, et al. Diversos autoanticuerpos funcionales en pacientes con COVID-19. Naturaleza 2021;595(7866):283–8.
86. Bhavana V, Thakor P, Singh SB, et al. COVID-19: fisiopatología, opciones de tratamiento, enfoques de nanotecnología y agenda de investigación para combatir la pandemia de SARS-CoV2. Ciencias de la vida Life Sci 2020;261:118336.
87. Alpert O, Begun L, Garren P, et al. Depresión de nueva aparición inducida por tormenta de citocinas en pacientes con COVID-19. Una nueva mirada a la asociación entre la depresión y las citocinas: informes de dos casos. Brain Behav Immun-Health 2020;9:100173.
88. Carvalho T, Krammer F, Iwasaki A. Los primeros 12 meses de COVID-19: una cronología de conocimientos inmunológicos. Nat Rev Immunol 2021;21(4):245–56.
89. Nalbandian A, Sehgal K, Gupta A, et al. Síndrome de COVID-19 posagudo. Nat Med 2021; 27(4):601–15.
90. Lutchmansingh DD, Knauert MP, Antin-Ozerkis DE, et al. Un plan clínico para la recuperación post-coronavirus en 2019: aprender del pasado, mirar hacia el futuro. Pecho 2021;159(3):949–58.
91. Ladds E, Rushforth A, Wieringa S, et al. Síntomas persistentes después de COVID-19: estudio cualitativo de 114 pacientes con "COVID prolongado" y borrador de principios de calidad para los servicios. BMC Health Serv Res 2020;20(1): 1144.
92. Chu L, Valencia IJ, Garvert DW, et al. Deconstrucción del malestar post-esfuerzo en la encefalomielitis miálgica/síndrome de fatiga crónica: un estudio transversal centrado en el paciente. PLoS One 2018;13(6): e0197811.
93. Pavli ATMMHC. Síndrome post-COVID: incidencia, espectro clínico y desafíos para los profesionales de atención primaria de salud. ARCMED Arch Med Res 2021;52(6):575–81.
94. Guía rápida de COVID-19: gestión de los efectos a largo plazo de COVID-19.
95. Siso Almirall A, Brito Zeron P, Conangla Ferrin L, et al. Long Covid-19: Propuesta de guías clínicas de atención primaria para el diagnóstico y manejo de enfermedades. Int J Environ Res Salud Pública 2021;18(8):4350.
96. Parkin A, Davison J, Tarrant R, et al. Un servicio multidisciplinario NHS COVID-19 para gestionar el síndrome post-COVID-19 en la comunidad. J Prim Care Salud Comunitaria 2021;12. 21501327211010994.
97. Usted J, Zhang L, Ni-Jia-Ti MY, et al. Función pulmonar anormal y anomalías residuales de la TC en la rehabilitación de pacientes con COVID-19 después del alta. J Infectar 2020;81(2):e150–2.
98. Huang Y, Tan C, Wu J, et al. Impacto de la enfermedad por coronavirus 2019 en la función pulmonar en la fase de convalecencia temprana. Respir Res 2020;21(1):163.
99. Smet J, Stylemans D, Hanon S, et al. Estado clínico y función pulmonar 10 semanas después de una infección grave por SARSCoV-2. Respir Med 2021;176:106276.
100. Shah AS, Wong AW, Hague CJ, et al. Un estudio prospectivo de 12-resultados respiratorios semanales en hospitalizaciones relacionadas con COVID-19-. Tórax 2021;76(4): 402–4.
101. Mo X, Jian W, Su Z, et al. Función pulmonar anormal en pacientes con COVID-19 al momento del alta hospitalaria. Eur Respir J 2020;55(6):2001217.
【Para más información:george.deng@wecistanche.com / WhatApp:8613632399501】






