Una formulación micelar de quercetina previene la nefrotoxicidad del cisplatino
Mar 16, 2022
para más información:ali.ma@wecistanche.com
Alfredo G. Casanova, Marta Prieto, Clara I. Colino, & et al.
El flavonoide antioxidantequercetinase ha demostrado que previenenefrotoxicidaden modelos animales y en un estudio clínico y, por lo tanto, es un candidato profiláctico muy prometedor en desarrollo.quercetinala solubilidad es muy baja, lo que dificulta la aplicación clínica. El objetivo de este trabajo fue estudiar, en ratas, la biodisponibilidad y la eficacia nefroprotectora de una formulación micelar de Pluronic F127-encapsuladoquercetina(P-quercetina), con hidrosolubilidad mejorada. Administración intraperitoneal de P-quercetinaconduce a un aumento de la concentración plasmática y la biodisponibilidad dequercetinaen comparación con la administración equimolar de naturalesquercetina. Además, P-quercetinaconserva las propiedades nefroprotectoras generales, e incluso mejora ligeramente algunos parámetros de la función renal, en comparación con la naturalquercetina. Específicamente, P-quercetinaredujo el incremento de creatinina plasmática (de 3.4±0.5 a 1.2±0.3 mg/dL) y urea (de 490.9±43.8 a 184.1± 50.1 mg/dL) y la disminución del aclaramiento de creatinina (de {{20}}.08±0.02 a 0.58±0.19 mL/min) inducida por el fármaco quimioterapéutico nefrotóxico cisplatino, y mejoró la evidencia histológica de daño tubular. Esta nueva formulación con propiedades cinéticas y biofarmacéuticas mejoradas permitirá una mayor exploración dequercetinacomo candidato a nefroprotector a dosis más bajas y por vías de administración orientadas a su uso clínico.
Palabras clave:cisplatino;nefrotoxicidad; flavonoide;quercetina; nefroprotección; biodisponibilidad;riñón;micelas; solubilidad; formulación

Prevención denefrotoxicidad
Click to Cistanche para que sirve para enfermedad renal
1. Introducción
Droganefrotoxicidades una preocupación médica y económica grave [1,2], ya que el 25 % de los 100 medicamentos más utilizados en las unidades de cuidados intensivos son nefrotóxicos [3], ynefrotoxicidadtambién es una causa importante de abandono de candidatos durante el proceso de descubrimiento de fármacos 4]. El cisplatino es un agente antitumoral a base de platino que se usa con frecuencia en el tratamiento de una diversidad de neoplasias malignas sólidas [5,6]. Casi el 30 por ciento de los pacientes muestran evidencia denefrotoxicidaddurante los diez primeros días tras la administración de cisplatino, lo que supone una importante limitación en su dosificación y eficacia terapéutica [5-8]. Cisplatino agudonefrotoxicidadprovoca una tubulopatía derivada de una acumulación de 5-veces en las células epiteliales del túbulo proximal, con respecto a su concentración plasmática [9-1l], y en menor medida en el túbulo distal [12,13 ].
La tubulopatía por cisplatino se caracteriza por alteraciones electrolíticas (principalmente hipomagnesemia e hipopotasemia) yagudoriñónlesión(AKI).AKI es un síndrome común caracterizado por una disminución abrupta en la tasa de filtración glomerular (GFR), azotemia severa y, a menudo, oliguria o anuria [7,14]. Además, la disfunción endotelial que aumenta la resistencia vascular renal y altera la autorregulación también contribuye a la LRA inducida por cisplatino[9]. Por lo general, la LRA es una afección reversible que, sin embargo, tiene un impacto relevante en los resultados de los pacientes, incluida una mortalidad hospitalaria elevada (más del 50 por ciento de los casos entre los enfermos críticos), hospitalización prolongada, costos adicionales de atención médica y, en el medio. y escenarios a largo plazo, mayor riesgo de desarrollarenfermedad renal cronicay de morbimortalidad general y cardiovascular [7,14]. A nivel subcelular y molecular, la citotoxicidad tubular del cisplatino está impulsada por la lesión mitocondrial, que reduce la respiración, produce estrés oxidativo e induce la muerte celular apoptótica y necrótica y una respuesta inflamatoria perjudicial [13,15,16]. El estrés oxidativo es reconocido como un mecanismo central de la citotoxicidad del cisplatino ynefrotoxicidad[12,13,15-17], que surge de una mayor producción de especies reactivas de oxígeno y una barrera enzimática antioxidante endógena debilitada [5,7,18].

Medidas profilácticas eficaces para el cisplatinonefrotoxicidadplantean una necesidad clínica no satisfecha para mejorar su perfil farmacotoxicológico y maximizar su utilidad. Las estrategias preventivas existentes, incluida la hidratación intensiva, solo han demostrado una protección limitada [6,19]. Se están desarrollando nuevas estrategias basadas en la administración conjunta de nefroprotectores. Los candidatos nefroprotectores incluyen formulaciones de magnesio |6,9 y, más prominentemente, una variedad de antioxidantes [6,20,21]. Los flavonoides son una familia de productos polifenólicos nefroprotectores derivados de vegetales, frutas, nueces y vino, con fuertes propiedades antioxidantes [22].quercetinaes un flavonoide destacado que ejerce muchos efectos beneficiosos [23,24], incluida la eliminación de especies reactivas de oxígeno, la supresión de la activación plaquetaria, la protección endotelial, la modulación de la inflamación, la inhibición de la apoptosis, la supresión de tumores y la nefroprotección. Coadministración dequercetinajunto con la terapia con cisplatino en un modelo de tumor animal proporciona nefroprotección sin interferir con el efecto antitumoral |25,26]. De hecho, un metanálisis actualizado identificóquercetinacomo un candidato muy prometedor como neuroprotector para un mayor desarrollo clínico [21]. Consistentemente, un estudio clínico reciente reportó un efecto protector dequercetinasobre la nefropatía inducida por contraste (NIC) [27].
Una fuerte limitación a la aplicación potencial dequercetina(compartido por los flavonoides en general) es su baja hidrosolubilidad derivada de su estructura química y fracciones, que reducen su absorción en el intestino delgado y, por lo tanto, su biodisponibilidad y eficacia [23,24,28]. Curiosamente, la glucosa lipofóbica-quercetinaLos conjugados (glucósidos) son sustancialmente más biodisponibles que las agliconas lipofílicas, porque estas últimas son menos solubles en la luz intestinal [24]. En realidad,quercetinaLos glucósidos de las cebollas muestran la tasa de absorción más alta y la grasa de la dieta mejoraquercetinaAbsorción de aglicona en el intestino delgado [29]. La muy baja hidrosolubilidad dequercetinano sólo impide su uso clínico por vías de administración prácticas (es decir, oral, intravascular) sino que también reduce la investigación preclínica. No obstante, en modelos animales, se pueden utilizar vías alternativas (es decir, intraperitoneal) con suspensiones de fármacos con fines de prueba de concepto [25,26].
quercetinaSe han desarrollado formulaciones con nuevos materiales portadores que tienen una hidrosolubilidad mejorada, cuyas propiedades biomédicas deben probarse. Los poloxámeros Pluronic son una clase de materiales portadores que albergan y mejoran la absorción de compuestos insolubles en agua debido a su capacidad para formar micelas en ambientes acuosos [30]. Aquí, planteamos la hipótesis de que una formulación micelar dequercetinaencapsulado con Pluronic F127 descrito previamente [31, conservaría las propiedades nefroprotectoras de losquercetinaal mismo tiempo que ofrece características biofarmacéuticas mejoradas para el manejo, la formulación y la administración.

Prevenirnefrotoxicidad:quercetina
2. Resultados
Se realizó un estudio de biodisponibilidad y nefroprotección con la nueva formulación micelar dequercetinaencapsulado con Pluronic F127[31, y nuestra fórmula tradicional dequercetina|25,26|(ver más adelante Materiales y Métodos). Mientras que este último era una suspensión que contenía un tensoactivo, el primero era una solución salina sin aditivos adicionales. Nuestra formulación tradicional de productos naturalesquercetinasolo era apto para fines experimentales, precipitaba cuando se dejaba quieto y era más difícil de manipular e inyectar. En cambio, la formulación micelar se comportó como una solución y no presentó inconvenientes de uso.
2.1.Estudio de biodisponibilidad
Como método de biodisponibilidad comparativa, la evolución dequercetina(Q) se estudió la concentración plasmática después de un único bolo intraperitoneal de natural y P-quercetina(PQ). La Figura 1 muestra la mediaquercetinacurvas de nivel plasmático obtenidas tras la administración de una dosis dequercetinao P-quercetina. Las concentraciones máximas de fármaco (Cmax) observadas en los grupos Q y PQ fueron 1,14±1,28 ug/mL y 8,90 ±4,62 ug/mL, respectivamente, es decir, un incremento de 7,8-veces para P-quercetina, lo que indica que la formulación micelar aumentó la absorción del fármaco.

Figura 1. Evolución de la concentración plasmática de quercetina tras la administración intraperitoneal de un único bolo de P-quercetina equimolar y quercetina natural.
Los valores se expresan como la media ± error estándar de la media (SEM) (n=5 por grupo). *pags<0.05;><0.01;><0.001 vs.qgroup.="">quercetina(50mg/kg,ip.);PQ:100mg/kgi.pP-quercetina(que contiene 50 mg/kgquercetina).
Tabla 1. Parámetros farmacocinéticos tras la administración intraperitoneal de P-quercetina y quercetina natural (n=5 por grupo).
P: quercetina(50 mg/kg, ip; PQ: P-quercetina(100 mg/kg,ip).AUCo24:área bajo la curva parcial; AUCo: área bajo la curva total; MRT: tiempo medio de residencia; t1/2: vida media de eliminación; X: pendiente de fase terminal.

La Tabla 1 muestra los parámetros farmacocinéticos independientes del modelo dequercetinaen ratas después de la administración de una sola dosis en bolo de naturalquercetinao P-quercetina. El tiempo hasta la Cmax se incrementó de 15 min (para naturalquercetina) a 1 h (para P quercetina). Este retraso puede atribuirse a la liberación sostenida delquercetinade la formulación micelar. La exposición general de las ratas al flavonoide fue significativamente mayor para P-quercetina, como lo demuestra el área más grande bajo la curva (AUC) que se traduce en una biodisponibilidad 302.5 por ciento más alta. Estos resultados sugieren que la mayor solubilidad de la formulación micelar mejora su absorción.
2.2. Estudio de Eficacia Nefroprotectora 2.2.1.Estado Fisiológico
Como lo demuestra la evolución del peso corporal (Figura 2a), la salud general se deterioró después del tratamiento con cisplatino, en comparación con los animales de control. ni naturalesquercetinani p-quercetinamodificó significativamente el efecto del cisplatino. Sin embargo, ambosquercetinatratamientos impidieron casi por completo el aumento de lariñón/proporción de peso corporal inducida por cisplatino (Figura 2b), un parámetro que se sabe que se correlaciona con la magnitud de la deserción paranefrotoxicidad[32].


Figura 2. Evolución del estado general de salud. (a) Variación porcentual en el peso corporal a lo largo del experimento; (b) Relación riñón/peso corporal en el día 9.
Los valores se expresan como la media ± SEM (n=3-5 por grupo). *pags<><0.01;><0.001vs.controlgroup.><0.05;><0.01 vs.="" cp="" group.cp:cisplatin(6.5="" mg/kg,="" i.p.)on="" day="">
CP más Q:quercetina(50 mg/kg, ip) durante 9 días y cisplatino (6,5 mg/kg, ip) el día 3; CP más PQ:P-quercetina(100 mg/kg, ip) durante 9 días y cisplatino (6,5 mg/kg, ip) el día 3.
2.2.2.Valoración de la función renal y del tejido renal
De acuerdo con los criterios internacionales, la LRA se define y diagnostica según las elevaciones de la concentración de creatinina plasmática (Crp)[33-35], un marcador subrogado de la tasa de filtración glomerular (TFG). Otros parámetros, como la concentración de urea en plasma, también se evalúan a menudo como indicadores de azotemia [36-38]. Los incrementos en la Crp y la urea plasmática son signos de TFG reducida y AKI. En nuestro estudio, la función renal se vio gravemente afectada por el cisplatino, y este efectoquercetina. P-quercetinamostró una actividad ligeramente más audaz que la naturalquercetina, como lo indica un daño más leve y un perfil de recuperación mejorado (Figura 3). Las ratas en el grupo de cisplatino (CP) sufrieron una LRA manifiesta, ya que experimentaron un aumento progresivo y significativo en sus niveles de urea y creatinina en plasma en comparación con los de los controles (Figura 3a,b). Estos parámetros también aumentaron en los grupos CP más Q y CP más PQ, pero en un grado significativamente menor. Las diferencias entre los grupos CP más Q y CP más PQ no fueron estadísticamente significativas, sin embargo, las ratas tratadas con P-quercetinamostraron niveles de creatinina y urea ligeramente más bajos que los tratados conquercetina. El aclaramiento de creatinina (ClCr) es un método estándar para medir la TFG [39,40]. De acuerdo con los datos de Cr, el cisplatino indujo una caída profunda, que fue parcialmente mitigada porquercetina(Figura 3c). En este caso, sin embargo, se observó una diferencia notable entre la P-quercetina y la quercetina natural, siendo la primera significativamente más efectiva para mejorar y acelerar la recuperación. Cabe destacar que Clcr y Crpl se comportan de manera inversamente proporcional, lo que solo es evidente en el estado estacionario. Sin embargo, durante la AKI, la función renal cambia continua y rápidamente, lo que resulta en un ligero desacoplamiento de esta relación.


Figura 3. Evolución de los parámetros renales.
(a) Concentración de creatinina en plasma; (b) Concentración de urea en plasma; (c) Aclaramiento de creatinina; (d) Proteinuria; y (e) KIM-1 excreción urinaria.
Los valores se expresan como la media ± SEM (n=3-5 por grupo). *pags<><><0.001 vs=""><0.05;><0.01vs.cp group.cp:cisplatin(6.5="" mg/kg,i.p.)on="" day="">
CP más Q:quercetina(50 mg/kg, ip) durante 9 días y cisplatino (6,5 mg/kg, ip) el día 3; CP más PQ: P-quercetina(100 mg/kg, ip.) durante 9 días y cisplatino (6,5 mg/kg, ip) el día 3. KIM-1:riñónlesiónmolécula1.
La proteinuria también se mide con frecuencia en el contexto de la patología renal. Dependiendo del patrón de daño subyacente, la proteinuria puede tener un origen glomerular (es decir, aumento de la permeabilidad de la barrera de filtración glomerular) o, como en el caso del cisplatinonefrotoxicidad[13], puede surgir de una reabsorción tubular defectuosa debido a una lesión tubular. Se detectó un aumento no significativo de proteinuria en los grupos CP y CP-Q (aunque menos marcado en el último) el día 7, que volvió a la normalidad el día 9. De manera similar, la excreción urinaria de un biomarcador de daño tubular (es decir,riñónlesiónmolécula 1; KIM-1)[41,42]fue aumentado notablemente por el cisplatino, y este aumento fue atenuado por ambas formas dequercetina, aunque P-quercetinafue de nuevo un poco más eficaz.
El estudio histológico del tejido renal fue congruente con los hallazgos bioquímicos. Los especímenes de ratas tratadas con cisplatino revelaron una necrosis tubular masiva en la franja superior de la médula externa, acompañada de cierta afección cortical, yquercetinalesión cortical reducida (Figuras 4 y 5). Las ratas que solo recibieron el agente nefrotóxico desarrollaron dilatación y obstrucción tubular (observada como material hialino acumulado) y necrosis tubular con desepitelización y desprendimiento de células. Ambas cosasquercetinalos tratamientos redujeron de manera similar el daño cortical inducido por el cisplatino pero no tuvieron efecto sobre el daño medular (Figuras 4 y 5).
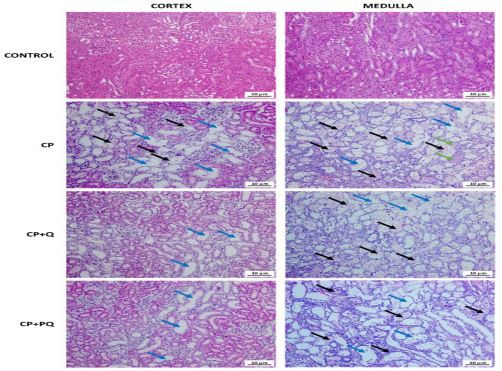
Figura 4. Imágenes representativas de especímenes renales teñidos con hematoxilina y eosina.
Flechas negras: necrosis tubular y desprendimiento celular; flechas azules: dilataciones tubulares; flechas verdes: depósitos intratubulares de material hialino. CP: cisplatino (6,5 mg/kg, ip) el día 3;
CP más Q:quercetina(50 mg/kg, ip) durante 9 días y cisplatino (6,5 mg/kg, ip) el día 3; CP más PQ: P-quercetina(100 mg/kg, ip) durante 9 días y cisplatino (6,5 mg/kg, ip) el día 3.

Figura 5. Cuantificación del daño renal.
Los valores se expresan como la media ± SEM (n =5 imágenes × 3 ratas por grupo). * pags<><0.001 vs.=""><0.05 vs.cp="">
CP: cisplatino (6,5 mg/kg, ip.) el día 3; CP más Q:quercetina(50 mg/kg, ip durante 9 días y cisplatino (6,5 mg/kg, ip) el día 3; CP más PQ: P-quercetina(100 mg/kg, ip) durante 9 días y cisplatino (6,5 mg/kg, ip) el día 3. AU: unidades arbitrarias.
3. Discusión
Nuestros resultados muestran que una formulación micelar dequercetinacon Pluronic F127 (P-quercetina), con propiedades biofarmacéuticas mejoradas, aumentó la biodisponibilidad de este flavonoide antioxidante y mantuvo (o incluso mejoró ligeramente) sus propiedades nefroprotectoras generales en comparación con las naturales.quercetina.
quercetinaha sido postulado como un candidato prometedor para proteger contra el daño renal causado por una serie de fármacos y toxinas, incluidos cisplatino [25,26], metotrexato [43,44], ciprofloxacina [45], NaF [46], HgCl [47l y cadmio [48]. Aunque estos estudios demostraron eficacia preclínica,quercetinano se ha probado en escenarios clínicos similares debido a impedimentos de formulación y baja biodisponibilidad, a excepción de un estudio clínico en el quequercetinaproporcionó cierta protección contra la NIC [27]. Ambas limitaciones son consecuencia de la solubilidad en agua muy pobre (apenas 0.01 mg/mL, a 25 grados [49]) dequercetina, y de su baja estabilidad (que se ve afectada por la temperatura, el pH, la hidroxilación, la actividad enzimática y los iones metálicos)[28,29,50]. administrado por vía oralquercetinase enfrenta a una degradación extensa durante el tránsito estomacal debido al pH gástrico muy bajo (es decir, 1,5) [50]. En el intestino delgado, químicamente protegido por un pH más alto (7,5), el restoquercetinase absorbe mínimamente. Por lo tanto, con el fin de aumentar su biodisponibilidad y eficacia biológica, se han desarrollado nuevas formulaciones de quercetina con el objetivo de mejorar su hidrosolubilidad y proteger sus fracciones activas de la degradación, incluidos liposomas, nanopartículas, nanoemulsiones y micelas [28].
Nuestra formulación micelar con Pluronic F127 aumentaquercetinadiez veces su solubilidad y, en estudios in vitro, ha mostrado un mejor comportamiento de disolución en fluidos gástricos e intestinales simulados, ya que consigue una importante reducción del tamaño de las partículas y una dispersión más homogénea dequercetinaen la matriz polimérica I3l. Esta formulación ofrece una cantidad significativamente mayor dequercetinaal torrente sanguíneo, lo que da como resultado una biodisponibilidad de 3-veces que, curiosamente, se traduce solo en un efecto nefroprotector ligeramente mayor. De acuerdo, no observamos un efecto nefroprotector adicional cuando usamos una dosis más alta (es decir, 100 mg/kg) dequercetinaen experimentos anteriores (nuestras observaciones no publicadas) [25,26]. En esos estudios, nuestra interpretación fue que, probablemente, dosis más altas de ipquercetina(i.e., >50 mg/kg) no se tradujo en una biodisponibilidad aumentada debido a la solubilidad reducida, lo que resultó en una absorción neta no significativamente mayor. Esto coincidió con depósitos amarillos de no absorbidosquercetinaencontrándose en la cavidad peritoneal en el momento del sacrificio. Además, nuestros resultados actuales muestran que incluso concentraciones plasmáticas más altas de quercetina (como las obtenidas con P-quercetina) se traducen en un efecto ligeramente mayor. Porquequercetinala distribución se ha explicado de forma simplificada mediante un modelo de dos compartimentos de primer orden [51], el acceso a las células diana desde el compartimento principal (es decir, el torrente sanguíneo) parece no ser la limitación. Por lo tanto, la razón por la cual el efecto nefroprotector máximo casi se logra con las concentraciones plasmáticas más bajas producidas por la quercetina natural sigue siendo difícil de comprender.
Esto tiene implicaciones prácticas para el desarrollo futuro dequercetinacomo nefroprotector profiláctico. Primero, estos resultados abren la posibilidad de estudiar si los regímenes de dosificación más bajos serán igualmente efectivos, ya que un amplio exceso de biodisponibilidad de P-quercetinapuede sacrificarse sin perder ningún efecto terapéutico pero maximizará el perfil de seguridad. En segundo lugar, ahora se abre la oportunidad para la administración oral, que, sin embargo, debe probarse para la nueva formulación. La absorción desde la cavidad peritoneal evita las barreras encontradas a través de la vía oral. Se plantea la hipótesis de que la mayor solubilidad en la luz intestinal podría conducir a un aumento y fraguadoquercetinabiodisponibilidad dentro de la ventana terapéutica. En tercer lugar, la vía intravenosa ahora podría ser una alternativa realista con una toxicidad minimizada, lo que evitaría las barreras de absorción. Hasta ahora, las formulaciones inyectables experimentales dequercetinautilizó dimetilsulfóxido (DMSO) como disolvente [51].
Se sabe que el cisplatino se acumula y daña los túbulos proximal y distal e induce apoptosis y necrosis de las células epiteliales de los túbulos, dependiendo de la concentración [16]. El segmento S3 proximal es el más afectado, aunque S1 y S2 también se dañan cada vez más con dosis más altas. De acuerdo con sus conocidas propiedades antiapoptóticas en las células de los túbulos [52,53],quercetinareducción de la desepitelización tubular cortical. El efecto idéntico observado con ambas formulaciones refuerza la idea de que elquercetinacinética de distribución a lariñonesestán saturados en nuestro estudio. Además, dentro delriñones, quercetinamuestra un comportamiento diferente a lo largo de la nefrona. En realidad,quercetinano tuvo efecto en la médula externa, donde se encuentra el segmento S3 de los túbulos proximales.quercetinaparece acumularse en los túbulos S1, S2 o distales, que se encuentran cerca de la corteza. Porque se desconoce cómo (es decir, qué transportadores o vías de difusión) y desde dónde (es decir, el lado luminal o basolateral)quercetinaaccede a las células tubulares, se necesita más investigación para explicar estos efectos diferenciales.
La conservación moderada del tejido cortical puede explicar sólo en parte el efecto dequercetinaen la función renal (es decir, GFR). Puede surgir protección adicional de los efectos vasculares dequercetina. La función endotelial participa en la regulación del flujo sanguíneo renal (RBF) y la TFG mediante la modulación del tono contráctil de las arteriolas aferentes y eferentes [54-57]. El cisplatino induce disfunción endotelial, y se cree que esto contribuye sustancialmente a la caída de la TFG, junto con la vasoconstricción aferente renal inducida por los mecanismos de retroalimentación tubuloglomerular (activados por daño tubular) y por citocinas inflamatorias [13,58]. De hecho, la reversión de la disfunción endotelial es un efecto ampliamente reconocido dequercetina(y de flavonoides en general)[59-61l, lo que puede explicar por quéquercetinamejora RBF (y por lo tanto GFR), como se informó anteriormente [25]. Además, estos efectos endoteliales-vasculares también podrían ayudar a explicar la efectividad ligeramente mayor de P-quercetinaen la mejora de la función renal y la recuperación de la función renal. Probablemente no sea descabellado especular que una mayor biodisponibilidad podría tener un efecto más audaz sobre la capa endotelial en contacto directo con la sangre.
Algunos de los efectos observados tras la administración dequercetinapodría ser ejercida por sus metabolitos.quercetinase metaboliza en la mucosa intestinal y el hígado mediante reacciones de glucuronidación, sulfatación y metilación [62], siendo los metabolitos más abundantes los metabolitos glucurónidos en el torrente sanguíneo [63]. Específicamente,quercetinaSe ha demostrado que -3-bO-glucurónido (Q3GA), un metabolito plasmático importante, ejerce efectos antiinflamatorios y vasculares, tanto directamente como después de la metabolización de nuevo a la forma de aglicona [64]. Se necesita más investigación para comprender los metabolitos específicos responsables de la neuroprotección y su producción diferencial y transformación desde diferentes sitios de administración hasta sus objetivos finales.
En conclusión, este estudio inicial muestra el potencial terapéutico de P-quercetinacomo una formulación mejorada con propiedades biofarmacéuticas y farmacocinéticas mejoradas, útil para un mayor desarrollo y uso clínico prospectivo en la profilaxis denefrotoxicidad.

Beneficios de la quercetina sobre la Nefrotoxicidad
4. Materiales y Métodos
Todos los productos químicos y reactivos se adquirieron de Merck (Darmstadt, Alemania) excepto donde se indique lo contrario.
4.1.Elaboración de la Formulación Micelar (P-quercetina)y lo naturalquercetinaFormulación
quercetinaEl hidrato (pureza mínima del 95 por ciento) se adquirió de Acros Organics (Madrid, España) y el copolímero de bloque de óxido de etileno-óxido de propileno Pluronic F127 (peso molecular promedio 12,6 kDa, balance hidrofílico-lipófilo 22) fue proporcionado por BASF (Ludwigshafen am Rhein, Alemania). Para la formulación micelar se utilizó la técnica de precipitación supercrítica con antisolvente para producirquercetina/Pluronic F127 partículas (P-quercetina) como se describió previamente [31]. El Pluronic resultantequercetinala formulación tenía una composición relativa de 50 por ciento/50 por ciento p/p Pluronic F127/quercetina. por lo naturalquercetinaformulación,quercetinase suspendió en 0.16 por ciento de Tween 20 en solución salina, como se describió anteriormente [25,26].
4.2. Animales y Bioética
Todos los procedimientos fueron aprobados por el Comité de Bioética de la Universidad de Salamanca y la Junta de Castilla y León, Ministerio de Agricultura y Ganadería (código: 0000037, de 27 de julio de 2015). Los animales fueron manipulados de acuerdo con las directrices de la Directiva del Consejo de la Comunidad Europea 2010/63/UE y con la legislación española vigente para el uso y cuidado de animales de experimentación (RD53/2013, de 01 de febrero de 2013). Se mantuvieron ratas Wis-tar macho (200-250 g) en condiciones ambientales controladas dentro de las instalaciones del Animalario de la Universidad de Salamanca, con libre acceso a agua y comida estándar.
4.3. Estudio de biodisponibilidad
Las ratas se dividieron en dos grupos experimentales: O (n=5), en el que los animales recibieron una dosis única dequercetina(50mg/kg); y PQ(n=5), en el que los animales recibieron una única dosis equimolar ip de P-quercetina(100 mg/kg (es decir, que contiene 50 mg/kgquercetina). Posteriormente, se tomaron muestras de sangre en tubos recubiertos con ácido etilendiaminotetraacético (EDTA) a partir de una pequeña incisión en la punta de la cola en los siguientes tiempos:0.25,0.5,1,2,8, 12, y 24 h. El plasma se obtuvo por centrifugación y 10μL de ácido ascórbico 10 mM (para evitarquercetinadegradación) se añadió a 100 μL de plasma y se congeló a -80 grados hasta su análisis.quercetinalas concentraciones se determinaron mediante un método de cromatografía líquida de alta resolución (HPLC) de fase inversa con detección UV. Se utilizó una columna Prosper C18 de tamaño de partícula de 3 um, con una fase móvil compuesta por 28 por ciento de acetonitrilo y 72 por ciento de una solución acuosa de 0,2 por ciento de ácido ortofosfórico, a una velocidad de flujo de 1 mL/min. La longitud de onda de detección fue de 371 nm. Previo a la inyección en el equipo de cromatografía, las muestras fueron sometidas a un proceso de glucuronidación para la cuantificación del totalquercetina. Para ello, se añadieron 1000 unidades de -glucuronidasa de Helix pomatia en tampón acetato 0,1 M (pH 5) a 100 μL de plasma, y esta mezcla se incubó a 37 grados durante 1h. . Luego, se realizó un proceso de extracción con 100 μL de una mezcla de acetonitrilo/acético 0.5M80∶20 (tres veces). Una vez que el sobrenadante se evaporó en una corriente de nitrógeno, el residuo seco se volvió a disolver en los 40 μL de la fase móvil y se inyectaron 20 μL en el sistema de HPLC.
4.4. Estudio de nefroprotección
Las ratas se dividieron en los siguientes grupos experimentales (Figura 6): los animales de control (n=3) recibieron vehículo (NaCl0, 9 por ciento) por vía intraperitoneal (ip) durante 9 días; Los animales CP(n=5) recibieron una dosis nefrotóxica única de cisplatino (6,5 mg/kg, ip) el día 3 del experimento; los animales CP más Q(n=5) recibieron una dosis diaria dequercetina(50 mg/kg, ip) durante 9 días y una dosis única de cisplatino (6,5 mg/kg, ip) el día 3; y CP más PQ (n=5) animales recibieron una dosis diaria de P-quercetina(100 mg/kg, ip (es decir, que contiene 50 mg/kgquercetina)) durante 9 días y una dosis de cisplatino (6,5 mg/kg, ip) el día 3.

Figura 6. Esquema del modelo de nefrotoxicidad.
CP: cisplatino (6,5 mg/kg, ip) el día 3; CP más Q:quercetina(50 mg/kg, ip) durante 9 días y cisplatino (6,5 mg/kg, ip) el día 3; CP más PQ:P-quercetina(100 mg/kg, ip.) durante 9 días y cisplatino (6,5 mg/kg, ip) el día 3.
Se recolectaron muestras de sangre (150 μL) los días 0, 3, 5, 7 y 9 en capilares heparinizados de una pequeña incisión en la punta de la cola. El plasma se separó por centrifugación (11.000 rpm durante 3 min) y se mantuvo a-80C. Los días 7 y 9, se recogió orina de 24 h en jaulas metabólicas, se aclaró mediante centrifugación (2000 × g durante 9 min) y se almacenó a -80 grados. Al final del experimento (día 9), las ratas fueron anestesiadas y susriñonesfueron disecados, pesados y fijados en paraformaldehído al 3,7 por ciento para estudios histológicos.
La creatinina en plasma y orina se midió utilizando un kit comercial basado en el método de Jaffe [65] (QuantiChrom Creatinine Assay Kit, BioAssay Systems, Hayward, CA, EE. UU.). La urea plasmática se determinó utilizando un kit comercial basado en el método de Jung [66] (Quan-tiChrom Urea Assay Kit, BioAssay Systems, Hayward, CA, EE. UU.). El aclaramiento de creatinina (Clcr) se calculó mediante la fórmula: Clcr=Crur × UF/ Crp); donde Crur corresponde a la concentración urinaria de creatinina, UF es el flujo de orina y Crp es la concentración plasmática de creatinina. La proteinuria se midió con el ensayo de Bradford [67]. KIM-1 se cuantificó usando el RatRiñónlesiónmolécula 1(KIM-1)Kit ELISA (Cusabio, Houston. TX, EE. UU.). siguiendo las instrucciones del fabricante.
Para los estudios histológicos, las muestras renales se incluyeron en parafina y las secciones de tejido de 5 um se tiñeron con hematoxilina y eosina. Las fotografías se tomaron con un microscopio Olympus BX51 conectado a una cámara digital a color Olympus DP70 (Olympus, Madrid, España). La cuantificación del daño se realizó de manera ciega como se describió anteriormente [68]. En resumen, se tomaron cinco fotografías aleatorias de la región cortical y cinco fotografías de la región medular externa (es decir, las áreas dañadas por el cisplatino), mapeando uniformemente estas áreas. Cada imagen se dividió en 10 secciones idénticas (utilizando el software Microsoft Office PowerPoint 2016), a cada una de las cuales se le asignó una puntuación de 0 (sin daño), 1 (presencia de daño en menos de 1/3 del área), 2 (presencia de daño entre 1/3-2/3 del área), o 3 (presencia de daño en más de 2/3 del área). El daño se evaluó teniendo en cuenta la presencia de necrosis tubular y desprendimiento celular, dilatación tubular, vacuolización, presencia de depósitos hialinos y pérdida del borde en cepillo.
4.5.Análisis estadístico
Los datos se presentan como la media ± error estándar de la media (SEM). Los valores atípicos se identificaron mediante la prueba de Grubbs|69]. La distribución normal de los datos se evaluó mediante la prueba de Shapiro-Wilk. En el estudio de biodisponibilidad, la comparación entre los dos grupos se realizó mediante la prueba t de Student o la prueba U de Mann-Whitney. El estudio farmacocinético se llevó a cabo mediante un análisis independiente del modelo de los niveles plasmáticos medios dequercetina. Los parámetros estimados para evaluar la biodisponibilidad relativa dequercetinafueron el área bajo la curva parcial de los niveles plasmáticos (AUC)24, el área bajo la curva total de los niveles plasmáticos (AUC)0~, la pendiente de la fase terminal, la vida media de eliminación (ti/2) , y el tiempo medio de residencia (TRM). La estimación de los parámetros farmacocinéticos se realizó combinando el método trapezoidal para la estimación del área bajo la curva parcial y la regresión no lineal de la fase terminal de la curva de nivel plasmático. Para el estudio de nefroprotección, se realizó un análisis de varianza (ANOVA) con pruebas de Scheffe o una prueba de Kruskal-Wallis para comparaciones entre grupos. El análisis estadístico se realizó con el software IBM SPSS Statistics 20.0 (International Business Machines, Armonk, NY, EE. UU.). Se utilizaron Microsoft Office Excel y PowerPoint 2016 (Microsoft, Redmond, WA, EE. UU.) para crear el arte y las ilustraciones.
Referencias
1. Awdishu, L.; Mehta, RLThe6R's of Drug-Inducednefrotoxicidad. BMCNephrol.2017,18,124. [CrossRefl[PubMed]
2. Perazella, MADuso de drogas ynefrotoxicidaden la Unidad de Cuidados Intensivos.RiñónInt.2012,81,1172-1178. [Referencia cruzada] [PubMed]
3. Taber, SS; Mueller, BADrug-Associated Renal Dysfunction. Crit.Care Clin.2006,22,357-374, vi. [Referencia cruzada] Huang, JX; Blaskovich, MA; Ensayos basados en Cooper, MACell y biomarcadores para predecirnefrotoxicidad.
Nota:lo anterior no es una lista completa de referencias
