El papel de la evaluación de la masa muscular por tomografía computarizada en la predicción de complicaciones quirúrgicas postoperatorias después del trasplante renal
Mar 16, 2022
Introducción
Trasplante renales el tratamiento de referencia para la etapa final Insuficiencia renal. En comparación con la diálisis prolongada, los pacientes trasplantados tienen una esperanza de vida promedio de 9 años más alta [1]. Las complicaciones quirúrgicas y médicas se han evaluado en la literatura para evaluar los posibles factores de riesgo y, en consecuencia, para optimizar la selección del paciente antestrasplante renal. Por lo tanto, los factores morfométricos intrínsecos, como la obesidad o la distribución del tejido adiposo, parecen asociados con un mayor riesgo de complicaciones postoperatorias [2]. Sin embargo, es necesario evaluar los cambios en la morfometría y la homeostasis debido a la hemodiálisis a largo plazo para predecir mejor los resultados posteriores al trasplante. La desnutrición proteico-energética es uno de los factores de riesgo conocidos que contribuyen significativamente a la mortalidad por diálisis [3]. Alrededor del 75% de los pacientes en hemodiálisis en la lista de espera sufren de desnutrición proteico-energética [4, 5]. En 2019, la Autoridad Nacional de Salud de Francia revisó su definición de desnutrición en adultos. Ahora se utilizan tres criterios fenotípicos: pérdida de peso, índice de masa corporal (IMC) y reducción de la masa muscular o la función [6]. Este último criterio, que aparecía en estas nuevas recomendaciones, introduce la noción de sarcopenia en la definición de desnutrición.

CISTANCHE MEJORARÁ LA FUNCIÓN RENAL/RENAL
Aunque la prevalencia de sarcopenia se estima entre el 5 y el 37% para los pacientes con enfermedades crónicasnefropatía, no hay datos claros entre la población de pacientes en hemodiálisis [7]. La sarcopenia se define por un deterioro muscular gradual y generalizado. Es un factor de riesgo de caídas, discapacidad o fracturas, y aumenta el riesgo de mortalidad [8, 9]. Para evaluar la sarcopenia, ahora existen criterios clínicos defnite que involucran la masa muscular y la disminución de la función (baja fuerza muscular, baja cantidad muscular y bajo rendimiento físico) [10]. La medición por tomografía computarizada (TC) del área de superficie muscular de los músculos psoas-ilíacos es una buena herramienta para evaluar la sarcopenia porque se correlaciona con la masa muscular [11-13] y se está convirtiendo en la medición de referencia para la evaluación nutricional y pronóstica de pacientes preoperatorios en el campo de la oncología [14].
Sin embargo, las asociaciones entre la sarcopenia ytrasplante renallos resultados postoperatorios han sido poco estudiados en la literatura actual, especialmente mediante exámenes por imágenes. Pinar et al. han demostrado una asociación entre la sarcopenia, calculada utilizando la superficie del psoas en la tomografía computarizada, y las complicaciones quirúrgicas posteriores al trasplante de 1 año [15]. En su estudio, los autores incluyeron solo a receptores obesos o con sobrepeso. Además, otro estudio elaboró una edad morfométrica basada en medidas de tomografía computarizada y mostró una asociación con la supervivencia general postoperatoria [16]. En este estudio, nuestro objetivo fue evaluar la correlación entre la sarcopenia definida por la masa muscular medida en la tomografía computarizada ytrasplante renalresultados en una cohorte de receptores no seleccionados.
Palabras clave (MeSH):trasplante renal; Sarcopenia; Insuficiencia renal en etapa terminal; Complicaciones; enfermedad renal; Insuficiencia renal

CISTANCHE MEJORARÁ LA INSUFICIENCIA RENAL/RENAL
Materiales y métodos
Diseño del estudioCada paciente consecutivo sometido atrasplante renalen nuestro hospital académico se incluyó retrospectivamente en este estudio entre 2011 y 2018. Se excluyeron los pacientes que recibieron más de untrasplante de riñón, trasplante multiorgánico, pacientes con tomografía computarizada preoperatoria realizada>12 meses antes del trasplante o tomografía computarizada con artefacto que distorsiona las mediciones radiológicas (líquido libre intraabdominal, hematoma de pared, movimientos del paciente durante la tomografía computarizada). Los datos relativos al período perioperatorio y al seguimiento de 1 año se recogieron mediante notas médicas. Se recogió la duración de la hospitalización, así como el retraso en la reanudación de la función, definido en caso de necesidad de diálisis dentro de los 7 días posteriores a la operación. Se especificaron protocolos de inmunosupresión, inducción y mantenimiento postoperatorio. También se indicó la necesidad de aminas o transfusión intraoperatoria.
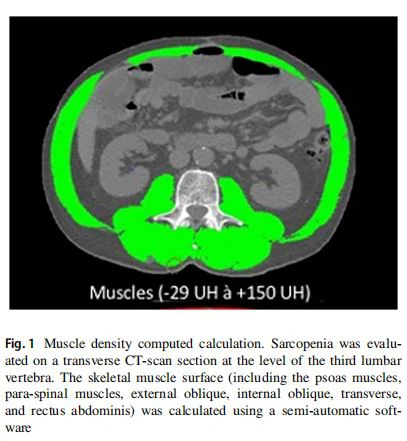
Para cada paciente incluido, la masa muscular se evaluó en la sección de tomografía computarizada axial a nivel de la tercera vértebra lumbar (L3) antes de la administración intravenosa de contraste (la configuración de la máquina se estableció en 120 Kvp y se utilizó modulación de corriente automatizada con un mAs de referencia de 400). La superficie del músculo esquelético (incluidos los músculos psoas, los músculos paraespinales, el oblicuo externo, el oblicuo interno, el transverso y el recto abdominal) se calculó utilizando un software semiautomático. Las mediciones fueron realizadas por un único operador experto, utilizando el software Slice-O-Matic (versión 5.0; TomoVision, Montreal, Quebec, Canadá). El músculo se detectó automáticamente entre -30 y 150 unidades de Hounsfield en la sección de tomografía computarizada. Esta evaluación calcula el índice del músculo esquelético (SMI) (cm2 / m2 ) dividiendo el área de sección transversal (cm2 ) del músculo esquelético a nivel de la tercera vértebra lumbar por el cuadrado de la altura del paciente (m2 ) en la TC. La densidad muscular, en unidades de Hounsfield, también se calculó en la misma sección de TC L3 y representó la densidad media de los músculos detectados (Fig. 1). Como la sarcopenia se define clínicamente, no hay definiciones consensuadas claras sobre las tomografías computarizadas y no fue posible utilizar ninguna definición validada de sarcopenia.
El estudio fue aprobado por el comité de ética local (octubre de 2019) y se llevó a cabo siguiendo los principios de la declaración de Helsinki. La base de datos fue declarada a la Junta Nacional de Informática y Libertad (Commission Nationale Informatique et Liberté, CNIL).
Gestión postoperatoriaLos pacientes fueron monitorizados en la unidad de cuidados intensivos de nefrología durante los primeros 3 días postoperatorios en ausencia de complicaciones antes de su traslado al servicio de nefrología. El catéter urinario y el drenaje fueron, respectivamente, retirados en los días 5 y 6. El catéter JJ se retiró sistemáticamente 1 mes después de la cirugía en una consulta dedicada. Se realizó una biopsia de protocolo del trasplante a los 3 meses.
ResultadosEl criterio de valoración primario fue la aparición de complicaciones mayores postoperatorias a 1 mes y 1 año después del trasplante. Las complicaciones se clasificaron según la clasificación de Clavien-Dindo y una complicación de grado 3 o superior según esta clasificación se consideró como mayor.
CISTANCHE MEJORARÁ EL DOLOR RENAL/RENAL
Análisis estadísticoLos análisis estadísticos se realizaron con el software Stata (versión 15; StataCorp, College Station, Texas, EE.UU.), considerando un riesgo de error bilateral de la primera especie del 5%. Se estableció significación estadística para un valor de p<0.05. categorical="" variables="" were="" described="" as="" numbers="" and="" percentages,="" whereas="" quantitative="" variables="" as="" mean="" (±standard="" deviation)="" or="" median="" [interquartile="" range]="" with="" respect="" to="" their="" statistical="" distribution="" (normality="" studied="" by="" the="" shapiro–wilk="" test).="" comparisons="" between="" independent="" groups="" for="" quantitative="" parameters="" were="" performed="" by="" student's="" t-test="" or="" by="" mann–whitney="" test="" if="" t-test="" conditions="" were="" not="" met="" (normality,="" homoscedasticity="" studied="" by="" fisher–snedecor's="" test).="" inter-group="" comparisons="" of="" qualitative="" parameters="" were="" performed="" by="" the="" chi="" 2="" test="" or="" by="" fisher's="" exact="" test.="" finally,="" in="" a="" multivariate="" situation,="" logistic="" regression="" was="" implemented="" by="" considering="" the="" covariates="" with="" respect="" to="" the="" univariate="" analysis="" results="" (p≤0.1),="" to="" study="" the="" factors="" associated="" with="" major="" complications.="" the="" results="" are="" expressed="" in="" terms="" of="" odds="" ratio="" (or)="" and="" 95%="" confidence="">
Resultados
PoblaciónEn total, se sometieron 397 pacientestrasplante renaldurante el período de estudio, 102 personas se sometieron a una tomografía computarizada preoperatoria de menos de 12 meses de edad, y fueron incluidas en el estudio. De los 102 pacientes incluidos, la edad media y la desviación estándar (DE) fue de 54±28,3 años, 67 (64,7%) eran hombres y 35 (35,3%) eran mujeres (Tabla 1). La duración media de la diálisis antes del trasplante y la DE fue de 104±31,6 días. En general

92 trasplantes (88,5%) fueron de donantes fallecidos a los que 40 (38,5%) habían ampliado los criterios. La media y el índice de masa corporal SD y el índice del músculo esquelético fueron, respectivamente, 25,1±4,2 kg/m2 y 44,8±12,1 cm2/m2. La superficie muscular media y la SD fueron de 126±46,2 cm2 y su densidad fue de 35,4±11,6 unidades de Hounsfield.
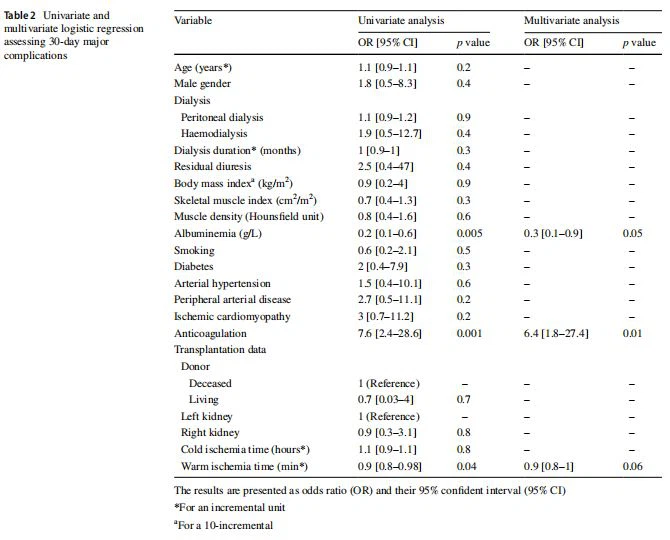
Complicaciones posteriores al trasplante de un mesA 1 mes después del trasplante, 67 pacientes (63,9%) tuvieron una complicación, de los cuales 14 (13,8%) se consideraron mayores, 3 pacientes (2,9%) se sometieron a la extracción del trasplante y 2 pacientes (2%) murieron. Los detalles de estas complicaciones se describen en la Tabla suplementaria 1. En el análisis de regresión logística univariada, la albuminemia plasmática, el uso de anticoagulación y tiempo de isquemia caliente se asoció significativamente con complicaciones postoperatorias de Clavien-Dindo≥3 [orinemia plasmática (IC del 95%), 0,2 (0,1-0,6), 7,6 (2,4-28,6) y 0,9 (0,8-0,98)] (Tabla 2). Finalmente, la albuminemia plasmática baja y el uso de anticoagulantes fueron factores de riesgo de complicación postoperatoria en el análisis multivariable [or (IC95%) respectivamente, 0,3 (0,1–0,9) p=0,05 y 6,4 (1,8–27,4) p=0,01].
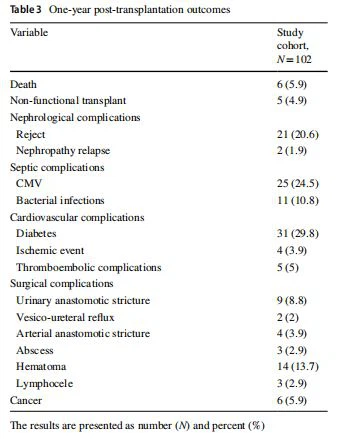
Complicaciones quirúrgicas posteriores al trasplante de un añoDespués de un seguimiento de 1 año, seis pacientes habían muerto (5,9%) y cinco pacientes (4,9%) regresaron a diálisis (Tabla 3). En general, 62 pacientes (60,8%) tuvieron una complicación médica y 30 (29,4%) una complicación quirúrgica en el año siguiente al trasplante. En el análisis univariado, la densidad muscular y el uso de anticoagulación se asociaron significativamente con la aparición de complicaciones quirúrgicas [or (IC 95% respectivamente), 0,6 (0,4–0,9) y 2,8 (0,9–10,6)] (Tabla 4). En un análisis multivariante que incluyó variables cuyo valor p ≤ 0,1, una baja densidad muscular y una diuresis residual siguieron siendo factores de riesgo de complicaciones quirúrgicas a 1 año [respectivamente OR (IC 95%), 0,6 (0,3–0,9) p=0,05 y 4,9 (1,2–23) p=0,05]. El área bajo la curva (AUC) de un modelo predictivo de complicaciones a 1 año que incluye diuresis residual y densidad muscular fue de 0,64 (Fig. 2).
Discusión
En nuestro estudio, evaluamos la asociación entre la sarcopenia y el corto plazotrasplante renalresultados mediante secciones de tomografía computarizada. Demostramos que los pacientes con albuminemia más baja tuvieron significativamente más complicaciones a 1 mes después del trasplante. A 1 año, una baja densidad muscular se asoció con complicaciones quirúrgicas cuando la albuminemia parecía no tener ningún impacto. El uso de anticoagulantes también se correlacionó con la tasa de complicaciones, a 1 mes y 1 año después del trasplante. La prevalencia de sarcopenia en la población en diálisis oscila entre el 5 y el 37%, dependiendo de la etapa deInsuficiencia renal[7, 17]. En este contexto, la desnutrición proteína-energética puede explicarse por varios mecanismos: (1) disminución de la ingesta, debido a dietas restrictivas; (2) interrupción del metabolismo de las proteínas causada por una baja actividad física, un aumento del catabolismo relacionado con la acidosis metabólica y una disminución del anabolismo relacionado con la resistencia periférica a la insulina; (3) pérdida de proteínas debido a proteinuria [18]. Por lo tanto, la diálisis prolongada contribuye al trastorno metabólico y nutricional provocado por los pacientes con etapa terminal.Enfermedad renal[19]. Aunque se ha demostrado que la sarcopenia se asoció con resultados postoperatorios en el campo de la oncología, su impacto entrasplante renalno está claramente establecido.

Algunos estudios retrospectivos en trasplante de pulmón e hígado destacaron el pronóstico peyorativo de la sarcopenia pre-trasplante [20, 21]. En consecuencia, nuestro estudio fue uno de los pocos en evaluar el impacto de la sarcopenia medida por tomografía computarizada y la densidad muscular en los resultados posteriores al trasplante. Nuestro método proporcionó una cuenta de pérdida objetiva y alteración del tejido muscular, incluso en individuos con IMC normal o supranormal [22]. Debido a que los pacientes en diálisis tienen una amplia gama de pesos, sentimos que este método era particularmente adecuado entre esta población. Además, ya ha sido validado como una herramienta eficiente para evaluar la sarcopenia [9, 23]. No fue posible evidenciar una asociación significativa entre la sarcopenia y las complicaciones a 1 mes y 1 año después del primer trasplante de riñón. Sin embargo, la definición de sarcopenia todavía no es consensuada en la actualidad. Sobre la base de la medición del área de superficie muscular en una sección de tomografía computarizada, actualmente no existe un valor de consenso para definir la sarcopenia. Además, su definición ha sido revisada por el Grupo de Trabajo Europeo sobre Sarcopenia en Personas Mayores (EWGSOP2) en 2018 y es principalmente clínica. De hecho, la coexistencia de dos de los siguientes tres factores ahora permite el diagnóstico de sarcopenia: una disminución en la fuerza muscular y / o una disminución en la cantidad muscular, y / o una disminución en el rendimiento en las pruebas físicas [10]. Por lo tanto, esta definición se basa ahora más en criterios funcionales que anatómicos. Por lo tanto, una alteración en la calidad muscular prevalece sobre la cantidad muscular en sí. Desde esta perspectiva, la densidad muscular podría ser una herramienta interesante y temprana para evaluar el estado nutricional de los pacientes en lista de espera. Sin embargo, se pudo evidenciar una relación entre la densidad muscular y los resultados posteriores al trasplante. De hecho, la disminución de la densidad muscular, reflejando el grado de infiltración grasa del tejido muscular, podría ser el primer paso en el proceso de degeneración muscular responsable de la alteración de la función. La densidad muscular también es comparable en pacientes independientemente de su sexo o índice de masa corporal, lo que garantiza la generalización [24].
Nuestro estudio presenta varias limitaciones. En primer lugar, el diseño de nuestro estudio (monocéntrico y retrospectivo) y el bajo número de sujetos podrían sesgar nuestros resultados. En segundo lugar, la mitad de los pacientes que se sometieron atrasplante renaldurante el período de estudio se excluyeron porque no se les realizó una tomografía computarizada en los últimos 12 meses antes de la cirugía. En este momento, se eligió la limitación para tener el perfil morfométrico del paciente más idéntico al del día del trasplante. Además, como es probable que la sarcopenia no sea estática y que cambie con el tiempo, el uso de la exposición de 18 meses de duración también podría sesgar nuestros resultados. El retraso ideal habría sido someterse a una tomografía computarizada el día anterior.trasplante renalentre un estudio prospectivo apropiado; sin embargo, creemos que este estudio debe considerarse como una prueba de concepto para estudios posteriores. Finalmente, la evaluación de la sarcopenia por tomografía computarizada aún no es un estándar y los pacientes podrían haber sido clasificados erróneamente. En este ámbito, la evaluación de la densidad muscular parece más objetiva y podría ser
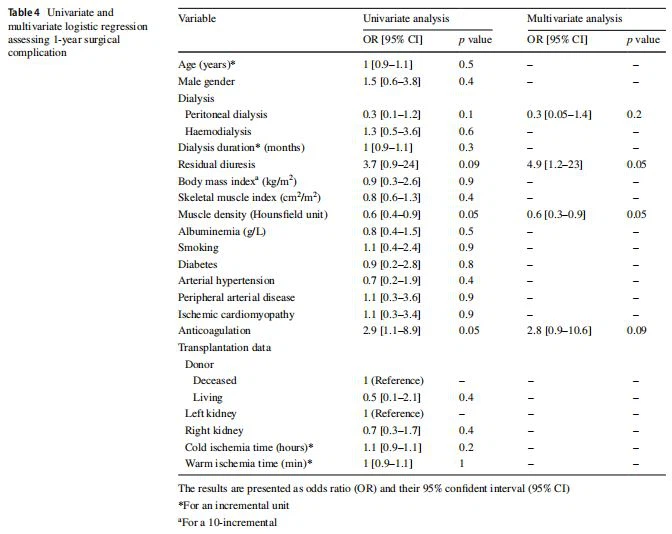
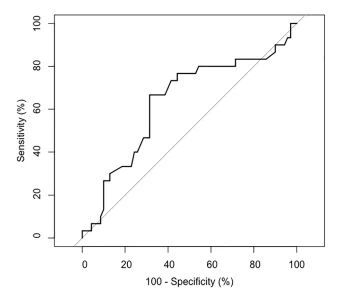
Fig. 2 Análisis ROC del modelo multivariable que predice la complicación quirúrgica a 1 año. El AUC de un modelo predictivo de complicaciones a 1 año que incluye diuresis residual y densidad muscular fue de 0,64 una ventaja para una mejor predicción de los resultados posteriores al trasplante. Todavía se necesitan más estudios sobre el tema para establecer más claramente el impacto de la sarcopenia en la aparición de complicaciones después del trasplante de riñón.
Conclusión
La aparición de complicaciones a 1 mes y 1 año después de un primertrasplante renalno pareció estar asociado con el estado sarcopénico de los pacientes. Sin embargo, la densidad muscular de la tomografía computarizada y la albuminemia plasmática se asociaron con resultados peyorativos posteriores al trasplante y podrían prefigurarse como herramientas predictivas tempranas para estos pacientes.
