Anomalías de las células B y las células T en pacientes con deficiencia selectiva de IgA
Aug 09, 2023
Abstracto
Fondo
La deficiencia selectiva de IgA (SIgAD) es el error congénito de la inmunidad más prevalente y de etiología casi desconocida. Este estudio tuvo como objetivo investigar los valores de diagnóstico y pronóstico clínico de los subconjuntos de linfocitos y su función en pacientes sintomáticos con SIgAD.
Métodos
En el presente estudio se incluyeron un total de 30 pacientes con SIgAD disponibles del registro iraní y 30 controles sanos de la misma edad y sexo. Analizamos los subconjuntos periféricos de células B y T y el ensayo de proliferación de células T mediante citometría de flujo en pacientes con SIgAD con fenotipos clínicos leves y graves.
Resultados
Nuestros resultados indicaron un aumento significativo en las células B vírgenes y de transición y una fuerte disminución en las células B de memoria conmutadas y de zona marginal en pacientes con SIgAD. Descubrimos que los subconjuntos de células T CD4+ de memoria central y vírgenes, así como las células T Th1, Th2 y reguladoras, han disminuido significativamente. Por otro lado, hubo una reducción significativa en los subconjuntos de células T CD8+ de memoria central y efectora, mientras que las proporciones de células T de memoria efectoras terminalmente diferenciadas (CD4+ y CD8+) (TEMRA) estuvieron significativamente elevados en nuestros pacientes. Aunque algunos subconjuntos de células T en SIgAD grave fueron similares, una disminución en las células B de la zona marginal y de memoria conmutada y un aumento en las células B bajas CD21 de pacientes con SIgAD grave fue ligeramente prominente. Además, la actividad de proliferación de las células T CD4+ se vio fuertemente afectada en pacientes con SIgAD con un fenotipo grave.
Conclusión
Los pacientes con SIgAD tienen diversas deficiencias celulares y humorales. Por lo tanto, la evaluación de las células T y B podría ayudar a comprender mejor la patogénesis heterogénea y la estimación del pronóstico de la enfermedad.
Palabras clave
Errores congénitos de la inmunidad, inmunodeficiencia primaria, deficiencia selectiva de IgA, subconjuntos de células B, subconjuntos de células T, citometría de flujo, proliferaciónensayo

cistanche tubulosa-mejora el sistema inmunológico

extracto de cistanche
Introducción
La deficiencia selectiva de IgA (SIgAD) es el trastorno de inmunodeficiencia primaria (EPI) o error congénito de la inmunidad (IEI) más prevalente, identificado por concentraciones séricas de IgA inferiores a 7 mg/dL y concentraciones normales de IgG e IgM en pacientes mayores de cuatro años. . La mayoría de los pacientes con SIgAD son asintomáticos, aunque algunos de ellos manifiestan diferentes manifestaciones clínicas, incluidas infecciones del tracto gastrointestinal y respiratorio, enfermedades alérgicas y trastornos autoinmunes. Se ha informado la progresión de la enfermedad a inmunodeficiencia común variable (IDCV) en un grupo seleccionado de pacientes con SIgAD con deficiencia de subclases de IgG o trastornos autoinmunes [1]. Aún no se han informado causas específicas para la patogénesis de SIgAD. Sin embargo, en casos no resueltos se han identificado defectos en el proceso de recombinación de cambio de clase de IgA (CSR), producción y secreción de IgA, así como en la supervivencia a largo plazo de IgA, células B de memoria conmutadas y células plasmáticas de pacientes con SIgAD [2 ]. Los defectos en estos procesos inmunológicos están asociados con anomalías en los linfocitos de los pacientes con SIgAD. Por lo tanto, la evaluación de los linfocitos, especialmente los subconjuntos de células B y T, podría ser valiosa y útil. Varios estudios han demostrado anomalías de las células B y T en algunos grupos de pacientes con SIgAD [3, 4]. Con respecto a los subconjuntos de células B, se ha informado una disminución en el número de células B de memoria conmutadas, células plasmáticas IgA y células B reguladoras IL-10+ de transición de pacientes con SIgAD [5–8]. Por otro lado, se ha informado de defectos en algunos subconjuntos de células T de casos de SIgAD que están relacionados con células B productoras de IgA insuficientes [5, 8, 9]. La inmunofenotipificación por citometría de flujo puede desempeñar un papel importante en el diagnóstico, pronóstico, clasificación y tratamiento de pacientes con SIgAD. Por lo tanto, por primera vez, nuestro objetivo fue investigar las principales subpoblaciones de linfocitos B y T junto con una evaluación de la función de las células T, para aclarar la correlación entre las características inmunológicas y las manifestaciones clínicas en pacientes sintomáticos con SIgAD.
material y métodos
Pacientes
En el presente estudio se incluyeron un total de 30 pacientes sintomáticos con SIgAD disponibles (del registro IEI iraní [10, 11]) y 30 controles sanos (HC) emparejados por edad y sexo. Después de evaluaciones clínicas y de laboratorio, se confirmó que los HC no tenían inmunodeficiencia ni ninguna enfermedad subyacente. Los pacientes habían sido remitidos al Centro Médico Infantil (Centro de Excelencia en Pediatría afiliado a la Universidad de Ciencias Médicas de Teherán, Teherán, Irán). Todos los pacientes fueron diagnosticados con SIgAD según la Sociedad Europea de Inmunodeficiencias [12]. El estudio fue aprobado por el Comité de Ética de la Universidad Médica de Teherán y se obtuvo el consentimiento informado por escrito de todos los individuos (IR.TUMS.VCR.REC.1396.2018). Las manifestaciones demográficas, clínicas y los datos inmunológicos de los pacientes se documentaron en forma de cuestionario.
Clasificación de pacientes
Para comparar datos demográficos, clínicos e inmunológicos, los pacientes se clasificaron en dos grupos: grave y leve (según las manifestaciones clínicas), así como grupos consanguíneos y no consanguíneos (según la consanguinidad de los padres). Los criterios mínimos de inclusión para que un paciente fuera considerado sintomático fueron diez señales de alerta de la Fundación Jeffrey Modell. Los pacientes se dividieron en dos grupos, leves y graves, ya que los pacientes con infecciones graves (p. ej., del torrente sanguíneo, del sistema nervioso central e infecciones profundas como osteomielitis y artritis), autoinmunidad o malignidad se clasificaron en el grupo grave y otras complicaciones. fueron considerados como un grupo leve. Dado que la neumonía y otras infecciones respiratorias son comunes en los pacientes con SIgAD y queríamos comprobarlo como un parámetro entre los grupos graves y leves, no lo categorizamos en el grupo grave.

Beneficios del suplemento cistanche: cómo fortalecer el sistema inmunológico
Haga clic aquí para ver los productos Cistanche Enhance Immunity
【Pregunte por más】 Correo electrónico:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
Ensayo de subconjuntos de linfocitos.
Se separaron células mononucleares de sangre periférica (PBMC) de muestras de sangre de 8 ml recogidas en tubos de heparina sódica utilizando una centrifugación en gradiente de densidad Ficoll-Hypaque a 600 g durante 25 minutos a 22 grados. Para la tinción extracelular, las PBMC se dividieron en 5-fracciones de panel y se tiñeron durante 20 minutos a 2-8 grados en un lugar oscuro y cada cóctel contenía anticuerpos monoclonales en concentraciones óptimas. El panel B1 se utilizó para determinar memoria ingenua (CD19+CD27−IgM+IgD+), memoria solo IgM (CD19+CD27+ IgM++IgD−), conmutada. memoria (CD19+CD27+IgM−IgD−) y células B tipo zona marginal (CD19+CD27+IgM++IgD+). El panel B2 se utilizó para identificar células B bajas CD21 (CD19+CD21-/lowCD38-/lowIgM+++), plasmablastos (CD19+CD21-/lowCD38++/{ {34}}IgM−) y células B de transición (CD19+CD21+CD38++IgM+). El panel T1 se utilizó para clasificar memoria naïve (CD4+ o CD8+ y CD45RA+CCR7+), efectora (CD4+ o CD8+ y CD45RA-CCR7-), memoria central (CD4+ o CD8+y CD45RA-CCR7+) y células T TEMRA (memoria efectora terminalmente diferenciada) (CD4+ o CD8+ y CD45RA+CCR7-). El panel T2 se utilizó para clasificar las células T reguladoras (TregsCD4+CD25+FOXP3+CD127−/low). Para la tinción intracelular, después de la tinción de la molécula de superficie, se fijaron y permeabilizaron en FOXP3/tampón de permeabilización (eBioscience, EE. UU.) de acuerdo con las instrucciones del fabricante para lo siguiente: Anti-Human FOXP3 (PE), Anti-Human IL{{67} } (PE), IL-4 antihumano (APC) y IFN-antihumano (FITC). Todos los anticuerpos y controles de isotipo se adquirieron en eBioscience, una corporación estadounidense. Para evaluar las células T colaboradoras (incluidas T1, T2 y T17), se cultivaron 1 x 106 (células/ml) de PBMC en el medio de cultivo celular del Roswell Park Memorial Institute (RPMI 1640), seguido de estimulación con acetato de miristato de forbol (PMA). , 50 ng/mL, Sigma-Aldrich, EE. UU.)/ionomicina (1 ug/mL, Sigma-Aldrich), y en presencia de brefeldina (5 ug/mL, eBioscience). Luego, las células se incubaron a 37 grados en una incubadora con 5% de CO2 y 95% de humedad durante 5 h. Las células estimuladas se lavaron con solución salina tamponada con fosfato (PBS) y se realizó una tinción de la superficie con CD4 antihumano (PerCp) -Cy5.5. Se agregaron y se incubaron anticuerpos de tinción de citoquinas intracelulares (anti-IFN-FITC, anti-IL-17 PE y anti-IL-4 APC para la evaluación de subconjuntos T y anti-FoxP3 PE para la evaluación de Treg). a temperatura ambiente durante 30 min. Las células se lavaron con tampón de permeabilización y se resuspendieron en tampón de tinción frío, y los recuentos se determinaron utilizando un citómetro de flujo BD FACSCalibur (BD Biosciences) (archivo adicional 1: Tabla S1). La estrategia de activación es similar a nuestro estudio anterior [13, 14].
Ensayo de proliferación de células T.
Para evaluar la proliferación de células T, se cultivaron PBMC con éster succinimidílico de 5,{1}}carboxifluoresceína fluorescente (CFSE, Biolegend, EE. UU.). Se preparó una solución madre de CFSE disolviendo CFSE en dimetilsulfóxido (DMSO) a una concentración de 5 mM/L, según las instrucciones del fabricante. Este caldo se congeló en pequeñas alícuotas para evitar ciclos excesivos de congelación y descongelación. Se añadió CFSE a un tubo de halcón transversal que contenía 500 μl de suspensión de PBMC (5 x 106 células/ml) en medio de cultivo celular RPMI 1640 que contenía FBS (suero bovino fetal) al 10 % con una concentración final de 5 μM y 2 mM. L-glutamina, 100 U/mL de penicilina y 100 ug/mL de estreptomicina (Lymphosep; Biosera, Francia). El tubo giró rápidamente y se agitó para asegurar una dispersión homogénea. Después del etiquetado, la suspensión celular se incubó durante 5 minutos a 37 grados. Luego, se agregaron 9 ml de RPMI1640 que contenía FBS al 10% a la suspensión celular y se centrifugó a 500 g durante 5 minutos. Las células se lavaron tres veces y se añadió 1 ml de RPMI1640 con FBS al 10 %. Con respecto a la estimulación y proliferación de células T específicas, se añadió un anticuerpo anti-CD3 (1 µg/ml) a 500 µl de PBS estéril y la placa se incubó a 37 °C durante 2 h. La placa recubierta se lavó dos veces con PBS estéril y las células marcadas se agregaron directamente y, finalmente, se agregó un anticuerpo anti-CD28 (2 µg/ml) como estimulante para las células T. La placa se incubó a 37 ºC en una incubadora con 5% de CO2 y 95% de humedad durante 96 h [15-17]. Se consideró un pocillo no estimulado como control de células no proliferativas. Después de 96 h, las células se recogieron y se lavaron. Después de teñir con Anti Human CD4 (PerCPCy5.5), las células finalmente se analizaron mediante el citómetro de flujo BD FACSCalibur ™ y el software CellQuest Pro (BD, Biosciences, San José, CA, EE. UU.). El análisis de proliferación se realizó comparando tres criterios, incluido el porcentaje de células divididas (% divididas), el número promedio de divisiones celulares que sufre una célula (Índice de división) y el número promedio de divisiones celulares que ocurren en toda la población de células primarias. (Índice de proliferación) mediante el software FlowJo 7.6.
análisis estadístico
Se utilizó el software SPSS (Windows versión 16.0; SPSS Inc., Chicago, IL, EE. UU.) para el análisis estadístico. Utilizamos la prueba de Kolmogorov-Smirnov para estimar si los datos estaban distribuidos normalmente. Los hallazgos se presentaron como valores de mediana (rango intercuartílico [RIC], presentado como un rango con percentiles 25 a 75). Para las comparaciones se utilizó la prueba de chi-cuadrado o la prueba exacta de Fisher. Para la comparación de más de dos grupos, si la distribución de los datos era normal, se utilizó ANOVA y si la distribución de los datos no era normal, se utilizó la prueba de Kruskal Wallis. Las diferencias se consideraron estadísticamente significativas para los valores de P que fueron<0.05.

Beneficios de cistanche para hombres: fortalece el sistema inmunológico.
Resultados
Hallazgos demográficos, inmunológicos y clínicos.
Entre todos los pacientes iraníes registrados con SIgAD, en el presente estudio se reclutaron 30 pacientes disponibles (23 hombres y siete mujeres). La mediana de edad (RIQ) de los pacientes fue de 11 (7,3-16) años en el momento del estudio. La consanguinidad parental estuvo presente en 16 (53,3% de) los pacientes. La neumonía (42,3%) fue la manifestación clínica más frecuente en los pacientes estudiados y no se diagnosticó malignidad en esta cohorte. Las características demográficas, clínicas e inmunológicas de los pacientes se resumen en la Tabla 1. Después de categorizar a los pacientes según los fenotipos graves y leves, se compararon los datos demográficos, clínicos e inmunológicos (Tabla 1, Fig. 1). Los pacientes con fenotipos graves manifestaron más complicaciones respiratorias que el grupo leve. Otros parámetros no han demostrado una diferencia significativa. Se realizaron las mismas comparaciones en pacientes con y sin consanguinidad, y ninguno de ellos tuvo una diferencia significativa. Por el contrario, los pacientes con fenotipos leves presentaron una tasa ligeramente mayor de alergia y manifestaciones gastrointestinales con un nivel elevado de IgE sérica, lo que sugiere un mayor cambio hacia la producción de IgE.
Tabla 1 Comparación de datos demográficos, clínicos e inmunológicos de pacientes con SIgAD con fenotipos graves y leves

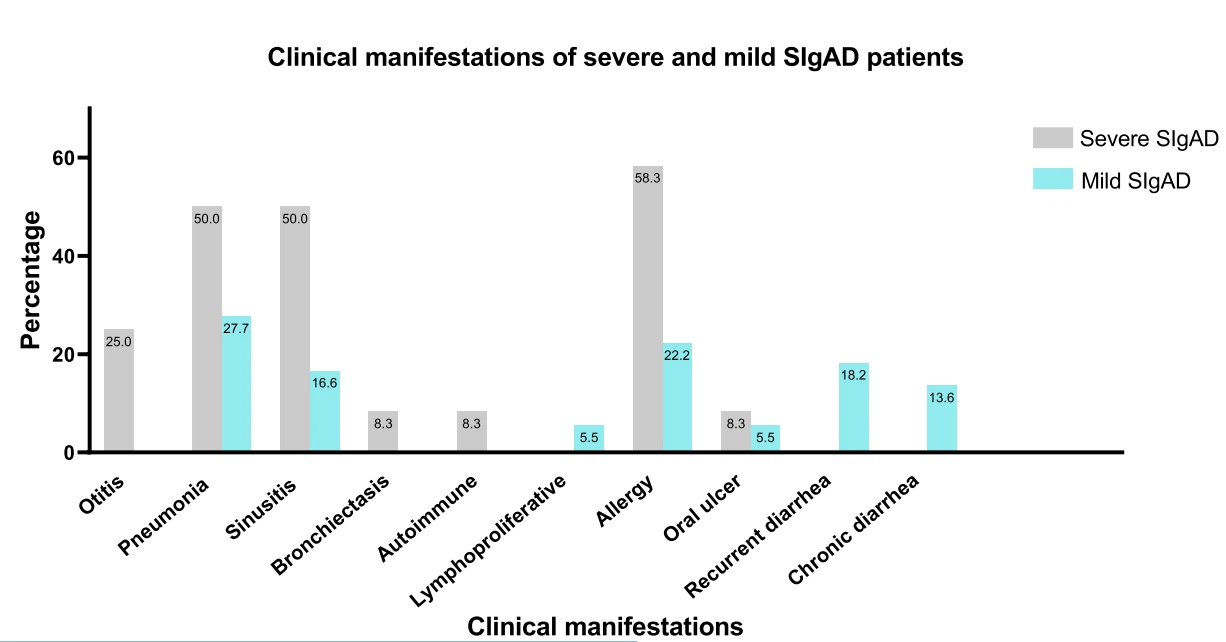
Fig. 1 Comparación de manifestaciones clínicas entre SIgAD grave y leve
Subconjuntos de células B
Los pacientes con SIgAD mostraron una frecuencia significativamente mayor de células B CD{{0}} [11,2% (9,4–13,07%) frente a 7,2% (6–8,6%), p < 0.001], con un aumento de células B vírgenes [71% (63,7–80%) frente a 66,5% (56,2–71,1%), p=0.036] y células B de transición [ 8% (3,6–13,5%) vs. 4,8% (2,6–9,5%), p=0.032] en comparación con los HC. En contraste, el porcentaje de células tipo zona marginal [2,3% (2–3,5%) vs. 3,4% (2,3–4,8%), p=0.022) y de memoria conmutada [3,5% (1,9 –5,5%) vs. 6% (3,5–8,4%), p=0.006] fueron significativamente más bajos que los HC. Sin embargo, la disminución de la memoria de solo IgM y los plasmablastos y el aumento de las células B bajas en CD21 en pacientes que en los de HC no fueron significativos (Fig. 2). Curiosamente, algunas comparaciones fueron significativas entre los grupos clínicos de pacientes. El porcentaje de células B CD19+ tanto en los fenotipos leves como en los graves fue significativamente mayor que el de las HC [11,6 % (8,7–13) frente a 7,2 % (6–8,6), p < 0,0001, 10,8 % (9,6–13,2 ) vs. 7,2% (6–8,6), p < 0,0001], respectivamente. Los pacientes con SIgAD grave demostraron un aumento significativo en el porcentaje de células B bajas en CD21 [1,5 % (1–2,2) frente a 2,7 % (1,6–5,6), p=0.025], y una disminución significativa en el porcentaje de subconjuntos de células B de zona marginal y de memoria conmutada [3,4% (2,3–4,8) frente a 2,2% [2, 3], p=0.040, 6% (3,5–8,4) frente a 2,7% ( 1,7–4,7), p=0.003], respectivamente. El porcentaje de células B transicionales en pacientes con SIgAD leve fue mayor que el de HC [10,7% (3,9–13,8) vs. 4,8% (2,6–9,5), p=0.047] (Fig. 3). El porcentaje de memoria sólo de IgM fue significativamente mayor en pacientes con consanguinidad que en aquellos sin consanguinidad. También categorizamos la frecuencia de subconjuntos de células B de pacientes con SIgAD en tres categorías: normal, disminuida y aumentada según el rango normal de HC (Tabla 2). Según este análisis, la mayor disminución en los subconjuntos de células B está relacionada con las células B de memoria conmutadas (23%), mientras que el mayor aumento está relacionado con las células B vírgenes (27%) en pacientes con SIgAD. Excepto por el aumento de células B bajas CD21 en pacientes con SIgAD grave en comparación con pacientes con SIgAD leve.
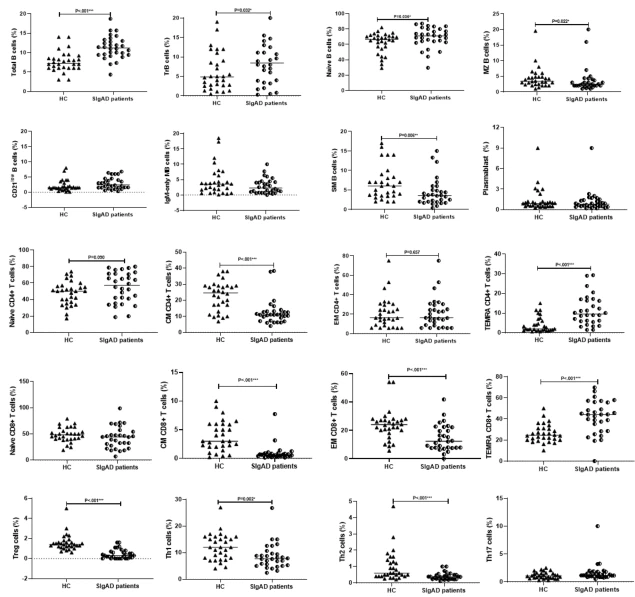
Fig. 2 Análisis cuantitativo de los porcentajes de subconjuntos de células B y T en pacientes con SIgAD y controles sanos. La mediana está representada por una línea horizontal. Los datos se analizaron mediante la prueba U de Mann-Whitney. *pag<0.05, statistical significance between patients and HCs. HC Healthy control
Subconjuntos de células T
La separación del subconjunto de células T CD4+ reveló una reducción significativa en el total de células T CD4+ [36,5% (30,8–41,2%) vs. 40,1% (37,3–47,2%), p{{14 }}.038)], células de memoria central [11% (7,3–13,1%) vs. 24,5% (16–29%), p<0.0001), T1 [7.7% (5.2–9.9%) vs. 12% (7.8–16%), p=0.002], T2 [0.3% (0.2–0.4%) vs. 0.6% (0.4–1.3%), p<0.0001] and Tregs [0.3% (0.03–0.7%) vs. 1.4% (1.1– 1.6%), p<0.0001] in patients compared with HCs. Oppositely, the percentage of TEMRA [9.5% (5.7–16.4%) vs. 2% (1.3–6.2%), p<0.0001] was meaningfully higher than HCs. Moreover, decreased effector memory and T17, and increased naïve helper T cells in patients in comparison with HCs were not significant (Fig. 2). Regarding the percentage of CD8+ T cell subsets, central memory [0.6% (0.3–0.8%) vs. 3% (2–6%), p<0.0001] and effector memory [12.3% (7.6–22.1%) vs. 23.9% (19.5– 27.2%), p<0.0001] were markedly diminished in patients compared with HCs. On the other hand, the percentage of cytotoxic TEMRA [44.1% (28.4–55.7%) vs. 24.4% (20– 31%), p<0.0001] was significantly higher than HCs. However, increased total CD8+ T cells and decreased naïve CD8+ T cells were not significant in patients compared to those in HCs (Fig. 2). Regarding the comparison of the percentage of CD8+ T cells subsets between severe SIgAD patients with HCs, naïve T cells, effector, and central memory cells demonstrated a significant reduction. Also, there was a significant decrease in the percentage of total CD4+ T-cells, central memory, T1, T2, and regulatory T cells, whereas TEMRA in both CD4+ and CD8+ T cells demonstrated an increase. On the other hand, the percentage of effector and central memory cells within CD8+ T cells, as well as central memory, TEMRA, T1, and regulatory T cells within CD4+ T cell subsets demonstrated a significant decrease in mild forms of SIgAD compared to HCs. In contrast, we found an increase in TEMRA CD8+ T cells and T2 CD4+ T cells in mild patients compared to controls (Fig. 3). Comparisons of the percentages of all T cell subsets between SIgAD patients with and without consanguinity have not indicated any significant difference. We also categorized the frequency of T cell subsets of SIgAD patients into three categories: normal, decreased, and increased based on a normal range of HCs (Table 2). Based on this analysis, the most decrease in T cell subsets is related to Tregs (67%), while the most increase is related to CD8+ TEMRA (37%) in SIgAD patients. Flow cytometry results of B cell and T cell subsets in 30 SIgAD patients have shown separately in Additional file 1: Tables S2 and S3. To evaluate the impact of the T cell subset on the switching process of B cells and the production of different Ig subtypes we performed a correlation analysis. Surprisingly only IgG but not IgM and IgE were significantly associated with specific T cell subsets (negative association with naïve CD4 and naïve CD8 T cells and positive association with CD4+ TEM and T17 cells, Additional file 1: Table S4) indicating the independent association of IgM to IgE from co-stimulation of T cell subsets in our patient cohorts. Moreover, correlation analysis of absolute counts and percentage of subsets should significant direct correlation in all measured parameters (Additional file 1: Table S5).

Fig. 3 Análisis cuantitativo de los porcentajes de subconjuntos de células B y T en pacientes con SIgAD grave y leve. La mediana está representada por una línea horizontal. Los datos se analizaron mediante la prueba U de Mann-Whitney. *pag<0.05, statistical signifcance between severe and mild patien
Tabla 2 Distribución de proporciones normales, aumentadas y disminuidas de subconjuntos de células T y células B en todos los pacientes con SIgAD. N=30

proliferación de células T
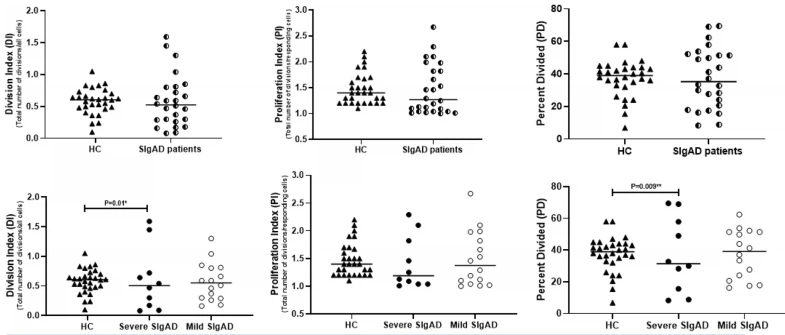
Los datos generados por los cultivos marcados con CFSE se analizaron para cuantificar la proliferación de células T CD4+. No hubo diferencias significativas en el índice de división (DI), el índice de proliferación (PI) y el porcentaje dividido (PD) entre los pacientes con SIgAD y los HC (Fig. 4). Curiosamente, cuando comparamos estos índices entre pacientes con SIgAD con fenotipos graves y leves, encontramos que la mediana de DI y PD en pacientes con SIgAD grave en comparación con los casos leves se anuló significativamente [0.1 (0 .08–0.4) frente a 0.5 (0.3–0,8), p=0.019 y 12,2 (8,4– 26,4) frente a 42,5 (26,8–52,6), p=0.009, respectivamente]. Sin embargo, no hubo diferencias significativas en el IP entre los grupos grave y leve (Fig. 4). Por otro lado, las comparaciones de DI, PI y PD entre pacientes con SIgAD con y sin consanguinidad no fueron significativas.
Fig. 4 Comparación de los índices de proliferación de linfocitos T en pacientes con SIgAD grave y leve. La mediana está representada por una línea horizontal. *pag<0.05, statistical significance between severe and mild patients
Discusión
SIgAD es la IEI más prevalente con diversas manifestaciones clínicas. Estos pacientes tienen un espectro diferente de manifestaciones clínicas. En consecuencia, son útiles las investigaciones inmunológicas en pacientes con un espectro diferente de manifestaciones clínicas. La manifestación clínica más prevalente en las IEI, especialmente en SIgAD, son las infecciones respiratorias recurrentes [18-20]. Encontramos la neumonía como la complicación más frecuente en nuestros pacientes sintomáticos registrados. Las infecciones respiratorias recurrentes comúnmente se manifiestan en forma de infecciones del tracto respiratorio superior y pueden permanecer sin diagnosticarse durante varios años; sin embargo, algunos pacientes con SIgAD manifiestan fenotipos más graves, como bronquiectasias o bronquiolitis obliterada, lo que obliga a realizar una investigación inmunológica en estos pacientes [21]. Dado que se ha informado que las infecciones respiratorias recurrentes son la causa más importante de morbilidad y muerte en niños con IEI, especialmente las deficiencias primarias de anticuerpos [22, 23], el diagnóstico temprano y el tratamiento de los trastornos respiratorios asociados con SIgAD son muy importantes [24, 25]. . Se ha indicado que se observan anomalías en los subconjuntos de células B en algunos pacientes con SIgAD [3, 4]. Nuestros resultados indicaron un aumento significativo en las células B vírgenes y de transición y una fuerte disminución en las células B de memoria conmutada y de zona marginal. Este patrón anormal de células B sugiere defectos en las etapas terminales de la diferenciación de las células B, similares a los pacientes con IDVC [26]. Dado que CVID y SIgAD comparten antecedentes genéticos casi similares y pueden acumularse como casos múltiples dentro de una familia, este parecido es predecible. En general, más de la mitad de los pacientes con IEI registrados en el registro iraní tienen consanguinidad parental, pero esta tasa aún es menos común en pacientes con SIgAD. En los pacientes iraníes con SIgAD en comparación con los pacientes occidentales, la consanguinidad es más prevalente. Aunque pueden existir causas monogenéticas, aún no se han identificado a pesar de la secuenciación de próxima generación en varios pacientes [27]. Detectamos una reducción en las células B de memoria conmutadas y similares a zonas marginales, especialmente en pacientes con SIgAD grave, como se informó anteriormente [28]. Recientemente, informamos una reducción similar en las células B de memoria conmutadas y similares a zonas marginales en pacientes con IDVC [14].

Beneficios del suplemento cistanche: aumentar la inmunidad.
Por otro lado, aunque observamos una disminución significativa en la memoria conmutada en pacientes con Ataxia Telangiectasia (AT), se observó un fuerte aumento en las células B similares a la zona marginal [29]. Los pacientes con SIgAD, especialmente un grupo de pacientes con manifestaciones clínicas graves (infección recurrente e intensiva y autoinmunidad), tienen células B de memoria conmutadas más bajas [28, 30, 31]. Se ha sugerido que la disminución en la subpoblación de células B de memoria conmutada se debe a defectos en el nivel del proceso de recombinación de cambio de clase de anticuerpos (CSR), causado por una deficiencia enzimática o anomalías en las redes de citoquinas y sus receptores [28]. Algunos pacientes con SIgAD con fenotipo grave progresan a CVID, lo que refleja que este subgrupo de SIgAD puede compartir con la CVID una patogénesis inmune común, particularmente en el desarrollo del paso CSR. En consecuencia, las células B de memoria conmutadas se consideran un biomarcador de diagnóstico en pacientes [28]. Sin embargo, la frecuencia de células B de memoria conmutadas es normal entre los niños de nuestra población de estudio, y la reducción se observó más en pacientes adultos; lo que sugiere que el envejecimiento probablemente conduce a la progresión de SIgAD a CVID, especialmente en pacientes con manifestaciones clínicas graves (datos no mostrados). Por otro lado, las células B de la zona marginal son una población especializada de células B que producen IgM para protección contra infecciones, especialmente bacterias encapsuladas [32]. Aunque estudios previos han demostrado que el número de células B similares a zonas marginales en pacientes con SIgAD no era diferente en comparación con los controles normales [33], obtuvimos una reducción significativa en las células B similares a zonas marginales en nuestros casos, similar a una informe anterior en pacientes con IDCV [34]. La reducción de los subconjuntos de células B marginales en otros pacientes con defectos en la producción de anticuerpos podría asociarse con un mayor riesgo de infección como neumonía y una disminución de los niveles séricos de IgM, similar a los pacientes con CVID [35]. Encontramos un aumento de células B bajas en CD21 en comparación con el control, principalmente en pacientes con SIgAD grave. Estudios anteriores han informado de un aumento en las células B CD21low tanto en pacientes con SIgAD [3] como con CVID [36], y otras enfermedades autoinmunes [37]. Recientemente también se ha informado de un aumento del nivel bajo de CD21 en pacientes con AT [29]. Un aumento en el número de células CD21low está directamente relacionado no sólo con la autoinmunidad sino también con la infección [36]. Por otro lado, la exposición crónica a una infección viral puede conducir a la conversión de células B reactivas al antígeno en células B bajas CD21 que no responden [38]. Para aclarar la causa de las células B CD21 bajas expandidas; es necesario realizar más investigaciones para esta subpoblación de células B. Dada la alta subpoblación de células B CD21low en pacientes con CVID y la progresión de algunos pacientes con SIgAD a CVID, el grupo grave de pacientes con SIgAD con aumento de células B CD21low tendrá más probabilidades de desarrollar CVID. Por tanto, necesitan un seguimiento más regular para evaluar el curso de la enfermedad. Las células B de transición se encuentran en una etapa intermedia en el desarrollo entre las células inmaduras de la médula ósea y las células B maduras en el bazo [39]. En el presente estudio, observamos un aumento significativo de células B transicionales en nuestros pacientes con SIgAD, especialmente en pacientes con SIgAD grave, aunque la cantidad de células B transicionales en niños con SIgAD fue normal (datos no mostrados). Recientemente observamos una disminución significativa en las células B de transición AT [29]. A diferencia de estudios previos que mostraron una disminución de las células B de transición [8, 28, 40], los pacientes adultos indicaron un ligero aumento de células B de transición. Además, Lemarquis et al. mostró una disminución en la actividad funcional de las células B de transición basada en la producción de IL-10 y la estimulación de CpG [40]. Dado el defecto en las etapas terminales de las células B en SIgAD, parece que un aumento en las células B transicionales y las células B vírgenes de nuestros pacientes se debe a un mecanismo compensatorio que aumenta el desarrollo temprano de las células B. En cuanto a los diferentes resultados entre nuestro estudio y otros, parece que esta diferencia se debe a diferentes procesos de selección, ya que todos nuestros pacientes eran sintomáticos, mientras que otros estudiaron de forma heterogénea a pacientes con SIgAD asintomáticos y sintomáticos. Con respecto a los subconjuntos de células T, observamos una disminución total de células T CD4+, T1, T2 y Treg, y un aumento de TEMRA tanto en células CD4+ como en CD8+. De acuerdo con nuestros resultados, estudios previos han demostrado un aumento y una reducción en la población de linfocitos T CD8+ y CD4+, respectivamente [4]. Además, encontramos que la memoria central en las células T CD4+ y CD8+ y la memoria efectora en los linfocitos T CD8+ estaban disminuidas en los pacientes con SIgAD en comparación con los HC. Observamos un aumento significativo en el subconjunto de células TEMRA en la población de linfocitos CD4+ y CD8+, especialmente en pacientes con SIgAD grave. TEMRA es un tercer subconjunto de memoria de células T en tejidos inflamatorios periféricos que expresan CD45RA pero carecen de expresión de CCR7 o CD27. En humanos, la acumulación de células TEMRA se ve afectada por infecciones crónicas, como el CMV [41, 42]. Un aumento en estos subconjuntos de células T terminadas podría deberse a una respuesta celular crónica a las infecciones en estos pacientes; sin embargo, es necesario realizar más estudios sobre este fenómeno. De acuerdo con nuestros resultados, Nechvatalova et al. demostraron células CD4+ y CD8+ TEMRA expandidas en pacientes con SIgAD que estaban relacionadas con la infección por CMV [43]. No examinamos la infección por CMV en pacientes con SIgAD, pero un aumento en la cantidad de subconjunto de células TEMRA en nuestros pacientes podría estar relacionado con infecciones crónicas. Recientemente evaluamos las respuestas de anticuerpos específicos a PPSV-23 en pacientes con SIgAD y AT y revelamos que el 18,6 % de los pacientes con SIgAD y el 81,3 % de los pacientes con AT tuvieron una respuesta inadecuada. El número de plasmablastos, células B de la zona marginal, células B de transición, células T CD8+ vírgenes y el porcentaje de células T CD8+, células B de memoria IgM y células B de memoria conmutadas en pacientes con SIgAD fueron significativamente menor en un grupo que no respondió que en un grupo que sí respondió. Aunque la deficiencia de anticuerpos específicos es más frecuente en pacientes con AT que en pacientes con SIgAD [44]. Las células T reguladoras desempeñan un papel importante en la producción de anticuerpos IgA al transformar la secreción del factor de crecimiento beta (TGF-) [45-47]. Encontramos Tregs significativamente disminuidas en nuestros pacientes de acuerdo con estudios previos publicados [48], aunque un estudio informó un aumento de Tregs en pacientes con SIgAD [43]. También se ha informado una correlación entre la reducción de las células Treg y la gravedad de la enfermedad SIgAD, especialmente en individuos con autoinmunidad, y la deficiencia de IgA CSR en pacientes con manifestaciones clínicas graves [30, 48]. La baja frecuencia de células Treg y otros subconjuntos de células T, incluidas T1 y T2 en nuestros pacientes, puede deberse a bajos emigrantes tímicos causados por una timopoyesis defectuosa o una mayor apoptosis de estas células [49]. El ensayo funcional de células T mediante estimulación mitogénica o antigénica es una característica importante en el diagnóstico de diversos trastornos inmunitarios e inmunodeficiencias [50]. Tradicionalmente, existe un protocolo para evaluar la función de las células T basado en la absorción de [3H] timidina después de la estimulación con PHA utilizando componentes radiactivos que necesita condiciones de laboratorio específicas y además no es específico de las células T, ya que puede estimular varias otras células inmunes como Bueno. Por otro lado, la debilidad más importante es que no se pudo obtener información sobre subconjuntos de células específicas. El ensayo de proliferación CFSE es una opción práctica para evaluar las respuestas de las células T a un antígeno o mitógeno en pacientes con IEI, especialmente SIgAD para apuntar a análisis adicionales de posibles defectos de las células T en estos pacientes [51]. Hasta el momento, hay pocos informes de defectos en la respuesta de las células T en pacientes con SIgAD. Como era de esperar, nuestro estudio no revela ninguna diferencia significativa en la respuesta de las células T entre pacientes y controles. Sin embargo, cuando categorizamos a los pacientes en dos grupos según los fenotipos graves y leves, los pacientes graves indicaron una menor proliferación de células T en comparación con los pacientes leves. Este resultado podría ser un hallazgo importante para categorizar a los pacientes con SIgAD para conocer el pronóstico del paciente. Recientemente informamos que la proliferación de células T se vio notablemente afectada en comparación con los controles sanos en pacientes con CVID y pacientes con AT [29, 52]. Además, esto indica que los pacientes con SIgAD con proliferación defectuosa de células T deben recibir un seguimiento más detallado para un tratamiento médico preciso. Recomendamos más estudios para evaluar la acción de la función de las células T en pacientes con SIgAD según los fenotipos graves y leves de otros estudios. Las limitaciones del experimento incluyeron el pequeño número de pacientes sintomáticos, la falta de disponibilidad de muchos de ellos e incluso la mejoría de algunos pacientes.
Conclusiones
Nuestros resultados indicaron malidades significativas en patrones de células B similares a los de los pacientes con IDVC. Dado que la CVID y las formas graves de SIgAD comparten fenotipos clínicos e inmunológicos casi similares y muy probablemente antecedentes genéticos, esta noción es predecible. Según los análisis de fenotipo, observamos algunas anomalías más en pacientes con SIgAD con fenotipos graves, como una subpoblación alta de células B bajas en CD21 y un defecto de proliferación de células T. En consecuencia, los pacientes graves manifiestan un mayor número de infecciones respiratorias en comparación con la SIgAD leve, y un gran número de ellos padecen sinusitis, otitis, neumonía yb, bronquiectasias, lo que sugiere un mayor seguimiento y un tratamiento más preciso en estos pacientes. Los autores del presente estudio sugieren que la investigación de los subconjuntos de células B y T podría ser útil para comprender mejor la patogénesis y el pronóstico de la enfermedad.
Referencias
1. Aghamohammadi A, Mohammadi J, Parvaneh N, Rezaei N, Moin M, Espanol T, et al. Progresión de la deficiencia selectiva de IgA a inmunodeficiencia común variable. Int Arch Allergy Immunol. 2008;147(2):87–92.
2. Bagheri Y, Sanaei R, Yazdani R, Shekarabi M, Falak R, Mohammadi J, et al. La patogénesis heterogénea de la deficiencia selectiva de inmunoglobulinas. Int Arch Allergy Immunol. 2019;179(3):232–46.
3. Nechvatalova J, Pikulova Z, Stikarovska D, Pesak S, Vlkova M, Litzman J. Subpoblaciones de linfocitos B en pacientes con deficiencia selectiva de IgA. J Clin Immunol. 2012;32(3):441–8.
4. Litzman J, Vlková M, Pikulová Z, Štikarovská D, Lokaj J. Subpoblaciones de linfocitos T y B y marcadores de activación/diferenciación en pacientes con deficiencia selectiva de IgA. Clin Exp Inmunol. 2007;147(2):249–54.
5. Lemarquis AL, Einarsdottir HK, Kristjansdottir RN, Jonsdottir I, Ludviksson BR. Las células B de transición y las respuestas de TLR9 son defectuosas en la deficiencia selectiva de IgA. Inmunol frontal. 2018;9:909.
6. Celiksoy M, Yildiran A. Una comparación de subconjuntos de células B en inmunodeficiencias primarias avanza con niños sanos compatibles con deficiencia de anticuerpos. Inmunopathol alergol. 2016;44(4):331–40.
7. Marasco E, Farroni C, Cascioli S, Marcellini V, Scarsella M, Giorda E, et al. La activación de células B con CD40L o CpG mide la función de subconjuntos de células B e identifica defectos específicos en pacientes inmunodeficientes. Eur J Immunol. 2017;47(1):131–43.
8. Lemarquis AL, Theodors F, Einarsdottir HK, Ludviksson BR. El mapeo de las vías de señalización vinculadas a sIgAD revela una activación alterada de las células B STAT3 impulsada por IL-21-. Inmunol frontal. 2019;10:403.
9. Borte S, Pan-Hammarstrom Q, Liu C, Sack U, Borte M, Wagner U, et al. La interleucina-21 restablece la producción de inmunoglobulinas ex vivo en pacientes con inmunodeficiencia común variable y deficiencia selectiva de IgA. Sangre. 2009;114(19):4089–98.
10. Abolhassani H, Kiaee F, Tavakol M, Chavoshzadeh Z, Mahdaviani SA, Momen T, et al. Cuarta actualización del Registro Nacional Iraní de inmunodeficiencias primarias: integración del diagnóstico molecular. J Clin Immunol. 2018;38(7):816–32.
11. Aghamohammadi A, Rezaei N, Yazdani R, Delavari S, Kutukculer N, Topyildiz E, et al. Registro de consenso de Oriente Medio y Norte de África sobre errores congénitos de inmunidad. J Clin Immunol. 2021;41(6):1339–51.
12. Seidel MG, Kindle G, Gathmann B, Quinti I, Buckland M, van Montfrans J, et al. Definiciones de trabajo del registro de la Sociedad Europea de Inmunodeficiencias (ESID) para el diagnóstico clínico de errores congénitos de inmunidad. J Allergy Clin Immunol Pract. 2019;7(6):1763–70.
13. Shad TM, Yousef B, Amirifar P, Delavari S, Rae W, Kokhaei P, et al. Anomalías variables en los subconjuntos de células T y B en la ataxia telangiectasia. J Clin Immunol. 2020:1–13.
14. TofghiZavareh F, Mirshafey A, Yazdani R, Keshtkar AA, Abolhassani H, Bagheri Y, et al. Subconjuntos de linfocitos en correlación con un perfil clínico en pacientes con IDCV sin defectos monogénicos. Experto Rev Clin Immunol. 2021;17(9):1041–51.
15. Moeini Shad T, Yousef B, Amirifar P, Delavari S, Rae W, Kokhaei P, et al. Anomalías variables en los subconjuntos de células T y B en la ataxia telangiectasia. J Clin Immunol. 2021;41(1):76–88.
16. Azizi G, Mirshafey A, Abolhassani H, Yazdani R, Ghanavatinejad A, Noorbakhsh F, et al. El desequilibrio de los subconjuntos T auxiliares circulantes y las células T reguladoras en pacientes con deficiencia de LRBA: correlación con la gravedad de la enfermedad. Fisiol de células J. 2018;233(11):8767–77.
17. Azizi G, Mirshafey A, Abolhassani H, Yazdani R, Jafarnezhad-Ansariha F, Shaghaghi M, et al. Subconjuntos de células T auxiliares circulantes y células T reguladoras en pacientes con inmunodeficiencia común variable sin la enfermedad monogénica conocida. J Investig Allergol Clin Immunol. 2018;28(3):172–81.
18. Reisi M, Azizi G, Kiaee F, Masiha F, Shirzadi R, Momen T, et al. Evaluación de complicaciones pulmonares en pacientes con trastornos de inmunodeficiencia primaria. Eur Ann Alergia Clin Immunol. 2017;49(3):122.
19. Cerutti A, Chen K, Chorny A. Respuestas de inmunoglobulina en la interfaz mucosa. Annu Rev Inmunol. 2011;29:273–93.
20. Bagheri Y, Babaha F, Falak R, Yazdani R, Azizi G, Sadri M, et al. IL-10 induce la secreción de TGF, la regulación positiva del receptor II de TGF y la secreción de IgA en las células B. Eur Cytokine Netw. 2019;30(3):107–13.
21. Ozkan H, Atlihan F, Genel F, Targan S, Gunvar T. Deficiencia de subclases de IgA y/o IgG en niños con infecciones respiratorias recurrentes y su relación con el daño pulmonar crónico. J Investig Allergol Clin Immunol. 2005;15(1):69–74.
22. Tavakol M, Jamee M, Azizi G, Sadri H, Bagheri Y, Zaki-Dizaji M, et al. Abordaje diagnóstico de los pacientes con sospecha de inmunodeficiencia primaria. Objetivos farmacológicos para los trastornos inmunitarios de Endocr Metab. 2020;20(2):157–71.
23. Resnick ES, Moshier EL, Godbold JH, Cunningham-Rundles C. Morbilidad y mortalidad en inmunodeficiencia variable común durante 4 décadas. Sangre. 2012;119(7):1650–7.
24. Yazdani R, Abolhassani H, Asgardoon M, Shaghaghi M, Modaresi M, Azizi G, et al. Complicaciones pulmonares infecciosas y no infecciosas en pacientes con trastornos de inmunodeficiencia primaria. J Investig Allergol Clin Immunol. 2017;27(4):213–24.
25. Ahmadi M, Nouri M, Babaloo Z, Farzadi L, Ghasemzadeh A, Hamdi K, et al. El tratamiento con inmunoglobulina intravenosa (IGIV) modula las células Th17 y las células T reguladoras de la sangre periférica en pacientes con abortos espontáneos recurrentes: un ensayo clínico abierto, no aleatorizado. Immunol Lett. 2017;192:12–9.
26. Yazdani R, Seify R, Ganjalikhani-Hakemi M, Abolhassani H, Eskandari N, Golsaz-Shirazi F, et al. Comparación de varias clasificaciones para pacientes con inmunodeficiencia común variable (IDCV) mediante la medición de subconjuntos de células B. Allergol Inmunopathol (Madr). 2017;45(2):183–92.
27. Aghamohammadi A, Abolhassani H, Rezaei N. Enfermedades de inmunodeficiencia primaria en Irán: pasado, presente y futuro. Arco Irán Med. 2021. https://doi. org/10.34172/aim.2021.18.
28. Aghamohammadi A, Abolhassani H, Biglari M, Abolmaali S, Moazzami K, Tabatabaeiyan M, et al. Análisis de células B de memoria conmutadas en pacientes con deficiencia de IgA. Int Arch Allergy Immunol. 2011;156(4):462–8.
29. Yousef B, Amirifar P, Delavari S, Rae W, Kokhaei P, Abolhassani H, et al. Anomalías variables en los subconjuntos de células T y B en la ataxia telangiectasia. J Clin Immunol. 2020. https://doi.org/10.1007/s10875-020-00881-9.
30. Abolhassani H, Gharib B, Shahinpour S, Masoom SN, Havaei A, Mirminachi B, et al. Autoinmunidad en pacientes con deficiencia selectiva de IgA. J Investig Allergol Clin Immunol. 2015;25(2):112–9.
31. Arkwright PD, Abinun M, Cant AJ. Autoinmunidad en enfermedades de inmunodeficiencia primaria humana. Sangre. 2002;99(8):2694–702.
32. Cerutti A, Cols M, Puga I. Células B de la zona marginal: virtudes de los linfocitos productores de anticuerpos de tipo innato. Nat Rev Inmunol. 2013;13(2):118–32.
33. Bukowska-Straková K, Kowalczyk D, Baran J, Siedlar M, Kobylarz K, Zembala M. El compartimento de células B en la sangre periférica de niños con diferentes tipos de inmunodeficiencia humoral primaria. Res. Pediatra. 2009;66(1):28–34.
34. Karaman SBES, Gülez N, Genel F. La importancia de los subconjuntos de células B en pacientes con hipogammaglobulinemia no clasificada y su asociación con el requisito de reemplazo de inmunoglobulina intravenosa. Irán J Immunol. 2018;15(1):1–13.
35. Patuzzo G, Mazzi F, Vella A, Ortolani R, Barbieri A, Tinazzi E, et al. Análisis inmunofenotípico de linfocitos B en pacientes con inmunodeficiencia común variable: identificación del CD23 como marcador útil en la definición de la enfermedad. Inmunol ISRN. 2013. https://doi.org/10. 1155/2013/512527.
36. Patuzzo G, Barbieri A, Tinazzi E, Veneri D, Argentino G, Moretta F, et al. Autoinmunidad e infección en la inmunodeficiencia común variable (IDCV). Autoinmune Rev. 2016;15(9):877–82.
37. Rakhmanov M, Keller B, Gutenberger S, Foerster C, Hoenig M, Driessen G, et al. Las células B CD21low circulantes en la inmunodeficiencia variable común se parecen a las células B innatas que se alojan en los tejidos. Proc Natl Acad Sci. 2009;106(32):13451–6.
38. Isnardi I, Ng YS, Menard L, Meyers G, Saadoun D, Srdanovic I, et al. Las células B humanas vírgenes con receptor de complemento 2/CD21 contienen en su mayoría clones autorreactivos que no responden. Sangre. 2010;115(24):5026–36.
39. Sims GP, Ettinger R, Shirota Y, Yarboro CH, Illei GG, Lipsky PE. Identificación y caracterización de células B transicionales humanas circulantes. Sangre. 2005;105(11):4390–8.
40. Lemarquis AL, Einarsdottir HK, Kristjansdottir RN, Jonsdottir I, Ludviksson BR. Las respuestas de las células B de transición y TLR9 son defectuosas en la deficiencia selectiva de IgA. Inmunol frontal. 2018. https://doi.org/10.3389/fmmu.2018. 00909.
41. Willinger T, Freeman T, Hasegawa H, McMichael AJ, Callan MF. Las firmas moleculares distinguen la memoria central humana de los subconjuntos de células T CD8 con memoria efectora. J Inmunol. 2005;175(9):5895–903.
42. Martín MD, vicepresidente de Badovinac. Definición de células T CD8 de memoria. Inmunol frontal. 2018;9:2692.
43. Nechvatalova J, Pavlik T, Litzman J, Vlkova M. Las células T de memoria diferenciadas terminalmente aumentan en pacientes con inmunodeficiencia común variable y deficiencia selectiva de IgA. Cent Eur J Immunol. 2017;42(3):244–51.
44. Khanmohammadi S, Shad TM, Delavari S, Shirmast P, Bagheri Y, Azizi G, et al. Evaluación de respuestas de anticuerpos específicos en pacientes con deficiencia selectiva de IgA y ataxia telangiectasia. Objetivos farmacológicos para los trastornos inmunitarios de Endocr Metab. 2022;22(6):640–9.
45. Cazac BB, Roes J. El receptor de TGF controla la capacidad de respuesta de las células B y la inducción de IgA in vivo. Inmunidad. 2000;13(4):443–51.
46. Van Vlasselaer P, Punnonen J, De Vries J. El factor de crecimiento transformante beta dirige la conmutación de IgA en células B humanas. J Inmunol. 1992;148(7):2062–7.
47. Cerutti A, Rescigno M. La biología de las respuestas de la inmunoglobulina A intestinal. Inmunidad. 2008;28(6):740–50.
48. Soheili H, Abolhassani H, Arandi N, Khazaei HA, Shahinpour S, Hirbod Mobarakeh A, et al. Evaluación de células T reguladoras naturales en sujetos con deficiencia selectiva de IgA: de la idea senior a oportunidades novedosas. Int Arch Allergy Immunol. 2013;160(2):208–14.
49. Yazdani R, Fatholahi M, Ganjalikhani-Hakemi M, Abolhassani H, Azizi G, Hamid KM, et al. Papel de la apoptosis en la inmunodeficiencia variable común y la deficiencia selectiva de inmunoglobulina A. Mol Inmunol. 2016;71:1–9.
50. McCusker C, Warrington R. Inmunodeficiencia primaria. Todo Asth Clin Immun. 2011;7(Suplemento 1):S11.
51. Marits P, Wikström AC, Popadic D, Winqvist O, Thunberg S. Evaluación de la función de los linfocitos T y B en la práctica clínica mediante un ensayo de proliferación basado en citometría de flujo. Clin Inmunol. 2014;153(2):332–42.
52. TofghiZavareh F, Mirshafey A, Yazdani R, Keshtkar AA, Abolhassani H, Mahdaviani SA, et al. Análisis inmunofenotípico y funcional de subconjuntos de linfocitos en pacientes con inmunodeficiencia común variable sin defectos monogénicos. Scand J Immunol. 2022;96(1):e13164.
