Enfermedad renal crónica de etiología desconocida (ERCd) en Sri Lanka: los cambios hematológicos y la proinflamación sugieren predictores probables de enfermedad avanzada, ya que los resultados renales muestran una normoalbuminuria prevalente
Jul 03, 2023
Abstracto
La ERCDu debe caracterizarse en áreas fundamentales para mejorar la comprensión etiológica y el manejo de la enfermedad. En un estudio transversal, el perfil de células sanguíneas y las citocinas inflamatorias en plasma se siguieron mediante análisis automatizado y ELISA tipo sándwich, respectivamente. Las etapas de desarrollo de la enfermedad y la proteinuria se determinaron mediante eGFR y UACR. La comparación entre el control y las etapas (ANOVA/MRT de Dunnett) reveló cambios específicos de tiempo (p < 0.{{10}}5), incluida la disminución de eritrocitos (G5) y hematocrito (G5), y aumento de MCHC (G3b, G4), MCV (G5) y MCH (G5). ERCDu disminuyó (p < 0.05) linfocitos (G3b, G4, G5), monocitos (G3b), MPV (G3b, G4, G5) y plaquetas (G3b, G4), y aumento de basófilos (G3a, G3b, G4), N/L (G4) y PLR (G4-G5). MCHC y las variables leucocitarias mencionadas anteriormente se correlacionaron (rho > ±0.03, p < 0.05, prueba de Pearson) con el desarrollo de la enfermedad. MCP-1 e IL-6 aumentaron (p > 0,05) en G3b. Los análisis multivariados confirmaron que la MCP-1, los linfocitos y el IMC estaban relacionados con la disfunción renal, lo que apunta a inflamación, inmunidad comprometida y atrofia muscular como efectos de la CKDu. La ERCDu no proteinúrica fue prevalente (23.2–35.6 por ciento de la ERCDu total) con (p < 0.05) basófilos elevados (G3a), N/L (G4) y linfocitos reducidos (G4). En ambas formas, G1-G2 no se vieron afectados y el cambio más temprano fueron los basófilos G3a. Los resultados sugieren que MCP-1, el recuento de linfocitos, N/L y PLR pueden verificar el estadio y predecir la ESRD inminente en la ERCd proteinúrica avanzada.
Palabras clave
enfermedad renal crónica de etiología desconocida; desarrollo de enfermedad renal crónica; hematología; no proteinuria; proteína quimioatrayente de monocitos-1; interleucina-6; basófilos; linfocitos; proporción de neutrófilos a linfocitos; volumen medio de plaquetas.

Pincha aquí para saber qué es el Cistanche
Introducción
La enfermedad renal crónica de etiología desconocida (ERCd) en Sri Lanka es una nefropatía endémica en las provincias del centro norte y Uva del país [1]. La ERCd es distinta ya que carece de una asociación etiológica con factores de riesgo de iniciación de la ERC, como la diabetes mellitus y la hipertensión [2]. Sin embargo, obedece a criterios diagnósticos basados en malos resultados renales en términos de tasa de filtración glomerular estimada (TFGe) y cociente entre albúmina y creatinina en orina (UACR) [3].
La ERCd temprana se caracteriza por infiltración inflamatoria en el tubulointersticio, tubulitis, fibrosis y cicatrización glomerular [4] que progresa a enfermedad renal terminal (ESRD) posiblemente a través de isquemia crónica atribuida al daño intersticial [5]. La histopatología y el daño tisular apuntan a un componente inflamatorio en la progresión de la enfermedad. Los efectos de la ERC como la anemia [6], la inmunidad comprometida [7] y la inflamación [8] se manifiestan en la sangre. En este contexto, la ERCd endémica en Sri Lanka debe caracterizarse por los cambios relacionados con los puntos temporales de aparición durante la progresión de la enfermedad. Los cambios celulares y bioquímicos de la sangre total son fácilmente detectables, por lo que dicha comprensión mejorará las capacidades de diagnóstico y predicción al tiempo que refuerza el conocimiento de la etiología. Para este propósito, el estudio siguió los cambios en la sangre, el perfil de células inmunitarias e inflamatorias y los niveles de citocinas durante la progresión de la ERCDu desde buenos resultados renales (control) hasta enfermedad renal en etapa terminal (ESRD). También examinó la dicotomía etiológica clave de ERC, proteinuria y no proteinuria (normoalbuminuria) en la ERCd endémica de Sri Lanka en un esfuerzo novedoso. La claridad, en este sentido, es importante ya que la albuminuria es un marcador clave en la detección y el diagnóstico de la enfermedad renal.
Materiales y métodos
Se realizó un estudio transversal en el área endémica de Girandurukotte/Mahiyanganaya (GK/MH) con ERCDu en la provincia de Uva de Sri Lanka. Después del consentimiento informado, participaron en el estudio (n > 205) voluntarios que presumiblemente estaban sanos o bajo atención médica por diagnóstico de ERC/ERCd (n > 205) (Esquema 1). Los participantes que tenían factores de riesgo de inicio (IRF) de ERC [9] antes del diagnóstico inicial con malos resultados renales se consideraron ERC y se excluyeron. La IRF se determinó mediante una entrevista al sujeto e incluyó diabetes, hipertensión, infecciones sistémicas, infecciones del tracto urinario, cálculos urinarios, obstrucciones del tracto urinario inferior y antecedentes familiares de enfermedad renal. Se recolectó sangre completa periférica (3-5 ml), orina puntual e información demográfica del resto bajo supervisión médica y ética. La recolección de muestras se realizó en el período 2017-2018 del estudio.
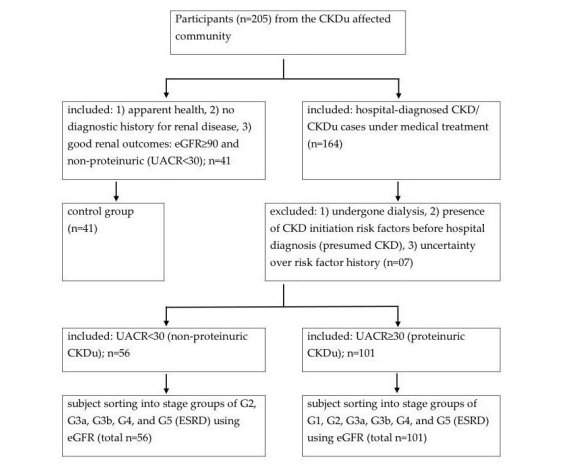
Esquema 1. Clasificación de sujetos en grupos de estudio en el área endémica de Girandurukotte/Mahiyanganaya con ERCDu, ERC: enfermedad renal crónica, eGFR: tasa de filtración glomerular estimada (ml/min/1,73 m2), UACR: proporción de albúmina a creatinina en orina (mg/g), G1–G5: estadios de desarrollo de CKD, ESRD: enfermedad renal en etapa terminal, el estudio se basó en sus determinaciones puntuales de eGFR y UACR.

suplemento de cistanche
1. Procesamiento inicial de muestras
Se enviaron alícuotas de sangre total con EDTA en hielo para recuentos de células el mismo día con un analizador de hematología automatizado (HumaCount 5 L, Wiesbaden) en un laboratorio comercial. El plasma y el suero se obtuvieron mediante centrifugación (3000 rpm × 10 min a temperatura ambiente) de sangre completa con EDTA y se dejó que la sangre completa se coagulara (30 min a temperatura ambiente), respectivamente. Los sobrenadantes se almacenaron en hielo seco para su transporte antes del almacenamiento final a -80 ◦C en un congelador en el laboratorio.
2. Marcadores de disfunción renal
La creatinina sérica (sCr, mg/dl), la albúmina en orina (mg/l) y la creatinina en orina (mg/dl) se midieron mediante ensayos enzimáticos colorimétricos, inmunoturbidimétricos y de Jaffe, respectivamente (analizador de química clínica Mindray BS-200 , Shenzhen, China). Se midió la cistatina C sérica (sCysC, mg/L) (analizador de proteína específica QR100- Heales, Shenzhen, China) mediante ensayo turbidimétrico mejorado con látex. Todos los ensayos se adhirieron a las respectivas medidas y protocolos de control de calidad del fabricante.
La tasa de filtración glomerular estimada (TFGe, ml/min/1,73 m2) se calculó mediante la ecuación de la colaboración epidemiológica de la enfermedad renal crónica (CKD-EPI) usando sCr [10]. Además, la eGFR también se estimó mediante las ecuaciones, la modificación abreviada de la dieta en la enfermedad renal (MDRD) por sCr, CKD-EPI por sCysC y CKD-EPI por sCr y sCysC como se describe en otro lugar [10,11]. La relación entre albúmina y creatinina en orina (UACR, mg/g) se estimó utilizando la albúmina en orina (mg/l) y la creatinina en orina (mg/dl).
3. Clasificación de materias en grupos de estudio
La eGFR (CKD-EPI, sCr) y la UACR se utilizaron para clasificar a los sujetos en estadios de control y ERC de conformidad con el protocolo aceptado en los estudios [3,12]. Brevemente, los sujetos con CKDu verificados por IRF se clasificaron provisionalmente por eGFR en grupos de estadios de CKD como G1 mayor o igual a 90, G2; 89–60, G3a: 59–45, G3b: 44–30, G4: 29–15 y G5 (enfermedad renal en etapa terminal/ESRD) < 15. Los sujetos en las etapas G1–G5 se clasificaron además como proteinúricos (UACR Mayor o igual a 30), o no proteinúricos (normoalbuminúricos, UACR < 30) como se describió antes [13]. El grupo de control se constituyó para tener eGFR mayor o igual a 90 y UACR < 30 y por lo tanto tener una buena salud renal.
4. Mediciones de citoquinas
Se determinó un rango de seis mediadores proinflamatorios en plasma mediante ensayo inmunoabsorbente ligado a enzimas tipo sándwich (ELISA). kits de prueba ThermoFisher Scientific® (Waltham, MA, EE. UU.); BMS243-2, KAC1261, BMS228, BMS2034 y BMS281 se usaron para interleucina-1 alfa (IL-1 ), interleucina-6 (IL-6), interferón -gamma (IFN-), factor de necrosis tumoral alfa (TNF-) y proteína quimioatrayente de monocitos-1 (MCP-1) respectivamente.
5. Estadística
Análisis Se probó la significación estadística de cada variable dependiente continua entre los grupos de control y de etapa de desarrollo de la enfermedad y la asociación lineal con la progresión de la enfermedad usando ANOVA unidireccional seguido de la prueba de rango múltiple de Dunnett y el método de correlación de Pearson, respectivamente. La significación estadística (p < 0.05) en la comparación de grupos era un requisito previo para que se probara la correlación de cualquier variable. Se realizaron análisis multivariados para determinar las relaciones no lineales entre las variables que mostraban una correlación mínima en o más allá de r=±0.03 y p < 0.05 (prueba de Pearson) con cualquiera de los marcadores de disfunción renal de el estudio. Posteriormente se realizó un análisis de componentes principales (PCA) por matriz basada en correlaciones para identificar variables agrupadas. Fue seguido por el desarrollo de un dendrograma de conglomerados para la visualización de datos adicionales, lo que implica un enlace completo y la distancia del coeficiente de correlación. Se esperaba que la selección variable progresiva mantuviera el rigor y destacara los candidatos a marcadores más confiables al final. Los procedimientos estadísticos y el trazado se realizaron en el software estadístico Minitab 17.

pastillas de cistanche
6. Evaluación de la no proteinuria
Log10 transformó eGFR y UACR se trazaron para visualizar la no proteinuria y la proteinuria conceptualmente y sobre el desarrollo de la enfermedad. Los datos del presente estudio de GK/MH se proyectaron con los datos de Padaviya (PDV) endémica de ERCDu en la Provincia Central del Norte para comparar. El estudio PDV fue ratificado (RP/2015/04) por el comité de revisión ética mencionado anteriormente (Sección 2) y tuvo procedimientos de muestreo, análisis de mercado y clasificación de sujetos idénticos a los del estudio GK/MH.
Discusión
Los casos de ERC y ERCDu coexisten en áreas endémicas de ERCDu de Sri Lanka [1,14,15]. Dado que la ERC se deriva de sus factores de riesgo de inicio [9], la falta de dicha historia en pacientes con ERC/ERCd diagnosticados en el hospital se consideró como prueba de un sujeto con ERCd. El presente estudio involucró a voluntarios de todos los niveles del desarrollo de la enfermedad y los sanos, que fueron clasificados en eGFR y verificados con UACR. Este enfoque permitió seguir la progresión de la enfermedad desde buenos resultados renales (control normoalbuminúrico con eGFR mayor o igual a 90) hasta estadios de ERC G1 a G5 (ESRD) en un punto de tiempo en un diseño transversal. Esencialmente, la eGFR, UACR y la clasificación por etapas establecieron la disfunción renal o el eje de progresión de la ERCd que permitió estudiar variables dependientes sobre ella.
Las variaciones hematológicas (p < 0.05) en el desarrollo de ERCd proteinúrica comenzaron con el recuento de basófilos G3a y se correlacionaron con disfunción renal progresiva, lo que sugiere que la insuficiencia renal podría ser la causa. Tales variables en conjunto pueden constituir un predictor de estadios avanzados de ERCd sujetos a reproducibilidad y detección temprana. Los candidatos son basófilos G3a y MCHC G3b, linfocitos, monocitos, MPV y PCT y G4 N/L. En ausencia de proteinuria, se pueden considerar basófilos G3a seguidos de linfocitos G4 y N/L.
Una tendencia celular común fue que un aumento en MCHC en G3b y G4 fue seguido por una disminución de RBC en ESRD (p < 0.05). Además, en ESRD, la hemoglobina total (HB) y el hematocrito (HCT) también se redujeron (variación entre grupos; p < 0.05 por ANOVA, p > 0.05 por MRT de Dunnett), mientras que MCV y MCH había aumentado significativamente (p <0,05). Los resultados confirman la anemia, que es un resultado de la ERC [6,16]. Los mecanismos plausibles incluyen la deficiencia de hierro y eritropoyetina y el acortamiento de la vida útil de los eritrocitos que emergen como complicaciones [17]. Las tendencias temporales muestran que las disminuciones de glóbulos rojos, HB y HCT se manifiestan hasta ESRD/CKDu, sin asociación estadística con los marcadores de disfunción. El ancho de distribución de glóbulos rojos (RDW) es una medida de la variación del tamaño de los glóbulos rojos. Los pacientes con ERC tienen niveles altos de RDW [16] que se perpetúan a lo largo de las etapas de la ERC [18]. El RDW no afectado en CKDu sigue siendo intrigante en el presente estudio.
Con la progresión de la ERCDu, los recuentos de neutrófilos y eosinófilos no cambiaron (p > 00,05), pero los números de basófilos permanecieron consistentemente altos en G3a, G3b y G4, y se correlacionaron con la progresión de la ERCDu. Los basófilos son los mediadores celulares clave de las reacciones de hipersensibilidad de tipo I, por lo que podría decirse que las células pueden tener un papel inflamatorio en la progresión de la ERCd. El N/L elevado también se ha postulado como un indicador de inflamación que se asocia con malos resultados renales [19], particularmente en estadios avanzados de ERC [20]. Se apreció el valor pronóstico de N/L, particularmente en la etapa 4 de la ERC [21]. Como muestran los resultados, N/L aumentó en G4 en correlación con la progresión de CKDu en el área GK/MH y podría estar relacionado con neutrófilos inalterados y recuentos de linfocitos disminuidos en la etapa.

Cistanche tubulosa
Disminución significativa del recuento de linfocitos en sangre periférica en G3b, G4 y ESRD se correlacionó con la disfunción renal. La depleción de linfocitos es compatible con la inmunodeficiencia en estadios avanzados de ERC [7,22–24]. El aumento transitorio de la MCP plasmática -1 en G3b (Figura 2) y los monocitos de sangre periférica agotados (G3b) en correlación con la disfunción renal podrían estar relacionados mecánicamente en el posible evento de infiltración de monocitos en el tejido renal [25]. El aumento de la MCP-I plasmática debería deberse a la regulación al alza de la expresión más que a un aclaramiento renal deficiente durante la enfermedad [26]. Se ha informado una elevación de MCP-1 en asociación con una disminución de la TFGe en la ERC [27]. El pico plasmático de IL-6 en sujetos con ERCDu en G3b es notable, ya que es una citocina multifuncional que tiene funciones moduladoras en facetas diferentes pero superpuestas de la ERC, como la anemia [28], la respuesta de fase aguda, la diferenciación de monocitos en macrófagos, y respuestas de células T [29]. El aumento de la IL-6 plasmática es común en la ERC, y la inflamación crónica, el aclaramiento renal deficiente y los factores de estrés emergentes pueden ser los inductores.
Las etapas avanzadas de la insuficiencia renal crónica afectan la integridad y función de las plaquetas. Los criterios de valoración comunes son las anomalías plaquetarias [30] y la disfunción plaquetaria urémica [31]. Entre los sujetos con ERC, se informó un VPM más bajo relacionado positivamente con la TFGe [32,33] y reactividades plaquetarias reducidas [33]. Las reducciones significativas en MPV y PCT de G3b en el presente estudio pueden mostrar un inicio de tendencias hemorrágicas mucho antes que ESRD en el desarrollo de CKDu, lo que sugiere un valor predictivo de las variables en cuestión. Se ha evaluado el aumento de la PLR por su papel inflamatorio y su aparición en las etapas de prediálisis y ESRD [34]. En sujetos GK/MH CKDu desde G4 en adelante, el recuento de plaquetas no afectado (p > 0,05) puede ser una razón para un PLR elevado en medio de una depleción concomitante de linfocitos.
La consideración de PCA y dendrograma (similitud > 60 por ciento) confirma que la MCP-1, los linfocitos totales y el IMC son los parámetros individuales que siguen de cerca la disfunción renal progresiva en la ERCd endémica. El IMC mostró una variación intergrupal significativa (p < 0.05) por ANOVA sin confirmación (p > 0.05) del MRT de Dunnett (datos no mostrados). Esto, junto con las respuestas N/L y PLR (Figura 1, Tabla 1), que se relacionaron con una similitud del 83,9 por ciento, indican que la inflamación continua, la inmunidad comprometida y la atrofia muscular aseguran el deterioro de la salud renal en ESRD.
La división de proteinuria y no proteinuria refleja dos vías, que convergen en la ESRD a través del daño tubular e intersticial [35]. El primero implica la reabsorción de albúmina del filtrado glomerular. Da como resultado la generación local de especies reactivas de oxígeno (ROS) y la activación de agentes inmunitarios e inflamatorios de manera sostenida [35]. La vía no proteinúrica parece depender de factores como la hiperfiltración en las nefronas [35], que está relacionada con un bajo número de nefronas al nacer. Sin embargo, aún no se sabe si tales factores de riesgo pueden describir la ERCd. La revisión de la literatura convenció a los autores de que la ausencia de proteinuria en la ERCd de Sri Lanka no se ha investigado ni revisado con atención. Curiosamente, la presencia de normoalbuminuria (23-35 por ciento entre la ERCd total) en el estudio sugiere dos etiologías desconocidas en el desarrollo de la ERCd en el país. Las parcelas conceptuales derivadas fueron consistentes entre las áreas endémicas estudiadas. Proporciona pruebas de que la ERCd endémica en GK/MH y PDV comprende enfermedad renal tanto proteinúrica como no proteinúrica. Es probable que esta tendencia también sea común en toda el área geográfica de endemicidad de ERCd. Los sujetos G1 no proteinúricos (UACR < 30) no existían en los datos ya que G1 representa eGFR mayor o igual a 90, y los criterios juntos clasifican los casos entre buenos resultados renales. Se identificó un sujeto cada uno (n=1) en no proteinuria/ESRD/CKDu en GK/MH (n=56) y PDV (n=41). La escasez de casos en ESRD en comparación con proteinúrico/ESRD (n=18 de GK/MH y n=33 de PDV) apunta a la probabilidad de que UACR pueda aumentar hacia etapas avanzadas en la no proteinuria. Las preguntas acerca de si la ERC no proteinúrica puede desarrollar proteinuria en o antes de la ESRD se habían planteado antes [14].
La ausencia de proteinuria entre los casos de ERCd debería comprometer el cribado comunitario y el diagnóstico inicial de la enfermedad renal crónica según los criterios actuales [36] como UACR mayor o igual a 30 solo apunta a ERCd proteinúrica. La práctica pasa por alto la ERCd normoalbuminúrica y la ERC. El problema puede evitarse confiando más en la medición en serie de eGFR y adoptando un marcador que ha sido validado para el daño renal temprano. La noción de que la ERCDu en Sri Lanka típicamente asocia proteinuria mínima en etapas tempranas [37] puede ser discutible ya que la presencia de ambas categorías de ERCDu puede subestimar la verdadera albuminuria en las estadísticas grupales. Los resultados del presente estudio mostraron albuminuria entre la mayoría de los casos de ERCd (64-76 por ciento), que abarcó de G1 a G5 (ESRD) en ambas áreas endémicas estudiadas.
Las variaciones de basófilos, linfocitos y N/L en la no proteinuria, y sus asociaciones con la disfunción renal, parecen corresponder a la proteinuria, considerando los puntos temporales de aparición durante la progresión de la ERCd. Sin embargo, sin cambios (p > {{0}}.05) MCP-1, IL-6 y recuentos de monocitos/macrófagos en sangre periférica durante la progresión de la enfermedad apuntan solo a una inflamación moderada en comparación con el desarrollo de la enfermedad proteinúrica. De manera similar, las variables de eritrocitos/hemoglobina y plaquetas no afectadas (p > 0,05) en la no proteinuria sugieren un menor impacto en el desarrollo de la enfermedad en comparación con la enfermedad proteinúrica. La escasez de no proteinuria en la ESRD planteó la limitación en la verificación de las respuestas sanguíneas asociadas, como la anemia, en la etapa final.

extracto de cistanche
Conclusiones
En particular, alrededor de una cuarta parte de las personas afectadas por ERCDu en áreas endémicas de Sri Lanka podrían ser normoalbuminúricas, que no se vieron afectadas a pesar de la progresión de la enfermedad. Este informe novedoso también indica que la detección y el diagnóstico comunitarios basados en la albuminuria pueden pasar por alto una fracción considerable de la enfermedad renal y enfatiza la necesidad de un marcador temprano de disfunción renal para complementar la eGFR y compensar la restricción. Los cambios en los recuentos de células sanguíneas periféricas, los índices y las citoquinas proinflamatorias surgieron a la mitad del desarrollo de la enfermedad y no calificaron para ser marcadores tempranos. Los cambios, sin embargo, eran atributos de la enfermedad avanzada. Los análisis mostraron que el pico de MCP-1 en G3b, el agotamiento de linfocitos que abarca G3b-G5 y N/L y PLR elevados en G4 y G4-G5, respectivamente, posiblemente verificarían la etapa y predecirían ESRD en CKDu proteinúrica. Los basófilos G3a-G5 aumentados y el MPV G3b-G5 disminuido fueron persistentes en la enfermedad avanzada y en asociación con la disfunción renal progresiva para ser candidatos adicionales como marcadores y predictores de estadio. Los esfuerzos de reproducibilidad, la elucidación mecanicista y los marcadores en concierto deberían ser otras direcciones.
Referencias
1. Ranasinghe, AV; Kumara, GWGP; Karunarathna, RH; de Silva, AP; Sachintani, KGD; Gunawardena, JMCN; Kumari, SKCR; Sarjana, MSF; Chandraguptha, JS; de Silva, MVC La incidencia, prevalencia y tendencias de la enfermedad renal crónica y la enfermedad renal crónica de etiología incierta (CKDu) en la provincia norte-central de Sri Lanka: un análisis de 30.566 pacientes. BMC Nephrol. 2019, 20, 338. [Referencia cruzada] [PubMed]
2. Kafle, K.; Balasubramanya, S.; Horbulyk, T. Prevalencia de la enfermedad renal crónica en Sri Lanka: un perfil de los distritos afectados que dependen de las aguas subterráneas. ciencia Entorno Total. 2019, 694, 133767. [Referencia cruzada] [PubMed]
3. Stevens, PE; Levin, A. Evaluación y manejo de la enfermedad renal crónica: sinopsis de la enfermedad renal: mejora de los resultados globales 2012 guía de práctica clínica. Ana. Interno. Medicina. 2013, 158, 825–830. [Referencia cruzada] [PubMed]
4. Badurdeen, Z.; Nanayakkara, N.; Ratnatunga, Nevada; Wazil, AW; Abeysekera, TD; Rajakrishna, PN; Alwis, AP La enfermedad renal crónica de etiología incierta en Sri Lanka es una posible secuela de la nefritis intersticial. perfil clinicopatológico de pacientes sintomáticos con ERCd de nuevo diagnóstico. clin. nefrol. 2016, 86 (Suplemento S1), 106–109. [Referencia cruzada] [PubMed]
5. Nangaku, M. Hipoxia crónica y lesión tubulointersticial: una vía común final hacia la insuficiencia renal terminal. Mermelada. Soc. nefrol. 2005, 17, 17–25. [Referencia cruzada] [PubMed]
6. McMurray, J.; Parfrey, P.; Adamson, JW; Aljama, P.; Berns, JS; Bohlius, J.; Weiss, G. Enfermedad renal: mejora de los resultados globales (KDIGO) grupo de trabajo de anemia. Guía de práctica clínica KDIGO para la anemia en la enfermedad renal crónica. Riñón Inter. Suplemento 2012, 2, 283–287.
7. Xiang, F.-F.; Zhu, J.-M.; Cao, X.-S.; Shen, B.; Zou, J.-Z.; Liu, Z.-H.; Zhang, H.; Teng, J.; Liu, H.; Ding, X.-Q. El agotamiento de linfocitos y la alteración de subconjuntos se correlacionan con la función renal en pacientes con enfermedad renal crónica. Ren. Fallar. 2016, 38, 7–14. [Referencia cruzada] [PubMed]
8. Mihai, S.; Codrici, E.; Popescu, ID; Enciu, A.-M.; Albulescu, L.; Necula, LG; Mambet, C.; Antón, G.; Tanase, C. Mecanismos relacionados con la inflamación en la predicción, progresión y resultado de la enfermedad renal crónica. J. Immunol. Res. 2018, 2018, 2180373. [Referencia cruzada]
9. Levey, AS; Eckardt, K.-U.; Tsukamoto, Y.; Levin, A.; Coresh, J.; Rossert, J.; Zeeuw, DD; Hostetter, TH; Lameire, N.; Eknoyan, G. Definición y clasificación de la enfermedad renal crónica: una declaración de posición de la enfermedad renal: mejora de los resultados globales (KDIGO). Riñón Int. 2005, 67, 2089–2100. [Referencia cruzada]
10. Entintador, LA; Schmid, CH; Tighiouart, H.; Eckfeldt, JH; Feldman, Hola; Greene, T.; Kusek, JW; Manzi, J.; van Lente, F.; Zhang, YL; et al. Estimación de la tasa de filtración glomerular a partir de creatinina y cistatina séricas CN Engl. J.Med. 2012, 367, 20–29. [Referencia cruzada] [PubMed]
11. Levey, AS; Coresh, J.; Balk, E.; Kausz, AT; Levin, A.; Steffes, MW; Hogg, RJ; Perrone, RD; Lau, J.; Eknoyan, G. Pautas de práctica de la fundación nacional del riñón para la enfermedad renal crónica: evaluación, clasificación y estratificación. Ana. Interno. Medicina. 2003, 139, 137–147. [Referencia cruzada] [PubMed]
12. Fundación Nacional del Riñón. Nefropatía. Iniciativa de Calidad de Resultados (K/DOQI). Guías de práctica clínica para la enfermedad renal crónica: evaluación, clasificación y estratificación. Soy. J. enfermedad renal. 2002, 2 (Suplemento 1), S1–S266.
13. Yamanouchi, M.; Furuichi, K.; Hoshino, J.; Úbara, Y.; Wada, T. Enfermedad renal diabética no proteinúrica. clin. Exp. nefrol. 2020, 24, 573–581. [Referencia cruzada] [PubMed]
14. Athuraliya, TNC; Abeysekera, DTDJ; Amerasinghe, PH; Kumarasiri, PVR; Dissanayake, V. Prevalencia de enfermedad renal crónica en dos hospitales de atención terciaria: alta proporción de casos con etiología incierta. Ceilán. Medicina. J. 2009, 54, 23–25. [Referencia cruzada] [PubMed]
15. Jayasekara, KB; Dissanayake, DM; Sivakanesan, R.; Ranasinghe, A.; Karunarathna, RH; Kumara, GWGP Epidemiología de la enfermedad renal crónica, con especial énfasis en la enfermedad renal crónica de etiología incierta, en la región centro-norte de Sri Lanka. J. Epidemiol. 2015, 25, 275–280. [Referencia cruzada] [PubMed]
16. Roumeliotis, SK; Stamou, A.; Panagoutsos, S.; Roumeliotis, AK; Thodis, E.; Passadakis, P. Asociación del ancho de distribución de sangre roja (RDW) con aterosclerosis carotídea y deterioro de la enfermedad renal crónica en pacientes con diabetes mellitus tipo 2. nefrol. Marcar. Transpl. 2016, 31 (Suplemento S1), 422–438. [Referencia cruzada]
17. Babitt, JL; Lin, HY Mecanismos de anemia en la ERC. Mermelada. Soc. nefrol. 2012, 23, 1631–1634. [Referencia cruzada] [PubMed]
18. Solak, Y.; Gaipov, A.; Turco, S.; Kayrak, M.; Yilmaz, MI; Caglar, K.; Verim, S.; Unal, HU; Gok, M.; Demirkaya, E.; et al. El ancho de distribución de los glóbulos rojos está relacionado de forma independiente con la disfunción endotelial en pacientes con enfermedad renal crónica. Soy. J.Med. ciencia 2014, 347, 118–124. [Referencia cruzada] [PubMed]
19. Yoshitomi, R.; Nakayama, M.; Sakoh, T.; Fukui, A.; Katafuchi, E.; Seki, M.; Tsuda, S.; Nakano, T.; Tsuruya, K.; Kitazono, T. La proporción alta de neutrófilos/linfocitos se asocia con malos resultados renales en pacientes japoneses con enfermedad renal crónica. Ren. Fallar. 2019, 41, 238–243. [Referencia cruzada] [PubMed]
20. Bien, GU; Inal, S.; Öneç, K.; Er, RE; Pa'sao ˘glu, Ö.; Pasaoglu, H.; Derici, U.; Erten, Y. Relación de neutrófilos a linfocitos en la evaluación de la inflamación en pacientes con enfermedad renal crónica. Ren. Fallar. 2013, 35, 29–36. [Referencia cruzada] [PubMed]
21. Yuan, P.; Wang, J.; Peng, Z.; Zhou, Q.; Xiao, X.; Xie, Y.; Wang, W.; Huang, L.; Tang, W.; Sol, D.; et al. Proporción de neutrófilos a linfocitos y enfermedad renal terminal incidente en pacientes chinos con enfermedad renal crónica: resultados del estudio de cohorte chino de enfermedad renal crónica (C-STRIDE). J. traducción Medicina. 2019, 17, 1–8. [Referencia cruzada]
22. Agarwal, R.; Light, RP Patterns y valor pronóstico de la cuenta leucocitaria total y diferencial en la enfermedad renal crónica. clin. Mermelada. Soc. nefrol. 2011, 6, 1393–1399. [Referencia cruzada]
23. Litjens, Nueva Hampshire; van Groninga, CJ; Betjes, M. La pérdida progresiva de la función renal se asocia con la activación y el agotamiento de los linfocitos T vírgenes. clin. inmunol. 2006, 118, 83–91. [Referencia cruzada] [PubMed]
24. Kato, S.; Chmielewski, M.; Honda, H.; Pecoits-Filho, R.; Matsuo, S.; Yuzawa, Y.; Tranaeus, A.; Stenvinkel, P.; Lindholm, B. Aspectos de la disfunción inmunológica en la enfermedad renal en etapa terminal. clin. Mermelada. Soc. nefrol. 2008, 3, 1526–1533. [Referencia cruzada] [PubMed]
25. Eardley, K.; Zehnder, D.; Quinkler, M.; Lepenies, J.; Bates, R.; Salvaje, C.; Howie, A.; Adu, D.; Cockwell, P. La relación entre albuminuria, MCP-1/CCL2 y macrófagos intersticiales en la enfermedad renal crónica. Riñón Int. 2006, 69, 1189–1197. [Referencia cruzada] [PubMed]
26. Heine, GH; Ortíz, A.; Massy, ZA; Lindholm, B.; Wiecek, A.; Martínez-Castelao, A.; Fliser, D.; Covic, A.; Orfebre, D.; Süleymanlar, G.; et al. Subpoblaciones de monocitos y riesgo cardiovascular en la enfermedad renal crónica. Nat. Rev. Nephrol. 2012, 8, 362–369. [Referencia cruzada] [PubMed]
27. Gregg, LP; Tío, MC; Li, X.; Adams-Huet, B.; de Lemos, JA; Hedayati, SS Asociación de la proteína quimioatrayente de monocitos-1 con la muerte y eventos ateroscleróticos en la enfermedad renal crónica. Soy. J. Nephrol. 2018, 47, 395–405. [Referencia cruzada]
28. Coyne, DW; Fleming, R. ¿Cambiar nuestro paradigma de tratamiento si nos dirigimos a la interleucina-6 en la anemia de la ERC? Mermelada. Soc. nefrol. 2021, 32, 6–8. [Referencia cruzada] [PubMed]
29. Su, H.; Lei, C.-T.; Zhang, C. Vía de señalización de la interleucina-6 y su papel en la enfermedad renal: una actualización. Frente. inmunol. 2017, 8, 405. [Referencia cruzada] [PubMed]
30. Kaw, D.; Malhotra, D. Disfunción plaquetaria y enfermedad renal terminal. Semin. Marcar. 2006, 19, 317–322. [Referencia cruzada] [PubMed]
31. Linthorst, GE; Avis, HJ; Levi, M. La trombocitopatía urémica no se trata de urea. Mermelada. Soc. nefrol. 2010, 21, 753–755. [Referencia cruzada] [PubMed]
32. Ju, HY; Kim, JK; Hur, SM; Woo, SA; parque, ka; Parque, MI; Choi, SJ; Hwang, SD ¿Podría significar que el volumen plaquetario es un biomarcador prometedor de la progresión de la enfermedad renal crónica? Plaquetas 2015, 26, 143–147. [Referencia cruzada]
33. Van Bladel, Urgencias; de Jager, RL; Walter, D.; Cornelissen, L.; Gaillard, California; Boven, LA; Fijnheer, R.; Roest, M. Las plaquetas de pacientes con enfermedad renal crónica demuestran una reactividad plaquetaria deficiente in vitro. BMC Nephrol. 2012, 13, 127. [Referencia cruzada] [PubMed]
34. Li, P.; Xia, C.; Liu, P.; Peng, Z.; Huang, H.; Wu, J.; He, Z. Relación de neutrófilos a linfocitos y relación de plaquetas a linfocitos en la evaluación de la inflamación en pacientes sin diálisis con enfermedad renal en etapa terminal (ESRD). BMC Nephrol. 2020, 21, 1–8. [Referencia cruzada] [PubMed]
35. Bolignano, D.; Zoccali, C. Las enfermedades renales no proteinúricas en lugar de proteinúricas son la principal causa de enfermedad renal en etapa terminal. nefrol. Marcar. Trasplante. 2017, 32, ii194–ii199. [Referencia cruzada] [PubMed]
36. Jayatilake, N.; Mendis, S.; Maheepala, P.; Mehta, FR Enfermedad renal crónica de etiología incierta: prevalencia y factores causales en un país en desarrollo. BMC Nephrol. 2013, 14, 180. [Referencia cruzada] [PubMed]
37. Redmon, JH; Elledge, MF; Womack, DS; Wickremesinghe, R.; Wanigasuriya, KP; Peiris-John, RJ; Lunyera, J.; Smith, K.; Raymer, JH; Levine, KE Perspectivas adicionales sobre la enfermedad renal crónica de etiología desconocida (CKDu) en Sri Lanka: lecciones aprendidas del estudio de prevalencia de la población de CKDu de la OMS. BMC Nephrol. 2014, 15, 125. [Referencia cruzada] [PubMed]
SH Nandana P. Gunawickrama 1, K. Imesha G. Hewavitharana 1, PG Chandra L. Nanayakkara 2 y KB Suneetha Gunawickrama 3
1 Instituto de Investigación y Educación Combinatorias Avanzadas, Universidad de Defensa General Sir John Kotelawala, Ratmalana 10390, Sri Lanka; kanchana.hewavitharana@yahoo.com
2 Departamento de Anatomía, Facultad de Medicina, Universidad de Ruhuna, Galle 80000, Sri Lanka; pgclnana@med.ruh.ac.lk
3 Departamento de Zoología, Facultad de Ciencias, Universidad de Ruhuna, Matara 81000, Sri Lanka; suneetha@zoo.ruh.ac.lk






