La supervivencia de COVID-19 y su impacto en la enfermedad renal crónica
Mar 27, 2022
ali.ma@wecistanche.com
JOSHUA D. LONG, IAN STROHBEHN, RANI SAWTELL, ROBY BHATTACHARYYA y MEGHAN E. SISE
Hasta el 87 % de los pacientes hospitalizados con enfermedad por coronavirus 2019 (COVID-19) experimentan secuelas crónicas después de la infección. El impacto a largo plazo deCOVILa D-19infección en la función renal se desconoce en gran medida en este momento de la pandemia de COVID-19. En esta revisión, destacamos la comprensión actual de la fisiopatología de la lesión renal asociada con COVID-19-y el impactoCOVID-19puede tener enfunción renal a largo plazo. COVID-19La lesión renal aguda inducida puede provocar lesión tubular, lesión endotelial y lesión glomerular. Destacamos las correlaciones histopatológicas de grandes series de autopsias y biopsias renales. Al realizar una revisión exhaustiva de la literatura publicada hasta la fecha, resumimos las tasas de recuperación de la LRA asociada a COVID-19-. Finalmente, analizamos cómo ciertas diferencias genéticas, incluidos los alelos de riesgo de APOL1 (un factor de riesgo para el colapso de la glomerulopatía), junto con las disparidades sistémicas en la atención médica, pueden conducir a una carga desproporcionada de disminución de la función renal pos-COVID-19-entre las minorías raciales y étnicas. grupos. Resaltamos la necesidad de estudios prospectivos para determinar la verdadera incidencia de la carga de enfermedad renal crónica después de COVID-19. (Investigación Traslacional 2022;241:70 82)
Abreviaturas: AKI=enfermedad renal aguda; aOR=razón de probabilidades ajustada; ATN=necrosis tubular aguda; COVAN=COVID-19-nefropatía asociada; COVID-19=enfermedad por coronavirus 2019; CKD=enfermedad renal crónica; eGFR=tasa de filtración glomerular estimada; ESKD=enfermedad renal en etapa terminal; relación HR =; MAT=microangiopatía trombótica

Haga clic para raíz de maca ginseng cistanche caballito de mar para la enfermedad renal crónica.
INTRODUCCIÓN
Al 30 de septiembre de 2021, más de 233 millones de pacientes en todo el mundo han sido infectados conSARS-CoV-2y más de 4,7 millones de personas han muerto.1 La enfermedad por coronavirus 2019 (COVID-19) es una enfermedad respiratoria que varía en gravedad desde síntomas respiratorios superiores asintomáticos o leves hasta insuficiencia respiratoria y muerte. Las manifestaciones agudas de COVID-19 han sido bien descritos y la COVID grave-19 puede causar fallas y lesiones en múltiples órganos.2-4
Recently, there has been increased coverage in the lay and scientific press about the chronic health consequences of COVID-19 in survivors. Accumulating data suggest that surviving patients may experience a wide array of persistent symptoms referred to as postacute sequelae of SARS-CoV-2 (PASC) or long COVID. Some studies suggests that symptoms of COVID-19 persist beyond 8-12 weeks in up to 25% to 50% of patients with mild COVID-19 (not requiring hospitalization) and up to 87% of patients hospitalized for COVID-19.5-7 In a large study of >1300pacientes hospitalizados con COVID-19 que sobrevivieron y fueron dados de alta con servicios de atención médica domiciliaria, solo el 40 por ciento de los pacientes fueron independientes en todas las actividades de la vida diaria por 30 días.8 La fatiga crónica es el síntoma a largo plazo más comúnmente informado, que afecta hasta 69 por ciento de los sobrevivientes.9 Los síntomas a largo plazo también pueden afectar los pulmones, lo que provoca intolerancia al ejercicio y tos crónica. Se han informado efectos neuropsiquiátricos a largo plazo en 33 a 61 por ciento de los pacientes e incluyen dolor de cabeza crónico, depresión, insomnio y deterioro de la memoria y la concentración. Las complicaciones cardiometabólicas persistentes incluyen dolor u opresión en el pecho.5 Las personas vacunadas también son susceptibles a una infección avanzada y a los efectos de una COVID prolongada; hasta el 19 por ciento de las personas con casos de avance informaron tener al menos un síntoma de COVID prolongado (pérdida del olfato, tos, fatiga, debilidad, dificultad para respirar o mialgia que persiste más de 6 semanas).10
En esta revisión, examinamos la comprensión actual de la fisiopatología de la lesión renal en pacientes infectados con COVID-19 y sus posibles efectos a largo plazo en el riñón, lo que puede promover la incidencia y la progresión de la enfermedad renal crónica (ERC) después de la COVID{{2 }}. Exploramos cómo la lesión renal aguda (AKI), así como la enfermedad renal crónica y en etapa terminal (ESKD), son factores de riesgo significativos para la mortalidad por COVID-19. Finalmente, exploramos cómo las disparidades raciales y étnicas pueden contribuir al riesgo de ERC en los sobrevivientes de COVID-19.

extracto de cistanche
EPIDEMIOLOGÍA DEL TRASTORNO RENAL AGUDO EN PACIENTES HOSPITALIZADOS CON COVID-19
La LRA es común en pacientes hospitalizados por COVID-19. Una revisión sistemática reciente y un metanálisis de 54 publicaciones que incluyeron 30 639 pacientes encontraron que la prevalencia combinada de LRA fue del 28 % (IC del 95 %, 22 %, 34 %) entre los pacientes hospitalizados y del 9 % (IC del 95 %, 7 %, 11 %) que requirieron diálisis por LRA (Etapa 3D).11 La LRA en etapa 3D es aún más común entre pacientes con COVID-19 que requieren cuidados intensivos; en un estudio multicéntrico en Estados Unidos, Gupta et al. encontró que 637 de 3,099 pacientes (21 por ciento) admitidos en cuidados intensivos requirieron terapia de reemplazo renal para AKI.12 Estudios bien diseñados antes de COVID-19 estimaron que solo el 5 por ciento de los pacientes en cuidados intensivos generalmente requieren TRR.13 Varios estudios han comparado el riesgo de LRA y necesidad de diálisis en pacientes hospitalizados con COVID-19 a pacientes hospitalizados con otras infecciones respiratorias (es decir, influenza) y encontró un riesgo sustancialmente mayor en COVID-19.14-16 Sin embargo, con el tiempo, la tasa de AKI en pacientes hospitalizados con COVID-19 parece estar disminuyendo; Charytan et al. determinaron que había una incidencia de LRA del 32,5 % en pacientes hospitalizados en la ciudad de Nueva York en marzo de 2020, que disminuyó al 17,2 % de los pacientes hospitalizados con COVID-19 en agosto de 2020.17 Dellepiane y sus colegas demostraron que las tasas de LRA en un sistema de atención médica de la ciudad de Nueva York continuó cayendo durante el otoño y el invierno de 2020.18
En cuanto a otras condiciones, la ERC preexistente es un factor de riesgo importante para AKI. Un estudio de cohorte prospectivo de 701 pacientes con COVID-19 encontró que la incidencia de LRA fue significativamente mayor en pacientes con creatinina inicial elevada que en pacientes hospitalizados con creatinina inicial normal (11,9 % frente a 4,0 %).19 Un estudio de 3993 pacientes hospitalizados en la ciudad de Nueva York encontró que la ERC era un predictor independiente de LRA grave (odds ratio ajustado [ORa] 2,8, IC del 95 por ciento: 2,1 a 3,7).20,21
Aunque AKI es una secuela adversa común de COVID-19, el público no la reconoce en gran medida. Si bien la mayoría de los estadounidenses conocen los efectos del COVID-19 comúnmente informados en los medios, como insuficiencia respiratoria aguda, neumonía y síndrome de dificultad respiratoria aguda (58 por ciento, 54 por ciento, 52 por ciento, respectivamente), una Fundación Nacional del Riñón-Harris Una encuesta realizada en mayo de 2020 encontró que solo el 17 % de los estadounidenses saben que la COVID- 19 puede causar LRA. Esto no es exclusivo de la LRA relacionada con COVID-19, ya que el conocimiento de la enfermedad renal es bajo en otros entornos, incluso entre el público lego, los trabajadores de la salud e incluso entre los pacientes que desarrollan LRA y ERC.22-25 Falta de conocimiento de los riesgos de la enfermedad renal asociada a la COVID-19-pueden obstaculizar los esfuerzos para garantizar un seguimiento posterior a la LRA adecuado para disminuir los efectos de la enfermedad renal en el individuo y la sociedad.
ENFERMEDADES RENALES AGUDAS, CRÓNICAS Y EN ETAPA TERMINAL FACTORES DE RIESGO DE MORTALIDAD POR COVID-19
La CKD y la ESKD preexistentes se encuentran entre los predictores más reproducibles y sólidos de enfermedades graves y críticas en pacientes con COVID-19. Un estudio de cohorte prospectivo de 701 pacientes hospitalizados con COVID-19 mostró que los pacientes con enfermedad renal tenían un riesgo de 2 a 4-veces mayor de muerte en el hospital, según cómo se defina la enfermedad renal. La proteinuria y la hematuria de cualquier grado, el nitrógeno ureico en sangre elevado al inicio, la creatinina sérica elevada y el AKI mayor que el estadio 2 (! 2-veces de aumento desde el inicio) se asociaron con muerte hospitalaria después del ajuste por edad, sexo y gravedad de la enfermedad. al ingreso, comorbilidades y recuento de linfocitos.19 Chan et al. encontraron una tasa de mortalidad del 50 por ciento entre pacientes con AKI, en comparación con el 8 por ciento en pacientes sin AKI.26 Gupta et al. encontraron que los pacientes críticamente enfermos que requieren terapia de reemplazo renal para AKI tenía una tasa de mortalidad del 55 por ciento.27 Entre los pacientes en estado crítico que requieren ventilación mecánica y diálisis, las tasas de mortalidad superan el 70 por ciento.28
Un metanálisis realizado en 2020 de cuatro estudios que incluyeron 1389 pacientes únicos encontró una asociación significativa entre la ERC y la COVID grave-19[OR 3,03 (95 % IC 1,09 8,47), I2=0. 0 por ciento, Q de Cochran, P=0.84], a pesar de que ninguno de los estudios encontró esta asociación individualmente.29 Un metanálisis separado con datos de 9 estudios encontró que la ERC se asoció con un mayor riesgo de mortalidad ( RR no ajustado 3,25 [1,13 a 9,28]).30 El estudio OPEN-SAFELY analizó aproximadamente 17 millones de adultos en Inglaterra desde el 1 de febrero de 2020 hasta el 6 de mayo de 2020 y descubrió que<30 were="" associated="" with="" a="" 1.33="" and="" 2.52="" increased="" risk="" of="" mortality="" from="" covid-19="" in="" fully="" adjusted="">
Los factores logísticos involucrados en cómo los pacientes con CKD y ESKD accedieron a la atención pueden haber colocado a estos pacientes en mayor riesgo de contraer COVID-19 durante la primera ola de la pandemia. Los pacientes con ESKD no pudieron ponerse en cuarentena debido a su necesidad de diálisis y problemas de salud frecuentes. interacciones de cuidado. Según un proveedor de diálisis nacional mediano, en clínicas con al menos 1 caso de COVID-19durante los primeros 3 meses de la pandemia en los Estados Unidos, el 5,5 % de todos los pacientes en esas clínicas se infectaron.32 La gravedad fue muy alta en la población de diálisis también: un estudio de cohorte retrospectivo de 7,533 pacientes con ESKD que recibieron diálisis en California encontró que entre sus 133 pacientes infectados con COVID-19 en diálisis, el 57 por ciento de la hospitalización requerida.33 Según la literatura existente, las tasas de mortalidad en pacientes con ESKD que fueron hospitalizados por COVID-19 han oscilado entre el 21 por ciento y el 32 por ciento.33-37 El riesgo de mortalidad entre los pacientes en diálisis que ingresaron en la unidad de cuidados intensivos debido a COVID-19 supera el 50 por ciento.38
Finalmente, los pacientes con CKD y ESKD pueden tener menos probabilidades de ser elegibles para tratamientos o ensayos de COVID-19. Remdesivir, la única terapia antiviral actualmente aprobada para pacientes hospitalizados en los Estados Unidos, no se estudió inicialmente en pacientes con eGFR < 30="" ml/="" min/1,73m2="" debido="" a="" preocupaciones="" sobre="" la="" acumulación="" del="" fármaco,="" su="" metabolito="" activo="" y="" su="" transportador="" de="" ciclodextrina.39="" sin="" embargo,="" múltiples="" series="" de="" casos="" pequeños="" han="" sugerido="" que="" remdesivir="" puede="" ser="" seguro="" en="" pacientes="" con="" egfr="">< 30="" ml/min/1,73m2="" o="" en="" diálisis="" .40-42="" un="" análisis="" post="" hoc="" de="" los="" datos="" de="" los="" ensayos="" clínicos="" mostró="" que="" los="" pacientes="" tratados="" con="" remdesivir="" tenían="" menos="" deterioro="" de="" la="" función="" renal;="" el="" 30="" %="" de="" los="" pacientes="" que="" recibieron="" placebo="" experimentaron="" una="" disminución="" en="" la="" depuración="" de="" creatinina,="" mientras="" que="" solo="" el="" 15="" %="" de="" los="" pacientes="" en="" un="" curso="" de="" remdesivir="" de="" 5-días="" experimentaron="" una="" disminución="" en="" la="" depuración="" de="" creatinina.43="" estudios="" que="" resumen="" los="" criterios="" de="" inclusión="" y="" exclusión="" de="" ensayos="" clínicos="" de="" tratamientos="" para="" la="" covid{{15}="" }="" han="" observado="" que="" la="" enfermedad="" renal="" es="" un="" criterio="" de="" exclusión="" en="" aproximadamente="" la="" mitad="" de="" los="" ensayos.44,45="" por="" lo="" tanto,="" además="" de="" tener="" un="" alto="" riesgo="" de="" malos="" resultados,="" hay="" una="" falta="" de="" evidencia="" adecuada="" para="" informar="" las="" decisiones="" de="" tratamiento="" en="" este="" grupo="" de="" pacientes="" de="" alto="">
Es probable que exista una relación bidireccional entre la COVID-19 y la ERC: la ERC aumenta el riesgo de sufrir una COVID grave-19 y una mayor gravedad de la COVID-19 conduce a un mayor riesgo de disfunción renal aguda y crónica. Los pacientes con una alta carga de comorbilidades crónicas y fragilidad, y los pacientes inmunodeprimidos, tienen un mayor riesgo tanto de ERC progresiva como de COVID grave-19.
ERC INCIDENTE Y PROGRESIVA COMO COMPLICACIÓN A LARGO PLAZO DEL COVID-19
Aunque el riesgo de AKI ha sido bien caracterizado; se desconoce la secuela a más largo plazo de COVID-19 en la función renal.46 Un estudio que utilizó registros de salud electrónicos de la Administración de Salud de Veteranos para realizar una evaluación de alta dimensión de COVID prolongado informó un mayor riesgo de manifestaciones renales adversas, que incluyen AKI, CKD y infecciones del sistema urinario que ocurrieron incluso después de los primeros 30 días posteriores al diagnóstico de COVID-19.47 Los mecanismos potenciales que impulsan la progresión de la ERC después de COVID-19 se pueden agrupar en gran medida en tres categorías: lesión tubular no resuelta, lesión micro o macrovascular, o podocitopatía/ glomerulopatía colapsante (Fig. 1).
Lesión tubular no resuelta que contribuye al riesgo de ERC.
Los posibles efectos virales directos en el riñón del SARS-CoV-2 incluyen daño endotelial por entrada viral y activación del complemento, inflamación local/liberación de citoquinas y glomerulopatía colapsante. Los efectos indirectos de la COVID-19 que pueden provocar LRA incluyen depleción de volumen, hipotensión/shock, rabdomiólisis, así como las causas comunes de LRA intrahospitalaria, como exposición a nefrotoxinas y sepsis.46 Una serie de autopsias tempranas de pacientes que fallecieron debido a COVID-19 en China encontró una lesión tubular aguda que varió de leve a grave en los 26 pacientes estudiados.48 La primera serie de autopsias en los Estados Unidos también encontró que la lesión tubular aguda fue el hallazgo más prominente en la microscopía óptica.49 Dado el potencial de LRA grave, el riesgo de ERC por necrosis tubular aguda (NTA) no resuelta puede afectar a un número significativo de pacientes con COVID grave-19 que sobreviven hasta el alta hospitalaria.
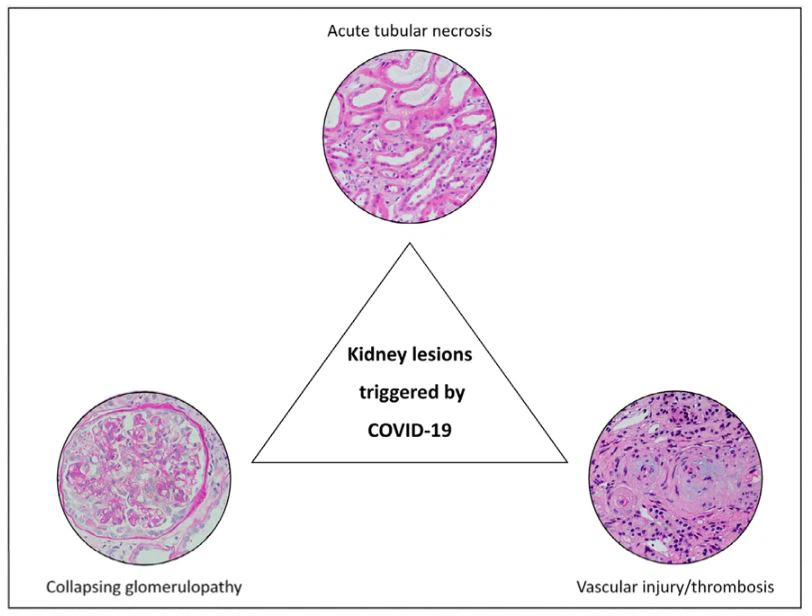
Figura 1.Hallazgos patológicos en la lesión renal aguda asociada a COVID-19.
Lo más probable es que la lesión tubular aguda sea causada por una respuesta local y sistémica a la COVID-19 que puede provocar hipotensión, activación del sistema renina angiotensina, lesión endotelial, activación de las vías de coagulación y lesión mitocondrial.49-51 Liberación local de citoquinas en respuesta a los patrones moleculares asociados al daño y asociados al patrón conduce al reclutamiento de células inflamatorias y al daño tisular. Las trampas extracelulares de neutrófilos liberadas por los neutrófilos activados tienen un papel importante en el aclaramiento viral, pero también contribuyen a la inflamación local, la inmunotrombosis y el daño tisular.52 Además, existen alteraciones hemodinámicas no específicas que conducen a la LRA en la COVID-19. La deshidratación por ingesta oral deficiente y las manifestaciones gastrointestinales pueden activar el sistema renina-angiotensina y alterar la perfusión renal. También existe una carga sustancial de LRA adquirida en el hospital; los pacientes con COVID grave-19 suelen estar expuestos a medicamentos nefrotóxicos y aquellos que se enferman críticamente pueden desarrollar shock, gasto cardíaco bajo, hipoxia e hipotensión.
La rabdomiolisis es una consecuencia rara pero informada de COVID{{0}} que también puede conducir a una lesión tubular aguda a través de la precipitación de mioglobina y la liberación de radicales libres.53May et al. encontró que 8 de 240 (3,3 por ciento) de las biopsias de riñón nativo realizadas en pacientes con COVID-19 tenían nefropatía por cilindros de mioglobina, que se elevó significativamente en comparación con el 0,1 por ciento de incidencia de nefropatía por cilindros de mioglobina en su base de datos de biopsias que consta de 63 575 controles.54 Se desconoce la probabilidad de recuperación de LRA en pacientes con nefropatía por cilindros de mioglobina.
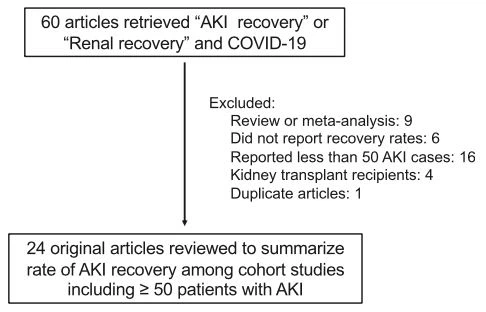
Figura 2.Identificación de artículos que informan tasas de recuperación de LRA en pacientes hospitalizados con COVID grave-19
To summarize the available literature reporting AKI recovery in patientst hospitalized with COVID-1, we performed a literature review using the natural library of medicine. Using the search terms "AKI recovery" or "Renal recovery" and "COVID-1900 we identified 60 articles. After the exclusions shown in Fig 2, we identified 24 unique cohort studies with ! 50 cases of hospi- talized patients with COVID-19-related AKI that reported AKI recovery rates (Table I).12,14,16,17,20,55-73Although "full recovery" is variably defined in these studies, the proportion of surviving patients that experience a full recovery by hospital discharge ranges between 19% to 79%, with the majority of studies reporting that that >El 50 por ciento de los sobrevivientes experimentan una "recuperación renal" al momento del alta hospitalaria.16,20,56 Entre aquellos con AKI lo suficientemente grave como para requerir TRS, la mayoría de los sobrevivientes pueden suspender la TRR antes del alta hospitalaria, con una dependencia continua de la TRR en el momento del alta hospitalaria que varía del 8 al 34 por ciento. porcentaje de pacientes sobrevivientes (Tabla I).12,20,55,58,59 Aunque solo una pequeña cantidad de publicaciones brindan seguimiento de la función renal posterior al alta, la literatura disponible sugiere que entre los días que sobreviven 30-90, las tasas de recuperación renal son muy alto, que va del 75 al 91 por ciento.14,56,57 Un estudio de cohorte prospectivo y no controlado siguió a 95 pacientes con AKI que sobrevivieron 4 meses y encontró que la ERC de nueva aparición se había desarrollado en solo 2 pacientes (2.1 por ciento);69 esto sugiere que la gran la mayoría de los pacientes con LRA inducida por COVID-19 que sobrevivan recuperarán la función renal.
Sin embargo, es importante tener en cuenta que el nivel de creatinina sérica es un marcador insensible del daño renal; y las estimaciones de recuperación deben tener en cuenta que los pacientes a menudo pierden masa muscular durante el curso de una enfermedad crítica, lo que puede hacer que las estimaciones de TFGe basadas en creatinina sean menos confiables.69 Aunque en muchos pacientes, la creatinina sérica vuelve a niveles casi normales después de la LRA, es posible que los riñones no se recuperen por completo y se necesitan estudios con un seguimiento más prolongado.
Encontrar las poblaciones apropiadas para comparar las tasas de recuperación de LRA y la disminución de eGFR después de la hospitalización es un desafío. Un estudio de cohortes de 182 pacientes hospitalizados con LRA asociada a COVID-19 encontró una mayor tasa de disminución de la TFGe posterior a la hospitalización en comparación con 1430 pacientes hospitalizados con LRA no asociada a COVID-19, incluso después de ajustar por comorbilidades y gravedad de la LRA.74 en contraste, dos estudios que compararon los resultados de LRA en pacientes con COVID-19 con pacientes hospitalizados con influenza encontraron tasas muy similares de recuperación a mediano y largo plazo y disminución de eGFR.14,16 En particular, la mayoría de los estudios observacionales de recuperación de LRA tienen tasas muy altas de pérdida durante el seguimiento; por lo tanto, para comprender la carga de la ERC y la disminución de la TFGe, se necesitan estudios prospectivos que incluyan la evaluación de biomarcadores en sangre y orina.
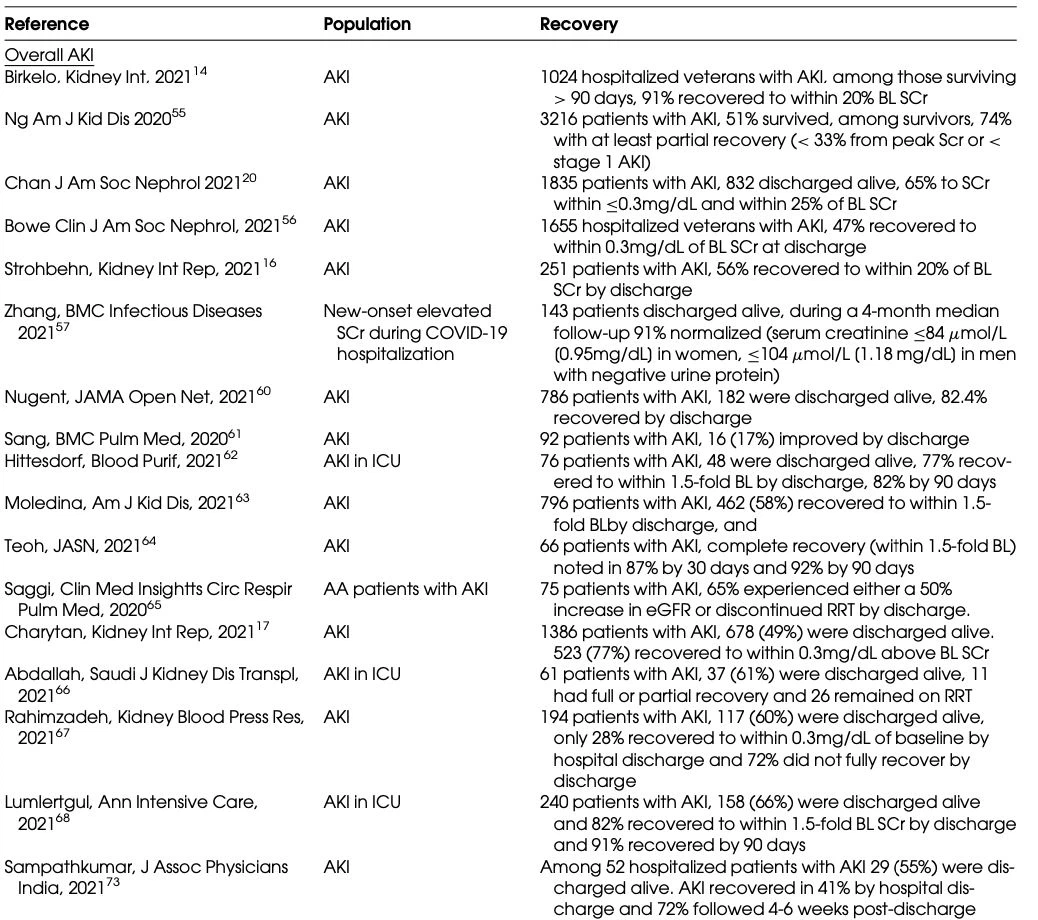
Tabla I.Recuperación de LRA en LRA asociada a COVID-19.
Lesión micro o macrovascular/activación endotelial que contribuye al riesgo de ERC.
Los primeros informes de autopsia sugirieron que la lesión microvascular puede ocurrir en múltiples órganos, con una lesión pulmonar endotelial prominente demostrada en las autopsias. ) identificados por biopsia renal y autopsia de pacientes hospitalizados con COVID-19.76-81 Sin embargo, May et al. revisaron 240 biopsias de riñón nativo y encontraron que solo el 3.3 por ciento tenía evidencia de MAT, que no estaba significativamente elevada en comparación con el cohorte de control de biopsia renal no infectada con COVID-19.54
La trombocitopenia, la LDH elevada y el dímero D son comunes en la COVID-19 y pueden ser una característica de la coagulación intravascular diseminada. A nivel celular, se ha postulado que la activación plaquetaria puede ser parte de la etiología del estado protrombótico que se observa en la COVID-19, ya que el SARS-CoV-2 puede unirse a las plaquetas a través de la enzima convertidora de angiotensina 2 , activando las plaquetas.82 La COVID grave-19 puede provocar el síndrome de liberación de citoquinas, la activación de macrófagos y la liberación de moléculas de patrones moleculares asociadas a patógenos y asociadas a daños que conducen a la liberación de factor tisular y la activación de factores de coagulación.83 La activación del complemento también puede regular al alza factor tisular y conducen a la pérdida de trombomodulina que promueve la hipercoagulabilidad.53,84 La evidencia emergente sugiere que la formación excesiva de trampas extracelulares de neutrófilos juega un papel importante en la fisiopatología de la lesión endotelial y la inmunotrombosis que caracterizan los casos graves de COVID-19.52,{{18} } La disfunción endotelial desencadenada por COVID-19puede exacerbar las enfermedades crónicas subyacentes que están asociadas con la disfunción endotelial crónica y son importantes causas de la ERC, como la hipertensión, la diabetes y la aterosclerosis.
La trombosis macrovascular también puede ocurrir en COVID-19. Se han documentado embolias pulmonares, accidentes cerebrovasculares, trombosis del ventrículo derecho, trombosis aórtica y eventos macrovasculares relacionados con el riñón en pacientes con COVID-19.88 Se han documentado tanto la trombosis de la arteria renal como la trombosis de la vena renal, incluidos casos con infarto renal asociado; sin embargo, es probable que estos sean eventos raros.88-92
Glomerulopatía colapsante y podocitopatía que contribuyen al riesgo de ERC.
La glomerulopatía colapsante es una complicación bien documentada de las infecciones virales, más comúnmente la infección por el virus de la inmunodeficiencia humana (VIH), el virus de Epstein-Barr, el citomegalovirus y el parvovirus B19.93 Recientemente, se informó que la infección por el SARS-CoV-2 puede ser una "golpe viral" adicional que puede causar glomerulopatía colapsante.94
La glomerulopatía colapsante se caracteriza por el colapso global o segmentario del penacho glomerular con hipertrofia e hiperplasia de los podocitos suprayacentes.95-98La glomerulopatía colapsante se asocia con variantes genéticas APOL1 de alto riesgo (G1/G1, G2/G2 o G1/G2 ).La gran mayoría de los casos documentados de glomerulopatía colapsante asociada a COVID-19se han notificado en pacientes de ascendencia africana occidental o afroamericana. Se estima que del 10 al 15 por ciento de las personas afroamericanas tienen dos alelos APOL1 de alto riesgo, lo que sugiere que una gran proporción de la población negra de EE. UU. puede estar en riesgo de sufrir una glomerulopatía colapsante.99 May et al. informó que de 44 de 48 (92 por ciento) de los pacientes con glomerulopatía colapsante asociada a COVID-19- tenían genotipos APOL1 de alto riesgo.54
Los casos de glomerulopatía colapsante asociada a COVID-19 generalmente se presentan con LRA, proteinuria intensa e hipoalbuminemia.95,100-105 También se encuentra lesión tubular aguda en la gran mayoría de los casos de glomerulopatía colapsante asociada a COVID-19 .54 La glomerulopatía colapsante asociada a COVID-19puede ocurrir en pacientes con síntomas respiratorios leves, lo que sugiere que, a diferencia de la NTA o la rabdomiolisis asociadas a COVID, el riesgo de glomerulopatía colapsante asociada a COVID-19 no está directamente relacionado con la gravedad de los síntomas respiratorios relacionados al COVID-19.95
Algunos pacientes se han presentado con cambios mínimos en la enfermedad o glomeruloesclerosis focal y segmentaria sin características de colapso en la biopsia, lo que sugiere que puede haber un espectro de podocitopatía que afecta a los pacientes con COVID-19. Mayo et al. realizó la tipificación del genotipo APOL1 en pacientes negros o hispanos que desarrollaron otras formas de glomeruloesclerosis segmentaria focal o enfermedad de cambios mínimos y encontró que 8 de 11 (72.7 por ciento) tenían genotipos APOL1 de alto riesgo, lo que sugiere que tal vez haya un espectro de enfermedad renal relacionada con APOL1 provocada por COVID{ {9}}.54 Es probable que los casos de glomerulopatía colapsante y podocitopatía asociados con COVID-19 informados en la literatura representen un fenotipo grave de esta enfermedad. Se necesitan estudios prospectivos para determinar la incidencia de proteinuria tras la COVID-19. Además, debido a que la glomerulopatía colapsante puede ocurrir en pacientes con COVID leve-19, incluso los pacientes que no requieren atención médica pueden correr el riesgo de desarrollar una glomerulopatía colapsante manifiesta o subclínica que solo puede detectarse mediante pruebas de laboratorio incidentales meses o años después de la infección. Esta es una consideración particularmente importante dada la alta prevalencia de genotipos APOL1 de alto riesgo entre los afroamericanos.99
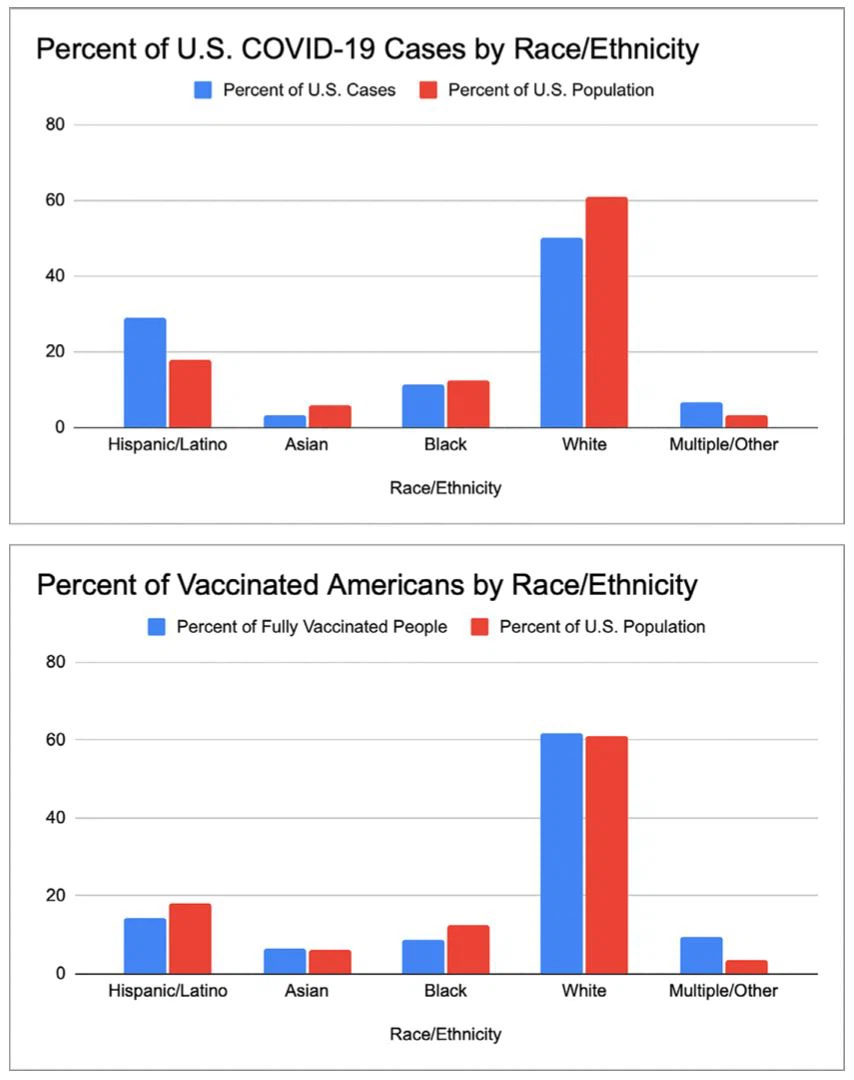
Fig. 3.Tasa de infección por COVID-19 entre grupos raciales ygrupos étnicos en la población estadounidense
No se ha dilucidado el mecanismo exacto por el cual la infección por SARS-CoV-2 conduce a una glomerulopatía colapsante. Las vías antivirales, en particular la regulación al alza del interferongamma, pueden ser importantes inductores de la enfermedad renal en personas con el genotipo APOL1 de alto riesgo. Hassler y sus colegas resumieron bien la evidencia a favor y en contra de la infección viral directa.108 En su revisión de los estudios hasta la fecha, al menos uno de los métodos utilizados (inmunohistoquímica, RT -PCR, o hibridación in situ) en riñones de 102 de 235 pacientes que se sometieron a biopsia (43 por ciento).108 La serie más grande de biopsias renales de May et al. no pudo confirmar el ARN del SARS-CoV-2 mediante hibridación in situ.54 Sigue habiendo incertidumbre, con la necesidad de obtener más datos de biopsias renales, particularmente en etapas más tempranas del curso de la enfermedad. Sin embargo, incluso sin invasión directa, los cambios inducidos por el virus en el microambiente los podocitos que rodean (aumento de la producción de citocinas) pueden desencadenar una glomerulopatía colapsante.98 Los alelos de riesgo de APOL1 también pueden desempeñar un papel mecánico: las infecciones virales estimulan la producción de interferón en el huésped, lo que estimula la expresión del gen APOL1, lo que podría exacerbar los efectos nocivos del polimorfismo APOL1 en la función renal y conducir a una glomerulopatía colapsante.109
Mayo et al. buscó determinar si la glomerulopatía colapsante asociada a COVID-19 se enriqueció en pacientes con COVID-19 mediante la realización de un estudio multicéntrico que comparó 240 biopsias de riñón nativo obtenidas en pacientes infectados con COVID-19 con un {{5} }año de la base de datos de patología renal de EE. UU. como control.54 Descubrieron que la glomerulopatía colapsante ocurrió en el 25,8 % de los casos de COVID-19 en comparación con el 1,8 % en la base de datos general de 5-años y el 28 % de los pacientes con VIH. Este estudio destaca la importancia de la evaluación comparativa frente a los pacientes de control. También es posible que algunas patologías renales se desarrollen al azar y simultáneamente con COVID-19, lo cual es difícil de saber cuando se basa en informes de casos y series de casos que pueden sufrir sesgo de publicación. Se necesitarán estudios prospectivos con controles cuidadosamente emparejados para estimar el riesgo de proteinuria y enfermedad glomerular de nueva aparición después de COVID-19.
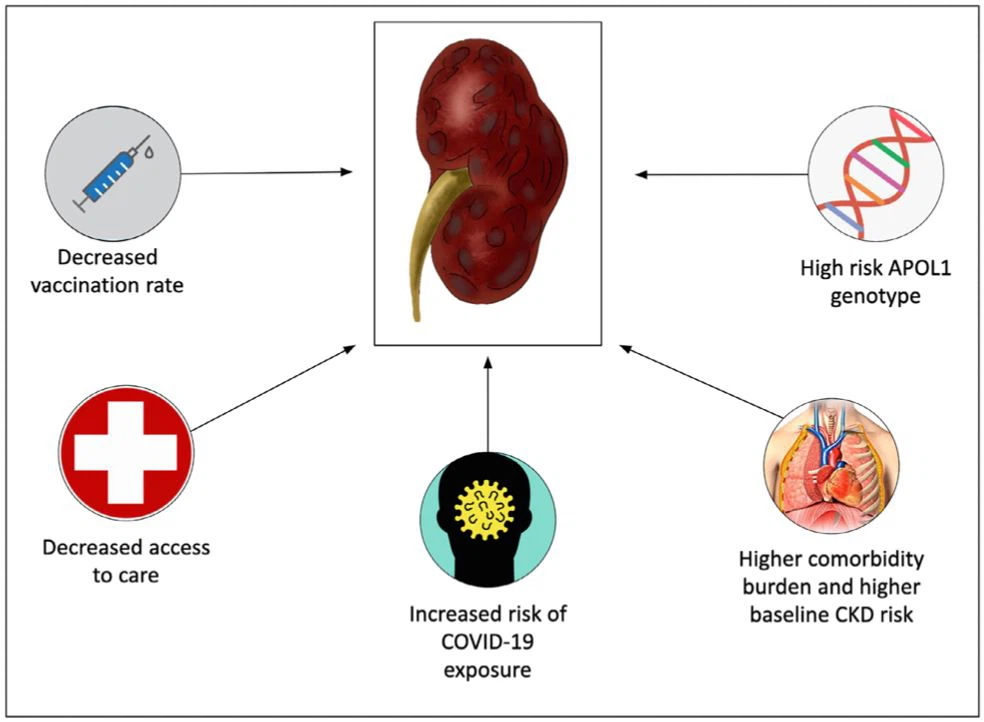
Figura 4.Factores que contribuyen a un mayor riesgo de resultados renales adversos entre las minorías raciales y étnicas.
LAS DISPARIDADES RACIALES Y ÉTNICAS Y EL RIESGO DE CKD DESPUÉS DEL COVID-19
COVID-19 ha afectado de manera desproporcionada a las poblaciones de minorías raciales y étnicas en términos de tasas generales de infección y mortalidad por enfermedad. Los pacientes afroamericanos y latinos tienen más probabilidades que los pacientes blancos de dar positivo por COVID-19.110 A partir de junio de 2021, los CDC informaron que el 28.8 por ciento de los casos de COVID-19 en los EE. UU. ocurrieron en personas hispanas o latinas, a pesar de que solo representan 18.5 por ciento de la población. La figura 3A muestra el desglose de los casos de COVID-19 en los EE. UU., así como el desglose de la población general de los EE. UU.111 Entre los pacientes hospitalizados, los pacientes negros tenían menos probabilidades que los pacientes blancos de enfermarse gravemente o morir; sin embargo, los pacientes negros tenían una tasa de mortalidad por COVID-19 fuera del hospital más alta, y la tasa de mortalidad general en los estadounidenses negros es más del doble de la tasa de mortalidad por COVID-19 en los estadounidenses blancos.110,112La enfermedad de células falciformes, que afecta principalmente a personas de ascendencia africana, también puede ser un factor de riesgo de hospitalización y muerte por COVID-19.112,113 La enfermedad renal asociada con COVID-19parece estar afectando a los negros de manera desproporcionada; en el estudio de May et al. Los pacientes negros se vieron afectados de manera desproporcionada, lo que representa el 44,6 % de las 240 biopsias renales nativas de COVID-19, en comparación con el 15,4 % de los pacientes en la base de datos de biopsias de EE. UU. que sirvió como control.
Las disparidades en la atención posthospitalaria también pueden afectar el riesgo de ERC. Se recomienda que los pacientes con LRA (incluida la LRA asociada a la COVID{{1}) reciban atención poshospitalaria con un nefrólogo para garantizar la resolución de la LRA, optimizar la presión arterial y minimizar la exposición a posibles nefrotoxinas. Existen disparidades bien documentadas en la atención posterior a la hospitalización en poblaciones minoritarias, por lo que las disparidades en el acceso a la atención de subespecialidades y el seguimiento posterior a la hospitalización pueden contribuir a la carga de ERC que enfrentan los miembros de grupos minoritarios raciales y étnicos afectados por COVID-19 .114La mayoría de los beneficiarios de Medicaid son afroamericanos o latinos; En general, los beneficiarios de Medicaid tienen menos probabilidades de ser transferidos a un centro de atención a largo plazo o de enfermería especializada después de estar en la unidad de cuidados intensivos. vida diaria después de una enfermedad crítica.115-117 Los pacientes negros y latinos que son dados de alta en un centro de enfermería especializada a menudo van a centros con tasas más altas de reingreso y tasas más bajas de alta exitosa en la comunidad.118 Para minimizar el riesgo de ERC después de la LRA relacionada con COVID-19-, es fundamental garantizar que los pacientes tengan acceso a atención post-aguda y nefrología cuando esté clínicamente indicado.
Las disparidades también se manifiestan en las tasas diferenciales de vacunación contra el COVID-19. Al 20 de junio de 2021, los CDC informaron que de los 92 millones de personas vacunadas en los Estados Unidos, el 8,7 % eran negros y el 14,1 % latinos, a pesar de que estos grupos representan el 12,5 % y el 18,5 % de la población de los EE. UU., respectivamente (Fig. 3B).111
Los médicos y el público deben ser conscientes de que la confluencia de factores biológicos, sociales y económicos, así como el racismo sistémico e institucional, pueden conducir a una mayor carga de ERC en pacientes de poblaciones de minorías raciales y étnicas que desarrollan COVID-19 (Fig. 4).

Cistanche tratar la enfermedad renal.
Para obtener más información, haga clic en la imagen.
CONCLUSIÓN Y DIRECCIONES FUTURAS
La lesión renal es un resultado adverso importante y común de la COVID-19. Tanto AKI como CKD están asociados con COVID-19 grave y riesgo de muerte. COVID-19 puede provocar ERC en los sobrevivientes a través de una lesión tubular aguda no resuelta que ocurre en pacientes con enfermedad grave; como resultado de la podocitopatía, que se ha relacionado fuertemente con los genotipos APOL1 de alto riesgo; o por causar lesión endotelial o vascular, que promueve la progresión de la ERC. Aunque varios estudios sugieren que las tasas de LRA en COVID-19 pueden ser más altas que los controles emparejados y la recuperación al alta hospitalaria puede ser más baja que los controles emparejados, la recuperación de LRA a medio y largo plazo parece ser alta entre los pacientes que son seguidos después del alta hospitalaria. La verdadera carga de la ERC después de la COVID-19 aún no se ha determinado con precisión, y estamos limitados a la hora de estimar el riesgo de ERC a partir de conjuntos de datos de observación debido a las altas tasas de pérdida durante el seguimiento. Son necesarios estudios prospectivos que midan longitudinalmente la función renal y la proteinuria. Con suerte, esto se abordará a través de los estudios de cohortes Researching COVID to Enhance Recovery (RECOVER) y otros estudios prospectivos planificados.119






