Secretoma de células madre mesenquimales dentales: un enfoque intrigante para la neuroprotección y la neuroregeneración, parte 2
Aug 14, 2024
Es importante señalar que la edad del donante y las condiciones microambientales in vitro también pueden influir en la composición del secretoma. Se informó que la DPSC-CM obtenida en condiciones normóxicas estaba enriquecida en moléculas con propiedades antiinflamatorias, reparadoras de tejidos y regenerativas en comparación con la CM obtenida en condiciones hipóxicas [44].
En el aprendizaje, la memoria y la cognición humanos, el microambiente in vitro juega un papel vital. Vivir en un buen microambiente in vitro puede ayudarnos a mantener mejor la memoria, mejorar los efectos del aprendizaje y promover la salud física en general.
En primer lugar, un buen microambiente in vitro puede promover la formación y el mantenimiento de conexiones neuronales. Las neuronas son un tipo de células del cerebro que se encargan de transmitir señales y formar recuerdos. Cuando aprendemos cosas nuevas, las conexiones entre las neuronas seguirán fortaleciéndose, lo que ayuda a la formación de nuevos recuerdos. Un buen ambiente puede ayudar a que las conexiones neuronales se mantengan estables sin verse perturbadas.
En segundo lugar, el microambiente in vitro puede afectar el metabolismo y la función de las células cerebrales. Una cantidad suficiente de oxígeno, nutrición y agua puede mejorar el nivel metabólico de las células cerebrales, evitar la muerte y el envejecimiento de las células cerebrales y, por tanto, beneficiar el desarrollo de la memoria y las capacidades cognitivas. Al mismo tiempo, un ambiente tranquilo o moderadamente cómodo puede ayudar a las personas a concentrarse y promover la mejora del aprendizaje y la eficiencia laboral.
Además, un entorno in vitro saludable también tiene un impacto positivo en otros aspectos de la salud física. Los esfuerzos en aspectos como el sueño adecuado, la elección de una dieta saludable y el ejercicio moderado pueden mejorar la memoria y la capacidad cognitiva. Un estilo de vida saludable que integre cuerpo y mente puede reducir las emociones negativas como la ansiedad, la depresión y el estrés, ayudando así a mejorar la eficiencia del trabajo del cerebro y la vitalidad del pensamiento.
En resumen, existe una conexión inseparable entre el microambiente in vitro y la memoria. Un entorno optimizado puede ayudar a fortalecer la conexión entre las neuronas y mejorar la función metabólica de las células cerebrales, favoreciendo así la formación y el mantenimiento de la memoria, y también es garantía de salud física y mental. Trabajemos juntos para construir un ambiente in vitro saludable y positivo para hacer mejores contribuciones a nuestra salud y éxito. Hombre Naranja:
Se puede ver que necesitamos mejorar la memoria, y Cistanche puede mejorar significativamente la memoria, porque
Cistanche es un material medicinal tradicional chino con muchos efectos únicos, uno de los cuales es mejorar la memoria. La eficacia de Cistanche proviene de los diversos ingredientes activos que contiene, incluidos ácido tánico, polisacáridos, glucósidos flavonoides, etc. Estos ingredientes pueden promover la salud del cerebro de muchas maneras.

Haz clic en conocer 10 formas de mejorar la memoria
Además, el secretoma recolectado de DPSC cultivadas con O2 al 5% mostró mayores efectos estimulantes sobre la proliferación y migración de células NIH3T3 de fibroblastos embrionarios de ratón y la diferenciación neuronal de células SH-SY5Y [45].
La cantidad y el tamaño de EXO y su expresión de tetraspanina pueden variar según el medio utilizado para el cultivo [46]. El secretoma de SHED y DPSC jóvenes contenía más factores de crecimiento y niveles más bajos de citocinas proinflamatorias en comparación con las DPSC obtenidas de sujetos mayores.
El potencial de diferenciación también fue mayor en SHED y DPSC jóvenes [47].
La CM puede ser obtenida por PDLSC sanos pero también por PDLSC inflamados. Los CM obtenidos por los inflamados aumentaron la proliferación de PDLSC tanto sanos como inflamados, pero redujeron la diferenciación hacia los osteoblastos. La CM sana rescató la diferenciación osteogénica deteriorada [48].
El tratamiento con diferentes sustancias también puede influir en el secretoma celular. El tratamiento de las DPSC con 2,3,5,40-tetrahidroxiestilbeno-2-O- -D-glucósido (THSG), un componente bioactivo de Polygonum multiflorum Thunb., indujo cambios en la secreción de proteínas asociadas al crecimiento en CM, aumentando algunas de ellas como AKT2 y el receptor de NGF [49].
En cambio, CM de GMSC modificadas con FGF-2-contenía más VEGF-A, FGF-2 y TGF-[50]. El tratamiento con ácido ascórbico de las SHED aumentó la liberación de factores de crecimiento necesarios para la regeneración y la homeostasis de los tejidos, incluidos VEGF, SCF, IGF-1, HGF, bFGF, Ang-1 y EGF, y citocinas antiinflamatorias, como como NO, indolamina 2,3-dioxigenasa (IDO), PGE-2, IL-10 e IL-6.
Por el contrario, las citoquinas inflamatorias CCL2 y TGF- 1 se redujeron [51].
La exposición al medio de diferenciación también podría inducir cambios en el ARN no codificante de los EV y EXO de los PDLSC.
Específicamente, se encontraron entre 69 y 557 ARN circulares (circRNA) y entre 2907 y 11,581 lncRNA en vehículos eléctricos aislados de PDLSC y PDLSC expuestos a un medio de diferenciación osteogénica en diferentes momentos.
En comparación con los PDLSCsEV indiferenciados, 3 circRNA y 2 lncRNA estaban regulados positivamente y 39 circRNA y 5 lncRNA estaban regulados negativamente de manera constante después de 5 y 7 días de exposición al medio de diferenciación [52].
Además, 72 miARN estaban regulados positivamente mientras que 35 estaban regulados negativamente en PDLSC EXO después de la inducción osteogénica [53]. En la Tabla 1 se puede encontrar un resumen de los principales factores encontrados en el secretoma de las diferentes MSC dentales.
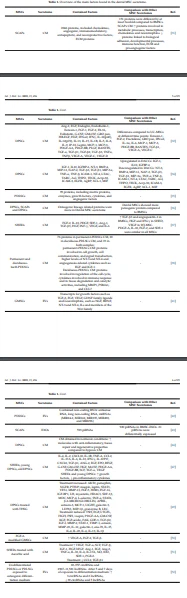
Ang, angiopoyetina; BDNF, factor neurotrófico derivado del cerebro; BMP, proteína morfogenética ósea; BMSC, MSC de médula ósea; circARN, ARN circular; CM, medio condicionado; CUL7, selección 7; CXCL, quimiocineligando con motivo CXC; DACC, que desarrollan células complejas apicales; DFSC, células madre del folículo dental; DPSC, células madre de la pulpa dental; ECM, matriz extracelular; EGF, factor de crecimiento epidérmico; ECM, matriz extracelular; VE, vesículas extracelulares; EXO, exosomas; FGF, factor de crecimiento de fibroblastos; G-CSF, factor estimulante de colonias de granulocitos; GDNF, factor neurotrófico derivado de células gliales; GM-CSF, factor estimulante de colonias de granulocitos y macrófagos; GMSC, MSC gingivales; HGF, factor de crecimiento de hepatocitos; ICAM, Molécula de Adhesión Intercelular; IDO, indolamina2,3-dioxigenasa; IFN, interferón; IGF, factor de crecimiento similar a la insulina; IL, interleuquina; lncRNA, ARN largo no codificante; MCP, proteína quimioatrayente de monocitos; miARN, microARN; MMP, metaloproteinasa de matriz; NGF, factor de crecimiento nervioso; NT, neurotrofina; PDGF, factor de crecimiento derivado de plaquetas; PDLSC, células madre del ligamento periodontal; piRNA, ARN que interactúan con PIWI; PSMA1, subunidad del proteasoma, tipo alfa; SCAP, células madre de la papila apical; SDF, factor derivado de células estromales; SHED, células madre de dientes de leche humanos exfoliados; TGF, factor de crecimiento transformante; THSG, 2,3,5,40-tetrahidroxiestilbeno-2-O- -D-glucósido; TIMP, inhibidor tisular de la metaloproteinasa; TNF, factor de necrosis tumoral; UC-MSC, células madre mesenquimales del cordón umbilical; VEGF, factor de crecimiento endotelial vascular ↑, aumento/mejoras; ↓, reducción.

3. Potencial neuroprotector y neuroregenerador del secretoma de células madre dentales en modelos preclínicos
Para evaluar el potencial neurodegenerativo y neuroprotector del secretoma dental de MSC, se han evaluado los efectos de CM y EV en modelos preclínicos de enfermedades neurodegenerativas y neurológicas y modelos de daño neuronal, como la lesión de la médula espinal (LME).
Además, también se han evaluado los efectos mediados por el secretoma sobre el crecimiento neuronal, su capacidad para estimular la diferenciación neuronal y sus efectos sobre las células gliales.
Realizamos una búsqueda en PubMed en busca de estudios que muestren el potencial neurodegenerativo y neuroprotector del secretoma de MSC dentales en modelos in vitro e in vivo.
3.1. Secretoma de células madre de pulpa dental
El secretoma de DPSC fue uno de los más estudiados. Diferentes estudios evaluaron su eficacia para inducir el crecimiento de neuritas. Se informó que DPSC-CM promovió el crecimiento de neuritas en las neuronas del ganglio de la raíz dorsal (DRG).
Específicamente, la longitud total y el número de articulaciones de las neuritas aumentaron después del tratamiento con CM. Además, DPSC-CM promueve la viabilidad de las células de Schwann y la formación de mielina [54]. Las DPSC-CM mejoraron la supervivencia celular e indujeron el crecimiento de neuritas de las células PC12, como lo demuestra la proteína nuclear neuronal (NeuN), la proteína 2 asociada a microtúbulos (MAP-2 ), y III-tubulina.
Específicamente, las DPSC-CM fueron más eficaces para inducir el crecimiento de neuritas de PC12 en comparación con los cocultivos de DPSC/PC12, lo que indica que los cocultivos celulares tuvieron un retraso en la producción de cantidades eficaces de factores tróficos.
Las DPSC-CM también mejoraron la migración celular. Curiosamente, el número de células PC12 supervivientes se redujo cuando a CM se le añadió anti-GDNF. En cambio, la adición de anticuerpos anti-NGF, anti-GDNF y anti-BDNF atenúa el crecimiento de neuritas PC12.
Estos datos demostraron que NGF, BDNF y GDNF están involucrados en la supervivencia y diferenciación de PC12 [55]. El secretoma de DPSC muestra un efecto quimioatractivo sobre las células SH-SY5Y. Además, se ha evaluado su efecto sobre la maduración neuronal. Con este objetivo, las células SH-SY5Y fueron inducidas hacia células neuronales después de ser expuestas al secretoma de DPSC.
Las células SHSY5Y sometidas al secretoma de DPSC mostraron un mayor crecimiento de neuritas, adquirieron características ultraestructurales de las células neuronales y presentaron una mayor reactividad inmune para los marcadores neuronales. Además, las células SH-SY5Y tratadas con CM desarrollaron características distintas, incluidas corrientes sensibles a Cd2+-, lo que sugiere que las SH-SY5Y maduradas con CM-DPSC adquirieron canales de Ca2+ dependientes de voltaje [56].
De acuerdo con el estudio anterior, la CM obtenida mediante la hoja DPSC indujo la formación y el crecimiento de neuritas en células de neuroblastoma SH-SY5Y neuronalmente diferenciadas. Estos efectos mejoraron cuando las hojas de DPSC se cultivaron con FGF2.
Los efectos promotores de neuritas fueron abolidos cuando se inhibieron los factores neurotróficos, lo que sugiere que son necesarios para el efecto positivo de las hojas de DPSC sobre la actividad de las células neuronales [57].
Recientemente, Chouaib et al. Se evidenció que la mejora de DPSC-CM del crecimiento de neuritas en las neuronas sensoriales depende de la concentración. Los autores también encontraron que 48 h de acondicionamiento con DPSC era la mejor opción para obtener CM con actividad eficiente, mientras que extender el tiempo de acondicionamiento no mejoraba los efectos de DPSC-CM.
Curiosamente, el almacenamiento congelado no influyó en los resultados experimentales. La CM contenía algunos factores conocidos por su papel en la neurogénesis y la neuroprotección, pero también en la angiogénesis y la osteogénesis. Además, el acondicionamiento de las DPSC con el suplemento de B-27 mejoró los efectos neurodegenerativos de su secretoma, induciendo un cambio en su composición en factores de crecimiento.
En particular, la CM fue más eficaz cuando se añadió B-27 a las DPSC antes del acondicionamiento [58]. La CM de las DPSC mejoró la neuritogénesis y ejerció un efecto quimioatrayente también sobre las células madre neuronales (NSC).
La preparación de las DPSC con fibrina rica en leucocitos y plaquetas (LPRF) aumentó la secreción de BDNF pero no ejerció efectos adicionales sobre los mecanismos de reparación mediados por paracrinos [59].
También se demostró que la CM derivada de DPSC es capaz de proteger y regenerar células neuronales del ganglio trigémino primario aislado (TGNC). De hecho, CM mejoró la supervivencia de TGNC asociada con un extenso crecimiento y ramificación de neuritas.
Paralelamente, DPSC-CM aumentó significativamente la expresión de los marcadores neuronales NeuN, III-tubulina y sinapsina-I, así como TRPV1. Curiosamente, DPSC-CM contenía NGF, BDNF, NT-3 y GDNF [60].
Las DPSC movilizadas por G-CSF expresaron factores neurotróficos más altos en comparación con las DPSC basales y su secretoma mostró un potencial de extensión de neuritas mejorado. De hecho, la CM DPSC movilizada tuvo un mayor efecto sobre el crecimiento de neuritas en las células TGW [61]. Anteriormente, se demostró que la CM de DPSC movilizadas mejoraba la proliferación y la actividad migratoria de las células neuronales Schwann RT4-D6P2T [62].
Curiosamente, se demostró que la CM de SHED y DPSC puede promover la regeneración de neuronas granulares cerebrales que inhiben las señales inhibidoras del crecimiento de los axones mediante mecanismos paracrinos [63]. El secretoma de las DPSC también muestra efectos superiores en comparación con otras MSC.

Kumar et al. demostraron que el secretoma derivado de DPSC, SCAP y DFSC inducía la diferenciación neuronal en células IMR-32, una línea celular preneuroblástica, de manera más eficiente que las BMSC.
En particular, la longitud de las neuritas fue mayor cuando las células IMR-32 se trataron con el secretoma de DPSC. El secretoma de DPSC contenía GCSF, IFN- y TGF-, que pueden promover la diferenciación neural [64].
Las DPSC, BMSC y AMSC promovieron un aumento en la supervivencia de células ganglionares de la retina cocultivadas. En particular, el aumento de la supervivencia mejoró en los cultivos de retina tratados con DPSC.
Curiosamente, el cocultivo con DPSC indujo un aumento significativo tanto en el número de células ganglionares de la retina portadoras de neuritas como en la longitud de las neuritas en comparación con los cocultivos con BMSC y AMSC. Sin embargo, estos efectos se bloquearon utilizando bloqueadores de los receptores Fc de los receptores de factores neurotróficos.
Los diferentes tipos de MSC mostraron un patrón diferente de expresión del factor neurotrófico y, específicamente, las DPSC liberaron niveles más altos de varios factores de crecimiento como NGF, BDNF y VEGF en comparación con las BMSC y AMSC.
En particular, el VGF puede mediar los efectos neuroprotectores de las DPSC [65]. Las CM-DPSC mostraron efectos protectores sobre la citotoxicidad inducida por la privación de oxígeno y glucosa (OGD) en los astrocitos de una manera dependiente de la dosis.
Específicamente, tanto el pretratamiento como el postratamiento con CM-DPSC, pero también con CM-BMSC, atenuaron la expresión de proteína ácida fibrilar glial (GFAP), nestina y musashi-1 inducida por OGD en astrocitos. El tratamiento con CM también bloqueó la producción de especies reactivas de oxígeno (ROS) inducida por OGD y la regulación positiva de IL-1. Curiosamente, las CM-DPSC confieren una citoprotección superior contra la muerte celular en comparación con las CMBMSC [66].
Venugopal et al. compararon el potencial neuroprotector de EXO, CM o sistema de cocultivo de neurona-MSC contra la excitotoxicidad inducida por ácido kaínico in vitro. Además, para identificar el tipo de MSC más adaptado, se probaron EXO y CM derivados de DPSC y BMSC.
Los tres enfoques mostraron potencial neuroprotector gracias al aumento de la expresión del factor de crecimiento y la inhibición de la apoptosis mediante la activación de la vía PI3K-Bcl-2.
Es importante señalar que los EXO demostraron mejores propiedades antinecróticas en comparación con el cocultivo de neurona-MSC o CM. Con respecto a la CM, sólo la fracción que contenía proteínas en el rango de 3 a 10 kDa mostró neuroprotección y rescató a las neuronas de la excitotoxicidad [67].
El secretoma de las DPSC también mostró efectos beneficiosos en modelos de enfermedades neurodegenerativas. El tratamiento con secretoma de DPSC redujo la citotoxicidad del amiloide (A) en un modelo in vitro de la enfermedad de Alzheimer (EA), aumentando la viabilidad celular y reduciendo la apoptosis.
Se demostró que el secretoma de DPSC contiene niveles elevados de VEGF, fractalquina, RANTES, proteína quimioatrayente de monocitos-1 (MCP-1) y GMCSF en comparación con las BMSC y las AMSC.
Curiosamente, también se encontró neprilisina, una proteasa capaz de degradar A, en el secretoma de DPSC. El secretoma de DPSC degrada proteolíticamente A 1–42 in vitro, lo que resulta en una degradación incompleta después de 12 h [68].

For more information:1950477648nn@gmail.com






