parte 2: Efectos anti-melanogénicos de vesículas extracelulares derivadas de hojas y tallos de plantas en células de melanoma de ratón y piel humana sana
Mar 23, 2023
Materiales y métodos
6. Ensayos de absorción celular
La internalización de los EV en las células se controló mediante la primera tinción de los LEV y los SEV con DiI lipofílico (MOP-D -3911) (Invitrogen, Carlsbad, CA, EE. UU.). Después de tratar las células con EV teñidas durante 1, 3, 6, 12, 24 y 48 h, se eliminó el medio de crecimiento y las células se fijaron con paraformaldehído al 4 por ciento (Wako, Japón). Se añadió Hoechst 33342 (Invitrogen) y las células se incubaron durante 15 min a temperatura ambiente para teñir los núcleos (azul). Finalmente, las células se lavaron con PBS que contenía albúmina de suero bovino al 1 por ciento y se observó la fluorescencia (roja y azul) bajo un microscopio de fluorescencia (Leica Microsystems, Wetzlar, Alemania). Se seleccionaron y analizaron al menos tres campos utilizando el software ImageJ.
7. Medición del contenido de melanina
Para evaluar el contenido de melanina, primero se inocularon células de melanoma B16BL6 en 24-placas de pocillos (5 × 104 células/pocillo) en un volumen de 500 μl. Después de 24 horas de incubación, las célulasfueron tratados con 100 nM -MSH (Sigma-Aldrich, St. Louis, MO) solo o 50 μL de LEV y SEV a 1, 5 y 10 μg/mL durante 48 horas. Después del tratamiento, las células se lavaron con PBS y luego se incubaron con tripsina al 2,5 por ciento (Gibco, Thermo Fisher Scientific) para el aislamiento. Las microesferas celulares se disolvieron en solución de hidróxido de sodio 1n (Sigma-Aldrich) que contenía 1 por ciento de DMSO (Sigma-Aldrich) durante 1 hora a 80 grados. Los lisados celulares se transfirieron a una placa de pocillos 96- y se determinó el contenido de melanina midiendo la absorbancia a 405 nm utilizando un marcador enzimático (BioTek). El contenido de melanina se determinó usando una curva estándar de melanina construida a partir de 0-100 \mu g/ml de solución de melanina sintética (Sigma - Aldrich) (vesículas extracelulares Figura como sigue). El contenido de melanina se calculó por comparación con los controles.
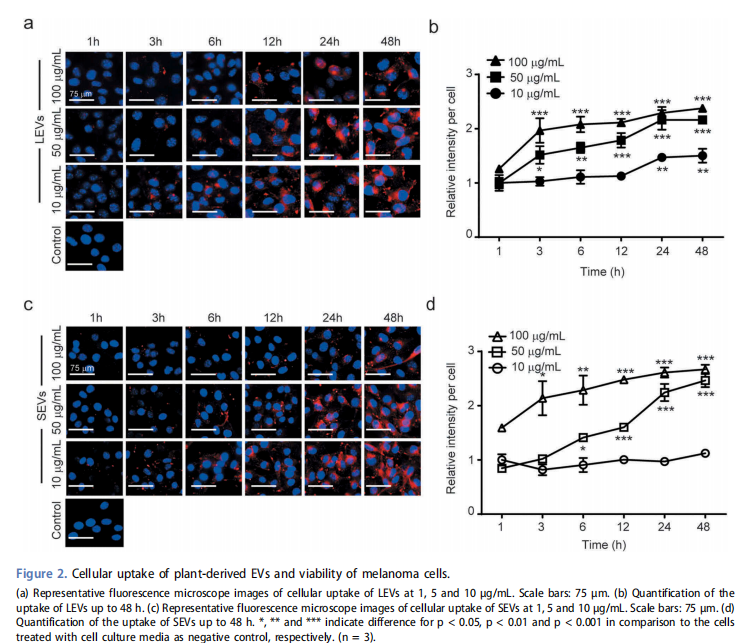
8. Ensayo de actividad de tirosinasa
La actividad de TYR se midió utilizando la actividad de L-DOPA oxidasa. Las células B16BL6 se inocularon en medio -MEM que contenía Sigma-Aldrich -MSH 100 nM (500 μL) y se cultivaron a una densidad de 1 × 105 células/pocillo en 24-placas de cultivo de pocillos. Después de tratar las células con 50 μL de LEV y SEV en concentraciones de 10, 50 y 100 μg/mL durante 24 h, las células se lavaron con PBS y se lisaron con Triton X-100 al 1 % (Sigma-Aldrich). Las células lisadas se incubaron a - 80 grados durante 30 min y luego se liofilizaron y almacenaron a temperatura ambiente durante 10 min. Las muestras resultantes se clarificaron mediante centrifugación a 12,000 × g durante 15 min, después de lo cual se añadieron 2 mg/ml de L-DOPA (Sigma-Aldrich) y se incubaron a 37 grados durante 1 h. Luego se midió la absorbancia a 490 nm utilizando un marcador enzimático (BioTek). Luego se midió la absorbancia a 490 nm usando BioTek.

9. Análisis de transferencia Western
Los niveles de proteína asociados con la vía antimelanogénica se determinaron intracelularmente mediante análisis de transferencia Western de extractos de células completas. Se inoculó un volumen de 500 μl de células de melanoma de ratón B16BL6 en 24-placas de pocillos (1 × 105 células/pocillo). Las células se lisaron mediante incubación en tampón RIPA (Thermo Fisher Scientific) durante 20 min en presencia de una mezcla de inhibidores de proteasa (Roche, Alemania) y se trataron con 50 μL de 10, 50 y 100 μg/mL de EV durante 24 h. Los lisados celulares se centrifugaron a 17 709 g durante 15 min y se determinó la concentración de proteína en los lisados resultantes utilizando un kit de ensayo BCA (Thermo Fisher Scientific). Se cargaron cantidades iguales de proteína (10-20 ug/muestra) en los pocillos de geles Bolt 4-12 por ciento Bis-Tris Plus (Invitrogen) y se electrotransfirieron a membranas de PVDF (fluoruro de polivinilideno) (GE Healthcare, Chicago, EE. IL, EE. UU.). Las membranas se lavaron con solución salina tamponada con Tris que contenía diez -20 (TBST) al 0,2 % (v/v), y se cerraron con TBST que contenía leche descremada al 5 % (p/v) (Gibco, Thermo Fisher Scientific) durante 1 hora. a temperatura ambiente y luego se incubó a 4 grados en una solución de anticuerpo primario diluida con leche descremada al 1 por ciento (p/v). La incubación se llevó a cabo durante la noche. Los anticuerpos primarios utilizados incluyeron anticuerpos anti-TRP-1 (1:1000), anti-TRP-2 (1:1000) y anti-MITF (1:1000) de Abcam, Cambridge, Reino Unido; anticuerpos anti-TYR (1:500) de Santa Cruz Biotechnology (Santa Cruz, CA, EE. UU.). Se utilizó anticuerpo anti- -actina (1:500; Santa Cruz) para la estandarización a nivel de proteína. Los anticuerpos primarios se detectaron con un anticuerpo secundario marcado con peroxidasa de rábano picante (HRP) de Genetex (Irvine, CA, EE. UU.). Las membranas se lavaron con TBST y se incubaron durante 1 ha TA con una dilución 1:2000 del anticuerpo secundario en TBST. La señal generada después de lavar la membrana con TBST y la incubación con reactivo de quimioluminiscencia mejorada (ECL) (GE Healthcare) se detectó utilizando un sistema de imágenes de gel ImageQuant 350 (GE Healthcare).
10. Detección por microscopía electrónica de la producción de melanina intracelular
Las células se procesaron con LEV o SEV y se incubaron durante 48 h. Después del tratamiento, las células se fijaron mediante incubación con tampón de cacodilato 200 mM que contenía glutaraldehído al 8 por ciento y paraformaldehído al 20 por ciento (Wako). Una vez deshidratadas con etanol, se prepararon secciones ultrafinas con un micrótomo Leica EM UC7 (Leica) y se recogieron en una rejilla de malla 200-de cobre. Las secciones se tiñeron con acetato de uranilo al 1 por ciento y citrato de plomo y las imágenes se adquirieron con un microscopio electrónico de transmisión JEOL JEM 1010 (JEOL) a 80 kV.

extracto de cistanche
11. Medición del efecto blanqueador utilizando un modelo de piel humana.
El modelo de piel humana derm-me (Tego Science, Seúl, Corea) se utilizó para probar el efecto blanqueador de los LEV. Se trató tejido de piel humana con 10 μ g/ml de lev durante 7 días como control negativo. La concentración de arbutina fue de 70 µg/mL. Se disolvió tejido de piel humana en NaOH 1 N y se midió la absorbancia a 405 nm utilizando un marcador enzimático (BioTek) para determinar el contenido de melanina. El día 7, se comparó la pigmentación de la piel mediante análisis microscópico de Fontana - muestras teñidas con albañil. Para la tinción de Fontana-Masson, las muestras de piel se fijaron durante la noche a temperatura ambiente en paraformaldehído al 4 por ciento (Waco), se seccionaron y se incluyeron en cera de parafina. Luego, las secciones incluidas en parafina se calentaron en un horno a 60 grados durante 1 hora para que se secaran. Luego, las secciones se empaparon tres veces en xileno, dos veces en etanol al 95 por ciento y dos veces en etanol al 100 por ciento, y luego se lavaron con agua destilada. La tinción de Fontana-Masson se realizó utilizando la solución de plata amoniacal a 56 grados y se lavó con agua destilada. Luego, los portaobjetos se fijaron en una solución de cloruro de oro al 0,2 por ciento y se sumergieron en una solución de tiosulfato de sodio al 5 por ciento a temperatura ambiente. Finalmente, los portaobjetos se deshidrataron en alcohol fresco.
12. Análisis estadístico
Los datos obtenidos de los experimentos se expresan como media ± SEM. Realizamos experimentos con cuatro lotes de actividad, contenido de melanina y actividad TYR (Fig. S3 complementaria). El análisis de varianza unidireccional (ANOVA) y la prueba de Dunnett se realizaron utilizando GraphPad Prism (GraphPad Prism Software Inc., San Diego, CA, EE. UU.). p < diferencias; 0.05, p < 0.01, p < 0.001 se consideraron estadísticamente significativos.
Extracto de Cistanche tubulosa
Discusión
A diferencia de la mayoría de las células eucariotas, las plantas tienen una pared celular compleja, lo que representa una barrera importante para el movimiento de los exosomas. Como resultado, las células vegetales liberan exosomas a través de una serie de cuerpos multivesiculares fusionados a la membrana plasmática. Los productos secretores liberados por las secreciones vegetales se depositan dentro del espacio periplásmico adyacente a la membrana plasmática; a medida que se acumulan, generan una presión que permite que la secreción atraviese la barrera de la pared celular. Como resultado, el material secretado, incluidos los exosomas, puede liberarse sin necesidad de energía. Los EV derivados de plantas son similares en tamaño o más grandes que los exosomas de células animales naturales y son similares a los observados en el fluido exosomal del girasol (50-200 nm) y los EV de Arabidopsis (50-300 nm). La eficiencia de captación celular se considera un determinante clave de la eficacia, ya que los objetivos de muchos agentes terapéuticos se encuentran intracelularmente. Por lo tanto, determinamos el momento y la concentración óptimos de absorción por las células de melanoma y observamos una transferencia rápida de LEV y SEV a las células de melanoma en 12 horas.
TYR es una glicoproteína que cataliza la conversión de L-tirosinasa a L-DOPA, el paso limitante de la velocidad en la síntesis de melanina. Ambos EV exhiben un efecto antimelanogénico, pero el efecto antimelanogénico de LEV es significativamente mayor que el de SEV.
La producción de melanina está regulada por -MSH-MC1R, y se sabe que la inhibición de PKC reduce la pigmentación de la piel y el cabello. Sin embargo, muchos estudios genéticos, bioquímicos y farmacológicos sugieren que la vía de señalización -MSH-MC1R es un importante impulsor de la melanogénesis. Aunque nuestros experimentos no mostraron una interacción directa entre MITF y TYR, se demostró que los LEV inhiben la melanogénesis al reducir la expresión de MITF a través de la vía -MSHMC1R dependiente de UV, que a su vez reduce la expresión de TYR, TRP-1, y PRT-2. Presumimos que las proteínas de la familia TRP están indirectamente vinculadas entre sí, pero es posible que se requieran más experimentos para demostrar una interacción directa entre ellas. Además, los modelos de piel humana reconstruidos muestran que los LEV inhiben eficazmente la síntesis de melanina inducida por UV y el contenido de melanina.

Cistanche dulce
Conclusión
Nuestros hallazgos sugieren que los LEV son candidatos para nuevos fármacos antimelanogénicos que reducen la melanogénesis al inhibir la expresión de proteínas relacionadas con la melanina. Los resultados confirmaron que los LEV redujeron el MITF y, por lo tanto, regularon a la baja los TRP en las células de melanoma B16BL6. levs y arbutina inhibieron TRY en un 66 por ciento y un 67 por ciento, respectivamente. El contenido de melanina de la piel reconstruida tratada con LEV se redujo en un 43 % y un 28 % en comparación con el control negativo no tratado y la arbutina como control positivo, respectivamente.
Según los primeros hallazgos, creemos que los vehículos eléctricos derivados de plantas podrían ser útiles como agente antimelanogénico para el desarrollo de cosméticos naturales. Se necesita más investigación en el futuro para desarrollar vehículos eléctricos derivados de plantas como un ingrediente eficaz para mejorar la piel y es necesario demostrar la seguridad de los vehículos eléctricos derivados de plantas en modelos de piel humana. Nuestros resultados sugieren que EV se puede utilizar para reducir la melanina y, por lo tanto, iluminar la piel. Sin embargo, EV puede tener efectos tóxicos en la piel, y se deben realizar otros experimentos, como pruebas de alergia o pruebas de Ames.
REFERENCIAS
[1] Nosanchuk JD, Nimrichter L, Casadevall A, et al. Un papel para el transporte vesicular de macromoléculas a través de las paredes celulares en la patogénesis fúngica. Common Integr Biol. 2008;1(1):37–39.
[2] Robinson DG, Ding Y, Jiang L. Secreción de proteína no convencional en plantas: una evaluación crítica. Protoplasma. 2016;253(1):31–43.
[3] Paiva EA. ¿Cómo cruzan los productos secretores la pared celular de la planta para ser liberados? Una nueva hipótesis que involucra acciones mecánicas cíclicas del protoplasto. Ana Bot. 2016;117(4):533–540.
[4] Hood JL, Scott MJ, Wickline SA. Maximización de la estabilidad coloidal del exosoma después de la electroporación. Bioquímica anal. 2014;448(1):41–49.
[5] Rutter BD, Innes RW. Las vesículas extracelulares aisladas del apoplasto de la hoja transportan proteínas de respuesta al estrés. Fisiol vegetal. 2017;173(1):728–741.
[6] Luan X, Sansanaphongpricha K, Myers I, et al. Ingeniería de exosomas como nanoplataformas biológicas refinadas para la administración de fármacos. Acta Pharmacol Sin. 2017;38(6):754–763.
[7] Videira IF, Moura DF, Magina S. Mecanismos que regulan la melanogénesis. Un Bras Dermatol. 2013;88(1):76–83.
[8] Park HY, Lee J, Kapasi S, et al. La aplicación tópica de un inhibidor de la proteína quinasa C reduce la pigmentación de la piel y el cabello. J Invest Dermatol. 2004;122(1):159–166.
[9] Yamanishi DT, Graham M, Buckmeier JA, et al. La expresión diferencial de los genes de la proteína quinasa C en melanocitos neonatales humanos normales y melanomas metastásicos. Carcinogénesis. 1991;12(1):105–109.
[10] Borovansky J, Riley PA. Melaninas y melanosomas: biosíntesis, biogénesis, funciones fisiológicas y patológicas. Hoboken, Nueva Jersey: Wiley-Blackwell; 2011
[11] D'Mello S, Finlay G, Baguley B, et al. Vías de señalización en la melanogénesis. Int J Mol Sci. 2016;17(7):1–18.






