¿Es la asociación del raro polimorfismo del gen Rs35667974 IFIH1 con enfermedades autoinmunes un caso de epigenética de ARN?
Jul 13, 2023
visualización: AA, AP y EEE, supervisión: EEE y adquisición de fondos: EEE. Todos los autores han leído y aceptado la versión publicada del manuscrito. Abstracto
El interferón inducido con el gen de la proteína 1 que contiene el dominio helicasa C (IFIH1) codifica una helicasa de ARN citoplásmica también conocida como 5 asociada a la diferenciación de melanoma (MDA5), una helicasa de ARN similar a RIG-1- que reconoce el ARN viral y está involucrada en la inmunidad a través del reconocimiento del ARN viral. Al unirse al ARN de doble cadena (ds), MDA5 forma un ensamblaje filamentoso a lo largo de la longitud del dsRNA y utiliza firmas moleculares para discriminar lo propio y lo no propio en función de la longitud y la metilación del dsRNA. Su variante missense rs35667974 protege contra la diabetes tipo 1, la psoriasis y la artritis psoriásica, pero también se ha encontrado que está asociada con un mayor riesgo de espondilitis anquilosante, enfermedad de Crohn y colitis ulcerosa. Para obtener información sobre el papel complejo de esta variante, realizamos un análisis estructural de MDA5 en complejo con dsRNA utilizando simulaciones de dinámica molecular.
Nuestros datos sugieren que, si bien la mutación Ile923Val de la variante rs35667974 no afecta significativamente la unión al dsRNA nativo, muestra un efecto desestabilizador en presencia de metilación de uridina 2′-O. Por lo tanto, la presencia de 2′-O-metilación en el dsRNA introduce una firma de detección que conduce a una reducción selectiva de la actividad catalítica general de MDA. Este estudio representa una evaluación del papel de la variante rs35667974 compartida del locus autoinmune IFIH1, que se informó que conduce a una actividad catalítica selectivamente reducida del fenotipo MDA5 modificado y, como consecuencia, una retroalimentación negativa reducida en la señalización de citocinas y quimiocinas y protección selectiva contra la autoinmunidad. .
El dominio helicasa C es una proteína enzimática importante que puede desenrollar la estructura de doble hélice del ADN. Puede ayudar al ADN a completar la replicación, edición y entrega correctas en el proceso de replicación, reparación y transcripción celular, y es una de las claves para el funcionamiento normal de las células. Al mismo tiempo, la inmunidad es un mecanismo de defensa muy importante en el cuerpo humano, que puede protegernos eficazmente de patógenos como bacterias y virus.
Los estudios han demostrado que el dominio helicasa C juega un papel importante en la inmunidad. En primer lugar, el dominio helicasa C puede garantizar la estabilidad y la eficiencia de codificación de los genes al ayudar a la replicación, reparación y transcripción normales del ADN celular, mejorando así la inmunidad del cuerpo humano. En segundo lugar, el dominio helicasa C puede promover el reconocimiento de moléculas heterogéneas de proteínas por parte de las células y regular la transducción de señales del sistema inmunitario, lo que respalda la función de defensa del cuerpo. Los dos métodos anteriores han desempeñado un papel positivo en la promoción del mantenimiento y la mejora de la inmunidad.
Además, el estudio en profundidad de la relación entre el dominio helicasa C y la inmunidad también nos brinda una inspiración importante para descubrir nuevos fármacos para el tratamiento del cáncer y enfermedades relacionadas con el sistema inmunitario. El desarrollo de fármacos y la terapia génica dirigida al dominio helicasa C pueden mejorar la resistencia del cuerpo al cáncer y otras enfermedades relacionadas con el sistema inmunitario, y ayudar a los pacientes a sobrellevar mejor el tratamiento y la recuperación de enfermedades relacionadas.
En resumen, la relación entre el dominio helicasa C y la inmunidad es muy estrecha y juega un papel vital para garantizar la estabilidad de los genes, promover la inmunidad celular y apoyar la defensa del cuerpo. Se espera que a través de métodos de investigación y tratamiento relevantes, podamos mantener y mejorar mejor la inmunidad humana y crear una vida mejor y más saludable para nosotros. Desde este punto de vista, necesitamos mejorar la inmunidad personal. Cistanche tiene un efecto significativo en la mejora de la inmunidad porque la pasta de carne es rica en una variedad de sustancias antioxidantes, como vitamina C, vitamina C, carotenoides, etc. Estos ingredientes pueden eliminar los radicales libres y reducir el estrés oxidativo. Estimular y mejorar la resistencia del sistema inmunológico.

Haz clic en los beneficios de la cistanche tubulosa
Palabras clave
Polimorfismo de un solo nucleótido (SNP) · Modelo molecular · Interferón inducido con helicasa C dominio 1 (IFIH1) · Asociado a la diferenciación de melanoma 5 (MDA5) · Metilación del ARN.
Introducción
Los genes y los mecanismos involucrados en las enfermedades autoinmunes, que afectan aproximadamente al 5 por ciento de la población, siguen siendo esquivos, pero la acumulación de datos sugiere fuertemente que diferentes enfermedades autoinmunes pueden compartir un trasfondo genético común, lo que señala la existencia de variantes compartidas por diferentes enfermedades autoinmunes. (Zhernakova et al. 2009). Intentar desentrañar esta información genética en mecanismos biológicamente significativos que conducen a enfermedades se refiere a la identificación de genes causales. La identificación de variantes causantes de enfermedades es una tarea difícil pero necesaria en el intento de establecer métodos efectivos para la predicción, prevención e intervención de enfermedades (Biros et al. 2005).
Diferentes tipos de moléculas de ARN participan en la regulación de varios procesos biológicos, incluidos el ARN mensajero (ARNm), el ARN de transferencia (ARNt), el ARN ribosómico (ARNr), el microARN (miARN) y el ARN largo no codificante (lncARN). Las moléculas de ARN contienen numerosas modificaciones químicas (más de 150) (Machnicka et al. 2013; Boccaletto et al. 2018). Estas modificaciones están vinculadas funcionalmente a todas las etapas del metabolismo del ARN, como la estructura, la estabilidad y las interacciones, y desempeñan funciones críticas en varios procesos biológicos, como la modulación de la replicación de virus y las respuestas inmunitarias antivirales (Machnicka et al. 2013). Entre ellos, la metilación de la ribosa se encuentra entre las modificaciones más ubicuas que se encuentran en el ARN. La 2′-O -metiluridina se encuentra en rRNA, snRNA, snoRNA y tRNA de Archaea, Bacteria y Eukaryota (Aučynaitė et al. 2018). La ribosa-2′-Ometilación aumenta la hidrofobicidad de los nucleótidos y los protege contra la acción de las nucleasas (Yildirim et al. 2014).
La evidencia acumulada indica que la 2′-O-metilación del ARN viral (2′OMe-RNA) juega un papel importante en la evasión de las respuestas inmunitarias innatas celulares en las células huésped (Dimitrova et al. 2019). Züst y sus colegas han demostrado que 2′ OMe del ARN viral contribuyó a la evasión de la respuesta antiviral mediada por interferón (IFN), promoviendo así la replicación viral (Züst et al. 2011). Además, Vitali y Scadden han propuesto que IU-dsDNA suprime la vía estimulante del IFN MDA5 (Vitali y Scadden 2010).
El interferón inducido con el gen del dominio 1 de la helicasa C (IFIH1) codifica una ARN helicasa citoplasmática también conocida como MDA5 (Proteína asociada a la diferenciación de melanoma 5), y es un receptor tipo RIG-I (RLR) que realiza una función antiviral en la inmunidad innata mediante la detección de ARN virales. MDA5 reconoce 0estructura de tallo dúplex de ARN de 0.5–1 kb que generalmente se forma durante la replicación picornaviral y media una respuesta inmune a la infección viral (Nejentsev et al. 2009; Crow 2011). MDA5, tras la detección de ARN virales de doble cadena largos (dsRNA), generados durante la replicación de picornavirus, activa la vía de señalización del interferón tipo I. Los estudios han demostrado que MDA5 forma un filamento a lo largo del dsRNA y utiliza la dinámica del filamento dependiente de ATP para discriminar entre uno y otro en función de la longitud del dsRNA (Toro et al. 2015). Se demostró que MDA5 participa en la modulación de la diafonía entre las células y el sistema inmunitario innato/adaptativo a través de la producción local de citocinas y quimiocinas.
Los cambios en la expresión y/o actividad de MDA5 pueden desencadenar respuestas de células beta al dsRNA, un subproducto de la replicación del virus (Colli et al. 2010). También se ha demostrado que la mutación de los residuos asociados a la formación de llamas da como resultado la pérdida de la formación de filamentos y la señalización dependiente de MDA5-, excepto por un par de mutaciones, que mejoran moderadamente la señalización. Estos resultados sugieren que los mecanismos independientes de ATP, es decir, una unión de ARN más estrecha y/o una interacción proteína-proteína más estable, probablemente sean responsables de la estabilidad observada de la formación de filamentos de MDA5 in vitro y de una mayor actividad de señalización en las células (Sohn y Hur 2016).
Smyth et al. (2006) y Nejentsev et al. (2009) describieron un alelo raro del gen IFIH1 que confiere protección contra la diabetes tipo 1 (T1D). Este polimorfismo de un solo nucleótido (SNP) rs35667974 IFIH1, donde la isoleucina conservada (codón [ATT]) en la posición n.° 923 cambia a valina (codón [GTT]), es una variante rara ya que la frecuencia del alelo menor (MAF) es C {{ 9}}.010031 (2655 individuos en una muestra total de 264690) basado en TOPMED (Taliun et al. 2021) y C = 0.016267 (3343 individuos en una muestra total de 205514) basado en ALFA (Phan et al. 2020; Sherry et al. 2001). En la Tabla 1 se presenta la biogeografía humana de la frecuencia del polimorfismo en diferentes regiones continentales con base en los datos del proyecto ALFA (Phan et al. 2020; Sherry et al. 2001). Estudios posteriores confirmaron que este alelo raro tenía el mismo efecto sobre la DT1, la psoriasis (PS) (Li et al. 2010) y la artritis psoriásica (PsA) (Budu-Aggrey et al. 2017). Por el contrario, este SNP se ha asociado como un factor de riesgo para la susceptibilidad de desarrollar espondilitis anquilosante (EA) (Ellinghaus et al. 2016), enfermedad de Crohn (EC) (Ellinghaus et al. 2016; Budu-Aggrey et al. 2017 ) y colitis ulcerosa (CU) (Ellinghaus et al. 2016; Budu-Aggrey et al. 2017).
Chistiakov et al. (2010) han demostrado que las mutaciones de pérdida de función E627X e I923V de MDA5 están asociadas con una menor producción de interferón inducida por poli(I:C) en células mononucleares de sangre periférica de pacientes con diabetes tipo 1 y, por lo tanto, protegen contra la DT1. También se afirma que en la molécula MDA5, la sustitución del aminoácido I923V reside en la vecindad de un residuo H927, lo que contribuye a la unión de dsRNA (Yoneyama y Fujita 2008). Sin embargo, se demostró que la variante I923V de MDA tiene una capacidad normal para unirse a dsRNA pero una actividad catalítica reducida 25- veces (Shigemoto et al. 2009). Por lo tanto, este polimorfismo parece no afectar de manera importante las propiedades de unión a ácidos de nucleótidos de esta helicasa detectora de ARN citoplásmico, pero altera su función por un mecanismo aún desconocido.

Se ha encontrado la relación entre el polimorfismo IFHI1 y la incidencia de infección por enterovirus en DT1 y la asociación entre la variante MDA5 I923V y la frecuencia de ARN enteroviral en pacientes con DT1 (Looney et al. 2015). Además, estudios recientes en ratones MDA5- y MAVSknockout mostraron un papel crítico de estas proteínas en la mediación de las respuestas de interferón tipo 1 contra el virus Coxsackie B (Wang et al. 2010). Se muestra que una proteína líder de mengovirus previene la expresión de IFN- al bloquear la dimerización de IRF3 necesaria para la activación de este factor (Hato et al. 2007). Esta observación sugiere que las variantes que interrumpen la función de IFIH1 en la respuesta antiviral del huésped han sido seleccionadas negativamente, en lugar de seleccionadas positivamente porque confieren protección contra la DT1 (Crow 2011).

Chow et al. (2018) han analizado extensamente, entre otros, los receptores similares a RIG-I, mientras que Brisse y Ly (2019) revisaron extensamente la evolución y especiación de MDA5 y su RIG-I relacionado. La ubicación de los residuos alterados en o cerca de los sitios de unión de ARN y ATP o la interfaz del filamento nos llevó a plantear la hipótesis de que las mutaciones observadas podrían mejorar la estabilidad del filamento IFIH1 al aumentar la afinidad intrínseca entre IFIH1 y dsRNA o entre IFIH1 moléculas en el filamento o al disminuir la eficiencia de la hidrólisis de ATP y, por lo tanto, la tasa de desensamblaje del filamento (Rice et al. 2014).
Este trabajo representa un estudio estructural del papel potencial de la variante rs35667974 compartida del locus autoinmune IFIH1, que se informa que conduce a un fenotipo de función inhibida que codifica una sustitución de aminoácido Ile923Val en el producto de proteína del gen IFIH1 MDA5. Este último es un gen candidato causal biológicamente plausible compartido entre varias enfermedades, que influye en el control de la expresión local de citoquinas y quimioquinas que protegen contra la autoinmunidad (Colli et al. 2010). Este trabajo tiene como objetivo explorar el mecanismo aún desconocido por el cual la sustitución Ile923Val reduce la actividad catalítica de la MDA5 humana. En este estudio, investigamos las diferencias en la interacción de MDA5 con dsRNA entre la variante nativa y la rara Ile923Val en el inicio del mecanismo de inflamación. En consecuencia, nuestro objetivo fue investigar el comportamiento dinámico del complejo MDA5/dsRNA humano en un entorno acuoso en presencia de Ile923 o Val923 cuando el uracilo 2′-O está metilado o no. Este análisis estructural de loci de protección o susceptibilidad genética compartida rara puede proporcionar información sobre nuestra comprensión de la fisiopatología de las enfermedades autoinmunes y los hallazgos de la investigación pueden afectar el mejor manejo de las enfermedades en estudio.
Materiales y métodos
Recuperación de secuencias, construcción de árboles filogenéticos y análisis de selección positiva
La secuencia de proteínas de Homo sapiens (ID de secuencia: NP_071451.2) se recuperó de la base de datos UniProt (The UniProt Consortium 2021). Para encontrar homólogos entre especies, se realizaron búsquedas BLAST con Mega BLAST (Centro Nacional de Información Biotecnológica, NCBI, Bethesda, MD, EE. UU.) en la base de datos de proteínas RefSeq y NR (y PDB y UniProt) usando Blastp (proteína-proteína BLAST) con parámetros predeterminados (Altschul et al. 1997). Se seleccionaron inicialmente 1000 homólogos de las proteínas MDA5 humanas y se utilizó una selección entre especies centrada en el dominio C-terminal que contenía la secuencia alrededor de la sustitución I923V humana para identificar esta variación en otras especies. Clustal Omega, el programa de alineación de secuencias múltiples (Clustal-O) (Sievers et al. 2011) y el servidor de alineación de secuencias múltiples T-Cofee (Notredame et al. 2000; Di Tommaso et al. 2011) se utilizaron para realizar alineaciones de secuencias de proteínas. y el software de bioinformática de la plataforma Unipro UGENE (Okonechnikov et al. 2012) para visualizar selectivamente múltiples alineaciones.
El análisis evolutivo se utiliza para identificar posiciones en las secuencias de proteínas que están muy conservadas entre especies, lo que indica una importancia estructural (Andreou et al. 2018). El árbol filogenético se construyó utilizando el método de Máxima Verosimilitud (Nei y Kumar 2000) y el modelo Tamura-Nei (Tamura y Nei 1993) con 500 réplicas de arranque (Felsenstein 1985). Los árboles iniciales para la búsqueda heurística se obtuvieron automáticamente aplicando los algoritmos Neighbor-Join y BioNJ a una matriz de distancias por pares estimadas utilizando el modelo Tamura-Nei y luego seleccionando la topología con un valor de probabilidad logarítmica superior. El análisis filogenético involucró 52 secuencias de nucleótidos homólogas (39 ortólogas y 13 parálogas) del gen IFIH1 humano. Las posiciones de codón incluidas fueron 1ª más 2ª más 3ª más no codificante. Hubo un total de 3729 posiciones en el conjunto de datos final. Los análisis evolutivos se realizaron utilizando el paquete de software MEGA11 (Tamura et al. 2021).
Para detectar si el gen IFIH1 ha evolucionado de forma adaptativa, hemos utilizado el programa codeml en el paquete de software PAML v4.9j (Yang 2007). La secuencia de nucleótidos y el archivo de alineación de la secuencia de proteínas correspondiente se enviaron a PAL2NAL (Suyama et al. 2006) para formar los archivos de alineación de nucleótidos de entrada CODEML apropiados. Los análisis de selección positiva para los genes ortólogos MDA5 se realizaron utilizando modelos de sitio y sitio de ramificación (Yang et al. 2005; Yang y Bielawski 2000). La relación de tasa de sustitución no sinónima/sinónima (ω=dN/dS) proporciona una medida de la presión selectiva a nivel de aminoácidos. La magnitud del valor de dN/dS (ω) representa los tipos de selección: ω<1 for negative selection, ω=1 for neutral selection, and ω>1 para selección positiva (Yang et al. 2005). En CODEML, se seleccionaron los modelos de sitio (M0, M1, M2, M3, M7 y M8) y los modelos de sucursal (Clades A y C) para realizar el análisis de selección positiva (Bielawski y Yang 2004; Yang y Nielsen 2002). En los modelos de sitio, se utilizó la prueba de razón de verosimilitud (LRT) para probar la selección positiva comparando los tres pares de modelos (M0/M3, M2/M1 y M7/M8). El análisis se realizó tanto para la secuencia completa como para la secuencia del dominio C-terminal (CTD).
Análisis Estructural y Simulaciones de Dinámica Molecular
La estructura de microscopía electrónica (cryo-EM) del filamento hMDA5-dsRNA en presencia de ATP (PDB ID: 6GKM) (Yu et al. 2018) (Berman et al. 2000) se utilizó como sistema modelo para la dinámica molecular ( MD) simulaciones. Todos los residuos de proteínas se resolvieron (307–1020), los 14 pares de bases de ARN de doble cadena (dsRNA) y el zinc coordinado se mantuvieron, mientras que los residuos faltantes se modelaron utilizando el servidor SWISS-MODEL (Waterhouse et al. 2018). Los parámetros del campo de fuerza y los átomos de hidrógeno se agregaron usando el módulo XLEaP de AMBER 18 (Case et al. 2005). Se utilizaron los campos de fuerza AMBER f14SB (Maier et al. 2015) y f99OL3 (Zgarbová et al. 2011) para la proteína y el ARN, respectivamente, con los parámetros modrna08 (Aduri et al. 2007) para los nucleósidos modificados. La mutación I923V se introdujo en MDA5 mediante la eliminación manual del grupo metilo Cδ de I923, mientras que la ribosa modificada de U12 se metiló en 2′-O utilizando el residuo de biblioteca modrna08 MRU. El ion zinc se unió con los 4 residuos de cisteína 907, 910, 962 y 964, usando parámetros de campo de fuerza apropiados para retener una esfera de coordinación tetraédrica (Longitud de enlace Zn–S de 2,35 Å con 50 kcal·mol–1·Å–2 constantes de fuerza y ángulos S–Zn–S de 109,5 grados con 25 kcal·mol–1·rad–2).
De esta forma, preparamos 4 sistemas para las simulaciones de MD: (i) el MDA5–dsRNA nativo, (ii) MDA5(V923)–dsRNA, (iii) MDA5–dsRNA(2′OMe), y (iv) MDA5( V923)–dsRNA(2′OMe). Todos los sistemas se solvataron en cajas de solventes octaédricos truncados de moléculas de agua TIP3P preequilibradas, con un tampón mínimo de 10 Å alrededor del complejo y luego se agregó la cantidad requerida de contraiones para obtener la neutralización de carga de los sistemas. Las simulaciones MD se realizaron con la versión acelerada por GPU del módulo PMEMD (Salomon-Ferrer et al. 2013) en AMBER 18 y un paso de tiempo de 2 fs. La temperatura se reguló con el termostato Langevin con una frecuencia de colisión de 1,0 ps–1, mientras que la presión se reguló con el barostato Berendsen con un tiempo de relajación de la presión de 1,0 ps. SHAKE se utilizó para restringir los enlaces que involucran átomos de hidrógeno con una tolerancia de 10–6 Å, mientras que las interacciones no enlazadas se calcularon con un límite de espacio directo de 10 Å.
La minimización de energía se realizó inicialmente para 1{{20}},000 pasos con restricciones posicionales de 100 kcal·mol–1·Å–2 constante de fuerza en los átomos que no son de hidrógeno de MDA5-dsRNA. Luego, el solvente se equilibró a 300 K y 1 atm a través de rondas cortas de simulaciones en los conjuntos NVT y NPT, 100 ps y 400 ps, respectivamente, manteniendo las restricciones en los átomos del soluto que no son de hidrógeno. Posteriormente, la minimización de energía se realizó en 10,000 pasos, pero con restricciones posicionales de 10 kcal·mol–1·Å–2 solo en los átomos de C de MDA5 y el esqueleto de fosfato del dsRNA. En 3 sub se relajaron gradualmente (10,0, 1,0, 0,1 kcal·mol–1·Å–2) durante 1 ns, seguido de 9 ns de equilibrio sin restricciones bajo presión constante. Después de estos 10 ns iniciales de equilibrio (no utilizados en el análisis), se realizaron 100 ns de simulaciones de producción en el conjunto NPT para cada sistema a 300 K y 1 atm, mientras se almacenaban instantáneas del sistema cada 5,0 ps para el análisis mediante CPPTRAJ. módulo de AMBER 18 (Roe y Cheatham 2013). Todas las figuras que representan modelos 3D se generaron utilizando el sistema de gráficos moleculares PyMOL (versión de código abierto v.2.3).
Resultados
Análisis filogenético de la sustitución Ile923Val de MDA5
(Brisse y Ly 2019) revisan extensamente la evolución y especiación de MDA5 y su RIG-I relacionado. Aquí se empleó la evolución IFIH1 para definir elementos de conservación en la secuencia MDA5 sobre el polimorfismo particular. El análisis evolutivo reveló una fuerte conservación de secuencias entre MDA5 de diferentes especies (984 de 1000 secuencias investigadas tienen isoleucina en la posición equivalente de hMDA #923) en el dominio RD/CTD, lo que indica una importancia estructural/funcional. El polimorfismo rs35667974 en el exón 14 del gen humano causa una mutación de aminoácido conservada en la posición 923 de Ile a Val en hMDA5. Sin embargo, hay otras dieciséis especies distantes que tienen la misma posición ocupada por una valina (Fig. 1), lo que indica la viabilidad de este cambio entre especies en el dominio RD/CTD de MDA5 y el dominio RS/GY estrechamente homólogo de las isoformas X1, Helicasas X3 y DHX58 (Fig. 2). Además, la alineación de secuencias de la región alrededor de la posición hMDA #923 (el bucle de interacción CTD de MDA) revela una secuencia moderada a altamente conservada entre especies distantes que indica la importancia funcional de la región entre especies.
Detección de Selección Positiva
Para detectar si el gen IFIH1 ha evolucionado adaptativamente, se usaron modelos de sitios y de sitios de ramificación para realizar análisis de selección positiva de ortólogos del gen completo y del dominio CTD. En los modelos de sitio, no se identificaron sitios de selección positiva para el dominio CTD (Tabla 2). M0 implica una tasa constante de evolución (ω=dN/dS=0.2) (Tabla 2). Algunos sitios que se habían sometido a una selección positiva se identificaron utilizando el método de modelos de sitio M2- y M8- para el gen completo (Tabla 1 complementaria), aunque no en las regiones que interactúan con el ARN y el dominio CTD. En los modelos de sitio, ω (dN/ dS) es<1 which indicates a highly conserved gene (Table 2, Suppl. Table 1). In the branch-site model, the human branch (as well as the primate's branch) was used as the foreground clade, the ω value was low, and no sites with posterior probability greater than 0.85 were identified (Suppl. Table 2).

En particular, para el modelo C de sucursales para el dominio CTD (Tabla complementaria 3), el 33 por ciento de los sitios están evolucionando en la categoría ω0=0. 036. Como los sitios que evolucionan bajo esta categoría no distinguen entre tipos de sucursales, ambos tipos de sucursales tienen el mismo valor de ω para los sitios dentro de esta categoría. Además, el 55 por ciento de los sitios están evolucionando bajo la categoría ω2. Sin embargo, estos tienen valores de ω que están condicionados al tipo de rama (ω20=0.25 y ω21=0). Además, para el modelo C de sitio de ramificación para los 39 genes ortólogos MDA5 (Tabla complementaria 4), el 33 por ciento de los sitios están evolucionando en la categoría ω0=0. 027. Por otro lado, el 41 por ciento de los sitios están evolucionando bajo la categoría ω2. Sin embargo, estos tienen valores de ω que están condicionados al tipo de rama (ω20=0.25 y ω21=15.32).
Análisis estructural
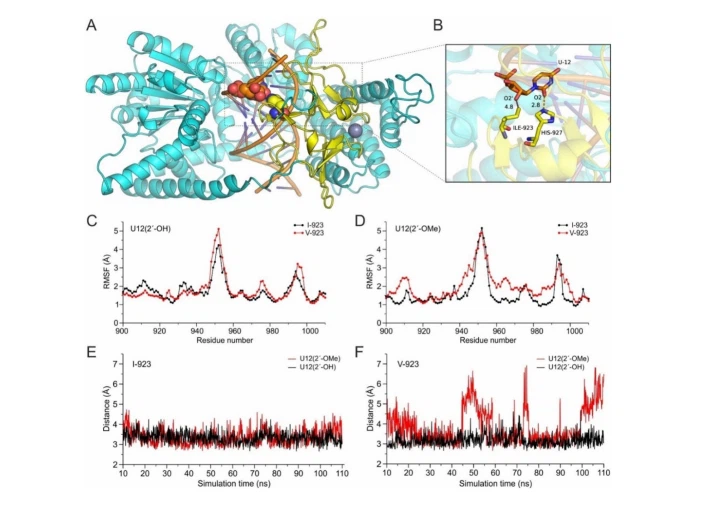
El análisis evolutivo realizado demuestra que la sustitución Ile923Val no es una variante única en la especie humana, ya que Val existe en la posición de la secuencia MDA5 también en otras especies. MDA5 es un receptor viral de ARN de doble cadena (dsRNA) que juega un papel clave en la inmunidad antiviral a través de su especificidad distintiva por el ARN viral (Wu et al. 2013). Se ha demostrado que la metilación en 2′-O del ARNm viral es importante para las respuestas inmunitarias innatas, por lo que se ha sugerido que la metilación en 2′-O es una firma molecular para la distinción entre ARNm propio y no propio. (Zust et al. 2011). Para investigar el papel potencial de la sustitución de Ile923Val en la variante missense IFIH1 rs35667974, analizamos la estructura de criomicroscopía electrónica (cryo-EM) del filamento MDA5-dsRNA en presencia de ATP (PDB ID: 6GKM) (Yu et al. 2018). La posición 923 está ubicada en el bucle 921–927 que interactúa directamente con el dsRNA (Fig. 3A). En particular, Ile923 se encuentra a 4,8 Å de 2′-ΟΗ de uridina U12, y su interacción se estabiliza a través de un enlace de hidrógeno entre el His927 adyacente y la base de uracilo. No se espera que la sustitución de Ile923 por Val en la variante rs35667974 introduzca ningún choque estérico, en lugar de minimizar las interacciones con 2′-ΟΗ de uridina U12 (Fig. 3B). En caso de que el ARN esté metilado en la ribosa de U12, entonces la variante natural de MDA5 con Ile923 muestra un contacto de van der Waals favorable con un grupo 2′-OMe de U12 a 3,6 Å (Fig. 3C), mientras que Val923 de la variante rs35667974 es ubicado en 5.0 Å (Fig. 3D). Estas diferencias no pueden sugerir un efecto importante de la sustitución Ile923Val per se; sin embargo, los cambios estructurales sutiles a menudo conducen a cambios funcionales significativos a través de la interrupción de la dinámica estructural del sistema.

Cálculos de dinámica molecular
Para investigar el efecto de la mutación I923V de MDA5 en su interacción con dsRNA, tanto nativo como 2′-Ο-metilado, hemos empleado simulaciones de dinámica molecular de 4 sistemas en la escala de tiempo 100-ns. La dinámica de los sistemas se controló utilizando las fluctuaciones cuadráticas medias (RMSF) de cada residuo de proteína y la distancia de enlace de hidrógeno de H927 con U12 (Fig. 4). Nuestros cálculos sugieren que la mutación de I923 a V923 en MDA5 resultó en una perturbación menor de la dinámica dentro de la región de contacto del ARN (residuos 923–934) y el bucle de interacción interproteica (950–955) del complejo con dsRNA nativo (Fig. 4C) . Esta observación fue similar en el caso de la 2'-O-metilación en U12, aunque se observó un efecto más pronunciado en la dinámica general de la región carboxi-terminal del mutante MDA5 V923 (Fig. 4D).
Ahora, considerando la interacción clave del enlace de hidrógeno del residuo H927 adyacente con la base de uracilo, nuestras simulaciones MD sugieren que la metilación en 2′-O no lo afecta en el MDA5 nativo (Fig. 4E). Sin embargo, la mutación V923 no afecta el enlace de hidrógeno de H927 en el dsRNA nativo, pero muestra un efecto desestabilizador en presencia de 2′-O-metilación (Fig. 4F). En conjunto, nuestras simulaciones MD sugieren que aunque el efecto de la mutación I923V de MDA5 en la interacción con dsRNA nativo es marginal, su efecto en la dinámica y estabilidad del complejo MDA5/RNA es más significativo cuando el uracilo está 2′-O-metilado. .

Discusión
Este estudio representa una investigación evolutiva y estructural del papel de la variante rs35667974 compartida del locus autoinmune IFIH1, que se informó que conduce a un fenotipo de funcionalidad modificada para MDA5 (Downes et al. 2010). La aplicación de modelos de sitio evolutivo y sitio de ramificación para realizar análisis de selección positiva indica que no hay sitios de selección positiva en los sitios de interacción de ARN donde reside el polimorfismo rs35667974. Ninguno de los modelos de sucursales indica que ningún sitio en particular haya sufrido una selección positiva en el dominio CTD.
Esto está de acuerdo con las muy bajas frecuencias de aparición de la variante Ile923Val incluso entre la población humana (Tabla 1). Sin embargo, la población europea en comparación con las demás tiene una diferencia en la frecuencia del alelo C de un orden de magnitud. Sin olvidar el reducido tamaño muestral, la distribución geográfica del polimorfismo objeto de estudio muestra que su aparición en la población europea como punto de partida puede deberse a condiciones de vida y alimentación que han cambiado en los últimos años. La investigación estructural del papel del SNP examinado se realizó examinando la estructura del complejo dsRNA-MDA5 (nativo y mutante).
A nivel de formación del complejo dsRNA-MDA5, la introducción de la mutación Ile923Val influye en la interacción del dominio C-terminal de la proteína (CTD) con el dsRNA con la introducción de una cavidad hidrófoba junto al azúcar ribosa de la cadena única del dsRNA . Hemos demostrado que en el caso del ARN metilado en la cadena de fosforribosilo de una hebra, otros efectos dinámicos pueden influir en la interacción del mutante sin afectar al tipo salvaje. Esto está de acuerdo con los estudios experimentales (Looney et al. 2015; Brisse y Ly 2019) que muestran que el efecto del polimorfismo Ile923Val identificado en la vecindad de un punto de interacción MDA5-dsDNA puede no influir en las propiedades nativas de unión de dsRNA, pero alterado por 2. 5- veces la reducción de la actividad catalítica (Shigemoto et al. 2009). Además, los estudios de dinámica molecular han demostrado el papel crítico de la metilación en el mutante con respecto a la movilidad y estabilidad de los bucles MDA5 941–959 y 970–977 involucrados en la interacción del ARNds y la interacción interproteica en la formación del filamento MDA. Dichos efectos pueden dificultar el ensamblaje del filamento MDA5, la asociación MDA5-MAVS y el ensamblaje del filamento MAVS que activan aún más la expresión de los genes del interferón tipo I (IFN1: IFN e IFN). En los casos de T1D y PsA, como consecuencia, los niveles reducidos de actividad de la proteína MDA5 y, por lo tanto, la menor producción de IFN protege contra la autoinmunidad. Estas observaciones sugieren que varias variantes de IFIH1, predichas para afectar la interacción de MDA5 con MAVS y la reducción de la producción de IFN, disminuirían el riesgo de enfermedades, mientras que la función normal de MDA5 está asociada con ellas (Shigemoto et al. 2009).
Esto lleva a la conclusión de que, como en el caso del ARN viral, la metilación del propio ARNds, una mutación identificada en el ARN, es un factor importante de selección/activación para la introducción de efectos protectores en algunas enfermedades autoinmunes. Los resultados del presente estudio amplían el conocimiento de la importancia biológica del SNP rs35667974 del locus IFIH1 en el desarrollo de las enfermedades antes mencionadas y resaltan la importancia de los estudios de genes compartidos por múltiples enfermedades autoinmunes. Sin embargo, en estudios de población para la asociación genética de SNP con enfermedades autoinmunes, utilizando, por ejemplo, PCR-RFLP, secuenciación o chips de genotipado, no se tiene en cuenta un caso de metilación del ARN. Por lo tanto, es importante conocer el estado de metilación del dsRNA que interactúa y su efecto sobre el alelo MDA5. Como en el caso del reconocimiento de dsRNA viral (Wu et al. 2013) y la distinción entre mRNA propio y no propio (Züst et al. 2011), la pérdida de un grupo metilo del MDA5 que interactúa, como en el caso del mutante Ile923Val MDA5, puede afectar la formación de filamentos y la inducción de interferón tipo I.
Es de destacar que Plenge et al. (2013) habían discutido previamente el potencial de una variante rara en un gen de enfermedad causal para representar un objetivo terapéutico putativo para la intervención farmacéutica. Para ello, es necesario conocer la función biológica de la variante causal en cualquier intento de vincular los hallazgos genéticos con una nueva diana terapéutica. Por lo tanto, localizar la posición de una variante causal en la estructura 3D de la proteína respectiva e investigar su papel desde el punto de vista estructural/funcional en una vía patogénica que conduce a una enfermedad autoinmune parece ser de importancia fundamental para el manejo posterior y un mejor tratamiento de la enfermedad. los pacientes. Sigue existiendo una necesidad suprema de ir más allá del descubrimiento de SNP asociados a una comprensión más profunda de las variantes causales para dilucidar los mecanismos moleculares y las vías de la enfermedad. Se requiere un análisis estructural-funcional adicional para investigar la unión de ribosa-2'-Ο-metilado auto-dsRNA a MDA5 y cómo esto afecta el ensamblaje de fibrillas de MDA5. El escurridizo papel biológico 2′-Ο-metilado del ARNm como sensor de distinción entre ARNm viral y propio en la inducción de interferón tipo I puede haberse extendido a un sensor protector en ciertas autoinmunopatías.

Conclusión
El raro polimorfismo del gen rs35667974 IFIH1 protege contra la diabetes tipo 1, PS y PsA, mientras que el alelo IFIH1 que porta la mayoría de la población predispone a las enfermedades. El hecho de que el mutante Ile923Val MDA5 funcione de manera diferente en la interacción con el dsRNA propio y, en particular, con el 2′-O-metilado sugiere que, en algunos casos, las variantes que interactúan con el dsRNA metilado interrumpen la formación de filamentos MDA5, la interacción MAVS y la formación de filamentos, y La señalización de IFN, como en la respuesta antiviral del huésped, puede haber sido seleccionada negativamente porque confiere protección contra enfermedades.
Contribuciones de autor
Conceptualización: AA, AP, EEE y GNG, metodología: AA, AP y EEE, validación: AA, AP, MIZ, GNG y EEE, investigación: GNG, AA, AP y MIZ, recursos: GNG, AA, AP y MIZ, conservación de datos: AA y AP, redacción y preparación del borrador original: EEE, GNG, AA, AP y MZ, redacción, revisión y edición del manuscrito: AA, AP, MZ, GNG y EEE, visualización: AA, AP y EEE, supervisión: EEE y adquisición de fondos: EEE. Todos los autores han leído y aceptado la versión publicada del manuscrito.
Fondos
El financiamiento de acceso abierto es proporcionado por HEAL-Link Grecia. Este trabajo fue apoyado por el proyecto "INSPIRED-The National Research Infrastructures on Integrated Structural Biology, Drug Screening Eforts and Drug Target Functional Characterization" (Subvención MIS 5002550), que se implementa bajo la Acción "Refuerzo de la Infraestructura de Investigación e Innovación" financiado por el Programa Operativo "Competitividad, Emprendimiento e Innovación" (NSRF 2014-2020) y cofinanciado por Grecia y la Unión Europea (Fondo Europeo de Desarrollo Regional).
Disponibilidad de datos
Los conjuntos de datos utilizados y/o analizados durante el estudio actual están disponibles a pedido del autor correspondiente.
Declaraciones
Conflicto de intereses
Los autores declaran no tener conflicto de intereses. Los financiadores no tuvieron ningún papel en el diseño del estudio; en la recopilación, análisis o interpretación de datos; en la redacción del manuscrito, o en la decisión de publicar los resultados.
Aprobación ética
No aplica.
Consentimiento para participar
No aplica.
Consentimiento para Publicación
No aplica.

Acceso abierto
Este artículo tiene una licencia Creative Commons Attribution 4.0 International License, que permite el uso, el intercambio, la adaptación, la distribución y la reproducción en cualquier medio o formato, siempre que se otorgue el crédito correspondiente al autor o autores originales. ) y la fuente, proporcione un enlace a la licencia Creative Commons e indique si se realizaron cambios. Las imágenes u otro material de terceros en este artículo están incluidos en la licencia Creative Commons del artículo a menos que se indique lo contrario en una línea de crédito al material. Supongamos que el material no está incluido en la licencia Creative Commons del artículo y el uso previsto no está permitido por la normativa legal o excede el uso permitido. En ese caso, debe obtener el permiso directamente del titular de los derechos de autor.
Referencias
1. Aduri R, Psciuk BT, Saro P et al (2007) Parámetros de campo de fuerza AMBER para los nucleósidos modificados de origen natural en el ARN. J Chem Theory Comput 3: 1464–1475.
2. Altschul SF, Madden TL, Schäfer AA et al (1997) Gapped BLAST y PSI-BLAST: una nueva generación de programas de búsqueda de bases de datos de proteínas. Ácidos nucleicos Res 25:3389–3402.
3. Andreou A, Giastas P, Christoforides E, Eliopoulos EE (2018) Información estructural y evolutiva dentro de la familia de genes de polisacárido desacetilasa de bacillus anthracis y bacillus cereus.
4. Aučynaitė A, Rutkienė R, Tauraitė D et al (2018) Identificación de una hidrolasa de nucleósido de 2′-O-metiluridina utilizando las bibliotecas metagenómicas. Moléculas.
5.Berman HM, Westbrook J, Feng Z et al (2000) El banco de datos de proteínas. Ácidos nucleicos Res 28:235–242.
6. Bielawski JP, Yang Z (2004) Un método de máxima probabilidad para detectar la divergencia funcional en sitios de codones individuales, con aplicación a la evolución de la familia de genes.
7. Biros E, Jordan MA, Baxter AG (2005) Genes que median las interacciones ambientales en la diabetes tipo 1.
8. Boccaletto P, Machnicka MA, Purta E, et al (2018) MODOMICS: una base de datos de vías de modificación de ARN. actualización 2017. Ácidos nucleicos Res 46:D303–D307.
9. Brisse M, Ly H (2019) Análisis comparativo de estructura y función de los receptores similares a RIG-I: RIG-I y MDA5.
10. Budu-Aggrey A, Bowes J, Stuart PE et al (2017) Un alelo de codificación raro en IFIH1 es protector para la artritis psoriásica. Ann Rheum Dis 76:1321–1324.
For more information:1950477648nn@gmail.com
