Las Células Intercaladas Del Riñón Son Fagocíticas Y Acidifican Escherichia Coli Uropatógena Internalizada
Feb 28, 2022
Riñónlas células intercaladas están involucradas en la homeostasis ácido-base a través de la expresión vacuolar de ATPasa. Aquí informamos seis subtipos de células intercaladas humanas, incluidas las células intercaladas principales híbridas identificadas a partir de la transcriptómica de células individuales. La maduración del fagosoma es un proceso biológico que aumenta en el rango de análisis de vías biológicas después de la exposición a Escherichia coli uropatógena en dos de los subtipos de células intercaladas. Visualización de microscopía confocal en tiempo real de murinorenalLos túbulos perfundidos con proteína verde fluorescente que expresan Escherichia coli o pHrodo Green E. coli BioParticles demuestran que las células intercaladas fagocitan activamente las bacterias y luego acidifican los fagolisosomas. Además, las células intercaladas han aumentado la expresión de ATPasa vacuolar después de una UTI experimental in vivo. En conjunto, las células intercaladas exhiben una respuesta transcripcional conducente a lariñóndefensa, engullir bacterias y acidificar las bacterias internalizadas. Las células intercaladas representan una célula epitelial con características de fagocitos profesionales como los macrófagos.
Palabras clave:enfermedad renal;tejido renal;células renales;riñón; renal
El túbulo colector del riñón es la ubicación terminal para la regulación ácido-base 1 . El túbulo colector consta de células principales y células intercaladas (CI). Las células principales (PC) median la reabsorción de agua y sal y se caracterizan por la acuaporina citoplasmática 2 (AQP2) 2 . Los CI ayudan a mantener la homeostasis ácido-base y tienen tres subtipos descritos, tipo A (A-IC), tipo B (B-IC) y no A-no B 2,3. Los A-IC secretan protones a través de la H-ATPasa vacuolar apical (V-ATPasa) y regeneran bicarbonato a través del transportador basilar de cloruro/bicarbonato (Cl − /HCO 3 ), intercambio aniónico 1 (AE1/banda 3/SLC4A1) 1,4 . Los B-IC secretan HCO 3 − a través de un transportador apical de Cl − /HCO 3 , pendrina (SLC26A4), y expresan V-ATPasa 2,3 basolateral. Los CI no A-no B de roedores tienen pendrina apical y V-ATPasa, pero no AE1, y se han identificado en el conducto colector y el túbulo conector (CNT) 3 . Cada vez hay más pruebas que respaldan una función inmunitaria innata de los circuitos integrados junto con su función tradicional de regulación del pH. En primer lugar, la mayoría de diez pacientes no relacionados con distalrenalacidosis tubular, una condición caracterizada por disfunción del CI, se informó que tenían antecedentes de ITU 5 . En segundo lugar, Escherichia coli uropatógena (UPEC), el organismo aislado en el 70 por ciento de la pielonefritis aguda en hombres y en el 80 por ciento en mujeres, se localiza selectivamente en el citoplasma de los IC 6,7. En tercer lugar, identificamos que los CI expresan péptidos antimicrobianos (AMP), como la ribonucleasa 7 (RNASE7) 8–11. Estos AMP tienen actividad directa contra una variedad de patógenos, incluidas las bacterias, al inicio y/o en respuesta a la infección 8–11. En cuarto lugar, nosotros y otros hemos informado de forma independiente que los ratones con desarrollo anormal de IC tienen una mayor susceptibilidad a las infecciones del tracto urinario (ITU) y/o pielonefritis 12,13. En quinto lugar, los CI detectan y median la inflamación 14 . Por último, hemos demostrado la expresión de genes inmunitarios innatos en IC murinos aislados 15,16

CITANCHE MEJORARÁ LA FUNCIÓN RENAL/RENAL
Es importante comprender cómo los CI defienden el tracto urinario de la infección porque las ITU se encuentran con frecuencia. Más del 50 por ciento de las mujeres experimentan una ITU durante su vida, y las ITU representan del 1 al 6 por ciento de todas las visitas médicas 17 . Cuando las bacterias ascienden alriñonesresultando en pielonefritis, las posibles complicaciones incluyen hipertensión,enfermedad del riñony urosepsis 18,19 . Aproximadamente 250,000 casos de pielonefritis ocurren anualmente en los Estados Unidos 17 . La resistencia a múltiples fármacos está emergiendo como un desafío crítico en relación con el tratamiento de las infecciones urinarias y otras infecciones 20 . Por lo tanto, los mecanismos que utilizan los CI para defenderse de los uropatógenos ascendentes podrían ser dianas terapéuticas que podrían explotarse para desarrollarriñón-terapia específica de la pielonefritis. Debido a que la mayoría de los estudios de IC involucran modelos animales, se necesitará una mejor comprensión de los IC humanos para guiar los estudios de ciencia básica hacia una mejor atención clínica.
Porque elriñónes un órgano complejo, los perfiles de ARNm pueden ser difíciles de interpretar. Por ejemplo, la nefrona tiene una especialización regional con distintos segmentos tubulares y subtipos de células. losriñóncontiene células endoteliales, epiteliales, intersticiales e inflamatorias reclutadas, todas con distintas funciones biológicas y patrones de expresión génica. La secuenciación de ARN de una sola célula (scRNA-seq) representa una metodología de rápido avance para identificar y perfilar distintos tipos de células al inicio o en respuesta a factores estresantes 21 . Aquí, mostramos usando la tecnología scRNA-seq que humanosriñónLos circuitos integrados constan de seis subconjuntos diferentes que incluyen tres A-IC, un IC-PC híbrido, un IC nonA-nonB y un B-IC. El análisis de la velocidad del ARN reveló un cambio transcripcional de las PC hacia los subconjuntos A-IC tras la exposición a UPEC. Ingenuity Pathway Analysis reveló que la maduración del fagosoma es la vía biológica clave en un subconjunto A-IC tras la exposición a UPEC. Dentro de esta vía, las V-ATPasas son los componentes clave involucrados. Utilizamos microscopía intravital para visualizar la captación de UPEC in vivo por los CI y confirmamos la acidificación de la UPEC internalizada en estos CI. Finalmente, un modelo de UTI murina demostró un aumento en la expresión de ARNm de V-ATPasa (Atp6v1b1). Este estudio proporcionará la base para explorar y manipular terapéuticamente las células epiteliales que expresan V-ATPasa como fagocitos bacterianos.
Resultados
Los IC humanos se pueden enriquecer a través de la clasificación de células activadas magnéticamente (MACS) con perlas magnéticas recubiertas del receptor del factor de crecimiento de células madre/mastocitos (CD117/c-KIT). Humanoriñóntejido, principalmente de los márgenes normales deriñónresecciones masivas, se diseccionó en piezas de 2–4- mm y luego se envió durante la noche a nuestro laboratorio en medio Eagle modificado de Dulbecco (DMEM) en hielo por la Red Cooperativa de Tejidos Humanos [https://www.chtn.org]. Evaluamos c-KIT como marcador de superficie celular para clasificar los circuitos integrados humanos porque c-KIT se ha utilizado con éxito para este propósito en ratones 22 . La expresión de c-KIT se localizó en IC humanos según el hallazgo de que c-KIT y el marcador de IC humano V-ATPasa, subunidad B1 (gen ATP6V1B1), comarcaron las mismas células en humanosriñónsección (Suplemento-mentary Fig. 1) 22,23 . Después de la clasificación magnética que incluyó la eliminación de células inmunitarias CD45 plus y células muertas; el enriquecimiento de los CI presuntos positivos para c-KIT se demostró mediante la expresión del ARNm de ATP6V1B1 que aumentó 8 12- veces en las células positivas para c-KIT en comparación con las células negativas para c-KIT. Tanto SLC4A1 como SLC26A4 se enriquecieron de forma variable en IC, lo que demuestra que tanto el enriquecimiento A-IC como el B-IC son posibles con esta metodología (Fig. 2 complementaria). Los antecedentes del tejido renal utilizado en este estudio se presentan en la Tabla complementaria 1.
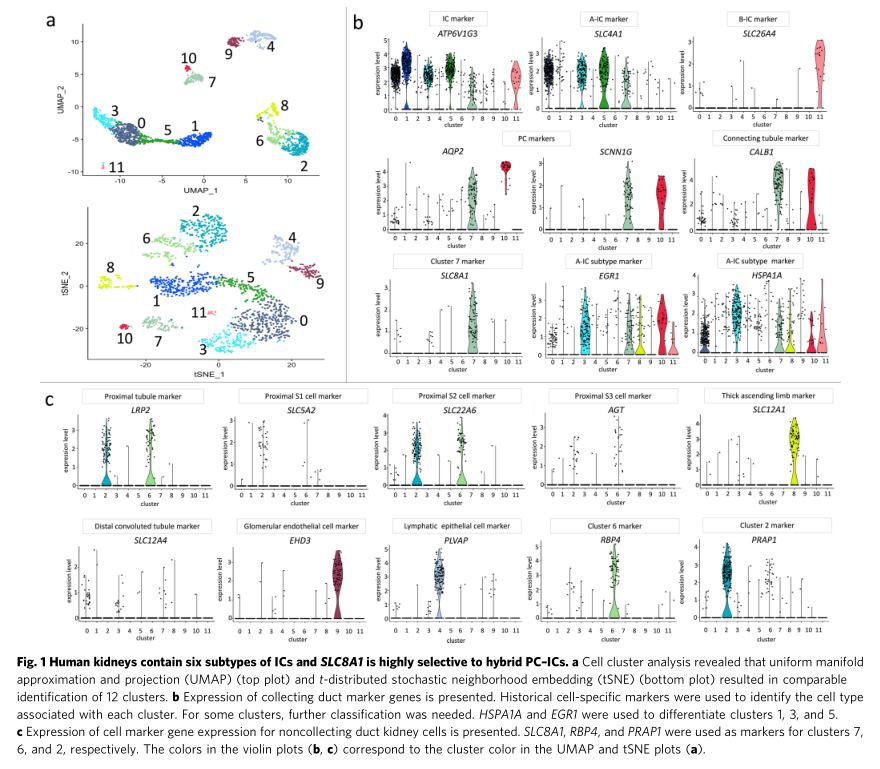
El análisis de conglomerados integrado identificó seis subtipos de CI.ScRNA-seq se completó en 1861 disociadoriñóncélulas que se enriquecieron para IC como se describe anteriormente. Los CI enriquecidos se obtuvieron de los márgenes normales de un soloriñónresección masiva. El filtrado de control de calidad (QC) pasó por 859 células expuestas a UPEC in vitro durante 1 hy 1002 células expuestas a solución salina in vitro durante 1 h. El análisis de función de Seurat identificó 12 grupos en la preparación de células clasificadas (Fig. 1a). Los nueve marcadores más conservados dentro de cada grupo se presentan en las figuras complementarias. 3–14. En general, los subtipos de CI representaron 1066 (57 por ciento) de las 1861 células. Seis de los grupos representaban subtipos de CI. Específicamente, encontramos tres subtipos A-IC, uno B-IC, uno no A-nonB-IC y uno híbrido PC-IC.RiñónEn la nomenclatura de células epiteliales recomendada por Chen y sus colegas, se usaron marcadores conservados que previamente se informó que eran marcadores de tipo celular o marcadores conservados que diferenciaban uno de los 12 grupos de otros para asignar un tipo de célula a cada grupo (Tabla complementaria 2 , Fig. 1b, c, Fig. 2) 24–28 .
El subtipo A-IC y la expresión de la proteína híbrida PC-IC se correlacionan con los resultados de scRNA-seq. Validamos hallazgos clave de scRNA-seq, en particular que SLC8A1 (también conocido como Na más /Ca más intercambiador 1 (NCX1)) es un marcador para PC-IC híbridos y que la familia de proteínas de choque térmico A (Hsp70) miembro 1A (HSPA1A) junto con la respuesta de crecimiento temprano 1 (EGR1) son marcadores que pueden diferenciar los subtipos A-IC (Fig. 3). Debido a que usamos los márgenes normales deriñónresecciones de cáncer, validamos que nuestro SLC8A1, HSPA1A y EGR1riñónlos patrones de expresión eran consistentes con los observados en personas normalesriñóntejido del Human Protein Atlas disponible en http://www.proteinatlas.org (Figura complementaria 15) 29
Recopilación de perfiles de marcadores de subtipos de células del conducto demostrados previamente en murinosriñónlas células permanecen en gran parte intactas en humanosriñóncélulas. Debido a que será importante contextualizar los hallazgos futuros del modelo murino en la fisiopatología humana, evaluamos la expresión de IC humana de los marcadores de células del conducto colector murino identificados previamente en estudios de scRNA-seq realizados por Chen et al. 22 y Ransick et al. 30 . En la Fig. 4 se presenta un diagrama de puntos de los resultados. Los marcadores de tipo celular del conducto colector murino se conservan principalmente en las células del conducto colector humano.
A-IC subtipo A aumenta en porcentaje relativo con 1 h de exposición a UPEC. Los porcentajes de celdas dentro de los grupos fueron consistentes entre el tipo de exposición con la excepción del subtipo A/grupo A-IC 0, que aumentó del 16,2 al 20,1 por ciento, y el subtipo C A-IC/grupo 5, que disminuyó del 9,4 a 6,6 por ciento, con exposiciones a solución salina frente a UPEC, P =0,03 (Tabla 1).
Las células híbridas PC-IC cambian su velocidad de ARN alejándose de las PC y hacia las A-IC en respuesta a 1 h de exposición a UPEC. La abundancia relativa de los pre-ARNm no empalmados recientemente transcritos frente al ARNm empalmado maduro se puede utilizar para calcular el cambio en la abundancia del ARNm, denominado velocidad del ARNm 31 . Una velocidad de ARNm positiva en estudios de una sola célula indica que los genes se regulan al alza, mientras que una velocidad de ARNm negativa significa que los genes se regulan a la baja 31 . La dirección de la velocidad del ARN infiere que una célula tiene una trayectoria de expresión de ARNm hacia otro tipo celular 31,32. La velocidad del ARNm en respuesta a la exposición a la UPEC se presenta en la Fig. 5. Es importante que los PC-IC híbridos cambien su velocidad de ARN alejándose de las PC y hacia los IC en respuesta a la UPEC. Además, los CI mantienen su actividad de transcripción, mientras que la actividad transcripcional se vuelve mínima en otrosriñóntipos de células
El perfil inmunitario innato del riñón demuestra algunos cambios tempranos en la expresión de una sola célula después de 1 h de exposición a UPEC.Los patrones de expresión de scRNA-seq de genes inmunitarios innatos seleccionados después de la exposición a UPEC frente a solución salina durante 1 h se presentan en las Figs. 16 y 17. Los hallazgos clave incluyen una alta expresión de la adrenomedulina AMP (ADM) en los subtipos A y B de A-IC, PC-IC híbridos y B-IC. Las PC no expresan adrenomedulina al inicio, pero tienen una expresión significativamente mayor en respuesta a la exposición a UPEC. La expresión de la proteína que contiene SH2- inducible por citoquinas (CISH) y la barrera para el factor de autointegración 1 (BANF1) se induce significativamente en los CI no A-no B después de la exposición a UPEC. Interleucina 18 (IL18), galectina 3 (LGALS3), beta defensina 1 (DEFB1) y transductor de señal CD24 lipocalina 2/lipocalina asociada a gelatinasa de neutrófilos (LCN2/NGAL) solo se identificó

en PC-IC híbridos y solo estaba presente una expresión mínima de ARNm del receptor 4 tipo toll. No identificamos la expresión de ribo-nucleasa 7 (RNASE7) en scRNA-seq. Evaluamos la expresión de ARNm de RNASE7 en IC y no IC combinados clasificados magnéticamenteriñóncélulas. La expresión de ARNm de RNASE7 se identificó en los circuitos integrados de uno de cuatroriñones(Fig. 18 complementaria).
El proceso biológico de maduración del fagosoma está asociado con los CI expuestos a UPEC durante 1 hora.Las diez rutas biológicas principales asociadas con cada grupo se clasificaron por valor de p según lo determinado por Ingenuity Pathway Analysis. Tres grupos asignados a conductos colectores A-IC subtipo A/grupo 0, A-IC subtipo B/grupo 3 y A-IC subtipo C/grupo 5 tenían procesos de vías biológicas diferenciales después de la exposición a UPEC en comparación con la solución salina (Fig. 6a–c). La maduración del fagosoma fue la función mejor clasificada en las células expuestas a UPEC y solución salina en A-IC subtipo C/grupo 5, pasó de la segunda a la primera posición en A-IC subtipo A/grupo 0 y de la cuarta a la tercera posición más alta en A-IC subtipo B/grupo 3. Ninguno de los subtipos restantes de células del conducto colector (Fig. 19 complementaria) tenía las diez principales vías asociadas que eran diferentes después de la exposición a UPEC en comparación con la solución salina. El perfil de expresión génica que resultó en la clasificación de la maduración del fagosoma para el subtipo A/grupo A-IC 0 se presenta en la Tabla complementaria 3.
La expresión del ARNm de IC Atp6v1b1 aumenta en respuesta apielonefritis experimental in vivo.La ruta de maduración del fagosoma de Ingenuity destacó que la V-ATPasa está involucrada en los circuitos integrados (Tabla complementaria 3). Para determinar si la V-ATPasa se activa tras la exposición a UPEC, utilizamos un modelo de UTI murino. Una hora después de la inoculación transuretral de UPEC frente a solución salina, los ratones "IC reporter", que tienen expresión de tdTomato (tdT, una variante de proteína fluorescente roja) en IC, se sacrificaron y los IC se enriquecieron a partir de disociadoscélulas renales. Los IC enriquecidos tenían una mayor expresión de ARNm de Atp6v1b1 en ratones con inoculación de UPEC en comparación con el control de solución salina (Fig. 6d).
Los circuitos integrados fagocitan UPEC in vivo.Desarrollamos una metodología para perfundir un soloriñóntúbulo con UPEC en un ratón vivo con un intactoriñón.Se visualizaron agregados de UPEC que expresan proteína fluorescente verde (GFP) microperfundidos en un solo lumen de túbulo renal de ratones "IC reporter" fluyendo a través de túbulos, adhiriéndose selectivamente a la superficie luminal y siendo internalizados por IC (Fig. 7) durante la microscopía intravital.
Los circuitos integrados acidifican los fagolisosomas que contienen UPEC in vivo yin vitro.También perfundimos los túbulos con biopartículas de E. coli pHrodo Green que solo emiten fluorescencia cuando se acidifican. La absorción y la fluorescencia de estas biopartículas solo se visualizaron durante la microscopía intravital en los IC (Fig. 8). El análisis de segmentación de Imaris demostró que la fluorescencia verde aumentó significativamente con el tiempo en tdT más IC dentro de 2 túbulos perfundidos con pHrodo Green E. coli BioParticles en comparación con un control tdT más túbulo (Fig. 9a, b). Cuando se evaluó la fluorescencia sobre una base celular, 12/16 (75 por ciento) de células tdT plus demostraron un aumento en la fluorescencia verde con el tiempo después de la perfusión tubular con biopartículas de E. coli pHrodo Green (Fig. 9b). Los resultados de la regresión lineal de cada celda se presentan en la Tabla complementaria 4. Los hallazgos de imágenes intravitales en vivo in vivo de fagocitosis y acidificación de biopartículas de E. coli PHrodo Green por IC se validaron mediante un ensayo de citometría de flujo in vitro. murinocelula renalSe expuso una suspensión de ratones "IC reporter" en los que los IC (CD45 - tdT plus) expresan endógenamente tdT a biopartículas de E. coli pHrodo Green frente a células con medio solo. Las células inmunitarias residentes CD45 más en suspensión celular se seleccionaron como control positivo y las células CD45 − tdT − (no IC) se seleccionaron como control negativo. Comparando los medios solos con

exposición a biopartículas, la fluorescencia verde indicativa de adquisición y acidificación de biopartículas aumentó de {{0}}.7 a 62.8 por ciento de células CD45 plus. Este hallazgo demuestra la captación bacteriana esperada por fagocitos profesionales como los neutrófilos. Curiosamente, el 22,2 % de los IC absorbieron biopartículas verdes en comparación con el 5,6 % de los no IC (Figura complementaria 20), el control de medios absorbió el 0,7 % de los IC y el 0 % de los no IC.
Discusión
Los circuitos integrados son difíciles de estudiar, particularmente en humanos, porque comprenden solo el 7 por ciento deriñónLas células, consisten en una variedad de subtipos, y no retienen su fenotipo en cultivo 33 . Chen et al. 22 informaron análisis unicelulares en murinosriñóncélulas y Lake et al. informó una tubería de secuenciación de ARN de un solo núcleo en humanosriñóncélulas 34,35 . Estos estudios identificaron dos subtipos de A-IC. Aquí, hemos desarrollado una metodología para realizar la secuenciación de una sola célula en circuitos integrados humanos enriquecidos viables. Enriquecimos los circuitos integrados viables en lugar de secuenciar todosriñónceldas para permitir un mayor enfoque en este tipo de celda. Nuestros hallazgos principales fueron (a) la identificación de que los PC híbridos-IC pueden cambiar la dirección de la velocidad del ARN lejos de las PC y hacia los A-IC en respuesta a la exposición a UPEC, (b) existen al menos tres subtipos de A-IC y su relación las frecuencias pueden cambiar en respuesta a la exposición a UPEC, (c) la maduración del fagosoma es una vía biológica líder en múltiples subtipos A-IC y puede aumentar en importancia relativa con la exposición a UPEC, y (d) los IC fagocitan y acidifican UPEC in vivo durante la obtención de imágenes de animales vivos. ratones.
Los CI se diferencian en respuesta a la acidosis invirtiendo su polaridad 36,37. Se ha informado que los CI surgen de células que expresan AQP2- 38 . En 2017, Chen y sus colegas identificaron células doblemente positivas que expresaban Aqp2 junto con Slc4a1 o Slc26a4 mediante perfiles de células individuales murinas. Estos hallazgos fueron validados por Park y colegas al año siguiente 22,35 . En 2019, demostramos mediante el inmunomarcaje de proteínas y ARNm que existen PC-IC híbridos 15 . Específicamente, el 9 por ciento de los CI murinos definidos por inmunomarcaje fluorescente con V-ATPasa B1 también expresaron ARNm de Aqp2 definido por hibridación fluorescente in situ 15 . El presente estudio definió una población de humanosriñón-Células de los conductos colectores que expresan AQP2, ATP6V1G3 y SLC4A1 en consonancia con los PC-IC híbridos. En los gráficos tSNE y UMAP, estas células híbridas se agruparon más cerca de las PC, pero eran distintas de las PC tradicionales según la expresión del marcador IC. La expresión de SLC8A1 era distinta a este tipo de células. Curiosamente, SLC8A1 está muy involucrado en la transición epitelial a mesenquimatosa. Específicamente, la ausencia de SLC8A1 transforma los fenotipos de las células epiteliales a través de la desestabilización de la E-cadherina mediada por -catenina 39 . Aquí, demostramos que los circuitos integrados se diferencian en respuesta a la exposición a uropatógenos. Las células PC-IC híbridas cambian su velocidad de ARN, la derivada temporal de la expresión de ARNm, lejos de las PC y hacia A-IC en respuesta a la UPEC. En ratones, Ransick et al. 30 identificaron la expresión de Slc8a1 principalmente en el túbulo contorneado distal y células que se asemejan a PC en el túbulo conector. En nuestras imágenes de microcopia confocal que evalúanriñónExpresión de SLC8A1, encontramos células aisladas que expresaban SLC8A1 en túbulos positivos para AQP2-(p. ej., conductos colectores o túbulos de conexión). También identificamos túbulos negativos AQP2-en los que la mayoría de las células expresaban SLC8A1, lo que podría ser coherente con la expresión de Slc8a1 del túbulo contorneado distal antes mencionada en ratones. Algunos subtipos de A-IC tienen vías biológicas principales diferenciales después de la exposición a UPEC y el subtipo A de A-IC aumentó en frecuencia relativa en respuesta a UPEC. Estos hallazgos indican que el subtipo A de A-IC puede representar una variante inmunitaria innata. El papel de SLC8A1 en la diferenciación de IC justifica la investigación en estudios futuros.

LA CITANCHE MEJORARÁ LA INSUFICIENCIA RENAL/RENAL
Realizamos scRNA-seq en 1861 humanosriñóncélulas de las cuales 1066 eran circuitos integrados. Para contextualizar los modelos experimentales murinos a la fisiopatología humana, será importante comparar los circuitos integrados humanos y murinos. Chen y sus colegas enriquecieron IC murinos con c-KIT y realizaron scRNA-seq 22 . Clasificaron 74 celdas como PC, 87 como A-IC y 23 celdas como B-IC 22 . Ransick et al. 30 realizaron scRNA-seq en 688 IC. No enriquecieron para los IC, sino que dividieron elriñónen la corteza, el bulbo raquídeo interno y el bulbo raquídeo externo para evaluar las diferencias zonales 30 . Demostramos que la expresión del marcador de tipo de célula del conducto colector murino parecía estar conservada en gran medida en las células del conducto colector humano. Si los ratones tienen subtipos A-IC comparables a los humanos probablemente requerirá una evaluación unicelular específica de un mayor número de IC murinos.
Identificamos la expresión de scRNA-seq IC de proteínas inmunitarias innatas, como el mediador inmunitario e inflamatorio galectina 3 (LGALS3) y el ADM que hemos informado previamente en IC de roedores 15,40–42. Sin embargo, algunas proteínas inmunitarias innatas clave informadas anteriormente en los CI, como la lipocalina 2 (LCN2/NGAL), RNASE7 y el receptor tipo toll 4 (TLR4) tenían una expresión mínima o no se observaron en los CI humanos a nivel de una sola célula en nuestro análisis 6,9 . La escasez de expresión de LCN2/NGAL y TLR4 en los circuitos integrados es consistente con lo informado en los circuitos integrados murinos por nuestro grupo de investigación junto con Ransick et al. 30riñónexplorador de celdas/] 15 . Chen et al. 22 informaron alguna expresión de ARNm de TLR4 y NGAL en IC, pero varias veces menos que en PC. Evaluamos los IC humanos agrupados para la expresión de RNASE7 y lo identificamos en IC de 1 de 4riñones(Fig. 18 complementaria), lo que indica que su expresión puede ser intermitente según la región, el momento y las condiciones fisiológicas. Se ha demostrado que la expresión de CISH, que se induce en CI no A no B en respuesta a UPEC, regula la respuesta inmune innata a Mycobacterium tuberculosis en el pulmón y el bazo 43 . Los circuitos integrados fagocitaron bacterias durante varios minutos, y nuestras células para scRNA-seq se expusieron a UPEC durante un período de tiempo relativamente corto de 1 hora. Se necesitan estudios futuros para determinar si otras vías de IC, como la expresión de AMP o la regulación de la muerte celular, se vuelven más prominentes en puntos de tiempo posteriores a la exposición a UPEC.
Phagocytosis involves the cellular uptake of particulates >0.5 μm por la envoltura de la membrana plasmática 44 . Los "fagocitos profesionales", células inmunitarias derivadas de mieloides, incluidos macrófagos, neutrófilos y osteoclastos, diferencian los microbios invasores de la microbiota y las células sanas, engullen el objetivo en un fagosoma, generan especies reactivas de oxígeno (ROS), secretan AMP y presentan antígenos para otras celdas 45–49 . De importancia, la acidificación robusta por V-ATPasa de los fagolisosomas creando un microambiente ácido suficiente para matar a la mayoría de los microbios es una característica distintiva de los fagocitos profesionales 48,50. Por ejemplo, la inhibición de la V-ATPasa con bafilomicina A1 suprime la actividad bactericida de los macrófagos 51 . Ciertas células epiteliales fagocitan microbios pero son menos eficientes en la eliminación de bacterias que los fagocitos profesionales y se han descrito como fagocitos no profesionales 52 . Los IC representan un linaje epitelial que tiene capacidades de fagocitosis y presentación de antígenos (figs. 6-9) junto con una expresión robusta de AMP y abundantes mitocondrias para generar ROS; por lo tanto, los CI parecen tener un potencial de eliminación de bacterias más comparable al de los macrófagos que los fagocitos no profesionales antes mencionados 8,53–55. Se ha demostrado previamente que los A-IC son capaces de alcanzar altas tasas de endocitosis apical de dextrano en vesículas citoplasmáticas 56 . Especulamos que la fagocitosis IC de UPEC es una extensión de las características compartidas con los macrófagos, incluida la expresión de V-ATPasa, el potencial redox, la secreción de AMP y las capacidades de endocitosis 8,16,49,57,58. Queda por determinar si los IC pueden fagocitar desechos celulares y bacterias distintas de UPEC de manera similar a los fagocitos profesionales.
Imágenes confocales de un soloriñóntúbulo perfundido in vivo con bacterias amplía las técnicas in vitro anteriores como el cultivo celular y la perfusión de túbulos disecados. Aquí, desarrollamos una metodología para probar directamente en ratones vivos si la fagocitosis es una función de IC. La microscopía intravital permite un estudio intrincado de procesos celulares dinámicos dentro de murino en funcionamientoriñones59 . Las estrategias anteriores para utilizar la microscopía intravital han implicado la inyección sistémica de colorantes o marcadores intravitales en ratones para estudiar la endocitosis del túbulo proximal,riñóndinámica del flujo sanguíneo y permeabilidad vascular o glomerular 60 . Cuando la microscopía intravital se combina con técnicas quirúrgicas sofisticadas, se pueden estudiar momentos tempranos difíciles de evaluar de los procesos infecciosos 61 . Anteriormente, se microperfundieron bacterias en los túbulos proximales de ratas para evaluar el flujo sanguíneo, el reclutamiento de neutrófilos y la obstrucción urinaria 62,63 . La gran mayoría de las ITU se deben a patógenos ascendentes e inicialmente encontrarían el conducto colector 64,65 . Por lo tanto, proponemos que el conducto colector es una región tubular crítica para evaluar las interacciones huésped-patógeno. Nuestro sistema de modelo intravital recrea efectivamente un clásico

LA CITANCHE MEJORARÁ LA ENFERMEDAD RENAL/RENAL
estudio de perfusión de túbulo colector único, pero en un ratón vivo con un intactoriñón,suministro sanguíneo, linfático y neuronal junto con la capacidad retenida de interactuar con las células inmunitarias. La fisiopatología de la pielonefritis tiene distinciones entre hombres y mujeres. Por ejemplo, en los seres humanos, las hembras tienen cinco veces más probabilidades de desarrollar pielonefritis aguda, pero los ratones macho tienen una mayor gravedad de la pielonefritis mediada por andrógenos 66,67. Ransick y sus colegas demostraron diferencias diferenciales entre hombres y mujeres en las células del túbulo proximal, particularmente en los transportadores de aniones orgánicos 30 . Los IC masculinos se evaluaron tanto en la secuenciación unicelular como en los estudios intravitales. Debido al papel de los circuitos integrados en la defensa bacteriana delriñóny el equilibrio de electrolitos, la diversidad relacionada con el sexo en las funciones de IC, como la fagocitosis y la expresión génica unicelular, serán áreas clave para futuros estudios. Este estudio tiene limitaciones. La exposición de UPEC a IC humanos en nuestro scRNA-seq fue in vitro a un soloriñóny puede tener diferencias en comparación con la exposición a UPEC in vivo. Además, nuestros hallazgos representan la región anatómica del ser humanoriñónLos estudios muestreados y futuros con diferentes ubicaciones pueden tener una diversidad regionalizada como lo demuestra Ransick et al. 30 . Los circuitos integrados comprendían el 57 % de las células en nuestro scRNA-seq, enriquecidos a partir de la composición de ~7 % de los circuitos integrados enriñonesen la línea base 33 . Nuestra muestra contenía algunos otros tipos de células epiteliales y endoteliales, pero fue negativa para CD45 más células inmunitarias que se clasificaron antes del enriquecimiento de los CI (Fig. 1, Fig. 1 complementaria). Con scRNA-seq, los circuitos integrados de destino podrían identificarse y evaluarse por separado. Las células madre hematopoyéticas expresan c-KIT, pero probablemente no representen elriñónpoblaciones de células mieloides residentes 68 . No identificamos otras células que expresan c-KIT presentes en humanos sanosriñones, como células estromales/telocitos 69 . Se ha informado previamente sobre algunos casos aislados de c-KIT en el asa de Henle y el túbulo proximal.riñóninmunohistoquímica consistente con nuestros resultados scRNA-seq 70
