Toxicología de metalotioneína y cadmio: reseña histórica y comentario
Dec 18, 2023
Resumen: Hace más de siglo y medio, se informaron efectos adversos para la salud humana después del uso de un agente para pulir plata que contenía cadmio. La exposición prolongada al cadmio provoca enfermedades renales o óseas, toxicidad reproductiva y cáncer en animales y humanos. En la minería a pequeña escala se producen altas exposiciones humanas al cadmio, lo que subraya la necesidad de medidas preventivas. Esto es particularmente urgente dada la creciente demanda de minerales y metales para la mitigación del cambio climático global. Esta revisión aborda una parte específica de la toxicología del cadmio que es importante para comprender cuándo aparecen los efectos tóxicos y, por lo tanto, es crucial para la evaluación de riesgos. El descubrimiento de la proteína de bajo peso molecular metalotioneína (MT) en 1957 fue un hito importante porque, cuando esta proteína se une al cadmio, modifica la toxicidad celular del cadmio. Los presentes autores aportaron evidencia en la década de 1970 sobre la unión del cadmio a la MT y la síntesis de proteínas en los tejidos. Demostramos que la unión del cadmio a la metalotioneína en los tejidos previno algunos efectos tóxicos, pero que la metalotioneína puedeaumentar el transporte de cadmio a los riñones. Estudios especiales demostraron la importancia de la relación Cd/Zn en MT para la expresión de toxicidad en los riñones. También desarrollamos modelos de toxicocinética del cadmio basados en nuestros hallazgos relacionados con la MT. Este modelo, combinado con estimaciones de los niveles de toxicidad en los tejidos, permitió calcular los riesgos esperados de exposición. Otros científicos desarrollaron aún más estos modelos y organizaciones internacionales han utilizado con éxito estos modelos modificados en publicaciones recientes. Nuestras contribuciones en las últimas décadas incluyeron estudios en humanos de biomarcadores relacionados con MT que muestran la importancia de la expresión del gen MT en linfocitos y autoanticuerpos MT para los riesgos de efectos adversos relacionados con Cd en grupos de población expuestos al cadmio. En un estudio sobre el impacto del nivel de zinc en el riesgo dedisfunción renalen un grupo expuesto al cadmio, los riesgos eran bajos cuando el nivel de zinc era bueno y altos cuando el nivel de zinc era deficiente. La presente revisión resume esta evidencia en un contexto de evaluación de riesgos y pide su aplicación para mejorar las medidas preventivas contra los efectos adversos de la exposición al cadmio en humanos y animales.
Palabras clave: toxicidad del cadmio; metalotioneína; cadmio y zinc en metalotioneína; unión de cadmio en el plasma sanguíneo; modelo toxicocinético para cadmio;toxicidad renal del cadmio; expresión del gen metalotioneína en linfocitos; autoanticuerpos contra metalotioneína; evaluación del riesgo de cadmio

Servicio de apoyo de Wecistanche: el mayor exportador de cistanche de China:
Correo electrónico:wallence.suen@wecistanche.com
Whatsapp/Tel:+86 15292862950
Compre para obtener más detalles de especificaciones:
https://www.xjcistanche.com/cistanche-shop
HAGA CLIC AQUÍ PARA OBTENER EXTRACTO DE CISTANCHE ORGÁNICO NATURAL CON 25% DE EQUINACOSIDO Y 9% DE ACTEÓSIDO PARA LA INFECCIÓN RENAL
1. Introducción
El cadmio (Cd) es un metal tóxico y sus efectos adversos para la salud humana se conocen desde hace más de siglo y medio [1]. Los gobiernos y las autoridades responsables de muchos países hicieron esfuerzos considerables para controlar las exposiciones yprevenir efectos adversos para la salud. Sin embargo, en algunos países existe minería artesanal y de pequeña escala (MAPE) donde se producen exposiciones incontroladas al cadmio y muchos otros metales [2]. Existe una necesidad urgente de evaluaciones de riesgos adecuadas y medidas preventivas en la MAPE, particularmente en el contexto de la creciente demanda de minerales y metales para la mitigación del cambio climático global. La presente revisión se centra en una parte específica de la toxicología del cadmio que es importante para comprender cómo ocurren los efectos tóxicos y qué tan graves serán en diversos niveles de exposición. Esta información es crucial para la evaluación de riesgos. Además de los efectos gastrointestinales y respiratorios agudos informados por los médicos clínicos en 1858 [1], los efectos tóxicos del cadmio en animales y humanos expuestos incluyen enfermedades pulmonares, renales y óseas, toxicidad reproductiva y cáncer [3]. Desde 1957 [4], se ha ido acumulando cada vez más evidencia sobre el papel de las metalotioneínas (MT) en la toxicología del cadmio. Las MT son proteínas de unión a cadmio de bajo peso molecular que se encuentran en tejidos humanos y animales. Piscator 1964 [5] sugirió que la unión de Cd a MT modifica la toxicidad del cadmio. Los presentes autores aportaron evidencia durante las dos primeras décadas después del descubrimiento de las MT, sobre la unión del Cd a las MT en los tejidos en relación con la exposición al Cd [6,7]. Además, describimos el papel de la MT en el transporte y la captación de Cd en el riñón [8,9] y su probable papel en la modulación de la interacción del Cd con objetivos intracelulares de importancia para la expresión de la toxicidad. Hemos contribuido continuamente al conocimiento sobre la toxicología del cadmio también en las últimas cuatro décadas y la presente revisión y comentario resume nuestros hallazgos y brinda nuestras opiniones sobre el papel de la metalotioneína en la toxicología del cadmio aplicada a la evaluación de riesgos. Otras revisiones brindan propiedades químicas detalladas de la metalotioneína [10] y vías moleculares detalladas de importancia para la cinética y toxicidad del Cd [11], que aún no se utilizan completamente en la evaluación de riesgos.

2. Metalotioneínas, su descubrimiento, aislamiento y propiedades químicas
En 1957, Margoshes y Vallee [1] publicaron datos sobre una proteína fijadora de Cd en el tejido renal equino, que contenía un alto contenido natural de Cd y zinc (Zn). En 1960 [12] y 1961, Kägi y Vallee [13] publicaron la primera caracterización detallada de la proteína de los riñones de caballo y la denominaron Metalotioneína (MT). En 1964, Piscator [5] describió que la MT podía ser inducida por la exposición al Cd en conejos, y en 1972, Nordberg et al. [7] aislaron tres formas de MT mediante enfoque isoeléctrico. El pI de estas tres formas fue 3,9, 4,5 y 6,0, respectivamente. Caracterizamos las dos formas principales mediante análisis de aminoácidos. Esta y otras investigaciones posteriores demostraron que las MT son proteínas de unión a metales de bajo peso molecular (alrededor de 6500 Da, que varían según el contenido de metal), ricas en cisteína. Una amplia variedad de organismos contienen estas proteínas, incluidas bacterias, hongos y todos los eucariotas, es decir, especies vegetales y animales [10,14].
Las MT son importantes para la toxicocinética y la bioquímica de metales esenciales y no esenciales. Las especies metálicas de Zn, Cd, mercurio y cobre se unen a la MT en grupos (ver más abajo). Otros metales/metaloides como el selenio y el bismuto también se unen a la MT in vivo, pero la naturaleza exacta de dicha unión no se ha caracterizado en detalle. Aunque se trata principalmente de proteínas intracelulares, las MT se han detectado en pequeñas cantidades en sangre y orina. Las MT se determinan en sangre y tejidos mediante métodos bioquímicos e inmunológicos [15].
Se han identificado cuatro formas de MT, es decir, MT 1 a 4. MT-1 y MT-2 son las formas más estudiadas, se expresan en la mayoría de los tejidos y ambas constan de 61 aminoácidos (aa). Se han identificado varias isoformas de MT-1. MT-3 se encuentra en el tejido cerebral, tiene 68 aa y es rico en zinc. A veces se le llama factor inhibidor del crecimiento, GIF. MT-4 se expresa en queratinocitos y tiene 64 aa. MT-1 y MT-2 tienen 20 residuos de cisteína (30%), contienen N-acetilmetionina y C-alanina, pero no contienen aromáticos ni histidina. La secuencia de aminoácidos es única y la estructura terciaria muestra grupos de metales. MT-1 y MT-2 tienen dos grupos A y B con cuatro y tres metales, respectivamente. El C-terminal es parte del grupo A y el N-terminal de la proteína forma el grupo B [16]. Zn, Cd, Hg y Cu constituyen entre el 5% y el 10% p/p. La absorción de rayos UV varía según el metal unido, es (en nm) 225 para Zn-MT, 250 para Cd-MT, 300 para Hg-MT y 275 para Cu-MT [14,17].
El vínculo entre MT y ADN para MT-1, -2, -3, -4 está relacionado con la edad; feto, recién nacido y adulto. Aspectos de género, es decir, existen diferencias entre hombres y mujeres. Los niveles de MT son más altos en el tejido hepático de las mujeres que en los hombres. En la deficiencia de hierro hay un aumento de MT-1 en la médula ósea y en el riñón la MT está disminuida. Existe un polimorfismo genético, con varios genes de MT ubicados en el mismo cromosoma. Es posible que estén codificando funciones MT específicas [14,17].
La MT está presente en el hígado, los riñones, la orina, el plasma y la sangre. Cumple varias funciones, incluido el transporte de metales, por ejemplo, Cd, Cu, Zn. Otra función es la desintoxicación de metales, por ejemplo, Cd, Zn y Hg. Las especies de metales no unidos a MT son más tóxicas que los metales unidos a MT; esta última forma se acumula en los tejidos. La MT también sirve como eliminador de radicales libres, sirve en el almacenamiento de metales y en el metabolismo de metales esenciales y tiene funciones relacionadas con la respuesta inmune. La unión del metal a la MT modifica la genotoxicidad y la carcinogenicidad [14,17].
La presente revisión resume la evidencia experimental y las observaciones en humanos sobre la unión a proteínas del Cd en la sangre y los tejidos. Debido a que el riñón ha sido considerado el órgano crítico en exposiciones prolongadas al cadmio, se presta especial atención a las concentraciones de Cd, Zn y MT en los riñones y la aparición de proteinuria tubular. Los datos analizados en las siguientes secciones provienen de estudios realizados durante 50 años. Todos los estudios en animales y humanos contaron con la autorización de los comités éticos correspondientes.
El desarrollo de la investigación en MT desde 1970 se centró en la purificación, identificación y nomenclatura, caracterización, biología molecular, confirmación de resultados en toxicología y caracterización química/bioquímica, discutidos durante la primera reunión internacional sobre metalotioneína en 1978 [18]. El resultado de este taller fue concluir sobre una terminología de lametalotioneína de proteína.
La purificación e identificación de metalotioneína en tejidos biológicos causó al principio problemas. En la década de 1970, la homogeneización, la ultrafiltración y la cromatografía en gel eran las formas convencionales de purificación. Se descubrió que el almacenamiento de los 105,000 g del sobrenadante en distintos momentos y temperaturas influyó en gran medida en el resultado de la separación de proteínas, algo que es importante tener en cuenta hoy en día. El registro de la absorbancia a 250 y 280 nm, la relación que indica la pureza de MT, se controló durante la cromatografía en gel. Se descubrió que cuando el almacenamiento se había realizado a temperatura ambiente, el pico de Cd MT aparecía con un peso molecular más alto que cuando normalmente se eluía la MT cuando las muestras se mantenían refrigeradas (+5 ◦C). La cromatografía en gel debe realizarse a dicha temperatura. Sin embargo, al agregar mercaptoetanol al sobrenadante, se revirtió la polimerización y el pico de MT estaba en su volumen de elución normal. Nuestros intentos preliminares de estudiar la MT mediante electroforesis en gel de poliacrilamida no tuvieron éxito debido a las dificultades para evitar la oxidación. Fue útil el almacenamiento en congeladores de baja temperatura. Después de un procedimiento de congelación de los sobrenadantes de homogeneizados de tejido gota a gota en nitrógeno líquido y almacenamiento a -65 grados Celsius, se demostró que el patrón de distribución de la relación de absorbancia y del patrón de distribución del cadmio no cambiaba y aparecía igual para las muestras tomadas directamente para separación de proteínas. Resultó muy eficaz y útil para estudiar Cd y MT en muestras de tejido con baja concentración de ambos. Algunos estudios utilizaron radiomarcaje de MT con Cd109, que es excelente para estudiar bajas concentraciones de Cd en tejidos biológicos [8]. El radiomarcado con Cd mostró que de los siete metales, uno de ellos, el zinc, siempre tenía que formar parte de la proteína. También explicó el éxito de los estudios sobre la unión del Cd a la MT y la cinética de la MT en sangre y plasma. Cuando no se utilizaron estos procedimientos, en la literatura se han informado malas interpretaciones y datos engañosos. La MT liofilizada se puede almacenar en viales herméticos a -80 ◦C durante mucho tiempo sin oxidación de la proteína.

3. Toxicocinética del cadmio: papel de las metalotioneínas
3.1. Captación de CD
La absorción de Cd de la piel a la sangre es limitada después de la aplicación dérmica. La inhalación es la principal vía de absorción después de la exposición a partículas de Cd en el aire en entornos industriales y también es una vía importante para los fumadores de tabaco. Entre el 7 y el 40 por ciento del cadmio inhalado pasará a la sangre; los porcentajes más altos son válidos para compuestos de cadmio solubles y cadmio en nanopartículas, por ejemplo, en el humo del cigarrillo [19]. El Cd se une a la MT en el tejido pulmonar y la MT es inducida por la exposición al Cd [20]. La unión a MT modifica los efectos tóxicos en los tejidos pulmonares.
Los estudios en humanos sobre la absorción de Cd desde el tracto gastrointestinal hacia la circulación sistémica mostraron aproximadamente un 5 por ciento de absorción en hombres y un 10 por ciento en mujeres. Las mujeres jóvenes con bajas reservas de hierro pueden consumir hasta el 40 por ciento del cadmio de la dieta (revisión [3]). Hay datos en animales que muestran un porcentaje similar de absorción sistémica de Cd unido a MT que para otras especies químicas de cadmio cuando se introduce en el tracto gastrointestinal, pero la distribución sistémica es diferente (ver Sección 3.2.) y parte del CdMT ingerido se toma intacto hasta convertirse en sangre. En los animales se produce una mayor absorción de cadmio no MT de la dieta cuando la ingesta de hierro, zinc, calcio o proteínas es baja (revisión [3]). Los estudios experimentales informaron que varias vías para metales esenciales como DMT 1 [21,22], CaT1 [23] y ZIP8 y ZIP14 [24] están involucradas en la absorción de Cd. Ohta y Ohba 2020 [25] citaron varios autores que habían informado sobre la participación de vías adicionales en la absorción intestinal de cadmio (ZIP4, ZnT1, ATP7A; TRVP6) y realizaron estudios in vivo en animales con dosis crecientes de Cd oral2+ y encontraron concentraciones aumentadas de Cd relacionadas y una mayor expresión genética de MT-1, MT-2 y ZIP14, DMT1, ATP7A y TRVP6, particularmente en el tejido duodenal. El papel exacto de estas proteínas/transportadores en la absorción de Cd aún no está completamente aclarado.
3.2. Cd en sangre y transporte a los tejidos
Los efectos adversos del Cd ocurren en gran medida después de la distribución sistémica a diversos tejidos como los riñones, el esqueleto y otros órganos. La transferencia a través de la sangre es una ruta importante de distribución. Las bajas concentraciones en plasma en combinación con la sensibilidad insuficiente de los métodos analíticos químicos dificultaron durante mucho tiempo la realización de estudios adecuados de la concentración química y la unión del Cd en el plasma sanguíneo. Friberg 1952 [26] demostró hace mucho tiempo que el Cd se encuentra principalmente en los glóbulos rojos de los animales de experimentación. El uso de Cd radiomarcado en combinación con cromatografía en gel también ofreció la oportunidad de estudiar la unión a proteínas en plasma [8,27,28].
La Figura 1 muestra que después de una dosis única de Cd iónico, la unión inicialmente es predominantemente a proteínas de alto peso molecular, probablemente albúmina, y en intervalos de tiempo más largos (96 y 192 h) después de la administración, una proporción considerable de cadmio plasmático se produce en un tamaño molecular. de TM [24]. La aparición de Cd unido a una proteína del tamaño de la metalotioneína indica un papel importante de esta forma de unión en el transporte de Cd al riñón. Como otras proteínas muy pequeñas, la MT pasa a través delmembrana glomerular del riñónen orina primaria. Posteriormente, la CdMT se reabsorbe en las células del túbulo proximal. El transporte de CdMT desde la sangre a las células tubulares renales es rápido y casi completo [8,29]. Otras especies de Cd, por ejemplo la Cd-albúmina presente en el plasma sanguíneo, no llegan en la misma medida a los riñones. Un ejemplo son los diferentesacumulación renal de Cden animales alimentados con CdMT y otros animales alimentados con cloruro de cadmio [30]. Parte del CdMT ingresa a la sangre de esta forma, que se acumula en la corteza renal, mientras que el Cd del CdCl2 se une a la albúmina en la sangre y se acumula principalmente en el hígado [27]. Después de una sola administración de Cd2+, hay una redistribución de Cd desde el hígado hasta el riñón con el tiempo (consulte el párrafo siguiente). Esta redistribución está relacionada con el cambio dependiente del tiempo en la unión en el plasma sanguíneo (Figura 1).
Como se ha mencionado, la concentración de Cd en las células sanguíneas es considerablemente mayor que en el plasma. En los experimentos descritos en la Figura 1, el Cd en las células sanguíneas fue 100 veces mayor que las concentraciones plasmáticas a las 96 h y más. También se estudió la unión del Cd en las células sanguíneas. Una parte importante del Cd estaba unida a una proteína con el mismo tamaño molecular que la MT, y no principalmente a las fracciones donde se eluía la hemoglobina [27]. Aunque la unión del Cd a la pequeña proteína de las células sanguíneas del mismo tamaño que el MT, no tiene un impacto inmediato en la acumulación renal de Cd, la degradación gradual de las células sanguíneas supondrá una liberación lenta que posiblemente acabe también en los túbulos proximales de el riñón. Actualmente se acepta ampliamente que la CdMT desempeña un papel en el transporte de Cd al riñón como un curso probable de los acontecimientos también en humanos [11], pero, como señalaron Thévenod y Wolff [11], falta evidencia cromatográfica en humanos. Por otro lado, la MT se ha detectado mediante métodos inmunológicos en sueros sanguíneos humanos de seres humanos normales y ocupacionalmente expuestos a Cd [31,32] y parece probable que se una al Cd. La CdMT se produce en la orina humana [31] (ver también la Sección 3.3). Como se mencionó en la introducción de esta sección, debido a la sensibilidad limitada de los métodos para el análisis químico del Cd, no ha sido posible estudiar la unión del cadmio a las proteínas plasmáticas en humanos con los niveles de exposición existentes. Recientemente, Li et al., 2021 [33] informaron que en 11 de 29 muestras de sangre (Cd plasmático promedio 0,08 ng/ml) el cadmio parecía estar unido a la apolipoproteína A1 (ApoA1). No pudieron identificar las proteínas de unión a Cd en muestras de plasma crudo y utilizaron procedimientos para eliminar las proteínas principales del plasma antes de examinar las proteínas restantes. No está claro si estos autores tomaron precauciones para evitar la oxidación y polimerización de la MT y es posible que los procedimientos para eliminar las proteínas principales influyeran en la distribución del Cd entre las proteínas. Sería interesante examinar esta posibilidad en futuros estudios.
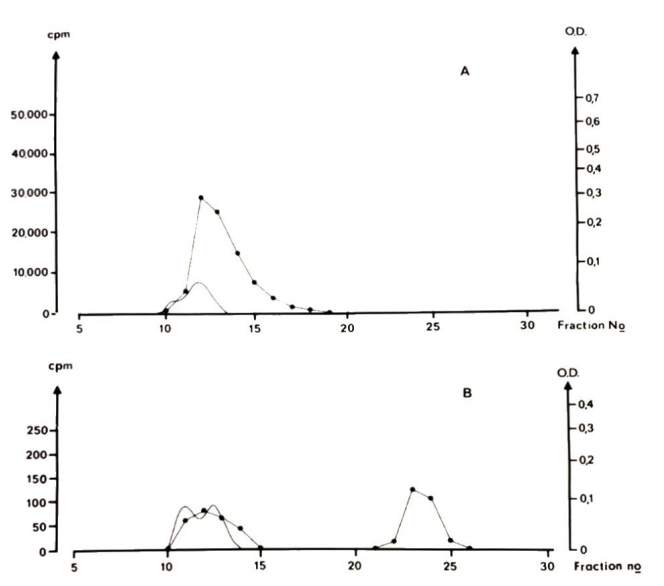
Figura 1. Unión de cadmio en plasma sanguíneo. Los paneles muestran los resultados de la separación cromatográfica en gel (G75) (a +5 ◦C) del plasma sanguíneo de ratones en varios momentos después de la inyección sc de una dosis única de CdCl2 radiomarcado. (A): 20 min después de la inyección, (B): 96 h después de la inyección, (C): 192 h después de la inyección. En el tiempo más corto (20 min), todo el Cd apareció en un pico de alto peso molecular (fracciones 12 a 14). En tiempos más prolongados (B, C), cuando la concentración de Cd en plasma era de 9 nanomol/kg, se detectó una proporción considerable de Cd en plasma en un segundo pico (fracciones 23-24) en el tamaño molecular de MT. Línea con puntos: radiocadmio, línea continua, densidad óptica 254 nm (OD). (Imagen del dibujo original de los resultados cromatográficos. Detalles experimentales descritos en [27]).
3.3. Distribución de cadmio entre órganos
Después de una única exposición a sales inorgánicas de Cd en animales de experimentación, inicialmente se produce una alta concentración de Cd en el hígado, que disminuye con el tiempo. Se produce una redistribución al riñón y este órgano luego muestra la mayor concentración entre los órganos del cuerpo [34-36]. El aumento de la concentración de Cd en los riñones puede continuar durante meses después de una sola exposición. La distribución de órganos depende de la dosis. Después de dosis altas, independientemente de la vía de exposición, hay una mayor proporción de Cd en el hígado que con dosis más bajas. En dosis bajas, la acumulación en el riñón es más prominente, por ejemplo, [37]. Además, en exposiciones prolongadas, el riñón tiene la concentración más alta de Cd [36]. Piscator 1964 [5] y Nordberg et al. [6] examinaron la unión de Cd en el tejido hepático de animales de experimentación expuestos a Cd y encontraron una proporción importante de Cd unido a MT. La exposición repetida al cadmio dio lugar a niveles más altos de Cd y MT en el hígado, lo que demuestra que la exposición al Cd indujo la síntesis de MT en ese tejido. Los autores consideraron que la unión del cadmio a la MT tiene una importancia considerable para la toxicología del cadmio. La exposición al cadmio induce la síntesis de MT-1 y MT-2 en muchos tejidos de animales y humanos (Sección 2). Como se mencionó (Figura 1), una proporción del Cd sanguíneo, tanto en el hemolizado de las células sanguíneas como en el plasma sanguíneo, está unido a una proteína similar a la MT. Por lo tanto, una explicación probable para la redistribución de Cd del hígado al riñón es la liberación de CdMT del hígado y su transporte al riñón mediante filtración glomerular y reabsorción en los túbulos renales. El transporte de CdMT inyectada, aislada de animales expuestos al Cd, fue rápido desde la sangre hasta el riñón. Aproximadamente el 95 por ciento de la dosis inyectada es absorbida por los túbulos renales [9,29]. La captación en las células tubulares proximales se produce a través de la megalina: endocitosis mediada por el receptor de cubilina (revisión [11,38]). La acumulación de Cd en estas células estimula la síntesis de MT y en estas células tiene lugar una nueva unión continua a MT. Esto explica por qué la vida media biológica del Cd en dichas células es tan larga. En humanos, se estima que la vida media es de 10 a 30 años. Por lo tanto, en exposiciones de fondo, el Cd se acumula continuamente durante la vida humana. Cuando aumenta la concentración de Cd en la corteza renal, se alcanza una concentración crítica y aparece la disfunción renal (ver Sección 4.1).
La Figura 2 describe un esquema del flujo probable de Cd unido a albúmina desde el plasma al hígado, donde la albúmina-Cd se absorbe y se degrada; el Cd2+ liberado induce la síntesis de MT y se une a la MT recién sintetizada.
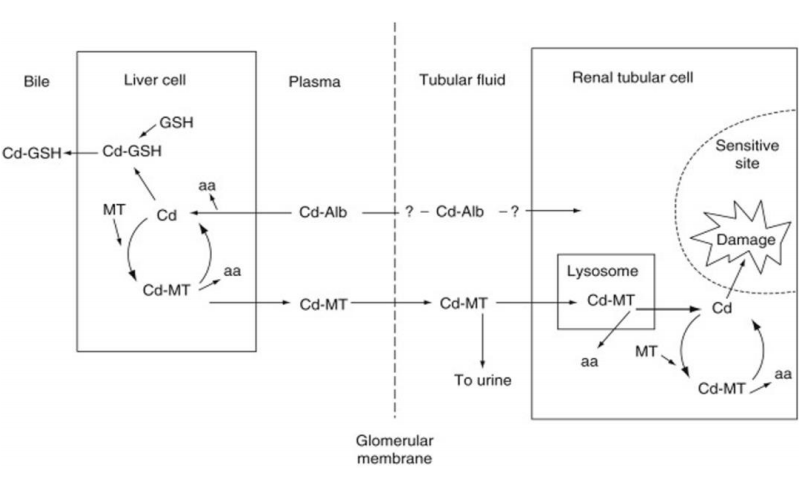
Figura 2. Esquema de flujo básico de Cd en el cuerpo que demuestra el papel de las formas de unión en la sangre y la síntesis y degradación de MT. aa, aminoácidos; Alb, albúmina GSH, glutatión; MT, metalotioneína. Modificado de [39]
Por tanto, en exposición continua, CdMT es la forma dominante de Cd en el hígado. Posteriormente, una pequeña proporción de CdMT hepática ingresa al plasma desde donde se filtra a través de la membrana glomerular y se absorbe en los túbulos renales, donde puede producirse daño celular (Sección 4.1). Presentado por primera vez en 1984 por uno de los autores [39], este esquema ha sido ampliamente aceptado y respaldado por datos aportados por otros científicos.
Chan et al., 1993 [40] brindaron apoyo para el transporte de CdMT desde el hígado al riñón al mostrar una absorción gradual de Cd en los riñones después del trasplante de hígados que contienen Cd a ratas no expuestas al Cd. Liu et al., 1996 [41] y Liu y Klaassen 1996 [42] mostraron diferencias en la cinética de Cd entre ratones transgénicos (MTnull) y de tipo salvaje. En ratones MTnull, la eliminación de Cd fue mucho más rápida que en ratones de tipo salvaje. Las concentraciones de Cd en el riñón aumentaron con el tiempo en ratones de tipo salvaje, pero no en ratones MTnull. Estas observaciones respaldan el papel de la MT en la retención tisular y el transporte de cadmio al riñón. Sabiolic et al. presentaron una revisión de la evidencia actualmente disponible, que brinda apoyo general al esquema explicativo descrito en la Figura 2, pero que incluye información detallada y actualizada sobre las vías bioquímicas que explican la cinética y la toxicodinámica del Cd. [43]-se remite al lector a esta revisión para obtener más detalles.
Como resultado de la unión de MT y los cambios de distribución relacionados con el tiempo mencionados, los humanos adultos con exposiciones prolongadas y de bajo nivel, por ejemplo, exposiciones de fondo en Suecia, tienen el 50 por ciento de su carga corporal de Cd en los riñones. En el riñón, la concentración más alta de Cd se encuentra en la corteza renal (revisión [3])
3.4. Excreción de cadmio-vida media biológica
El Cd induce la síntesis de MT en el hígado, el riñón y otros tejidos (Secciones 1 y 2) y una gran proporción del Cd tisular se une a la MT y queda atrapado en los tejidos de esta forma. Esto explica la larga vida media biológica del cadmio en los tejidos de humanos y animales. Sólo 0.01 a 0,02 por ciento por día de la carga corporal de Cd se excreta en la orina y las heces. La vida media biológica del Cd en los tejidos humanos es muy larga en la fase de acumulación de Cd en el riñón. Cuando el nivel de Cd en la corteza renal alcanza una concentración que causa disfunción tubular renal (ver Sección 4.1), la excreción urinaria de Cd aumenta dramáticamente y la vida media del Cd en el riñón disminuye.
En la fase de acumulación, la vida media en tejidos humanos como los músculos, la corteza renal y el hígado es de 10 a 30 años, según estimaciones basadas en estudios de tejidos humanos y patrones de excreción. En la sangre, hay un componente rápido (100 días) y un componente lento (7 a 16 años) que describen los niveles decrecientes después del cese de la exposición ocupacional en humanos. En animales, la vida media en el plasma sanguíneo cambia desde minutos inmediatamente después de la exposición hasta días en tiempos de observación posteriores (revisado en [3]). Akerstrom et al., 2013 [44] informaron una vida media en la corteza renal humana de 23 años con una concentración de Cd en la corteza renal de 8 mg/kg y de 43 años con 23 mg/kg. La retención más prolongada probablemente esté relacionada con una inducción más eficiente de la síntesis de MT en niveles algo más altos de Cd. Las concentraciones de Cd en los riñones de los seres humanos mayores disminuyen después de los 60 años, posiblemente debido a la inducción de MT menos eficiente en los grupos de mayor edad.
La excreción urinaria de Cd tiene lugar mediante la transferencia de Cd desde los túbulos renales a la orina y mediante la excreción de una pequeña proporción de filtrado glomerular que no es absorbido por las células tubulares renales como lo indican los experimentos con animales (revisado en [3] y la Sección 3.2). En la fase de acumulación, antes de que se induzca el daño tubular renal, la orinaEl CD es un buen indicador de la carga renal y corporal.de CD. Cuando se alcanza un nivel tóxico de cadmio en los túbulos renales, la reabsorción tubular se verá afectada y la excreción urinaria de Cd aumentará dramáticamente. La relación entre el Cd renal y el Cd urinario cambia cuando se induce una disfunción tubular. El Cd urinario se une en gran medida a MT tanto en la fase de acumulación como cuando hay disfunción tubular [31,45–47] (ver también la Sección 4.2).
3.5. Modelo toxicocinético de acumulación de cadmio en los riñones
Aunque se está debatiendo si los efectos adversos del Cd en los riñones o el esqueleto deben considerarse efectos críticos, es decir, efectos que ocurren con las exposiciones externas más bajas, los efectos en los riñones ocurren con exposiciones bajas y todavía se consideran efectos críticos. 19]. Kjellstrom y Nordberg 1978 [48] presentaron un modelo toxicocinético multicompartimental para la cinética y la acumulación de Cd en los riñones basado en la identificación de un papel crucial de la MT, en gran medida como se describe en la Figura 2 (ver también [49]). Choudhury et al., 2001 [50] desarrollaron más este modelo, utilizando evidencia posterior. El modelo modificado, en combinación con cálculos basados en la distribución de la concentración crítica de Cd en la corteza renal, se ha utilizado con éxito en evaluaciones de riesgos por Diamond et al., 2003 [51], ATSDR 2012 [52] y la Unión Internacional de Cd puro. y Química Aplicada 2018 [19]. En el último documento, estos cálculos del modelo proporcionaron una perspectiva de los hallazgos de los estudios epidemiológicos. Los cálculos muestran que el nivel de exposición más bajo al Cd que da lugar adisfunción renalEs muy bajo.
Servicio de apoyo de Wecistanche: el mayor exportador de cistanche de China:
Correo electrónico:wallence.suen@wecistanche.com
Whatsapp/Tel:+86 15292862950
Compre para obtener más detalles de especificaciones:
https://www.xjcistanche.com/cistanche-shop
OBTENGA EXTRACTO DE CISTANCHE ORGÁNICO NATURAL CON 25% DE EQUINACOSIDO Y 9% DE ACTEÓSIDO PARA LA INFECCIÓN RENAL







