Evolución molecular de la proteína bactericida/que aumenta la permeabilidad (BPIFA1) que regula las respuestas inmunitarias innatas en los mamíferos, parte 2
May 29, 2023
3. Resultados
Se estudiaron las secuencias de la proteína BPIFA1 codificadas en el genoma de los mamíferos para determinar el papel de la evolución y la selección adaptativa. La proteína BPIFA1 es el mediador clave de la señalización innata contra infecciones microbianas por bacterias y hongos. Una vez que las secuencias se combinaron con MSA, se utilizaron para crear árboles filogenéticos bayesianos y se sometieron a más investigaciones. Para iniciar cascadas de señalización intracelular, es necesario activar un conjunto de genes identificados en las especies de mamíferos apropiadas y que posean un dominio funcional (LBP-BPI). Para el fosfolípido tensioactivo dipalmitoilfosfatidilcolina (DPPC), este dominio de unión a lípidos tiene un grado muy alto de selectividad. El sistema inmunitario innato de las vías respiratorias superiores se activa en respuesta a numerosas señales genéticas, como el aumento de las tasas de sustitución no sinónima, haplotipos homólogos significativos y la ausencia de variación genética en las proteínas BPIFA1, lo que demuestra que la presencia de estas proteínas se ha visto favorecida por positivos selección.
El dominio de unión a lípidos (LBD) es un dominio estructural contenido en muchas proteínas, que puede unirse a algunas moléculas de lípidos específicas para regular la función o la localización de las proteínas.
Varios estudios han demostrado que los dominios de unión a lípidos pueden afectar la inmunidad. Por ejemplo, en algunos órganos linfoides secundarios como el bazo y los ganglios linfáticos, una molécula de lípido llamada S1P (esfingolípido-1-fosfato) regula la migración y la migración de las células T y las células B al interactuar con los dominios de unión a lípidos. retener. Además, algunos receptores de superficie de células inmunitarias importantes, como TLR4, TLR7 y TLR8, también contienen dominios de unión a lípidos, que pueden unirse a diferentes tipos de moléculas lipídicas y regular la activación y la respuesta de las células inmunitarias.
Por lo tanto, existe una cierta relación entre los dominios de unión a lípidos y la inmunidad, lo que también proporciona nuevas ideas para estudiar la regulación de las respuestas inmunes por parte de los dominios de unión a lípidos. Se puede ver que debemos mejorar nuestra inmunidad para resistir los virus. Cistanche puede mejorar significativamente la inmunidad. Cistanche también tiene efectos antivirus y anticancerígenos, que pueden fortalecer la capacidad del sistema inmunológico para combatir y mejorar la inmunidad del cuerpo.

Haga clic en beneficios para la salud de la cistanche
3.1. Evolución molecular del gen BPIFA1
En este trabajo, buscamos signos de adaptación en el gen BPIFA1, que van desde señales de selección progresivamente débiles a fuertes durante la evolución adaptativa en el genoma de los mamíferos. Se determinó el porcentaje típico de codones en el gen BPIFA1 que experimentan evolución adaptativa. Siguiendo el mismo procedimiento para cada secuencia de codificación, calculamos la proporción promedio de codones seleccionados positivamente en todas las ramas. Usando BUSTED y variación de tasa de sinónimos en ramas de prueba cuidadosamente elegidas de la filogenia BPIFA1, determinamos rastros de selección de diversificación episódica en todo el gen. Como resultado, concluimos que se produjo una selección divergente a lo largo de las tres líneas de descendencia examinadas. Usando la variación de la tasa de sinónimos, observamos una selección de diversificación episódica de todo el gen en las ramas de prueba de la filogenia BPIFA1. Se utilizó una selección de diversificación episódica de todo el gen para lograr esto (LRT). Dos ramas de prueba exhibieron evidencia de selección diversificada, lo que sugiere que el sitio había estado sujeto a este tipo de evolución (Figura 1).
Las proporciones promedio de dN/dS para BPIFA1 en todos los sitios y linajes fueron mayores que uno. Como resultado, se llevó a cabo una investigación sobre esta proteína para identificar las firmas de selección positiva. Se encontró que la proteína tenía una estructura de aminoácidos conservada, lo que permitía su purificación, y tenía un valor de omega superior a 1. Se realizó una prueba de log-verosimilitud a esta proteína, se analizaron todos sus sitios y la Se calculó la tasa de sustitución. Para evaluar si se produjo o no una selección positiva, utilizamos tres conjuntos diferentes de modelos de probabilidad: M0 frente a M3, M1 frente a M2 y M7 frente a M8. Se compararon las estimaciones de parámetros bajo M1 y M2 y se encontró que el valor de M2 para estas proteínas era positivo. Los porcentajes de sitios seleccionados positivamente fueron significativos para los tres modelos, con valores de 422.86, 64.5 y 93.63, respectivamente (Cuadro 1).

Para proporcionar evidencia adicional que respalde los hallazgos de la selección positiva, aplicamos el modelo de combinación mecanicista-empírica a sitios específicos utilizando el servidor de selección. Durante este proceso, descubrimos que varios sitios habían sido identificados como sujetos a presión selectiva en varios puntos durante la evolución (Figura 1). Por ello, podríamos estimar el grado de conservación evolutiva de este gen. Descubrimos que la gran mayoría de los sitios seleccionados positivamente se habían conservado en todos los clados de mamíferos. Esto se debió a que los aminoácidos conservados representaron la mayoría de las señales utilizadas para la selección positiva en el algoritmo de la red neuronal (Tabla 2).

El método de selección del modelo de codones evaluó 9113 modelos diferentes. El mejor modelo (log(L)=−18,910, mBIC=39,340.92) contenía tres tasas y era el más preciso. Con este modelo, se lograron mejoras de 218,66 log(L) y 398,33 mBIC puntos en comparación con un modelo de tasa única, en el que todas las sustituciones no sinónimas ocurrieron a la misma tasa, como se muestra en la Tabla 1. Cada modelo en el conjunto creíble tenía una relación de evidencia de al menos 0,01 en comparación con el mejor modelo, lo que significa que estaba dentro de las 9,21 unidades mBIC del mejor modelo, o de manera equivalente, que tenía una relación de evidencia de al menos 0,01 en comparación con el mejor modelo. El promedio del modelo estimó la tasa de cambio en esta colección de modelos (Figura 2). El patrón de selección evolutiva en las posiciones de los aminoácidos en la proteína BPIFA1 también se evaluó mediante el análisis de selección del modelo de codones, que mostró que la sustitución de los sitios de aminoácidos se produjo durante la evolución adaptativa de las proteínas. Revelamos que las posiciones de aminoácidos básicos de las proteínas exhibieron una evolución adaptativa debido a las diferentes proporciones de sustitución. Según la distribución de sitios de aminoácidos en BPIFA1, la tasa de sustitución máxima fue de aproximadamente 1,19, mientras que la más baja fue de 0,14 (Figura 2).


La identificación de regiones fisiológicamente significativas de una proteína se puede realizar contrastando la frecuencia de sustituciones sinónimas (Ks) y no sinónimas (Ka) en la proteína. Esto proporciona la base para concluir la existencia de la selección purificadora y la selección darwiniana positiva localizada. Usamos Selecton v. 2.2 (accesible en http://selection-bio info-tau.ac.il, consultado el 29 de septiembre de 2021), un servidor web que calcula automáticamente la proporción de Ka a Ks (u) en cada sitio en la proteína Los diferentes colores representan diferentes tipos de selección (selección positiva, selección purificadora y no selección) y se utilizan para mostrar gráficamente esta proporción en cada sitio. El modelo de selección es una colección de diferentes hipótesis evolutivas que se pueden usar para probar estadísticamente la probabilidad de que una proteína dada haya sido sometida a selección positiva. Opera a través de una interfaz gráfica de usuario. El modelo mecanicista-empírico recientemente establecido influyó en las propiedades físicas del aminoácido (Cuadro 3).

3.2. Selección adaptativa del gen BPIFA1
Para determinar el grado en que las diferentes especies de mamíferos se han adaptado a sus entornos, utilizamos múltiples alineaciones de las secuencias codificantes del gen BPIFA1 de cada una de las 34 especies. Estas pruebas se pueden emplear individualmente o en combinación. La variedad más común de pruebas se conoce como prueba de rama. Durante la evolución de las especies de vertebrados, la selección de linajes específicos se utilizó para reconocer distintos linajes sujetos a presión de selección. Las probabilidades de selección específicas del linaje se calcularon para cada grupo filogenético utilizando un modelo de probabilidad de efectos aleatorios de sitio de ramificación adaptativo (aBS-REL). Además, se utilizó la técnica aBS-REL para diseccionar cada gen para determinar qué linajes habían estado sujetos a selección adaptativa en diferentes momentos de la historia evolutiva.
Cuando se aplicó a linajes de mamíferos, el modelo aBS-REL confirmó que los genes predichos por BUSTED estaban bajo selección positiva. Nuestros resultados, que sugirieron que la presión selectiva estaba actuando sobre los genes BPIFA1 en linajes de mamíferos, demostraron que las dos hipótesis eran congruentes (Tabla 4). En la filogenia del gen BPIFA1, hubo evidencia de selección diversificadora episódica en ocho ramas. La importancia de los hallazgos se evaluó mediante la prueba de razón de verosimilitud (p > 0.05), que se llevó a cabo después de considerar los resultados de muchas otras pruebas (Figura 3). En total, 63 líneas distintas se sometieron a esta prueba específica para diversificar la selección. Se llevaron a cabo múltiples pruebas y la significación de los hallazgos se estableció mediante la aplicación de la Prueba de razón de verosimilitud con un umbral de valor de p de 0,05.

Esta tabla informa un resumen estadístico del ajuste de los modelos a los datos. Línea base MG94xREV se refiere al modelo de línea base MG94xREV que infiere una sola categoría de tarifa ω por sucursal. El modelo adaptativo completo se refiere al modelo aBS-REL adaptativo, que implica un número optimizado de categorías de tarifas ω por sucursal.
Durante el proceso evolutivo, examinamos los valores omega empleando los métodos SLAC, FUBAR, MEME y FEL para localizar indicaciones de selección positiva (Tabla 5). Según nuestros hallazgos, el gen BPIFA1 en los clados de mamíferos ha estado sujeto a una selección evolutiva positiva. Pudimos detectar qué regiones del genoma estaban sujetas a presión selectiva utilizando el método bayesiano. Esta técnica implica determinar la probabilidad posterior de cada codón. Es más probable que los sitios con un mayor número de posibilidades hayan sido objeto de una selección diversificada, lo que conduce a tasas más altas de sustitución no sinónima y sinónima que los sitios con un menor número de probabilidades (Cuadro 2). Usando el análisis BEB, encontramos que varias ubicaciones en todo el dominio LBP-BPI de la proteína bactericida habían estado sujetas a selección positiva con una alta probabilidad posterior del 95 por ciento. Este fue el caso para todos los sitios. Los sitios estaban dispersos por todo el dominio en varios lugares. Los hallazgos de PAML se examinaron utilizando el conjunto de datos encontrado en el servidor de selección. Este servidor pudo identificar la selección adaptativa en ciertos sitios dentro de la proteína, lo que nos permitió validar la existencia de selección positiva. Para determinar las tasas de sustitución se aplicó el modelo MEC. Los hallazgos demostraron que la selección adaptativa ocurrió en varios lugares en BPIFA1 (Tabla 5).


3.3. Análisis de recombinación
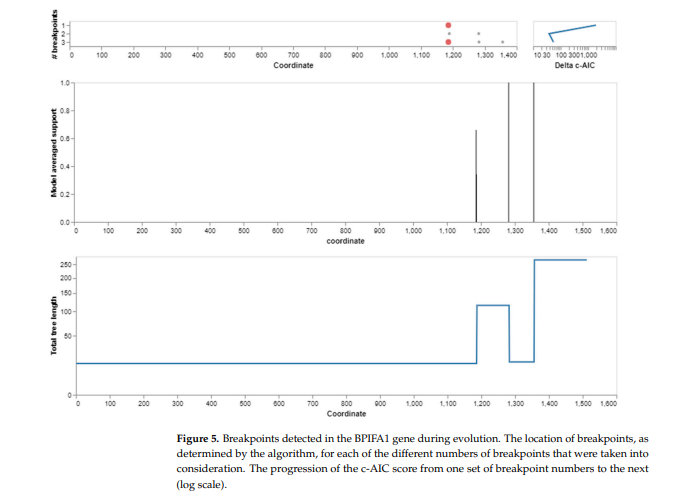
Para el gen BPIFA1, se realizó un análisis de recombinación para encontrar vínculos evolutivos potenciales entre genes. La investigación reveló tres eventos de recombinación. Cada una de las secuencias de recombinación, incluidos los progenitores principal y secundario, provenían del gen BPIFA1. Identificamos puntos de corte de recombinación utilizando el análisis GARD. A una velocidad de 30.30 modelos por segundo, GARD inspeccionó 5120 modelos. El espacio de búsqueda de 72.874.879 modelos con hasta tres puntos de ruptura fue generado por los 759 posibles puntos de ruptura de la alineación, de los cuales el algoritmo genético solo examinó el 0,01 por ciento. Con una relación de evidencia de 100 o superior, se prefirió el modelo de árbol múltiple al modelo de árbol único, lo que indica que al menos uno de los puntos de ruptura reflejaba una incongruencia topológica. Esto se validó comparando las puntuaciones AICc del modelo GARD de mejor ajuste, que permitía topologías variables entre segmentos (37.996,2), y el modelo, que asumía el mismo árbol para todas las particiones determinadas por GARD, pero permitía longitudes de rama variadas entre particiones. Específicamente, la puntuación AICc del modelo GARD de mejor ajuste fue 37 996,2, mientras que la puntuación AICc del modelo fue 37 996,2. (Figuras 4 y 5).

3.4. Interacciones proteína-proteína y análisis de unión de ligandos
Utilizamos la base de datos STRING para buscar proteínas expresadas con BPIFA1, identificando varios pares de interacciones proteína-proteína. Había 13 nodos y 35 bordes indicados por las proteínas expresadas con BPIFA1. Los bordes del diagrama PPI son las redes de líneas que unen los nodos individuales (Figura 6). El valor promedio del coeficiente de agrupamiento local fue 0.978. El enriquecimiento con PPI tuvo un valor p de 5,25 × 10−12. La red PPI representó las interacciones del gen BPIFA1 con otros genes inmunitarios coexpresados. COX7B2, BPIFB6, BPIFB4, BPIFB2, BPIFB3, PLTP, CETP, BPI, LBP y ODF2L fueron los 10 genes involucrados en la red PPI de BPIFA1 (Figura 6).

Los genes BPIFB6, BPIFB4, BPIFB2 y BPIFB3 fueron los más importantes porque están involucrados en las vías de señalización biológica, que juegan un papel esencial en la inmunidad innata contra la infección bacteriana. Además, estos genes están regulados positivamente por BPIFA1, que es otra razón por la que se consideraron tan significativos (Tabla 6). Las vías moleculares son esenciales para erradicar los gérmenes invasores a través de la actividad de alteración de la membrana compuesta por todas las proteínas relacionadas con diversas funciones. La actividad disruptiva de la membrana era necesaria para la eliminación de los gérmenes invasores. Dos proteínas cruciales en la mediación de señales en respuesta a los lipopolisacáridos incluyen la proteína de unión a LPS (LPSBP) y la proteína que aumenta la permeabilidad bactericida (BPI). Mostraron una fuerte afinidad por el lípido A, una sustancia que se encuentra en LPS, y eran sorprendentemente similares entre sí. A pesar de tener estructuras similares, LBP y BPI realizan varias funciones biológicas que son claramente diferentes entre sí. Por ejemplo, LBP se une con frecuencia a LPS y facilita en gran medida la presentación de LPS a células CD14 plus, como macrófagos y monocitos, mientras que BPI inhibe y reduce la bioactividad de LPS. Estas dos proteínas están presentes en las bacterias.
Los ligandos son componentes críticos en el proceso de control de la expresión y actividad de las proteínas. Las fuerzas de unión intermoleculares, como los enlaces iónicos, los enlaces de hidrógeno, la interacción hidrofóbica y las fuerzas de Vander-Waals, contribuyen al proceso de unión de ligandos. Debido a las interacciones entre los ligandos y las proteínas, se alterará la estructura tridimensional de la proteína. Debido a estos cambios en el estado conformacional de la proteína, algunas de las funciones de la proteína pueden inhibirse o activarse. Por lo tanto, realizamos un estudio de interacción de unión proteína-ligando utilizando las características fisicoquímicas de los aminoácidos para determinar qué residuos interactúan con el ligando y cuáles no. Para lograr esto, utilizamos un sitio web (http://crdd.osdd.net/raghava/lpicom, consultado el 18 de octubre de 2021) que calcula la fracción de residuos que interactúan con un ligando determinado. Se demostró que residuos clave, como cisteína, glicina, alanina, lisina, ácido aspártico, histidina, leucina, valina, arginina, triptófano, serina, treonina y tirosina, interactúan con siete ligandos (1BP1, BPH, XE, NEH, CLA, CU y MG) y PC1. En comparación con la interacción con PC1, los aminoácidos cargados, especialmente los aminoácidos esenciales, tuvieron una mayor ventaja al interactuar con 1BP1, BPH, XE, NEH, CLA, CU y MG (Figura 7). Los aminoácidos pequeños y polares que se correlacionaron con ellos se caracterizaron en cada uno de los tres ligandos.
Utilizamos dos enfoques distintos para hacer predicciones con respecto a los sitios de unión complementarios: el primero se basó en la comparación de subestructuras específicas de unión (TM-SITE), mientras que el segundo se basó en la alineación de los perfiles de secuencia (S-SITE). Estas técnicas evaluaron la proteína BPIFA1 frente a 500 proteínas no redundantes que se combinaron con 814 compuestos orgánicos, sintéticos y de iones metálicos. Comenzando con predicciones de estructuras de proteínas de baja resolución, los enfoques identificaron con éxito los residuos de unión de BPIFA1, logrando un coeficiente de correlación de Matthews (MCC) promedio que fue mucho más alto. Además, las técnicas descubrieron ligandos que se unen a los residuos (Tabla 7).


4. Discusión
Los fondos heterogéneos ofrecen plataformas en las que las poblaciones que experimentan una selección divergente pueden distinguirse en subpoblaciones adaptadas de forma nativa [44]. La influencia de la selección en el flujo de genes entre poblaciones, como el equilibrio entre migración y selección, determina la posibilidad de una adaptación innata y una divergencia continua. Esto también se conoce como equilibrio entre migración y selección. Existe una tendencia a que la variabilidad genética local dentro de las poblaciones se homogeneice debido al flujo de genes cuando el efecto de la selección es menos significativo que el efecto del flujo de genes. En cambio, las variantes genéticas pueden acumularse y retenerse en loci específicos susceptibles a una fuerte selección divergente si la presión selectiva es mayor que la fuerza integradora del flujo de genes [45].
En el posible resultado alternativo, los beneficios del flujo de genes se ven limitados por la selección contra inmigrantes que tienen un ajuste genético deficiente, lo que también allana el camino para la adaptación local [45,46]. Debe haber una conexión entre el flujo de genes y la selección para comprender las diferencias de población en la frecuencia del flujo de genes [46]. Bajo tales circunstancias, la selección determina si la población continúa evolucionando o diverge como un grupo distinto. El enfoque empírico de Bayes calculó el LRT en cada sitio de sucursal y ubicó todos los diferentes sitios donde puede ocurrir una selección diversificada. Basándose en el enfoque empírico de Bayes, se aplicó la aproximación bayesiana rápida y sin restricciones, también conocida como FUBAR, para localizar la selección diversificadora que se produce en el gen BPIFA1. FUBAR permitió la dispersión de codones de sitio a sitio y de rama a rama y se utilizó para explorar la evolución adaptativa que se produjo a nivel genético. El método de MEME se utilizó para investigar la evolución adaptativa que se produjo a nivel de genes [25,32,47]. SLAC encontró los sitios de codificación de diversificación episódica con un valor p de menos de 0.01 (Tabla 1).
Este modelo se usó para estimar las tasas de sustitución de sinónimos y no sinónimos, y la codificación de sitios con tasas de sustitución de sinónimos mayores o iguales a la tasa de no sinónimos se consideró importante para identificar sitios que estaban pasando por una selección diversificada. En MEME, se obtuvieron estimaciones de máxima verosimilitud para los codones 130, 167, 168, 190, 243, 265 y 289 del gen BPIFA1 (Tabla 2). En base a sus señales no significativas, estos codones no se identificaron como sitios seleccionados positivamente, lo que se debe al carácter episódico de la selección natural. La selección natural que tuvo lugar esporádicamente a lo largo de breves intervalos de evolución adaptativa fue enmascarada por la frecuente ocurrencia de selección purificadora o natural. En consecuencia, no se pudieron encontrar signos de evolución adaptativa mediante pruebas de sensibilidad y selección positiva [48].
Encontramos diecisiete sitios que se eligieron favorablemente con el método PAML, quince sitios que se eligieron con el algoritmo IFEL y cuatro sitios que se eligieron con el algoritmo FEL. La presión de selección adaptativa sobre las secuencias de codones del gen BPIFA1 se calculó utilizando el modelo MEC. Esto resultó en la identificación de setenta y cuatro aminoácidos (Figura 1). Se utilizó un modelo de evolución basado en selección positiva, revelando diferencias a nivel de codón (M8). La aplicación MrBayes en el servidor de selección utilizó un modelo MCMC para determinar previamente las diferencias en el gen MAVS en mamíferos a nivel de codón [49].
Según los resultados de las alineaciones de proteínas MAFFT, estudios previos han demostrado que el dominio Ig permanece en las secuencias codificantes de MAVS. Estos resultados sugieren que los cambios de proteína alternativos en la purificación de regiones seleccionadas son perjudiciales y, por lo tanto, es poco probable que se mantengan a lo largo de la evolución [50,51]. Los sitios para múltiples vías evolutivas se identificaron mediante una distribución de tasas de parámetros múltiples, un modelo de efectos aleatorios con un intervalo de confianza del 95 por ciento y valores sustanciales de Pr [ > ]. Los sitios podrían entonces ser localizados gracias a este método (Cuadro 3). En el caso de selección positiva, el peso de la tasa de clase se determinó utilizando una distribución discreta general bivariada para cada sitio de codificación. La convergencia del modelo MCMC se demostró por el hecho de que se encontró que las estimaciones medias posteriores para BPIFA1 estaban más cerca del valor del factor de reducción considerado (Tabla 2).
Estos valores variaron de {{0}}.95 a 0.99. Durante el proceso de diversificación de la selección, solo se consideraron los sitios de codificación con valores empíricos de factor de Bayes (EBF) de más de 50. Los cálculos se realizaron usando el tamaño de muestra efectivo neto para determinar los valores de EBF para cada sitio de codificación evaluado usando selección positiva. Inferir la distribución de los parámetros de selección específicos de genes podría mejorar las selecciones detectadas en un gran número de sitios de codificación. Las áreas de codificación que se seleccionaron e identificaron positivamente brindan evidencia significativa de la selección diversificada en los genes BPIFA1 que ahora están experimentando un linaje selectivo. Como resultado, algunas mutaciones que inicialmente parecen ser neutrales (y no tienen un impacto inmediato en la aptitud física) pueden ser "permisivas", lo que permite que la proteína resista cambios posteriores que de otro modo serían perjudiciales y causarían diferencias fenotípicas [52]. Las mutaciones neutrales en la epistasis sientan las bases para la posterior selección y adaptación, que recientemente ha atraído mucha atención y se ha ofrecido como una forma de reconciliar los modelos de evolución neutral y de selección [53].
La tasa de sustitución del par FWY y HKR fue de aproximadamente el 50 por ciento, la tasa de sustitución de DENQ fue del 50 por ciento y la tasa de sustitución de ACGILMPSTV fue del 90 por ciento. La red PPI representó las interacciones de la proteína BPIFA1 con otras proteínas inmunitarias coexpresadas. COX7B2, BPIFB6, BPIFB4, BPIFB2, BPIFB3, PLTP, CETP, BPI, LBP y ODF2L fueron los diez genes que determinamos que son responsables de estas interacciones de proteínas (Figura 6). Los genes BPIFB6, BPIFB4, BPIFB2 y BPIFB3 son los más significativos porque están implicados en las vías de señalización biológica, que desempeñan un papel fundamental en la inmunidad innata frente a la infección bacteriana. Además, estos genes están regulados positivamente por BPIFA1, lo que proporciona otra razón por la que son tan significativos (Tabla 6). Las interfases contienen agrupaciones de residuos conservados con una composición de aminoácidos compatible con el núcleo de la interfase (residuos con el mayor cambio en el entierro al unirse) y una región conservada [54], y las regiones calientes que evolucionan a partir de la agrupación de puntos calientes corresponden a regiones estrechamente empaquetadas. y regiones conservadas.
Por lo tanto, las interfaces están bajo presión evolutiva para mantener las conexiones actuales mientras evitan interacciones desfavorables y no específicas. Ciertas características fisicoquímicas pueden modificarse para reducir la probabilidad de que las interfaces proteína-proteína puedan formar interacciones disfuncionales [55]. Como resultado de nuestra investigación, encontramos que los valores eran más de 1 para los codones seleccionados positivamente presentados en la Tabla 1. Esto ilustra que el desarrollo de sitios sinónimos requirió más tiempo que el desarrollo de sitios no sinónimos (sitios dN). Este impacto benéfico de la selección darwiniana, que fomenta variaciones novedosas y mayor polimorfismo alelo, opera como una selección equilibrante o purificadora [56], que provoca una alteración en la proteína estructural y afecta la vía de señalización [57]. A pesar de que se originan en el mismo linaje, las sustituciones de aminoácidos en la descendencia de diferentes especies pueden tener consecuencias muy diferentes [56,57]. Esto contrasta con el hecho de que su pedigrí coincide con presentaciones anteriores. Los genes BPIFA1 elegidos en este estudio brindan información para el bioanálisis, que tiene como objetivo seleccionar genes en función de la escala de tiempo evolutiva desde los períodos más recientes hasta los más prolongados.
Además, el mecanismo evolutivo fundamental que se ha descubierto como resultado de investigaciones recientes puede ser insuficiente debido a la ausencia de las características estructurales y funcionales de un gran número de proteínas en el genoma. La evolución y adaptación de los genes que codifican proteínas en Drosophila melanogaster se examinaron minuciosamente para determinar los determinantes más relevantes de la evolución y la adaptación a nivel de los genes que codifican proteínas. Esto se logró comparando D. melanogaster con especies estrechamente relacionadas y sus poblaciones. Nuestro equipo llevó a cabo aplicaciones a gran escala de bioinformática y análisis estructural para determinar las características estructurales y funcionales de las proteínas. Posteriormente, dividimos los residuos en una variedad de sitios estructurales y funcionales usando nuestro sistema de categorización. Las tasas de evolución y adaptación de la secuencia se compararon en una variedad de proteínas y ubicaciones, lo que permitió la identificación de puntos críticos de adaptación en todo el genoma. Además, se ha demostrado que las proteínas de adaptación rápida interactúan entre sí a velocidades más altas de lo que podría predecirse por casualidad; este descubrimiento muestra que la coadaptación es probablemente omnipresente entre las proteínas de rápida adaptación.
Como resultado de sus conexiones físicas, los siguientes son ejemplos de mecanismos que tienen el potencial de contribuir a la coadaptación: (1) a menudo se encuentra que las proteínas de rápida adaptación están enriquecidas en actividades químicas similares y expuestas a una presión de selección similar, y (2 ) las proteínas de adaptación rápida coevolucionan. En esta investigación se demostraron dos casos diferentes de evolución adaptativa en los PPI, lo que lleva a los autores a plantear la hipótesis de que estas interacciones físicas pueden haber desempeñado un papel en la coadaptación de proteínas de adaptación rápida en D. melanogaster. Además, mostramos que el fenómeno de la coadaptación puede tener lugar en un sentido más general que solo entre proteínas de rápida adaptación. La tasa de adaptación suele ser mayor en proteínas que interactúan con proteínas de adaptación rápida. Dado que las interacciones moleculares juegan un papel en la evolución adaptativa, es justo anticipar que estas interacciones también pueden gobernar la coadaptación a un nivel más global. Se ha postulado que la coevolución de los contactos físicos es el mecanismo responsable de las tasas evolutivas similares observadas en las proteínas que interactúan.

5. Conclusiones
Nuestro objetivo fue identificar las presiones selectivas que han contribuido al desarrollo del sistema BPIFA1 de plantas y mamíferos, cuya expresión se modula en una amplia variedad de enfermedades. La proteína BPIFA1 evolucionó rápidamente en respuesta a la presión selectiva en el linaje humano y pudimos identificar los determinantes de la selección genética que explican su actividad bactericida. Durante su historia evolutiva, la selección positiva puede haber tenido un papel crucial en la mejora de la respuesta de virulencia a diferentes estímulos, lo que podría explicar la diversidad observada en la estabilidad de la función del gen. Nuestros hallazgos brindan una comprensión más completa de la historia evolutiva de los genes BPIFA1, lo que mejorará el análisis genómico funcional de la patogenicidad en los procesos biológicos. Se anticipa que estos hallazgos también pueden ayudar a mejorar la comprensión de la prevención de enfermedades. Además, el estudio de estos genes podría facilitar el diseño de un método único que podría ayudar a determinar las diversas proteínas de virulencia presentes en los patógenos bacterianos. Nuestros hallazgos nos llevan a plantear la hipótesis de que las restricciones durante el proceso evolutivo han jugado un papel clave en la configuración de nuestros descubrimientos. Como resultado de estas limitaciones, pudimos identificar algunos límites numéricos cuando acoplamos características como la longitud de la proteína a complejos complicados. Las características únicas de las proteínas son intrigantes porque pueden proporcionar una indicación de factores estresantes inusuales o ajustes homeostáticos que han permitido su presencia en las células. Por lo tanto, son una opción prometedora para futuras investigaciones.
Contribuciones de autor:
Conceptualización, HIA y JC; metodología, HIA, MAK, FAK, SI, RWA y NSP; software, HIA, WN, NSP, RWA y SI; validación, MAK, JC, FAK y HIA; análisis formal, HIA, MAK, FAK, SI, RWA y NSP; investigación, HIA, MAK, FAK, SI, RWA y NSP; recursos, HIA, MAK y JC; curación de datos, HIA, MAK, FAK, SI, RWA y WN; redacción—preparación del borrador original, EIS; redacción: revisión y edición, HIA, SI, RWA, WN y NSP; visualización, JC y MAK; supervisión, MAK, FAK, NSP y WN Todos los autores han leído y aceptado la versión publicada del manuscrito.
Fondos:
Esta investigación no recibió financiación externa.
Declaración de la Junta de Revisión Institucional:
No aplica.
Declaración de consentimiento informado:
No aplica.
Declaración de disponibilidad de datos:
Todos los datos relevantes para este artículo estarán disponibles abiertamente para los lectores.
Expresiones de gratitud:
Este estudio fue apoyado por el Proyecto Especial Financiero Provincial de Guangdong de 2022 para la Construcción Forestal Ecológica.
Conflictos de interés:
Los autores declaran no tener conflicto de intereses.
Referencias
1. Li, J.; Xu, P.; Wang, L.; Feng, M.; Chen, D.; Yu, X.; Lu, Y. Biología molecular de BPIFB1 y sus avances en la enfermedad. Ana. Traducir Medicina. 2020, 8, 651. [CrossRef] [PubMed] 2. Saferali, A.; espiga, CA; Strug, LJ; Quon, BS; Zlosnik, J.; Sandford, AJ; Turvey, SE Función inmunomoduladora del gen modificador de fibrosis quística BPIFA1. PLoS ONE 2020, 15, e0227067. [Referencia cruzada] [PubMed]
3. Nam, B.-H.; Luna, J.-Y.; Park, E.-H.; Kim, Y.-O.; Kim, D.-G.; Kong, HJ; Kim, W.-J.; Jee, YJ; una, CM; Parque, NG; et al. Actividad antimicrobiana de péptidos derivados de la proteína de unión a lipopolisacáridos de platija de oliva/proteína que aumenta la permeabilidad bactericida (LBP/BPI). Mar. Drugs 2014, 12, 5240–5257. [Referencia cruzada] [PubMed]
4. Kirschning, CJ; Au-Young, J.; Lámparas, N.; Reuter, D.; Pfeil, D.; Seilhamer, JJ; Schumann, RR Una organización similar de los genes de la proteína de unión a lipopolisacáridos (LBP) y la proteína de transferencia de fosfolípidos (PLTP) sugiere una familia de genes común de proteínas de unión a lípidos. Genomics 1997, 46, 416–425. [Referencia cruzada] [PubMed]
5. Balakrishnan, A.; Marathé, SA; Joglekar, M.; Chakraborty, D. Proteína bactericida/que aumenta la permeabilidad: una proteína multifacética con funciones más allá de la neutralización de LPS. Inmunidad innata 2012, 19, 339–347. [Referencia cruzada]
6. Wright, SD; Ramos, RA; Tobías, PS; Ulevitch, RJ; Mathison, JC CD14, un receptor para complejos de lipopolisacárido (LPS) y proteína de unión a LPS. Ciencia 1990, 249, 1431–1433. [Referencia cruzada]
7. Shao, Y.; Li, C.; Che, Z.; Zhang, P.; Zhang, W.; Duan, X.; Li, Y. Clonación y caracterización de dos genes de proteína de unión a lipopolisacárido/proteína que aumenta la permeabilidad bactericida (LBP/BPI) del pepino de mar Apostichopus japonicas con función diversificada en la modulación de la producción de ROS. desarrollo compensación inmunol. 2015, 52, 88–97. [Referencia cruzada]
8. Schaefer, N.; Li, X.; Seibold, MA; Jarjour, NN; Denlinger, LC; Castro, M.; piedra de cobertura, AM; Teague, WG; Boomer, J.; Bleecker, ER El efecto de la variación genética BPIFA1/SPLUNC1 en su expresión y función en el epitelio de las vías respiratorias asmáticas. JCI Insight 2019, 4, e127237. [Referencia cruzada]
9. Brito, CJ; Cohn, L. Miembro de la familia A1 que contiene pliegues de proteína bactericida/que aumenta la permeabilidad en la protección del huésped de las vías respiratorias y la enfermedad respiratoria. Soy. J. Respir. Mol celular. Biol. 2015, 52, 525–534. [Referencia cruzada]
10. Musa, M.; Wilson, K.; Sol, L.; Mulay, A.; Binglé, L.; Marriot, HM; LeClair, EE; Bingle, CD Localización diferencial de BPIFA1 (SPLUNC1) y BPIFB1 (LPLUNC1) en las cavidades nasal y oral de ratones. Res. de tejido celular. 2012, 350, 455–464. [Referencia cruzada]
11. Tsou, Y.-A.; Tung, MC-C.; Alejandro, KA; Chang, W.-D.; Tsai, M.-H.; Chen, H.-L.; Chen, C.-M. El papel de BPIFA1 en infecciones microbianas de las vías respiratorias superiores y enfermedades relacionadas. Res. biomédica. En t. 2018, 2018, 2021890. [Referencia cruzada] [PubMed]
12. Caikauskaite, R. BPIFA1 Interacciones con bacterias y su importancia para la defensa del huésped de las vías respiratorias. Doctor. Tesis, Universidad de Sheffield, Sheffield, Reino Unido, 2018.
For more information:1950477648nn@gmail.com
