Segunda parte Asociación de MAFLD con diabetes, enfermedad renal crónica y enfermedad cardiovascular: un estudio de cohorte de 4.6-años en China
Jun 15, 2023
Resultados
Las características generales de los 6873 participantes al inicio del estudio se presentan en la Tabla 1. Entre los individuos con una mediana de edad de 61,6 años (rango intercuartílico, 58,7- 65,2 años), el 57,6 % eran mujeres; el 10,1 por ciento consumía alcohol en exceso y el 20,4 por ciento eran fumadores activos; 47.2 por ciento fueron diagnosticados con hígado graso; el 72,6 por ciento, el 20,4 por ciento y el 17,4 por ciento tenían sobrepeso/obesidad, diabetes y desregulación metabólica, respectivamente; y el 5,3 por ciento había dado positivo para el VHB.

ALT, alanina aminotransferasa; AST, aspartato aminotransferasa; IMC, índice de masa corporal; PAD, presión arterial diastólica; FPG, glucosa plasmática en ayunas; GGT, gamma-glutamil transpeptidasa; HbA1c, hemoglobina glicosilada A1c; HBsAg, antígeno de superficie de la hepatitis B; VHB, virus de la hepatitis B; HDL-C, colesterol de lipoproteínas de alta densidad; HOMA-IR, evaluación del modelo de homeostasis de la resistencia a la insulina; hs-CRP, proteína C reactiva de alta sensibilidad; LDL-C, colesterol de lipoproteínas de baja densidad; MAFLD, enfermedad del hígado graso asociado a disfunción metabólica; NAFLD, enfermedad del hígado graso no alcohólico; PAS, presión arterial sistólica; CT, colesterol total; TG, triglicéridos.
a. Los datos se presentan como mediana (rango intercuartílico).
b. Sobrepeso/obesidad: IMC de 23.0 o mayor; obesidad central: circunferencia de cintura mayor o igual a 90/80 cm en hombres y mujeres; hipertensión: presión arterial mayor o igual a 130/85 mm Hg o tratamiento farmacológico específico; diabetes: GPA mayor o igual a 7,0 mmol/L, o HbA1c mayor o igual a 6,5 por ciento o antecedentes de diabetes; prediabetes: FPG de 5,6 a 6,9 mmol/L o HbA1c de 5,7 a 6,4 por ciento en participantes sin diagnóstico previo de diabetes; TG elevados: TG mayores o iguales a 1,70 mmol/L o tratamiento farmacológico específico; HDL-C reducido: HDL-C inferior a 1,0 mmol/L para hombres y inferior a 1,3 mmol/L para mujeres o tratamiento farmacológico específico; HOMA-IR elevado: HOMA-IR mayor o igual a 2,5; hs-CRP elevada: hs-CRP superior a 2 mg/L; el consumo excesivo de alcohol se definió como más de 140 g semanales de consumo de alcohol en hombres y más de 70 g semanales en mujeres; La infección por VHB se definió como HBsAg positivo o antecedentes de infección por VHB.

Haga clic aquí para comprar productos Cistanche
1. Tasas de prevalencia e incidencia de la enfermedad del hígado graso asociado a la disfunción metabólica y la enfermedad del hígado graso no alcohólico
Entre 6873 participantes, 2771 (40.3 por ciento) y 3212 (46.7 por ciento) fueron diagnosticados con NAFLD y MAFLD, respectivamente; y 321 (4,7 por ciento) y 156 (2,3 por ciento) tenían MAFLD con consumo excesivo de alcohol e infección por VHB, respectivamente (Fig. 2A). Después de un seguimiento promedio de 4.6-años, entre 3632 personas con hígado no graso (no LF) al inicio del estudio, las tasas de incidencia de NAFLD y MAFLD fueron del 22,7 % (95 % IC, 21,3 % {{ 24}}.0 por ciento) y 27.0 por ciento (IC del 95 por ciento, 25.5 por ciento -28.4 por ciento), respectivamente (Fig. 2B).

Figura 2. A, Prevalencia, y B, incidencia, de enfermedad del hígado graso no alcohólico (NAFLD) y enfermedad del hígado graso asociada a disfunción metabólica (MAFLD).
2. Asociaciones de disfunción metabólica: enfermedad del hígado graso asociada y enfermedad del hígado graso no alcohólico con diabetes
La prevalencia de diabetes al inicio del estudio fue del 12,4 % (IC del 95 %, 11,3 % -13,5 %), 29,6 % (IC del 95 %, 28,0 % -31,2 %) , y 29,5 por ciento (95 por ciento IC, 27,8 por ciento -31,2 por ciento) entre aquellos con no FL, MAFLD y NAFLD, respectivamente; y fue del 31,4 por ciento (IC del 95 por ciento, 26,3 por ciento -36,4 por ciento) y del 23,7 por ciento (IC del 95 por ciento, 17,0 por ciento -30,4 por ciento) en los subgrupos de MAFLD con consumo excesivo de alcohol e infección por VHB, respectivamente. En comparación con aquellos sin FL, los pacientes con MAFLD y NAFLD tenían riesgos significativamente más altos de diabetes prevalente tanto en el modelo 1 como en el modelo 2. Además, MAFLD con consumo excesivo de alcohol e infección por VHB también se asoció con mayores riesgos de diabetes prevalente (Fig. 3).

Figura 3. Asociaciones de enfermedad del hígado graso asociada a disfunción metabólica (MAFLD) y enfermedad del hígado graso no alcohólico (NAFLD) con diabetes prevalente. *La disfunción metabólica se definió como la presencia de al menos 1 de 3 criterios: sobrepeso/obesidad, diabetes o desregulación metabólica. †Modelo 1 ajustado por edad y sexo. ‡Modelo 2: modelo 1 más un ajuste por antecedentes educativos, tabaquismo y ejercicio en el tiempo libre al inicio del estudio. VHB, virus de la hepatitis B; hígado no graso, no FL; O, razón de probabilidades.

extracto de cistanche
Después de un seguimiento promedio de 4.6-años, de 5440 personas sin diabetes al inicio del estudio, las tasas de incidencia de diabetes fueron del 6,5 % (IC del 95 %, 5,6 % -7).3 por ciento), 12,4 por ciento (IC del 95 por ciento, 11,1 por ciento -13,8 por ciento) y 12,0 por ciento (IC del 95 por ciento, 10,6 por ciento -13,5 por ciento) entre aquellos con no FL, MAFLD y NAFLD, respectivamente; y fueron 14.8 por ciento (95 por ciento IC, 10.1 por ciento -19.6 por ciento) y 12.0 por ciento (95 por ciento IC, 6.1 por ciento -17.9 por ciento) en los subgrupos MAFLD con consumo excesivo de alcohol e infección por VHB , respectivamente. En comparación con aquellos sin FL, los pacientes con MAFLD y NAFLD tenían un mayor riesgo de diabetes incidente (RR 2,08; IC del 95 %, 1,72-2,52; RR 2,01; IC del 95 %, 1,{{51} }.46, respectivamente) después de ajustar por edad, sexo, nivel educativo, tabaquismo y ejercicio en el tiempo libre. Asociaciones positivas de MAFLD con consumo excesivo de alcohol (RR 2,49; IC del 95 %, 1,64-3,78) e infección por VHB (RR 1,98; IC del 95 %, 1,11-3,52) con diabetes incidente se observaron (Fig. 4).

Figura 4. Asociaciones de enfermedad del hígado graso asociada a disfunción metabólica (MAFLD) y enfermedad del hígado graso no alcohólico (NAFLD) con diabetes incidente. *La disfunción metabólica se definió como la presencia de al menos 1 de 3 criterios: sobrepeso/obesidad, diabetes o desregulación metabólica. †Modelo 1 ajustado por edad y sexo. ‡Modelo 2: modelo 1 más un ajuste por antecedentes educativos, tabaquismo y ejercicio en el tiempo libre al inicio del estudio. VHB, virus de la hepatitis B; hígado no graso, no FL; RR, razón de riesgo.
3. Asociaciones de la disfunción metabólica asociada con la enfermedad del hígado graso y la enfermedad del hígado graso no alcohólico con la enfermedad renal crónica y la enfermedad cardiovascular
Después de un seguimiento promedio de 4.6-años, de 6176 participantes sin ERC al inicio del estudio, las tasas de incidencia de ERC entre aquellos sin FL, MAFLD y NAFLD fueron del 8,2 % (IC del 95 %, 7,3 % { {10}},2 por ciento), 12,9 por ciento (95 por ciento IC, 11.7- 14.1) y 13,4 por ciento (95 por ciento IC, 12.0 por ciento {{ 23}}.7 por ciento), respectivamente; y fueron 8.1 por ciento (95 por ciento IC, 4.9 por ciento {{30}}.2 por ciento) y 11.0 por ciento (95 por ciento IC, 5.8 por ciento -16.3 por ciento) en los subgrupos MAFLD con exceso consumo de alcohol e infección por VHB, respectivamente (tabla 2). La Tabla 3 muestra que, de 6395 personas sin CVD al inicio, las tasas de incidencia de CVD (por 1000 años-persona de seguimiento) entre aquellos con no FL, MAFLD y NAFLD fueron 8,7 (IC del 95 %, 7).{{ 50}},3), 12,3 (IC del 95 %, 10,6-14,4) y 12,6 (IC del 95 %, 10,7-14,9), respectivamente; y fueron 9,0 (IC del 95 %, 5,1-15,8) y 12,8 (IC del 95 %, 6,4-25,7) en los subgrupos de MAFLD con consumo excesivo de alcohol e infección por VHB, respectivamente. En comparación con aquellos sin FL, se observaron mayores riesgos de incidentes de ERC y CVD entre pacientes con MAFLD y NAFLD, pero no se observaron en los pacientes con subgrupos de MAFLD con consumo excesivo de alcohol e infección por VHB tanto en el Modelo 1 como en el Modelo 2 (consulte las Tablas 2 y 3).
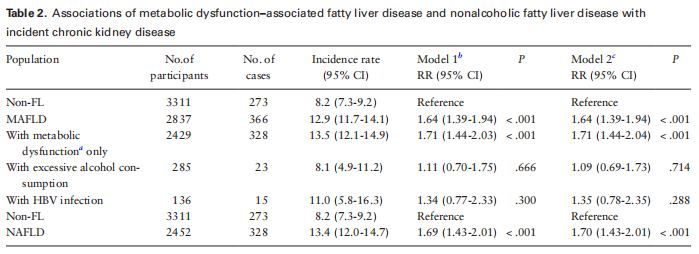
Abreviaturas: VHB, virus de la hepatitis B; MAFLD, enfermedad del hígado graso asociado a disfunción metabólica; NAFLD, enfermedad del hígado graso no alcohólico; hígado no graso, no FL; RR, razón de riesgo.
a. La disfunción metabólica se definió como la presencia de al menos 1 de 3 criterios: sobrepeso/obesidad, diabetes o desregulación metabólica.
b. El modelo 1 fue ajustado por sexo y edad.
C. El modelo 2 se ajustó por sexo, edad, nivel educativo, tabaquismo y ejercicio en el tiempo libre al inicio del estudio.

Cistanche en polvo
Discusión
En esta cohorte retrospectiva basada en la comunidad de 6873 individuos chinos de mediana edad y ancianos, las tasas de prevalencia e incidencia de MAFLD fueron del 46,7 % y del 27,0 %. En comparación con NAFLD, la prevalencia y la tasa de incidencia aumentaron un 6,4 % y un 4,3 %, respectivamente. Tanto MAFLD como NAFLD aumentaron los riesgos incidentes de diabetes, ERC y ECV, pero estos riesgos fueron prácticamente equivalentes entre los dos. Además, la definición de MAFLD identificó una porción adicional considerable de pacientes con hígado metabólicamente graso concomitante con el consumo excesivo de alcohol y la infección por VHB, que tenían un mayor riesgo de incidencia y prevalencia de diabetes en comparación con los que no tienen FL.
Este estudio mostró que MAFLD y NAFLD eran altamente prevalentes. Después de un seguimiento de 4.6-años, entre los participantes chinos de mediana edad y ancianos, casi una cuarta parte desarrolló MAFLD o NAFLD. Dado que la exclusión de otras enfermedades hepáticas concomitantes no era un requisito previo para el diagnóstico de MAFLD, como era de esperar, hubo una mayor prevalencia de MAFLD que de EHGNA en nuestro estudio. De manera similar, 3 estudios (7, 20, 21) en Asia informaron una mayor prevalencia de MAFLD que de NAFLD, mientras que la Tercera Encuesta Nacional de Examen de Salud y Nutrición (6) observó un hallazgo opuesto, que podría deberse a (i) una falta de una prueba de hepatitis viral; o (ii) menores proporciones de anomalías metabólicas. Nuestro estudio informa por primera vez la tasa de incidencia de MAFLD diagnosticada por ultrasonido y mostró una tasa de incidencia ligeramente mayor de MAFLD que la de NAFLD. Sin embargo, otro estudio de cohortes de Hong Kong mostró que la tasa de incidencia de MAFLD era un 25 % más baja que la de NAFLD (9). Estas diferencias en las tasas de prevalencia e incidencia de MAFLD y NAFLD pueden verse afectadas por las proporciones de anormalidades metabólicas y otras condiciones coexistentes entre sus poblaciones de estudio.
Recientemente, un metanálisis actualizado de 33 estudios encontró un aumento de 2.2-veces en el riesgo de diabetes incidente asociada con NAFLD durante un período de seguimiento medio de 5-años (22). De acuerdo con estos hallazgos anteriores, nuestros resultados mostraron que NAFLD se asoció con un riesgo 2.01-veces mayor de diabetes incidente durante un período de seguimiento de 4.6-años. También encontramos una asociación similar entre MAFLD y diabetes incidente con un RR de 2,08. Hasta la fecha, faltan datos sobre la asociación entre MAFLD (diagnosticada por ultrasonido) y diabetes incidente.
Compared with the NAFLD definition, excessive alcohol consumption was no longer excluded from diagnosing MAFLD, making it possible to assess the interaction between alcohol consumption and metabolic risk factors. In this study, 4.7% of participants were diagnosed with MAFLD with excessive alcohol consumption. Previous cohort studies showed that in the general population, excessive alcohol consumption was associated with a 1.4- to 1.8-fold greater risk of incident diabetes (23-25). Our study observed that MAFLD with excessive alcohol consumption (> 140 g/week for men; > 70 g/week for women) was associated with an approximately 2.5-fold greater risk of incident diabetes. Similarly, a cohort study of 9948 Japanese men demonstrated that individuals with fatty liver concomitant with excessive alcohol consumption (>280 g/semana) tenían 3,45 veces más riesgo de diabetes en comparación con aquellos sin hígado graso y que consumían menos de 40 g de alcohol por semana durante un período de seguimiento medio de 6-años (25). Además, nuestro estudio encontró que los pacientes con MAFLD con consumo excesivo de alcohol, en comparación con aquellos con disfunción metabólica solamente, tienen un riesgo ligeramente mayor de diabetes. Este hallazgo indica el posible efecto sinérgico del consumo excesivo de alcohol, el hígado graso y la disfunción metabólica en el desarrollo de la diabetes. Por lo tanto, se debe recomendar a los pacientes con MAFLD que eviten el consumo excesivo de alcohol para prevenir la diabetes, que es un problema de salud importante que afecta a casi 500 millones de personas en todo el mundo y causa muchas complicaciones que amenazan la salud (26).
Además de los factores de riesgo metabólicos y el consumo excesivo de alcohol, la infección por VHB se incluyó en la definición de MAFLD. En nuestro estudio, el 2,3 por ciento de los participantes tenían MAFLD con infección por VHB. La infección por VHB puede causar daño hepático y provocar una desregulación de la homeostasis de la glucosa e incluso diabetes. Nuestros resultados muestran que MAFLD con infección por VHB se asoció con un riesgo 2-veces mayor de incidencia de diabetes. Estudios prospectivos previos demostraron que la NAFLD y la infección por VHB podrían exacerbar colectivamente la lesión hepática y aumentar el riesgo de fibrosis hepática y carcinoma hepatocelular (3, 27). Además, la diabetes se asoció con un aumento significativo del riesgo de carcinoma hepatocelular en personas con infección por VHB (28, 29). Dado que todavía hay entre 77 y 97 millones de personas con infección por VHB en China (30), era más práctico utilizar la definición de MAFLD para identificar a más pacientes con hígado graso e infección por VHB para controlar la progresión de la enfermedad. Se deben diseñar ensayos clínicos adicionales para evaluar los beneficios clínicos de intervenciones específicas en subgrupos de pacientes con MAFLD con diferentes etiologías.

Cistanche tubulosa
Dos metanálisis integrales encontraron mayores riesgos de ERC y ECV asociados con NAFLD (31, 32). Nuestro estudio indicó que MAFLD y NAFLD se asociaron con un mayor riesgo de CKD y CVD, pero no se observaron asociaciones entre MAFLD y CKD o CVD en los subgrupos con consumo excesivo de alcohol e infección por VHB. Recientemente, un estudio de cohorte retrospectivo de más de 8 millones de surcoreanos mostró que el MAFLD (identificado por el índice de hígado graso) concomitante con otra etiología se asoció con un riesgo significativamente mayor de ECV después de una mediana de seguimiento de 10,1 años (20). En nuestro estudio no se encontró una asociación positiva entre MAFLD con el consumo excesivo de alcohol y la infección por VHB y ECV, lo que podría atribuirse a un tamaño de muestra más pequeño y una duración de seguimiento más corta.
Fortalezas y limitaciones
El estudio de cohorte de Shanghai Nicheng se diseñó inicialmente como una cohorte prospectiva basada en la comunidad para investigar la prevalencia y la incidencia de enfermedades cardiometabólicas. Este estudio recopiló datos clínicos completos y detallados al inicio del estudio, como el consumo de alcohol, HBsAg, anticuerpos contra el virus de la hepatitis C, HOMA-IR y hs-CRP, y evaluó múltiples eventos de resultado. Además, nuestro estudio, por primera vez, informó la tasa de incidencia de MAFLD diagnosticada por ultrasonido y evaluó los efectos de MAFLD y sus subgrupos con consumo excesivo de alcohol e infección por VHB en diabetes, ERC y ECV incidentes.
Hay algunas limitaciones en este estudio. En primer lugar, se utilizó la ecografía, en lugar de una biopsia hepática, para diagnosticar la esteatosis hepática. Tenía una sensibilidad limitada del 60 por ciento al 94 por ciento (33) y no detectaba con precisión la esteatosis cuando la infiltración de grasa hepática era inferior al 20 por ciento (34, 35), y su precisión diagnóstica era subóptima en participantes con un IMC superior a 40,0 (36). Sin embargo, la ecografía es la modalidad de imagen de primera elección para detectar la esteatosis hepática en la práctica clínica y en estudios epidemiológicos a gran escala (37, 38). En segundo lugar, la duración del seguimiento es comparativamente más corta y podría limitar los hallazgos de asociaciones significativas entre MAFLD y CKD o CVD. En tercer lugar, no se evaluaron otros posibles factores de confusión, como la dieta, los factores genéticos y los medicamentos. Finalmente, debido a que realizamos nuestro estudio con una población china de mediana edad a mayor, cuya disfunción metabólica era particularmente común, y excluimos a 19 individuos por falta de datos para el diagnóstico de MAFLD, podría haber un sesgo de selección y una limitación a la generalización de nuestro resultados.
En resumen, MAFLD y NAFLD son muy frecuentes entre los chinos de mediana edad y ancianos. El cambio de NAFLD a MAFLD no afectó los riesgos incidentes de diabetes, ERC y ECV. Sin embargo, la definición MAFLD capturó una porción adicional considerable de pacientes con hígado metabólicamente graso acompañado de un consumo excesivo de alcohol o infección por VHB. Estos pacientes tendrían una mayor prevalencia y riesgos de incidencia de diabetes en comparación con los de las personas sin FL. Por lo tanto, se debe prestar más atención a aquellos con alto riesgo de trastornos metabólicos y estratificación para el manejo en la práctica clínica.

suplemento de cistanche
Rreferencias
1. Younossi ZM, Koenig AB, Abdelatif D, Fazel Y, Henry L, Wymer M. Epidemiología global de la enfermedad del hígado graso no alcohólico: evaluación metaanalítica de prevalencia, incidencia y resultados. hepatología. 2016;64(1):73-84.
2. Zhou F, Zhou J, Wang W, et al. El inesperado y rápido aumento de la carga de NAFLD en China de 2008 a 2018: una revisión sistemática y un metanálisis. hepatología. 2019;70(4):1119-1133.
3. Choi HSJ, Brouwer WP, Zanjir WMR, et al. La esteatohepatitis no alcohólica se asocia con resultados relacionados con el hígado y mortalidad por todas las causas en la hepatitis B crónica. Hepatología. 2020;71(2):539-548.
4. Chiang DJ, McCullough AJ. El impacto de la obesidad y el síndrome metabólico en la enfermedad hepática alcohólica. Clin enfermedad del hígado. 2014;18(1):157-163.
5. Eslam M, Newsome PN, Sarin SK, et al. Una nueva definición para la enfermedad del hígado graso asociada a la disfunción metabólica: una declaración de consenso de expertos internacionales. J Hepatol. 2020;73(1):202-209.
6. Lin S, Huang J, Wang M, et al. Comparación de los criterios de diagnóstico de MAFLD y NAFLD en el mundo real. Hígado Int. 2020;40(9):2082-2089.
7. Yamamura S, Eslam M, Kawaguchi T, et al. MAFLD identifica a los pacientes con fibrosis hepática significativa mejor que NAFLD. Hígado Int. 2020;40(12):3018-3030.
8. Sun DQ, Jin Y, Wang TY, et al. MAFLD y riesgo de ERC. Metabolismo. 2021;115:154433.
9. Wai-Sun Wong V, Lai-Hung Wong G, Woo J, et al. Impacto de la nueva definición de enfermedad del hígado graso asociada al metabolismo en la epidemiología de la enfermedad. Clin Gastroenterol Hepatol. Publicado en línea el 31 de octubre de 2020. doi:10.1016/j. cgh.2020.10.046
10. Ciardullo S, Perseghin G. Prevalencia de NAFLD, MAFLD y fibrosis avanzada asociada en la población contemporánea de los Estados Unidos. Hígado Int. 2021;41(6):1290-1293.
11. Semmler G, Wernly S, Bachmayer S, et al. La enfermedad del hígado graso asociado a la disfunción metabólica (MAFLD, por sus siglas en inglés) es más un espectador que un impulsor de la mortalidad. J Clin Endocrinol Metab. 2021;106(9):2670-2677.
12. Chen P, Hou X, Hu G, et al. Tejido adiposo subcutáneo abdominal: ¿un depósito adiposo favorable para la diabetes? Diabetes cardiovascular. 2018;17(1):93.
13. Guo F, Moellering DR, Garvey WT. La progresión de la enfermedad cardiometabólica: validación de un nuevo sistema de estadificación de la enfermedad cardiometabólica aplicable a la obesidad. Obesidad (Silver Spring). 2014;22(1):110-118.
14. Luepker RV, Evans A, McKeigue P, Reddy KS. Métodos de encuesta cardiovascular. 3ra ed. Organización Mundial de la Salud, 2004.
15. Matthews DR, Hosker JP, Rudenski AS, Naylor BA, Treacher DF, Turner RC. Evaluación del modelo de homeostasis: resistencia a la insulina y función de las células beta a partir de las concentraciones de insulina y glucosa plasmática en ayunas en el hombre. Diabetología. 1985;28(7):412-419.
16. Farrell GC, Chitturi S, Lau GK, Sollano JD; Grupo de Trabajo de Asia-Pacífico sobre EHGNA. Directrices para la evaluación y el tratamiento de la enfermedad del hígado graso no alcohólico en la región de Asia y el Pacífico: resumen ejecutivo. J Gastroenterol Hepatol. 2007;22(6):775-777.
17. Asociación Americana de Diabetes. 2. Clasificación y diagnóstico de la diabetes: estándares de atención médica en diabetes—2021. Cuidado de la diabetes. 2021;44(Suplemento 1):S15-S33.
18. Levey AS, Stevens LA, Schmid CH, et al; CKD-EPI (Colaboración de Epidemiología de la Enfermedad Renal Crónica). Una nueva ecuación para estimar la tasa de filtración glomerular. Ann Intern Med. 2009;150(9):604-612.
19. Becker GJ, Wheeler DC, Zeeuw DD, et al. Enfermedad renal: grupo de trabajo de presión arterial para mejorar los resultados globales (KDIGO, por sus siglas en inglés). Guía de práctica clínica KDIGO para el manejo de la presión arterial en la enfermedad renal crónica. Riñón Int Supl. 2012;2(5):337-414.
20. Lee H, Lee YH, Kim SU, Chang Kim H. La disfunción metabólica asociada con la enfermedad del hígado graso y el riesgo de enfermedad cardiovascular incidente: un estudio de cohorte a nivel nacional. Clin Gastroenterol Hepatol. Publicado en línea el 22 de diciembre de 2020. doi:10.1016/j. cgh.2020.12.022
21. Huang SC, Su HJ, Kao JH, et al. Características clínicas e histológicas de pacientes con enfermedad del hígado graso asociada a disfunción metabólica comprobada por biopsia. Hígado intestinal. 2021;15(3):451-458.
22. Mantovani A, Petracca G, Beatrice G, Tilg H, Byrne CD, Targher G. Enfermedad del hígado graso no alcohólico y riesgo de diabetes mellitus incidente: un metanálisis actualizado de 501 022 individuos adultos. Intestino. 2021;70(5):962-969.
23. Lee DY, Yoo MG, Kim HJ, et al. Asociación entre el patrón de consumo de alcohol y el riesgo de incidencia de diabetes tipo 2 en hombres coreanos: un estudio de seguimiento de 12-años. Sci Rep. 2017;7(1):7322.
24. Kao WH, Puddey IB, Boland LL, Watson RL, Brancati FL. El consumo de alcohol y el riesgo de diabetes mellitus tipo 2: Estudio de riesgo de aterosclerosis en comunidades. Am J Epidemiol. 2001;154(8):748-757.
25. Okamura T, Hashimoto Y, Hamaguchi M, Obora A, Kojima T, Fukui M. Efecto del consumo de alcohol y la presencia de hígado graso en el riesgo de diabetes tipo 2 incidente: un estudio longitudinal basado en la población. BMJ Open Diabetes Res Care. 2020;8:e001629.
26. Federación Internacional de Diabetes. Atlas de diabetes de la FID. 9ª ed. Federación Internacional de Diabetes; 2019.
27. Chan AW, Wong GL, Chan HY, et al. El hígado graso concurrente aumenta el riesgo de carcinoma hepatocelular en pacientes con hepatitis B crónica. J Gastroenterol Hepatol. 2017;32(3):667-676.
28. Tan Y, Zhang X, Zhang W, et al. La influencia del síndrome metabólico en el riesgo de carcinoma hepatocelular en pacientes con infección crónica por hepatitis B en China continental. Biomarcadores de Epidemiol de Cáncer Prev. 2019;28(12):2038-2046.
29. Chen CL, Yang HI, Yang WS, et al. Factores metabólicos y riesgo de carcinoma hepatocelular por infección crónica por hepatitis B/C: un estudio de seguimiento en Taiwán. Gastroenterología. 2008;135(1):111-121.
30. Colaboradores del Observatorio Polaris. Prevalencia mundial, tratamiento y prevención de la infección por el virus de la hepatitis B en 2016: un estudio de modelado. Lancet Gastroenterol Hepatol. 2018;3(6):383-403.
31. Targher G, Byrne CD, Lonardo A, Zoppini G, Barbui C. Enfermedad del hígado graso no alcohólico y riesgo de enfermedad cardiovascular incidente: un metanálisis. J Hepatol. 2016;65(3):589-600.
32. Mantovani A, Petracca G, Beatrice G, et al. Enfermedad del hígado graso no alcohólico y riesgo de enfermedad renal crónica incidente: un metanálisis actualizado. Intestino. Publicado en línea el 10 de diciembre de 2020. doi:10.1136/gutjnl-2020-323082
33. Schwenzer NF, Springer F, Schraml C, Stefan N, Machann J, Schick F. Evaluación no invasiva y cuantificación de la esteatosis hepática por ultrasonido, tomografía computarizada y resonancia magnética. J Hepatol. 2009;51(3):433-445.
34. Saadeh S, Younossi ZM, Remer EM, et al. La utilidad de la imagen radiológica en la enfermedad del hígado graso no alcohólico. Gastroenterología. 2002;123(3):745-750.
35. Fishbein M, Castro F, Cheruku S, et al. Resonancia magnética hepática para cuantificación de grasa: su relación con la morfología, el diagnóstico y la ecografía de la grasa. J Clin Gastroenterol. 2005;39(7):619-625.
36. Ryan CK, Johnson LA, Germin BI, Marcos A. Cien biopsias hepáticas consecutivas en el estudio de donantes vivos para trasplante hepático del lóbulo derecho. Trasplante de hígado 2002;8(12):1114-1122.
37. Hernáez R, Lazo M, Bonekamp S, et al. Precisión diagnóstica y confiabilidad de la ecografía para la detección de hígado graso: un metanálisis. hepatología. 2011;54(3):1082-1090.
38. Chang Y, Ryu S, Kim Y, et al. Bajos niveles de consumo de alcohol, obesidad y desarrollo de hígado graso con y sin evidencia de fibrosis avanzada. hepatología. 2020;71(3):861-873.
Yebei Liang 1, Hongli Chen 1, Yuexing Liu 1, Xuhong Hou 1, Li Wei 1, Yuqian Bao 1, Chunguang Yang,1 Geng Zong,2,3 Jiarui Wu,4 y Weiping Jia,1
1 Instituto de Diabetes de Shanghái, Sexto Hospital Popular afiliado a la Universidad Jiao Tong de Shanghái, Laboratorio Clave de Diabetes Mellitus de Shanghái, Departamento de Endocrinología y Metabolismo, Centro Clínico de Diabetes de Shanghái, Centro Clínico Clave de Enfermedades Metabólicas de Shanghái, Shanghái 200233, China;
2 Instituto de Nutrición y Salud de Shanghái, Universidad de la Academia de Ciencias de China, Academia de Ciencias de China, Shanghái, 200031, China;
3 Sexto Hospital Popular afiliado a la Universidad Jiao Tong de Shanghái, Shanghái, 200233, China;
4 CAS Laboratorio clave de biología de sistemas, Instituto de bioquímica y biología celular de Shanghái, Centro de excelencia en ciencia celular molecular, Academia de Ciencias de China, Shanghái 200031, China






