Potencia del bisresorcinol de Heliciopsis terminalis sobre el envejecimiento de la piel: bioactividades in vitro e interacciones moleculares, parte 2
May 10, 2023
Análisis de interacción molecular
Se aplicó el acoplamiento molecular para predecir los sitios de unión de los compuestos de prueba a los receptores de proteínas, como la colagenasa, la elastasa y la tirosinasa, en comparación con los inhibidores conocidos de una enzima correspondiente (Información complementaria). De acuerdo con publicaciones anteriores, se evaluó la afinidad de unión relativa mientras que las interacciones de unión se ilustraron a través de la conformación mejor predicha (Teajaroen et al., 2020; Jewboonchu et al., 2020; Tanawattanasuntorn et al., 2020; Saeloh et al., 2017). ).

Según estudios relevantes, la cistanche es una hierba común conocida como "la hierba milagrosa que prolonga la vida". Su principal componente es el cistanosido, que tiene diversos efectos como antioxidante, antiinflamatorio y promotor de la función inmunológica. El mecanismo entre la cistanche y el blanqueamiento de la piel radica en el efecto antioxidante de los glucósidos de cistanche. La melanina en la piel humana se produce por la oxidación de la tirosina catalizada por la tirosinasa, y la reacción de oxidación requiere la participación de oxígeno, por lo que los radicales libres de oxígeno en el cuerpo se convierten en un factor importante que afecta la producción de melanina. Cistanche contiene cistanosido, que es un antioxidante y puede reducir la generación de radicales libres en el cuerpo, inhibiendo así la producción de melanina.

Haga clic en Cistanches Herba para blanquear
Para más información:
david.deng@wecistanche.com WhatsApp:86 13632399501
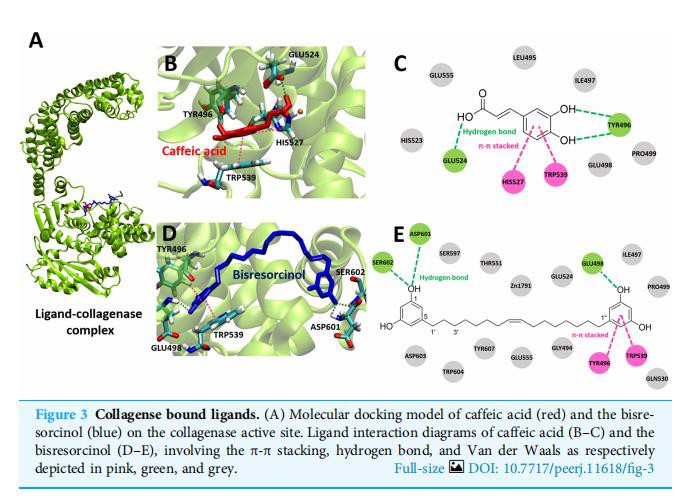
Para la enzima colagenasa, los resultados de las interacciones ligando-proteína se demostraron en la Fig. 3 y la Tabla S1. La energía de unión de −5,89 kcal mol−1 a la colagenasa clostridial (PDB ID 2Y6I) la presentó el bisresorcinol. Se determinó un rango de energía de unión entre -3,68 y -7,90 kcal mol-1 para otros inhibidores de colagenasa conocidos, incluido el ácido cafeico.
Tanto el bisresorcinol como el ácido cafeico compartían los sitios de unión de la colagenasa (Fig. 3A). Cuatro aminoácidos responsables de la unión del ácido cafeico incluyeron His524, Trp496, His527 y Trp539 (Fig. 3B). His524 y Trp496 interactuaron con el ácido cafeico mediante enlaces de hidrógeno a través de grupos hidroxilo carboxílicos y fenólicos. His527 y Trp539 se unieron al anillo fenólico mediante apilamiento π-π. Otros aminoácidos dentro del bolsillo de la enzima contribuyeron a su unión a través de la fuerza de Van der Waals (Fig. 3C). Las interacciones entre la colagenasa y el bisresorcinol se muestran en las Figs. 3D y 3E, que involucran a los aminoácidos Trp496 y Trp539 que donaron electrones π para unirse al anillo fenólico del bisresorcinol. Se observó la presencia de puentes de hidrógeno entre los grupos hidroxilo del bisresorcinol y los aminoácidos Asp601 y Ser602. Además, el átomo de Zn en el sitio activo de la enzima podría estar coordinado tanto con el bisresorcinol como con el ácido cafeico.
Hubo una similitud en la unión a la elastasa del bisresorcinol y el ácido ursólico (Fig. 4A). En cuanto al ácido ursólico, se propusieron puentes de hidrógeno para un grupo hidroxilo alifático cíclico y Ser96, así como para un grupo carboxílico y Asn192 (Figs. 4B y 4C). Curiosamente, se supuso el plegamiento estructural del bisresorcinol. Esto podría facilitar las interacciones entre los grupos hidroxilo fenólicos del compuesto y aminoácidos como Asn147, Ser190, Phe215 y Ser217 a través de enlaces de hidrógeno (Figs. 4D y 4E).

Para investigar la afinidad de unión a la tirosinasa de los compuestos, se aplicó la estructura cristalina de la tirosinasa de hongo (PDB ID 2Y9X). Los resultados se muestran en la Fig. 5 y la Tabla S3, lo que indica que la energía de unión del bisresorcinol fue de -6,57 kcal mol-1, estando en un rango de -4,63 a -8,12 kcal mol-1 para otros inhibidores conocidos. Por el contrario, todos los sustratos conocidos se unieron estrechamente a la tirosinasa de acuerdo con una enorme disminución de la energía de unión a un rango de -15,46 y -23,94 kcal mol-1.
Los enlaces covalentes coordinados entre los iones metálicos y la -arbutina o el bisresorcinol en el sitio activo de la tirosinasa probablemente ocurrieron. Sin embargo, los iones de cobre (Cu2 plus) fueron reemplazados por iones de zinc (Zn2 plus) en AutodockTool, porque el campo de fuerza para Cu2 plus no está disponible y los iones Cu2 plus y Zn2 plus son bastante idénticos en carga y tamaño (Santos-Martins et al. ., 2014). Para la -arbutina, un ion de zinc podría unirse covalentemente al grupo hidroxilo fenólico, y otro ion de zinc interactuaba con el anillo de fenol a través de un enlace catiónico π con los residuos His259 e His263 (Figs. 5B y 5C). Además, los aminoácidos, como Asn260, Ser282 y Val283, están unidos a sus grupos hidroxilo mediante enlaces de hidrógeno. Dado el bisresorcinol, el grupo hidroxilo fenólico formó enlaces de hidrógeno con Met280, Ala 246 y Glu239. Se observaron claramente la interacción apilada π-π entre el anillo de fenol e His263, y la atracción del catión π entre otro anillo de fenol y Arg321.

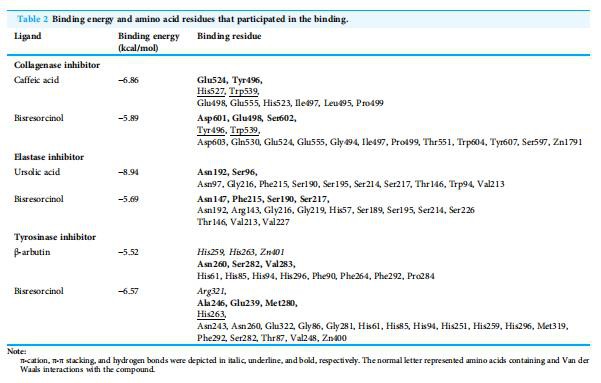
En resumen, las interacciones moleculares y la afinidad de unión entre el bisresorcinol y la colagenasa, la elastasa o la tirosinasa se tabularon en la Tabla 2.
DISCUSIÓN
El curcuminoide, un compuesto fenólico de Curcuma longa L., se ha incluido en varios productos cosméticos como antioxidante por sus propiedades antienvejecimiento (Gopinath & Karthikeyan, 2018). Dado que existían determinantes hidroxifenólicos, se anticipó que el bisresorcinol del tronco de H. terminales albergaría actividad antienvejecimiento en consecuencia (Fig. 1). En los recientes ensayos de inhibición in vitro, se encontró que el bisresorcinol inhibía predominantemente las actividades de la elastasa y la tirosinasa en lugar de la contraparte de la colagenasa (Fig. 2). En consecuencia, se realizaron experimentos de acoplamiento in silico para determinar la afinidad de unión del bisresorcinol relevante para estas enzimas de envejecimiento. Se asumió que las interacciones con respecto a los electrones π y los enlaces de hidrógeno eran determinantes clave para sus enlaces. Además, las interacciones hidrofóbicas que ocurrieron entre los grupos hidroxilo fenólicos y los residuos de aminoácidos en los sitios activos de las enzimas o cerca de ellos podrían contribuir a la pérdida de las funciones de las enzimas, de acuerdo con la literatura previa (Medvidović-Kosanović et al., 2010; Pientaweeratch, Panapisal & Tansirikongkol, 2016). En este documento, las características de unión del bisresorcinol a cada enzima se explicaron claramente en base a la comparación estructural correspondiente a un inhibidor específico. Se ha documentado la inhibición de la colagenasa clostridial por el ácido cafeico, EGCG, quercetina y catequina (Szewczyk et al., 2020; Pluemsamran, Onkoksoong & Panich, 2012; Hong et al., 2014). De manera similar a otros inhibidores conocidos, se sugirió que los grupos hidroxifenol del bisresorcinol interactúen con los aminoácidos clave del sitio de unión de la colagenasa a través de la interacción π-π y los enlaces de hidrógeno. Curiosamente, la estructura larga y flexible del bisresorcinol podría plegarse o alargarse. Por lo tanto, cuando se alarga, el anillo de fenol no unido en el otro lado podría unirse a los residuos de aminoácidos en el sitio activo, dando como resultado una mayor fuerza de unión. De esta forma, se planteó el potencial inhibitorio del bisresorcinol sobre la actividad colagenasa (fig. 6).

De acuerdo con un estudio anterior (Huang et al., 2013), la unión a la enzima elastasa tanto del bisresorcinol como de los inhibidores conocidos, como la procianidina, la quercetina y el ácido ursólico, fue idéntica, lo que implica la formación de enlaces de hidrógeno. Además, se especuló que las interacciones entre el bisresorcinol y los aminoácidos aparte del bolsillo de la enzima median en el anillo de fenol desplegado de la sustancia (Fig. 7).
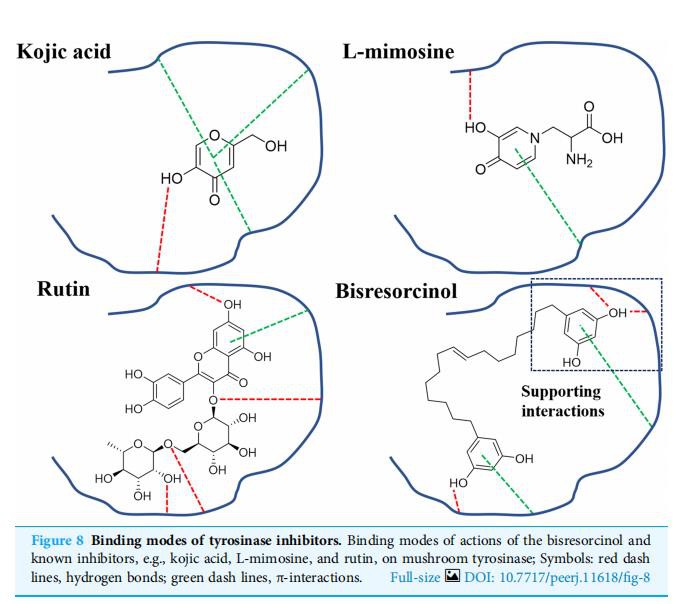
Dada la actividad inhibidora de la tirosinasa, los inhibidores como el ácido kójico, la rutina y la L-mimosina parecen unirse competitivamente a la enzima tirosinasa con la L-tirosina, lo que lleva a la inhibición de la síntesis de melanina (Channar et al., 2018; Nguyen & Tawata, 2015). ; Si et al., 2012). En la Fig. 8, se sugirieron las interacciones π-π entre cualquier compuesto de prueba y residuos de histidina del sitio activo de cobre de la tirosinasa. De acuerdo con investigaciones anteriores, esto proporcionó una explicación particular para otros efectos antagónicos sobre la actividad tirosinasa de dichos compuestos (Lai et al., 2017). El esqueleto fenólico de las estructuras se ha implicado en el diseño de derivados de indanona (Jung et al., 2019) y tiazolil resorcinol (Mann et al., 2018), lo que respalda la posibilidad de utilizar el bisresorcinol como antagonista de la enzima tirosinasa.
CONCLUSIÓN
El bisresorcinol podría servir como inhibidor competitivo de la colagenasa, la elastasa y la tirosinasa con modos de unión comparables a los de los inhibidores conocidos. Sin embargo, la estructura larga y flexible del bisresorcinol fue interesante porque podrían ser evidentes interacciones adicionales hacia un anillo de fenol no unido a los aminoácidos vecinos de las enzimas. Este hallazgo se informó por primera vez y podría dar una idea para el desarrollo de nuevos productos cosméticos que contengan bisresorcinol para efectos antienvejecimiento y blanqueamiento. Sin embargo, hubo más necesidades para examinar su potencia in vivo ya través de ensayos clínicos.

AGRADECIMIENTOS
Los autores agradecen sinceramente a otros proveedores de instalaciones de investigación, como la Escuela de Graduados de la Universidad Prince of Songkla; Centro de Excelencia del Sistema de Administración de Medicamentos, Facultad de Ciencias Farmacéuticas, Universidad Prince of Songkla; la Escuela de Graduados en Ciencias Biomédicas y de la Salud (Ciencias Farmacéuticas), Universidad de Hiroshima, Hiroshima, Japón; y Departamento de Ciencias Biomédicas e Ingeniería Biomédica, Facultad de Medicina, Universidad Prince of Songkla, Tailandia.
Fondos
Este proyecto de investigación fue apoyado financieramente por The Royal Golden Jubilee Ph.D. (Ph.D./0151/2556), el Fondo de Investigación de Tailandia (TRF), Tailandia y el Consejo Nacional de Investigación de Tailandia (NRCT). Los financiadores no tuvieron ningún papel en el diseño del estudio, la recopilación y el análisis de datos, la decisión de publicar o la preparación del manuscrito.
Divulgaciones de subvenciones
Los autores divulgaron la siguiente información sobre la subvención: The Royal Golden Jubilee: Ph.D./0151/2556. Fondo de Investigación de Tailandia (TRF). Tailandia y el Consejo Nacional de Investigación de Tailandia (NRCT).
Conflicto de intereses
Los autores declaran que no tienen intereses contrapuestos.
Contribuciones de autor
·Charinrat Saechan concibió y diseñó los experimentos, realizó los experimentos, analizó los datos, preparó figuras y/o tablas, redactó o revisó los borradores del artículo y aprobó el borrador final.
·Uyen Hoang Nguyen realizó los experimentos, analizó los datos, preparó figuras y/o tablas y aprobó el borrador final.
·Zhichao Wang realizó los experimentos, analizó los datos, preparó figuras y/o tablas y aprobó el borrador final.
· Sachiko Sugimoto concibió y diseñó los experimentos, escribió o revisó los borradores del artículo y aprobó el borrador final.
·Yoshi Yamano concibió y diseñó los experimentos, escribió o revisó los borradores del artículo y aprobó el borrador final.
·Katsuyoshi Matsunami concibió y diseñó los experimentos, escribió o revisó los borradores del artículo y aprobó el borrador final.
·Hideaki Otsuka realizó los experimentos, escribió o revisó los borradores del artículo y aprobó el borrador final.
·Giang Minh Phan realizó los experimentos, escribió o revisó los borradores del artículo y aprobó el borrador final.
·Viet Hung Pham realizó los experimentos, escribió o revisó los borradores del artículo y aprobó el borrador final.
·Varomyalin Tipmanee concibió y diseñó los experimentos, realizó los experimentos, analizó los datos, preparó figuras y/o tablas, redactó o revisó los borradores del artículo y aprobó el borrador final.
·Jasadee Kaewsrichan concibió y diseñó los experimentos, analizó los datos, preparó figuras y/o tablas, redactó o revisó los borradores del artículo y aprobó el borrador final.
Disponibilidad de datos
Se proporcionó la siguiente información con respecto a la disponibilidad de datos:
Los datos sin procesar para los valores de IC50 de los estándares bisresorcinal y positivos para los ensayos de inhibición enzimática con respecto a la colagenasa, la elastasa y la tirosinasa están disponibles en los archivos complementarios.
Información suplementaria
La información complementaria para este artículo se puede encontrar en línea.
REFERENCIAS
1. Abhijit S, Manjushree D. 2010. Antihialuronidasa, la actividad antielastasa de Garcinia indica. Revista Internacional de Botánica 6(3):299–303 DOI 10.3923/ijb.2010.299.303.
2. BIOVIA. 2020. Estudio de descubrimiento. San Diego: Dassault Systèmes.
3. Channar PA, Saeed A, Larik FA, Batool B, Kalsoom S, Hasan MM, Ashraf Z. 2018. Síntesis de arilpirazol a través de la reacción de acoplamiento de Suzuki, ensayo de inhibición de la enzima tirosinasa de hongo in vitro y análisis de acoplamiento molecular silico comparativo con kojic ácido. Química bioorgánica 79:293–300 DOI 10.1016/j.bioorg.2018.04.026.
4. Chaturvedula VP, Schilling JK, Miller JS, Andriantsiferana R, Rasamison VE, Kingston DG. 2002. Nuevos derivados citotóxicos de bis 5-alquilresorcinol de las hojas de Oncostemon bojerianum de la selva tropical de Madagascar. Revista de productos naturales 65(11):1627–1632 DOI 10.1021/np0201568.
5.Dobos G, Lichterfeld A, Blume-Peytavi U, Kottner J. 2015. Evaluación del envejecimiento de la piel: una revisión sistemática de escalas clínicas. Revista británica de dermatología 172(5):1249–1261 DOI 10.1111/bjd.13509.
6. Comisión Europea, Comité Científico sobre Seguridad del Consumidor. 2010. Opinión sobre el resorcinol, SCCS/1270/09.
7.Giang PM, Nga NT, Van Trung B, Anh DH, Viet PH. 2019. Evaluación de las actividades antioxidante, hepatoprotectora y antiinflamatoria del bisresorcinol aislado del tronco de terminales de Heliciopsis. Revista de Química Farmacéutica 53(7):628–634 DOI 10.1007/s11094-019-02051-7.
8. Gopinath H, Karthikeyan K. 2018. Cúrcuma: condimento, cosmético y cura. Indian Journal of Dermatology Venereology and Leprology 84(1):16 DOI 10.4103/idol.IJDVL_1143_16.
9. Hong YH, Jung EY, Noh DO, Suh HJ. 2014. Efectos fisiológicos de una formulación que contiene extracto de té verde convertido en tanasa sobre el cuidado de la piel: estabilidad física, actividades de colagenasa, elastasa y tirosinasa. Investigación en Medicina Integrativa 3(1):25–33 DOI 10.1016/j.imr.2013.12.003.
10. Huang Y, Chen L, Feng L, Guo F, Li Y. 2013. Caracterización de los componentes fenólicos totales de los tallos de Spatholobus suberect usando LC-DAD-MSn y su efecto inhibitorio sobre la actividad de la elastasa de neutrófilos humanos. Moléculas 18(7):7549–7556 DOI 10.3390/moléculas18077549.
11. Humphrey W, Dalke A, Schulten K. 1996. VMD: dinámica molecular visual. Revista de gráficos moleculares 14(1):33–38 DOI 10.1016/0263-7855(96)00018-5.
12. Jewboonchu J, Saetang J, Saeloh D, Siriyong T, Rungrotmongkol T, Voravuthikunchai SP, Tipmanee V. 2020. Visión atomística y elucidación modelada de conessine hacia la bomba de salida de Pseudomonas aeruginosa. Diario de Estructura y Dinámica Biomolecular 8(4):1–10
13.Jiratchayamaethasakul C, Ding Y, Hwang O, Im ST, Jang Y, Myung SW, Lee JM, Kim HS, Ko SC, Lee SH. 2020. I. Cribado in vitro de las actividades inhibidoras y antioxidantes de elastasa, colagenasa, hialuronidasa y tirosinasa de 22 extractos de plantas halófitas para nuevos cosmecéuticos. Pesca y Ciencias Acuáticas 23(1):1–9 DOI 10.1186/s41240-020-00149-8.
14. Jung HJ, Noh SG, Park Y, Kang D, Chun P, Chung HY, Moon HR. 2019. I. Perspectivas in vitro e in silico sobre los inhibidores de la tirosinasa con derivados de (E)-bencilideno-1-indanona. Computational and Structural Biotechnology Journal 17 (suplemento 2): 1255–1264 DOI 10.1016/j.csbj.2019.07.017.
15.Lai X, Wichers HJ, Soler-Lopez M, Dijkstra BW. 2017. La estructura de la proteína 1 relacionada con la tirosinasa humana revela un sitio activo de zinc binuclear importante para la melanogénesis. Angewandte Chemie Edición internacional 56(33):9812–9815 DOI 10.1002/anie.201704616.
16.Mann T, Scherner C, Röhm KH, Kolbe L. 2018. Relaciones estructura-actividad de los tiazolil resorcinoles, inhibidores potentes y selectivos de la tirosinasa humana. Revista Internacional de Ciencias Moleculares 19(3):690 DOI 10.3390/ijms19030690.
17.Medvidović-Kosanović M, Šeruga M, Jakobek L, Novak I. 2010. Propiedades electroquímicas y antioxidantes de (más) -catequina, quercetina y rutina. Croatica Chemica Acta 83(2):197–207.
18. Nguyen BCQ, Tawata S. 2015. Enantiómeros de dipéptido de mimosina: inhibidores mejorados contra la melanogénesis y la ciclooxigenasa. Moléculas 20(8):14334–14347 DOI 10.3390/moléculas200814334.
19.Pientaweeratch S, Panapisal V, Tansirikongkol A. 2016. Actividades antioxidantes, anticolagenasa y antielastasa de Phyllanthus emblica, Manilkara zapota y silimarina: un estudio comparativo in vitro para aplicaciones antienvejecimiento. Biología farmacéutica 54 (9): 1865–1872
20.Pluemsamran T, Onkoksoong T, Panich U. 2012. El ácido cafeico y el ácido ferúlico inhiben la metaloproteinasa de matriz inducida por UVA-1 mediante la regulación del sistema de defensa antioxidante en las células HaCaT de queratinocitos. Fotoquímica y fotobiología 88(4):961–968 DOI 10.1111/j.1751-1097.2012.01118.x.
21. Saeloh D, Wenzel M, Rungrotmongkol T, Hamoen LW, Tipmanee V, Voravuthikunchai SP. 2017. Efectos de la rodomirtona sobre el homólogo de tubulina bacteriana grampositiva FtsZ. PeerJ 5(9):e2962 DOI 10.7717/peerj.2962.
22. Santos-Martins D, Forli S, Ramos MJ, Olson AJ. 2014. AutoDock4Zn: un campo de fuerza AutoDock mejorado para el acoplamiento de moléculas pequeñas a metaloproteínas de zinc. Revista de información y modelado químico 54(8):2371–2379 DOI 10.1021/ci500209e.
23. Selvaraj S, Krishnaswamy S, Devashya V, Sethuraman S, Krishnan UM. 2014. Complejos de iones metálicos y flavonoides: una nueva clase de agentes terapéuticos. Medicinal Research Reviews 34(4):677–702 DOI 10.1002/med.21301.
24. Sherratt MJ, Hopkinson L, Naven M, Hibbert SA, Ozols M, Eckersley A, Newton VL, Bell M, Meng QJ. 2019. Ritmos circadianos en la piel y otros tejidos elásticos. Matrix Biology 84(14):97–110 DOI 10.1016/j.matbio.2019.08.004.
25. Si YX, Yin SJ, Oh S, Wang ZJ, Ye S, Yan L, Yang JM, Park YD, Lee J, Qian GY. 2012. Un estudio integrado de la inhibición de la tirosinasa por la rutina: progreso mediante una simulación computacional. Diario de Estructura y Dinámica Biomolecular 29(5):999–1012 DOI 10.1080/073911012010525028.
26.Szewczyk K, Miazga-Karska M, Pietrzak W, Komsta Ł, Krzeminska B, Grzywa-Celinska A. 2020. Composición fenólica y propiedades relacionadas con la piel del extracto de partes aéreas de diferentes cultivares de Hemerocallis. Antioxidantes 9(8):690 DOI 10.3390/antiox9080690.
27. Tanawattanasuntorn T, Thongpanchang T, Rungrotmongkol T, Hanpaibool C, Graidist P, Tipmanee V. 2020. (-) -Kusunoquinina como posible inhibidor de la aldosa reductasa: equivalencia observada a través de la simulación dinámica de AKR1B1. ACS Omega 6(1):606–614 DOI 10.1021/acsomega.0c05102.
28.Teajaroen W, Phimwapi S, Daduang J, Klaynongsruang S, Tipmanee V, Daduang S. 2020. Una función del sitio auxiliar recién encontrado en la fosfolipasa A1 de la avispa tigre de bandas tailandesas (afinidades de Vespa) en su mejora enzimática: homología in silico conocimientos de modelado y dinámica molecular. Toxinas 12(8):510 DOI 10.3390/toxins12080510.
29. Thring TS, Hili P, Naughton DP. 2009. Actividades anticolagenasa, antielastasa y antioxidante de extractos de 21 plantas. Medicina alternativa y complementaria de BMC 9(1):1–11 DOI 10.1186/1472-6882-9-27.
30. Widyowati R, Sugimoto S, Yamano Y, Sukardiman, Otsuka H, Matsunami K. 2016. Nuevas isolinariinas C, D y E, glucósidos flflavonoides de Linaria japonica. Boletín químico y farmacéutico 64(5):517–521 DOI 10.1248/CPB.c16-00073.
Para más información: david.deng@wecistanche.com WhatApp:86 13632399501






