Piroptosis: una nueva frontera en las enfermedades renales, parte 1
Mar 15, 2023
La piroptosis es un patrón de muerte celular programada que difiere significativamente de la apoptosis y la autofagia en términos de morfología y función celular. El proceso depiroptosisse caracteriza predominantemente por la formación de la familia de proteínas gastrina mediada por la perforación de la membrana, el colapso celular y la liberación de factores inflamatorios, incluidos IL-1 e IL-18. En los últimos años, con el auge deinvestigación de piroptosis, los académicos han dedicado tiempo a estudiar el mecanismo de la piroptosis en enfermedades relacionadas con los riñones.piroptosisprobablemente está involucrado en enfermedades renales a través de dos vías: la vía canónica mediada por caspasa-1-y la vía no canónica mediada por caspasa-4/5/11-. Además, algunos académicos han identificado objetivos para el tratamiento de enfermedades relacionadas con los riñones desde el punto de vista depiroptosisy desarrolló los medicamentos correspondientes, que pueden convertirse en una recomendación para el pronóstico, el tratamiento dirigido y el diagnóstico clínico de enfermedades renales. Este artículo se centra en los últimos avances en el campo de lapiroptosis, especialmente en el papel patógeno clave depiroptosisen el desarrollo y progresión de las enfermedades renales. Presenta una comprensión más profunda de la patogenia de las enfermedades renales e introduce nuevos objetivos terapéuticos para la prevención y el tratamiento clínico de las enfermedades renales.
1. Introducción
Las enfermedades renales son un problema de salud global, afectando a más de 750 millones de personas en todo el mundo; son enfermedades con una alta incidencia y mortalidad. Las enfermedades renales representativas incluyen lesión renal aguda (AKI) y enfermedad renal crónica (CKD). Se estima que la AKI provoca aproximadamente 1,7 millones de muertes cada año en todo el mundo, y la incidencia de la ERC en todo el mundo es aproximadamente del 11 al 13 por ciento. La prevalencia de los factores de riesgo para la enfermedad renal continúa aumentando. Sin embargo, dada la gran variación entre países en la economía social, la cultura y la política, existen muchas diferencias en los métodos de examen y los planes de evaluación, lo que conduce a una eficiencia curativa deficiente y a una alta carga de atención médica.
La muerte celular programada juega un papel muy importante en el mantenimiento de la homeostasis celular.piroptosises un tipo de muerte celular programada proinflamatoria; es activado por un miembro de la familia de caspasas relacionado con la inflamación, que escinde la gasdermina para exponer su terminal NT, se traslada a la membrana y perfora la membrana, modificando la presión osmótica intracelular y finalmente provocando el colapso celular.piroptosisocurre principalmente en fagocitos derivados de mieloides, como macrófagos, células dendríticas y granulocitos neutrófilos. Estudios recientes han indicado quepiroptosistambién se observa en células T CD4 plus, queratinocitos, células epiteliales y neuronas.piroptosisestá regulada principalmente por la vía canónica mediada por caspasa-1-y la vía no canónica mediada por caspasa-4/5/11-.

Estudios posteriores en profundidad revelaron quepiroptosisestá involucrado en la aparición y desarrollo de muchas enfermedades, particularmente enfermedades renales. Esta revisión destaca los avances realizados en la investigación sobre la relación entrepiroptosisyriñónenfermedadesy discute los objetivos terapéuticos potenciales relacionados con el mecanismo depiroptosisenriñónenfermedades.
Según estudios relevantes, en los últimos años, la investigación sobre el uso de células madre y un remedio herbal chino para el tratamiento deriñónenfermedadesha llamado mucho la atención. El mecanismo principal de las dos terapias es promover la reparación de los tejidos renales lesionados y proteger las funciones renales restantes.
El remedio herbal chino,cistanche, se ha utilizado en la medicina tradicional china para tratar diversascrónicoriñónenfermedadesdesde la antigüedad. Se informa que la cistanche tiene el potencial de reducir la inflamación, reducirriñónfibrosis y promover la síntesis de los componentes de la matriz extracelular. Se ha revelado que estos efectos se deben a sus componentes bioactivos, que incluyen muchas sustancias fenólicas, triterpenoides y cumarinas.
Por otro lado, la tecnología de células madre ha supuesto una revolución en la práctica médica. La investigación ha demostrado que las células madre pueden diferenciarse en varios tipos de células renales y realizar actividades terapéuticas, incluida la protección de los tejidos renales funcionales restantes, la ralentización de la fibrosis tisular y la reparación de los tejidos renales dañados.

Haga clic en el suplemento Cistanche Tubulosa para la enfermedad renal
Pregunta por más:
david.deng@wecistanche.com WhatsApp:86 13632399501
En última instancia, la combinación de la medicina tradicional china con la ciencia moderna podría ser la clave para tratar diversasriñónenfermedades. Esta estrategia ha sido aceptada gradualmente por la comunidad médica y los estudios ya han demostrado que la terapia combinada decistanchey el tratamiento con células madre puede reducir considerablemente la tasa de mortalidad deriñónenfermedades.
En conclusión, el uso de la cistanche y el tratamiento con células madre en el tratamiento deriñónenfermedadesmuestra un gran potencial y requiere más investigación. La terapia combinada de los dos tratamientos podría brindar una mejor opción de tratamiento para aquellos que enfrentanriñónenfermedades.
2. Piroptosis
Brennan y Cookson descubrieron que Salmonella typhi podía inducir la muerte de macrófagos a través de un mecanismo dependiente de caspasa-1-, que era diferente del conocimiento previo sobre la apoptosis. Este tipo de muerte celular se conoce comopiroptosis. piroptosisdifiere de la apoptosis y la necrosis en términos de morfología y mecanismo (Tabla 1). Durantepiroptosis, la membrana celular se daña y se forma una perforación de 1,1 a 2,4 nm; debido a los cambios en la presión osmótica intracelular y extracelular, las células se tuman y se agrietan, se pierde la integridad de la membrana y se liberan factores inflamatorios. Sin embargo, durante este proceso, la estructura y función de las mitocondrias permanecen intactas.
3. Vía de señalización relacionada con la piroptosis
La evidencia acumulada ha identificado dos vías relacionadas conpiroptosis(Figura 1): la vía canónica mediada por caspasa-1-que es inducida por cuerpos inflamatorios y la vía no canónica mediada por caspasa-4/5/11-que es activada por lipopolisacárido (LPS).
3.1. Vía de piroptosis canónica.el canónicopiroptosisrutaestá mediada por cuerpos inflamatorios, principalmente la familia NLR del receptor tipo dominio de oligomerización de unión a nucleótidos (NOD) y la familia de proteínas PYHIN. Los cuerpos inflamatorios pueden ser activados por patrones moleculares asociados a patógenos (PAMP) o patrones moleculares asociados a daños (DAMP). La activación de la caspasa-1 por tales cuerpos inflamatorios puede conducir apiroptosis.
La familia de proteínas NLR se compone principalmente de un dominio de oligomerización de unión a nucleótidos (NOD/- NACHT), un dominio C-terminal que contiene repeticiones ricas en leucina (LRR) y un dominio N-terminal reclutador de caspasa (CARD) o dominio de pirina (PYD). ). El dominio NOD/NACHT es compartido por la familia NLR y su señal aguas abajo es activada por oligomerización dependiente de ATP. Las funciones principales de los LRR están relacionadas con el sentido del ligando y la autorregulación, mientras que los dominios CARD y PYD son los principales mediadores de la interacción entre proteínas similares en las señales posteriores.
Los cuerpos inflamatorios observados con frecuencia en la familia NLR incluyen NLRP3, NLRP1, NLRP6 y NLRP6; ellos inducenpiroptosisa través del reclutamiento de caspasa-1 a través de la proteína adaptadora de CARD-PYRIN [19]. Se ha prestado mucha atención al cuerpo inflamatorio NLRP3; como sensor intracelular, puede ser activado por la mayoría de los factores de riesgo endógenos y estimulantes ambientales [20]. Actualmente, se sabe que NLRP3 puede activarse de dos formas: una es dependiente de moléculas microbianas o citoquinas endógenas; el otro es inducido por APT, toxinas formadoras de poros, ARN viral y partículas [21]. Otro estudio reveló que la activación de NLRP3 podría conducir a la liberación de citocinas proinflamatorias mediadas por caspasa-1-, como IL-1 e IL-18, e inducirpiroptosis[20]. Se informó que la toxina letal (LT) del ántrax podría activar los macrófagos mediados por caspasa-1-piroptosis, mientras que la caspasa-1 se activó mediante la escisión mediada por LT de los 10 loci de NLPR1 y la activación de cuerpos inflamatorios [22]. En consecuencia, la activación del cuerpo inflamatorio NLRP1 juega un papel muy importante en la liberación de factores inflamatorios inducidos por IL, como IL-1 e IL-18, ypiroptosis[23, 24]. El cuerpo inflamatorio NLRP6 generalmente se activa por metabolitos asociados a la microbiota, como la taurina o Porphyromonas gingivalis. También puede regular la caspasa-1-mediadapiroptosisde células epiteliales intestinales o fibroblastos gingivales humanos [25, 26]. En 2017, Zhu et al. [27] encontraron que NLRP9 podía reconocer una extensión corta de ARN de doble cadena a través de la ARN helicasa Dhx9 y formar un complejo inflamatorio con las proteínas adaptadoras ASC y caspasa-1, promoviendo así la liberación de IL-1 y IL-18 e inducirpiroptosis.

Elpiroptosismencionado anteriormente se ocupa de la interacción entre la proteína adaptadora ASC y la caspasa-1. Por lo tanto, se ha examinado si la proteína adaptadora ASC es necesaria durante todo el proceso de inflamación mediada por el cuerpo.piroptosis. Un estudio previo de macrófagos ha demostrado que cuando NAIP1/2 y NAIP5/6, dos miembros de la familia de proteínas inhibidoras de la apoptosis NLR (NAIP), fueron activados por el sistema de secreción tipo III (T3SS) y flflagelina, pueden formar el NLRC{ {6}}complejo NAIP1/2, o el complejo NLRC4-NAIP5/6, y reclutar caspasa-1 a través de la interacción CARD-CARD para desencadenarpiroptosis[28–30]. ASC no participa en este proceso. En su lugar, NLRC4 recluta directamente caspasa-1 para activarpiroptosis. Esto probablemente se deba a que NLRC4 contiene el dominio CARD [31].
Además de la familia NLR, otros cuerpos inflamatorios también participan en la aparición y desarrollo depiroptosis. Por ejemplo, el dsDNA citoplásmico y el virus vaccinia dsDNA podrían unirse al dominio HIN200 en ausencia de melanoma 2 (AIM2), lo que lleva a la activación del PYD de AIM2 y la formación de un complejo proteico con AIM2, ASC y caspasa{ {5}} y, en última instancia, inducirpiroptosis[32, 33]. El mecanismo de regulación depiroptosispor pirina, la proteína codificada por MEFV, es similar a la de AIM2. La proteína pirina humana tiene cuatro dominios funcionales, el dominio pirina (PYD), un dominio con dedos de zinc (recuadro), un dominio en espiral (CC) y un dominio B30.2/SPRY. La pirina de ratón tiene tres dominios: PYD, bBox y CC. Como receptor de reconocimiento de patrones, la pirina no reconoce directamente los factores de riesgo de patógenos o huéspedes. En cambio, la inactivación de RhoA GTPasa inducida por patógenos puede activar la interacción entre pirina y caspasa-1 y PYD, que finalmente induce la inmunidad mediada por caspasa-1-piroptosis[34].
El reclutamiento directo o indirecto de caspasa-1 por cuerpos inflamatorios para regularpiroptosisha sido bien estudiado. Sin embargo, el mecanismo a través del cual la caspasa activada- 1 mediapiroptosispermanece desconocido. En 2015, Shao et al. descubrió, en un experimento in vitro, que cuando la caspasa-1 se activaba en los macrófagos de la médula de ratón, podía escindir específicamente los fragmentos de gastrina-N y gastrina-C de la gasdermina (GSDMD) [35]. Se confirmó además que el fragmento GSDMD-N podría inducir una muerte celular extensa, que está mucho más cerca depiroptosis. Las pruebas in vitro sugirieron que la formación de GSDMD-NT y la activación de caspasa-1 probablemente ocurrieron simultáneamente y que ASC no fue necesaria para la activación de GSDMD. Esto implica que la caspasa escindida -1 no solo puede escindir GSDMD sino también activar directamente GSDMD [36]. Cuando el GSDMD se escinde en una masa de GSDMD-NT, dichos fragmentos migran a la membrana mientras se agregan y perforan la membrana, lo que lleva a la liberación de factores inflamatorios, como IL-1 e IL-18. A medida que aumenta el número de orificios, la membrana se rompe y el contenido celular, como IL-1 y la proteína de caja 1 del grupo de alta movilidad (HMGB1), se descarga, provocando los cambios característicos depiroptosis[37, 38].

3.2. Vía de señalización de piroptosis no canónica.Además de la canónicapiroptosisvía de señalización, la no canónicapiroptosisLa vía de señalización también ha sido bien estudiada. En 2011,piroptosisen macrófagos infectados con E. coli, Citrobacter corynii o Vibrio cholera no depende de cuerpos inflamatorios, sino de caspasa-11 [39]. El lipopolisacárido (LPS) es el principal componente de la membrana externa de las bacterias gramnegativas, y el receptor tipo Toll 4 (TLR-4) puede reconocer el LPS extracelular para estimular la transcripción de citoquinas. Se encontró que el LPS en los macrófagos podría activar la caspasa-11 y, durante la activación, la toxina del cólera B es el portador citoplasmático de LPS y que el LPS podría activar la caspasa-11 independientemente de TLR4, lo que sugiere que la caspasa{{ 9}} responde directamente al LPS citoplásmico [40–42]. También se encontró que la caspasa-11 y homóloga a la caspasa humana-4 y la caspasa-5 podrían unirse directamente a LPS para autoactivarse, induciendo asípiroptosis, aunque el papel del LPS en la activación de la caspasa-11 y la homología de la caspasa humana requiere más investigación [43]. También se encontró que GSDMD era necesario parapiroptosisen macrófagos de ratón mediados por caspasa-4/5- [44]. Del mismo modo, Aglietti et al. [45] informó que los fragmentos de proteína p30 derivados de la escisión de GSDMD después de la activación de caspasa-11 podrían unirse a la membrana, lo que lleva a la morfología característica depiroptosisy perforación de la membrana. Un estudio actualizado encontró que los loci Asp289/285 de caspasa- 4/11 eran cruciales para la inducción depiroptosis, que nuevamente amplió nuestro conocimiento depiroptosis[46].
Por lo tanto, debe considerarse si caspasa-11- mediadapiroptosisestaba relacionado con la caspasa-1. La pannexina-1 es una proteína del canal de la membrana que se expresa ampliamente en todo tipo de tejidos y células y puede ser escindida y lisada por la caspasa-11, dañando el canal para la liberación de moléculas pequeñas de la membrana, lo que lleva a la salida de ATP intracelular , activando los canales iónicos controlados por ligandos (P2X7) del receptor purinérgico P2X y mediando lapiroptosisde macrófagos [47]. También se encontró que la APT exógena podría activar P2X7 para formar un canal para K más eflujo, que es crucial para la activación del cuerpo inflamatorio NLRP3. Por lo tanto, es probable que la vía de inflamación no canónica mediada por caspasa-11-pueda promover el flujo de salida de K más la vía de la pannexina-1, activando así el cuerpo inflamatorio NLRP3 y la caspasa-1 y, finalmente, conduciendo apiroptosis, maduración y liberación de factores inflamatorios [48, 49].
Varios estudios han demostrado que la caspasa-8 desempeña un papel importante en la respuesta inflamatoria de los macrófagos inducida por patógenos. En 2018, se descubrió que la caspasa activada-8 podría provocar daños en la membrana celular y K más out Fellow, lo que activa aún más el inflamasoma NLRP3 y desencadena la oligomerización de ASC. Como resultado, se libera IL-1 y, durante este proceso, GSDMD juega un papel central [50]. En el mismo año, otro grupo también descubrió que la caspasa-8 podría conducir a la lisis de GSDMD y GSDME en macrófagos murinos, desencadenando la liberación de IL-1 ypiroptosis. Además, en un modelo de colitis en ratones, también se encontró que la respuesta inflamatoria estaba estrechamente relacionada con la respuesta mediada por caspasa-8-piroptosis[51]. Por lo tanto, se propone que la caspasa-8 sea un interruptor parapiroptosis[52]. Sin embargo, no está claro si la caspasa-8 divide directamente el GSDMD o si se requieren intermediarios. Hasta 2020, se creía que la caspasa-8 funciona a través de la escisión directa de GSDMD y que la actividad de la caspasa-8 en diferentes complejos se correlaciona con su capacidad para escindir directamente GSDMD [53, 54]. En la actualidad, los estudios sobre la correlación entre caspasa-8 ypiroptosistodavía están surgiendo, y muchos conceptos científicos relacionados requieren una mayor investigación.
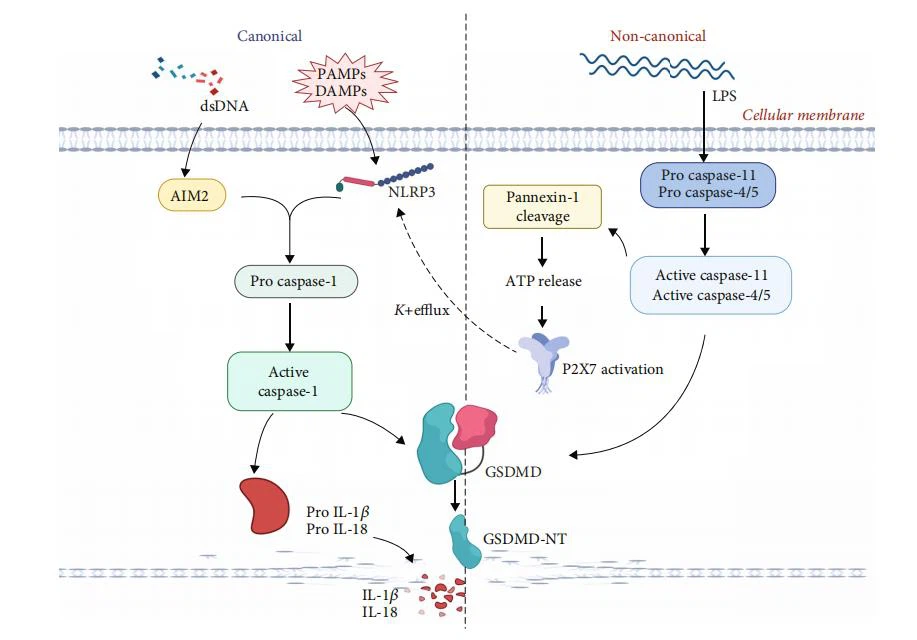
Figura 1:Vías de piroptosis mediadas por caspasa canónica-1-dependiente y no canónica{1}}/5/11-[20, 33, 36, 37, 39, 43, 44, 48, 49]. La vía de señalización de la piroptosis canónica: el cuerpo inflamatorio NLRP3 se activa mediante un patrón molecular asociado a patógenos (PAMP) o un patrón molecular asociado a daños (DAMP), y el cuerpo inflamatorio AIM2 se activa mediante ADNds. Inducen la activación de la caspasa corriente abajo-1. Por un lado, favorece la liberación de los factores inflamatorios IL-1 e IL-18; por otro lado, esto escinde específicamente GSDMD. El fragmento terminal de GSDMD-N se agrega en la membrana celular para causar la perforación de la membrana e inducir la piroptosis. Vía de señalización de piroptosis no canónica: el lipopolisacárido (LPS) activa directamente la caspasa-11 (caspasa de homología humana-4/5) y luego escinde el GSDMD para formar el terminal GSDMD-N, lo que induce la piroptosis. La pannexina-1 es escindida y lisada por la caspasa activada-11 (homóloga a la caspasa humana-4/5), que daña el canal para la liberación de moléculas pequeñas de la membrana, conduce a la fuga de ATP intracelular, activa los canales activados por ligandos (P2X7) del receptor purinérgico P2X, acelera el flujo de salida de K+, interviene en la vía de señalización NLRP3/caspasa-1 e indirectamente promueve la liberación de los factores inflamatorios IL-1 e IL{{ 36}}.
Además, la caspasa activada-3 también podría lisar GSDME para inducir piroptosis [55]. En 2019, el Comité de Nomenclatura sobre Muerte Celular (NCCD) modificó la definición de piroptosis y la definió como un patrón de muerte celular dependiente de la proteína de la familia de las gasderminas involucrada en la perforación de la membrana. Sin embargo, la piroptosis no siempre depende de la inducción de caspasas inflamatorias. Además, el tipo de muerte celular no está determinado por el tipo de caspasa, sino por los sustratos escindidos por la caspasa [5].
4. Asociación entre Piroptosis y Enfermedad Renal
Las enfermedades renales comunes que pueden conducir a la enfermedad renal en etapa terminal (ESRD, por sus siglas en inglés) incluyen lesión renal aguda, enfermedad renal diabética, fibrosis renal e inflamación renal. Se ha confirmado que todos los tipos de enfermedad renal son inducidos por un cierto nivel de reacciones inflamatorias.piroptosis, regulada por una variedad de cuerpos inflamatorios, juega un papel muy importante en la progresión de la enfermedad renal. Además, existen varios mecanismos moduladores de las enfermedades renales.
4.1. Lesión renal aguda. Lesión renal aguda (LRA)es inducida por múltiples factores que se caracterizan por una rápida disminución de la función renal y la acumulación de toxinas y desechos metabólicos; eventualmente, pueden ocurrir complicaciones y la falla de otros órganos. Las principales características patogénicas de la LRA son la lesión de las células epiteliales de los túbulos renales, la inflamación intersticial y la disfunción de los vasos sanguíneos. La reperfusión isquémica, las nefrotoxinas endógenas y exógenas, incluido el medio de contraste, son factores comunes de la LRA [56]. Numerosos estudios han indicado que estos factores mencionados que inducen el DRA se asocian conpiroptosis.
En 2010, Shigeoka et al. [57] informaron que NLRP3 se expresaba en gran medida en células epiteliales tubulares renales de ratones y humanos, pero aumentaba significativamente en IRI renal, lo que sugiere el papel crucial de NLRP3 en IRI en el riñón. Yang et al. [58] fue el primer grupo en informar quepiroptosisfue un evento clave durante la IRI del riñón; la sobreactivación de la vía de señalización CHOP-caspasa- 11 desencadenada por estrés del retículo endoplásmico juega un papel crucial en la piroptosis de las células epiteliales tubulares renales después de la IRI renal. Esto probablemente apoyará estudios adicionales de la relación entrepiroptosisy agudoriñónlesión. AKI se conocía anteriormente como insuficiencia renal aguda, y el estudio encontró que el LPS repurificado puede activar la vía de la caspasa-1/IL-1 durante la insuficiencia renal aguda, lo que lleva a la piroptosis [59].
En 2019, se demostró que la expresión de caspasa-11 aumenta notablemente en modelos de células tubulares de LRA inducida por cis-platino. La activación de la caspasa-11 escinde GSDMD en GSDMD-NT, que luego se translocó a la membrana plasmática, desencadenando piroptosis y promoviendo la liberación de IL-18 [60]. Los agentes de contraste yodados también pueden causar enfermedad renal. Es probable que los agentes de contraste dañen la membrana de las células epiteliales y entren en las células para activar la caspasa-4/5/11, escindir la GSDMD e iniciarpiroptosis[61]. Un estudio actualizado encontró que la piroptosis mediada por la vía de señalización de caspasa-11/GSDMD no solo afectó la liberación de citocinas, sino que también determinó la gravedad de la LRA después del shock séptico [62]. Estos resultados sugieren una estrecha correlación entre la patogénesis de AKI y la vía atípica mediada por caspasa-4/5/11-enpiroptosis. Además, un estudio reciente encontró que la piroptosis mediada por caspasa-3/GSDME también está relacionada con la aparición y el desarrollo de LRA. La intervención genética y los estudios farmacológicos con ratones deficientes en GSDME y células epiteliales tubulares renales humanas demostraron que la caspasa-3 podría aliviarpiroptosisy retrasar la LRA bloqueando la lisis de GSDME [63]. Por lo tanto, dirigidopiroptosispuede ser un enfoque novedoso para el tratamiento de la LRA.
4.2. Enfermedad renal diabética. Enfermedad renal diabética (NDD)es una complicación microvascular de la diabetes. Este es un tipo de enfermedad causada por un metabolismo disfuncional del azúcar. La DKD se caracteriza por cicatrización glomerular, proteína en la orina y función renal reducida. La principal propiedad histológica de la DKD es el grosor de la membrana basal glomerular, la dilatación del mesangio glomerular, la pérdida de células de Sertoli, la fibrosis de los glomérulos y la fibrosis progresiva. Actualmente, la DKD se trata principalmente con hipoglucemia y un mejor control de la glucosa en sangre. Sin embargo, esto no conduce a una reducción de la DKD. Por lo tanto, es importante investigar la patogenia de la ND [63].
En 2011, se descubrió que la vía de señalización NLRP3-ASC-caspasa-1 promueve la diabetes al regular la liberación de IL-1 y otros factores inflamatorios [64]. También se descubrió que la hiperglucemia continua podría activar el cuerpo inflamatorio NLRP3, promover la liberación de IL-1 e IL-18 y, finalmente, conducir a la aparición y progresión de la ND [65]. La eliminación del gen NLRP3 en ratones retrasó la DKD y alivió la lesión renal mediante la inhibición de las reacciones inflamatorias [66]. El ARNm de NLRP3 en suero también es un biomarcador que se utiliza para identificar a los pacientes con ND [67]. Esto es indicativo del importante papel de NLRP3 en la regulación de la aparición y progresión de DKD.

El cuerpo inflamatorio NLRP3 es uno de los objetivos más comunes para la regulación depiroptosis. Por lo tanto, consideramos si la piroptosis participó en la aparición y el desarrollo de DKD. Los resultados del estudio in vitro mostraron que la expresión depiroptosisLas proteínas relacionadas, como la caspasa escindida-1, la GSDMD y la terminal N de la GSDMD (GSDMD-NT), aumentaron durante la progresión de la DKD, y también se observó una marcada liberación de factores inflamatorios [68 , 69].
En los últimos años, la estrecha correlación entre los ARN largos no codificantes (lncRNA),piropotosis, y DN ha recibido mucha atención. Se ha demostrado que el ARN MALAT1 puede inhibir la expresión de miR-23c y promover la hiperglucemia inducidapiroptosisde las células epiteliales tubulares renales mediante la inhibición de miR-30c a través de la activación de NLRP3 [70]. Un estudio reciente mostró que NEAT1/miR-34c/NLRP3-modulópiroptosisy la inflamación posterior podría promover la progresión de la ND [71]. En resumen, la expresión de lncRNAs se correlaciona positivamente conpiroptosisy es un biomarcador potencial para DKD. En la actualidad, la mayoría de los estudios relacionados con la DKD se concentran en la típica mediada por caspasa-1-piroptosisvía, que puede proporcionar una mejor comprensión y un método más eficaz para la prevención y el tratamiento de la ND.
4.3. Fibrosis Renal.La herida, la infección, la inflamación, el trastorno circulatorio sanguíneo, la respuesta inmunitaria y muchos otros factores patógenos pueden aumentar los fibroblastos y la acumulación masiva de colágeno en el intersticio renal, lo que lleva a la fibrosis intersticial renal y, finalmente, a la ESRD.

Se observó una mayor expresión de NLRP3 y caspasa-1, así como una mayor liberación de los cuerpos inflamatorios IL-1 e IL-18, tanto en muestras de biopsia renal de ratones UUO como en humanos con UUO. (oclusión ureteral unilateral), mientras que el grado de fibrosis renal se alivió notablemente en ratones NLRP3-/- [72, 73]. En un estudio a largo plazo, Miao et al. [74] descubrió en 2018 que en ratones UUO, la caspasa-11 podría activar las caspasas-1, mejorar la liberación de factores inflamatorios y promover la progresión de la fibrosis renal; la piroptosis es una UUO mediada por la vía atípica de la caspasa-11. El ADN necrótico puede exacerbar la enfermedad y lesión renal inducida por OUU al activar el cuerpo inflamatorio AIM2 [75]. La relación entrepiroptosisy la fibrosis renal ha sido bien estudiada. En 2012,piroptosisse encontró que participaba en la fibrosis intersticial renal en un modelo de ratón de UUO; esta participación probablemente esté relacionada con la inflamación, pero el mecanismo sigue siendo desconocido [76]. En 2016, Xu et al. [77] encontraron que la pérdida de MAP1S condujo a una acumulación de proteínas relacionadas con la fibrosis renal de ratón y fibrosis renal en ratones más viejos. Además, la inhibición de MAP1S en las células tubulares renales cercanas al extremo puede conducir al desarrollo o progresión depiroptosis, lo que sugiere aún más la estrecha relación entrepiroptosisy fibrosis renal. Además, un estudio reciente mostró que el UUO mediado por caspasa-3/GSDME está relacionado con el desarrollo tubular renal.piroptosisen ratones. Esto sugiere un papel de la obstrucción intrauretral en la lesión tubular renal, lo que resulta en fibrosis renal [78]. Sin embargo, solo unos pocos estudios han abordado su correlación y se requiere un estudio más profundo en el futuro.
Pregunta por más:david.deng@wecistanche.com WhatsApp:86 13632399501
