Toxicidad renal inducida por radiación: patogénesis molecular y celular
Mar 23, 2022
ricardo klaus1, Maximiliano Niyazi2,3y Bärbel Lange-Sperandio1*
Resumen
La nefropatía por radiación (RN) es unariñónlesióninducida por radiaciones ionizantes. En un entorno clínico, la radiación ionizante se utiliza en radioterapia (RT). El uso y la intensidad de la radioterapia están limitados por el daño al tejido normal, incluida la toxicidad renal. Diferentes umbrales parariñónexiste toxicidad para diferentes entidades de RT. Las características histopatológicas de la RN incluyen daño vascular, glomerular y tubulointersticial. Los diferentes mecanismos patogénicos moleculares y celulares involucrados en la RN no se comprenden completamente. La radiación ionizante provoca roturas de doble cadena en el ADN, seguidas de muerte celular, incluida la apoptosis y la necrosis de las células endoteliales, tubulares y glomerulares renales. Especialmente en la fase latente de la RN, el estrés oxidativo y la inflamación se han propuesto como posibles mecanismos patogénicos, pero hasta el momento no se han encontrado pruebas claras. La senescencia celular, la activación del sistema renina-angiotensina-aldosterona y la disfunción vascular pueden contribuir a la RN, pero solo se dispone de datos limitados. Se han identificado varias vías de señalización en modelos animales de RN y se han investigado diferentes enfoques para mitigar la RN. Se probaron fármacos que atenúan la muerte celular y la inflamación o reducen el estrés oxidativo y la fibrosis renal. Se ha demostrado que el bloqueo del sistema renina-angiotensina-aldosterona, los fármacos antiapoptóticos, las estatinas y los antioxidantes reducen la gravedad de la RN. Estos resultados proporcionan una base para el desarrollo de nuevas estrategias para prevenir o reducir la radiación inducida.riñóntoxicidad.
Palabras clave:Nefropatía por radiación, Irradiación corporal total, Radioterapia,Renal fibrosis, Senescencia celular, daño en el ADN,Renal inflamación
Contacto: ali.ma@wecistanche.com

Haga clic paraCistanche tubulosa beneficios y efectos secundarios parariñón enfermedad
Radioterapia
La radioterapia (RT) sola o en combinación con quimioterapia, cirugía o ambas es una opción de tratamiento importante para las neoplasias malignas sólidas. A nivel mundial, la incidencia de cáncer aumenta debido a que la esperanza de vida humana y la exposición a los factores de riesgo de cáncer aumentan [1]. En 2018, aproximadamente 18 millones de personas fueron diagnosticadas con cáncer y más de 9 millones de personas murieron de cáncer [2]. Las predicciones concluyen que el cáncer puede convertirse en la principal causa de muerte en el siglo XXI, y más del 60 por ciento de los pacientes con cáncer recibirán RT a lo largo de su régimen de terapia [3]. La RT se puede administrar como radioterapia de haz externo (teleterapia). La radioterapia interna incluye la braquiterapia, en la que se implanta una fuente de radiación [4], la radioterapia intraoperatoria o la terapia con radionúclidos, en la que los radionúclidos terapéuticos se administran por vía parenteral [5].
La RT de haz externo que utiliza aceleradores lineales es la forma más común de RT [6, 7]. Con los avances tecnológicos de los últimos años, se han introducido nuevas técnicas de radiación, como la radioterapia de intensidad modulada (IMRT) y su subforma rotacional de arcoterapia volumétrica modulada (VMAT) [8, 9]. Paralelamente, se ha mejorado la radioterapia guiada por imágenes (IGRT), y las opciones más utilizadas son imágenes planares kV/MV, TC de haz cónico, ultrasonido, escáneres de superficie con imágenes de rayos X y RT guiada por resonancia magnética (MRgRT). ) [10– 12]. Y, sin embargo, la terapia de partículas con protones o haces de iones pesados se puede utilizar en indicaciones específicas, ya que su perfil de dosis en profundidad permite gradientes pronunciados más allá del objetivo. Este proceso ha ido acompañado de una mejor delineación del volumen objetivo, planificación del tratamiento de radiación inversa y la opción de administración de dosis de radiación adaptativa [13, 14]. Aparte de la RT dirigida, la irradiación corporal total (TBI) es una tecnología ampliamente utilizada. Es uno de los regímenes de acondicionamiento para preparar a los pacientes para el trasplante de médula ósea (TMO). Anualmente hay más de 20,000 BMT en todo el mundo [15].

Toxicidad por radiación
En primer lugar, se presentan los principios generales de la toxicidad de la radiación. La evidencia específica de la contribución de esos supuestos mecanismos patogénicos en la nefropatía por radiación se discutirá por separado más adelante.
Aunque la radioterapia es muy eficaz para controlar el crecimiento tumoral y prolongar la supervivencia general, tiene efectos adversos en el tejido sano dentro del campo de radiación. Alcanzar selectivamente solo el tejido canceroso sigue siendo uno de los principales desafíos en RT [16]. La toxicidad para el tejido sano limita las dosis aplicadas de RT y, por lo tanto, conduce a un control tumoral subóptimo. Además, la combinación con quimioterapia aumenta la toxicidad del tejido normal y, por lo tanto, conduce a una reducción aún mayor de la dosis máxima tolerable [7].
El objetivo principal de la radioterapia es el ADN. La radiación ionizante causa daño directo al destruir enlaces químicos y eliminar electrones. La radiación ionizante también causa daños indirectos a través de la generación de especies reactivas de oxígeno (ROS) [17]. Cuando las ROS superan a los antioxidantes, surge el estrés oxidativo. Las ROS dañan macromoléculas celulares, por ejemplo, lípidos, proteínas o ADN [17, 18]. Las roturas de doble cadena de ADN (DSB) son el evento más grave de RT [19]. Las células detectan DSB por un sistema llamado respuesta al daño del ADN (DDR). El DDR se inicia minutos después de la irradiación y activa los puntos de control del ciclo celular y la reparación del ADN para lograr la supervivencia. Cuando los procesos de reparación no tienen éxito, la DSB finalmente provoca inestabilidad genómica, muerte celular o senescencia celular [20]. La reacción a DSB depende del tejido afectado y de la integración de DDR en las células afectadas. En los tejidos que se reproducen rápidamente (como las células tumorales objetivo, pero también las células hematopoyéticas y el epitelio de la mucosa), el DSB no reparado y las rondas posteriores de mitosis aberrante culminan en un morfotipo de catástrofe mitótica y muerte celular [21]. Esto refleja el beneficio terapéutico con la destrucción de células tumorales, pero también la toxicidad clínica aguda de la radioterapia como consecuencia de la muerte de células tisulares normales. Esto generalmente ocurre dentro de las primeras dos semanas. Los tejidos que se reproducen lentamente (como los fibroblastos) reaccionan con una detención prolongada del ciclo celular en lugar de una inducción de muerte celular [22]. Mientras que la toxicidad por radiación aguda se caracteriza por muerte celular aguda, los procesos de toxicidad crónica generalmente se caracterizan por fibrogénesis y depósito de matriz extracelular. Es muy probable que esos procesos sean secundarios a través de la inflamación crónica y la senescencia celular [23]. La inflamación está presente, por ejemplo, en lesiones por radiación gastrointestinales [24] y pulmonares [25]. La reorganización fibrótica conduce a la degeneración y la disminución de la función específica del órgano [26].
funciones del riñon
losriñonesson órganos esenciales para regular los fluidos, los electrolitos y el metabolismo ácido-base del organismo. Los riñones excretan metabolitos de desecho, modulan la presión arterial, producen eritropoyetina para estimular la eritropoyesis y activar la vitamina D [27]. Después de una lesión por radiación,riñónla disfunción conduce a hipertensión, anemia y osteodistrofia. Los metabolitos de desechos tóxicos se acumulan y causan uremia, trastornos electrolíticos como hiperpotasemia, hiperfosfatemia, hipocalcemia y, en última instancia, insuficiencia renal crónica [28]. La enfermedad renal en etapa terminal (ESRD) con pérdida de la función renal da como resultado una terapia de reemplazo renal con la necesidad de diálisis o trasplante renal [29].

El curso clínico de la nefropatía por radiación
El curso clínico de la nefropatía por radiación fue descrito por primera vez por Luxton et al. [30] (Cuadro 1). Además de dosis de radiación muy altas por encima de 50 Gy, que son irrelevantes para la experiencia humana, no hay síntomas ni signos clínicos en los primeros 6 meses después de la irradiación. Este es el llamado período latente de RN. El primer daño clínico se hace evidente en la fase aguda [6 a 18 meses] después de la irradiación. Luxton et al. observó los primeros signos clínicos de 6 a 13 (media de 8,5) meses después de la irradiación [30]. El daño renal crónico se manifiesta clínicamente más de 18 meses después de la RT.
La RN aguda puede comenzar sin síntomas. La azotemia o la proteinuria pueden detectarse antes de que se presenten los síntomas. Cuando presentan síntomas, los pacientes pueden presentar fatiga, edema, dolores de cabeza y anemia grave desproporcionada con respecto al deterioro de la función renal [31]. Incluso pueden aparecer crisis hipertensivas con encefalopatía o insuficiencia cardiaca congestiva [31]. La RN crónica (RNC) se presenta con hipertensión, proteinuria e insuficiencia renal crónica [32]. La atrofia renal, que es típica en la CRN, se puede medir por la pérdida de volumen renal [33] (Tabla 1). En conclusión, la NRC es clínicamente indistinguible de la enfermedad renal crónica (ERC) de cualquier otra causa. Podría argumentarse que el deterioro de la función renal tras la RT en pacientes con neoplasias malignas es consecuencia de la quimioterapia o de múltiples fármacos nefrotóxicos como los antimicrobianos. Sin embargo, hay dos grandes series de pacientes con TMO sin TCE, en los que no se informó enfermedad renal crónica [34, 35]. Además, la NRC es menos frecuente en pacientes sometidos a TCE con protección renal parcial [36]. Las observaciones de pacientes con RT de la década de 1970 han demostrado que la latencia de la NRC puede ser de 8 a 19 años [37]. Cuando los pacientes con NRC alcanzan ESRD, la supervivencia es mucho peor que para otras causas de ESRD [38].

Umbrales de dosis e implicaciones especiales de toxicidad renal por radiación
The severity of the clinical features of RN depends on the kind of application (e.g. partial vs. total body irradiation, internal beam vs. external beam radiation), the applied dose, and the affected kidney volume [39, 40]. Clinical apparent kidney injury promptly after irradiation is observed only at higher doses than currently used. It has been reported in animal models using >50 Gy [41, 42]. Las dosis utilizadas en entornos clínicos en irradiación corporal total o parcial y radiación interna son mucho más bajas, como se especifica a continuación, y causan efectos tardíos que afectan a los glomérulos, tubulointersticio y vasculatura renal [43]. No hay datos de umbrales específcos de radioterapia para los diferentes compartimentos del riñón.
In partial body irradiation, clinical studies recommend keeping the mean dose for both kidneys below 18 Gy to limit renal toxicity. 15 to 17 Gy in 2 Gy fractions were considered safe, doses of 23 Gy can cause CKD in 5% of cases, and 28 Gy cause CKD in 50% of cases [44]. In a study with 19 patients with irradiated paraaortic lymph nodes in gynecologic tumors, those with a mean dose for both kidneys of 18 Gy stayed clinically asymptomatic for 12 to >48 meses de tiempo de observación [45]. Hay datos de los Análisis Cuantitativos de Efectos de Tejido Normal en la Clínica (QUANTEC). Los datos de QUANTEC muestran que hasta el 50 por ciento de los pacientes desarrollan disfunción renal clínicamente relevante si ambos riñones son irradiados con una dosis media > 18 Gy. Si menos del 20 por ciento del volumen del riñón está expuesto a 28 Gy (V28 < 20="" por="" ciento)=""><5% of="" patients="" will="" develop="" a="" clinically="" relevant="" kidney="" dysfunction="" [40].="" recently,="" in="" a="" series="" with="" 663="" patients="" published="" in="" 2020="" only="" 2%="" of="" patients="" with="" adjuvant="" radiotherapy="" for="" gastric="" cancer="" developed="" renal="" function="" impairment.="" the="" volume="" of="" the="" kidney="" receiving="" a="" dose="" of="" 20="" gy="" (v20)="" is="" predictive="" for="" renal="" function="" impairment="">
Para los pacientes sometidos a TBI en preparación para BMT, la nefropatía por radiación con CKD y la hipertensión arterial aún pertenecen a las secuelas tardías comunes. Sin embargo, debido a los nuevos flujos de trabajo y técnicas, los números han disminuido [31, 47, 48]. En una serie de 1993, hasta el 25 por ciento de los pacientes desarrollaron nefropatía por radiación [31]. En un metanálisis de 2006 Kal et al. sugirió que la dosis biológicamente efectiva (BED) debería ser inferior a 16 Gy en fracciones<2 gy="" [49].="" below="" this="" threshold,="" the="" clinical="" renal="" dysfunction="" is="" close="" to="" zero.="" above="" a="" bed="" of="" 21="" gy,="" the="" frequency="" of="" clinical="" renal="" dysfunction="" exceeds="" 20%.="" therefore,="" the="" authors="" suggest="" kidney="" shielding="" above="" a="" bed="" of="" 16="" gy="">
El fraccionamiento de las dosis permite dosis totales más altas, ya que permite la reparación del daño subletal, la repoblación, la reoxigenación y la redistribución de células en el ciclo celular. En los estándares actuales, la radiación externa se aplica en fracciones de 1,5 a 2 Gy [16]. Las estimaciones sugieren que en humanos expuestos a una dosis única de 4 Gy puede provocar daño renal [50]. La exposición a dosis únicas de alta tasa de dosis ya no se usa en la práctica clínica, pero podría ocurrir en accidentes de radiación o terrorismo radiológico. Anno et al. estimó que una dosis única de 7 Gy de radiación ionizante de alta tasa de dosis puede sobrevivir con el apoyo médico óptimo actualmente disponible [51]. Hace décadas, las dosis letales del 50 por ciento en Nagasaki y Chernobyl eran de 2 a 4 Gy y de 5 a 6 Gy, respectivamente. Estos hallazgos implican que la nefropatía por radiación sería un tema relevante en los sobrevivientes de tales escenarios [52].
En la terapia con radionúclidos, una forma de RT interna utilizada para varios tipos de cáncer, incluidos los tumores neuroendocrinos, los riñones son especialmente susceptibles a la toxicidad de la radiación debido a la filtración glomerular, la absorción tubular y la retención de los túbulos proximales de los radionúclidos [5]. Después de la filtración glomerular, aproximadamente el 3 por ciento de la actividad total se reabsorbe y retiene en la tubulina proximal, lo que lleva a una exposición prolongada de los riñones a la radiación [53]. Se produjo nefrotoxicidad grave con hasta un 14 % de eventos adversos de grado 4-5 (ESRD o muerte) en pacientes tratados con radionúclidos [50]. Debido a la diferente naturaleza de la aplicación, los umbrales difieren de la radioterapia externa. Mientras que la radiación externa se aplica de manera homogénea a altas tasas de dosis, los radionúclidos se distribuyen de manera heterogénea a través del órgano y las tasas de dosis son mucho más bajas, variables con el tiempo y con una disminución exponencial. Para las dosis de 90Y-DOTATOC y 177Lu-DOTATATE, menos de 40 Gy fueron seguras para pacientes sin ningún factor de riesgo, mientras que para pacientes con factores de riesgo de ERC, principalmente hipertensión y diabetes, se recomendó un umbral de 28 Gy [54]. Para reducir la absorción tubular proximal, se recomienda la coinfusión de aminoácidos cargados positivamente, como L-lisina y L-arginina. Reduce la dosis absorbida entre un 9 y un 53 por ciento. Adaptar la dosimetría a los pacientes individuales es una medida importante para mejorar el potencial terapéutico y reducir la toxicidad renal.
Aunque los umbrales de dosis y la BED del riñón pueden diferir entre los diferentes modos de radioterapia, no es de esperar que los mecanismos patogénicos moleculares y celulares sean diferentes. El estímulo dañino, la radiación ionizante, permanece siempre igual. Por lo tanto, los mecanismos patogénicos se analizan independientemente del formulario de solicitud.
Histopatología
Los cambios morfológicos agudos en el riñón tras la RT son principalmente vasculares y glomerulares. La pérdida de células endoteliales con la expansión subendotelial es un signo temprano de lesión por irradiación. Las asas capilares están ocluidas y congestionadas. Tanto la trombosis como los cilindros de eritrocitos degenerados están presentes en los capilares glomerulares. La mesangiolisis es otro hallazgo frecuente. La microscopía electrónica muestra lesión de las células endoteliales y ensanchamiento subendotelial de la membrana basal glomerular [55, 56]. Los cambios crónicos se caracterizan por un aumento de la fibrosis intersticial renal y una pérdida de masa de nefronas. La esclerosis de las arterias interlobulillares y arcuatas, la atrofia tubular y la cicatrización glomerular son características tardías de la RN [56, 57].
Patomecanismos de la toxicidad de la radiación
Los mecanismos patogénicos moleculares y celulares de la enfermedad renal crónica (ERC) en general son de gran interés porque la ERC afecta a más de 700 millones de pacientes en todo el mundo [58]. Si bien existen muchas etiologías para la ERC, parece haber una vía final común con la glomeruloesclerosis, la fibrosis intersticial renal y la atrofia tubular con deterioro de la función renal [23]. La inflamación crónica y la senescencia celular son factores impulsores de los procesos fibróticos en casi todas las etiologías de la ERC [59, 60].
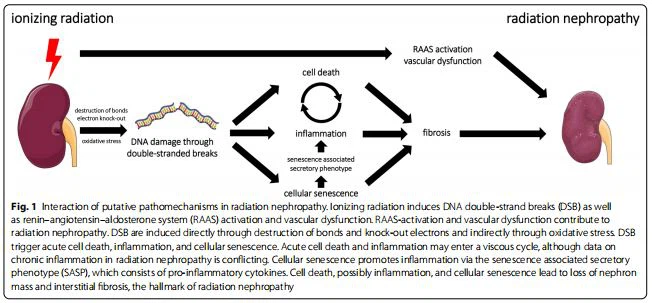
En la RN, la lesión inicial de las células renales, que puede iniciar la cascada hacia la ERC, es la DSB del ADN a través de la radiación ionizante, ya sea por eventos de ionización directa en el ADN o indirectamente a través de la mediación de productos de ionización del agua y/o especies reactivas de oxígeno. 61] (fig. 1). Este daño agudo en el ADN puede causar la muerte celular inmediata en el riñón [62-64]. En pacientes con cáncer sometidos a RT, los estudios de perfiles transcriptómicos muestran nefrotoxicidad con regulación al alza de genes para la necrosis renal y la apoptosis [65]. En las células que sobreviven a la fase aguda, los mecanismos de reparación del ADN están muy activados [66]. Incluso cuando las células no mueren por daño agudo, el DSB mal reparado puede inducir la muerte celular o la senescencia celular a largo plazo [20]. Las citocinas liberadas tras la muerte celular [67], la senescencia celular [60] y la propia radiación ionizante [7] desencadenan la inflamación crónica. Finalmente, la inflamación crónica y la senescencia celular pueden provocar fibrosis renal [23].
Por lo tanto, las supuestas rutas de señalización molecular y celular de RN comienzan dentro del espectro del daño del ADN y sus mecanismos de reparación en el riñón. La muerte celular, el estrés oxidativo, la disfunción vascular, la senescencia celular, la inflamación, la liberación de agentes profibróticos y la activación del sistema renina-angiotensina-aldosterona (RAAS) son los mecanismos patogénicos putativos en la nefropatía por radiación (Tabla 2). Estos mecanismos patogénicos y los datos actualmente disponibles se discutirán en los siguientes párrafos.
Estrés oxidativo
El estrés oxidativo (OS) está presente cuando las especies reactivas de oxígeno (ROS) superan a los antioxidantes enzimáticos y no enzimáticos. Las ROS reaccionan con lípidos, proteínas y ADN [17]. Esto conduce al daño celular y la senescencia [92]. En el daño tisular inducido por radiación, el papel del OS en la fase aguda con daño en el ADN está bien establecido [17]. Además, el OS es un mecanismo patológico importante en la ERC, las complicaciones de la ERC y la progresión de la ERC [93, 94]. Por lo tanto, OS también podría desempeñar un papel en RN.
Sin embargo, es importante comprender la diferencia entre OS generado inmediatamente después de la irradiación y OS en el período latente de RN. Para demostrar que el OS juega un papel en la etiología de la nefropatía por radiación crónica, el OS debe estar presente en el período latente. Tales datos son raros y aún contradictorios. Zhao et al. planteó la hipótesis de que el OS crónico es responsable de la RN. Los autores mostraron una oxidación del ADN regulada al alza en glomérulos y tubulina viables en ratas de 4 a 24 semanas después de una dosis única de irradiación con 20 Gy [71]. Por el contrario, Lenarczyk et al. no encontró evidencia de SG crónica en el período de latencia en ratas que se sometieron a TBI con 18,8 Gy en 6 fracciones o 10 Gy en una sola dosis. No hubo evidencia de peroxidación de lípidos u oxidación de proteínas en la orina en los primeros 42 días. Después de 89 días, el tejido renal no mostró evidencia de oxidación de ADN o proteína [74]. Del mismo modo, el análisis de la expresión génica no reveló un aumento relevante en los genes relacionados con la SG en los primeros 49 días después de una dosis única de TBI con 10 Gy [73]. Las ratas se volvieron sintomáticas con proteinuria aproximadamente 6 semanas después de la irradiación y se produjo morbilidad urémica después de 26 semanas. Por lo tanto, los puntos de tiempo investigados estaban en la fase latente de la RN experimental, y no mostraron evidencia de OS en el período latente.
Cohen et al. no encontraron mitigación de RN para la deferiprona, la genisteína y la apocinina del agente antioxidante cuando se administraron en el período de latencia después de una dosis única de TBI de 10 Gy en ratas [72]. Por el contrario, la protección contra OS se mostró en entornos experimentales, cuando las sustancias antioxidantes se administraron antes de la irradiación. Mercatepe et al. mostró que el antioxidante N-acetilcisteína eliminador de ROS aumentó los niveles de glutatión en ratas irradiadas con 6 Gy TBI. La N-acetilcisteína mitigó la RN histopatológica y redujo la expresión de caspasa-3. En este estudio, se administró N-acetilcisteína desde 5 días antes hasta 2 días después del TCE. Los autores concluyeron que los beneficios se obtuvieron al reducir la SG [68]. Resultados similares provinieron de Amiri et al. utilizando estatinas hipolipemiantes en RN experimental. Además de los efectos sobre el metabolismo de los lípidos, las estatinas tienen efectos antiinflamatorios, antiapoptóticos y antioxidantes [95]. El tratamiento diario con atorvastatina 7 días antes de 2 Gy TBI disminuyó la peroxidación de lípidos como marcador de OS, mejoró la función renal, redujo la expresión de caspasa 3- y mejoró el daño tubular en ratones [70]. También se demostraron efectos nefroprotectores y antioxidantes para los antagonistas de los receptores de leucotrienos. Montelukast es un antagonista selectivo del receptor de leucotrieno CysLT1-, que se desarrolló para la disfunción respiratoria. Este fármaco antiinflamatorio también mejoró la SG [96]. Hormati et al. encontró que montelukast administrado 2 semanas antes de 3 Gy TBI en ratones fue capaz de reducir la OS y mitigar la RN [69].
En conjunto, los datos sobre OS en la nefropatía por radiación muestran una clara evidencia de que OS juega un papel importante en el daño del ADN inmediatamente después de la irradiación. Además, la aplicación de antioxidantes antes de la irradiación mitiga la RN. Por el contrario, en la fase latente OS no fue detectable en una cantidad significativa, ni la atenuación farmacológica de OS pudo mitigar la RN. Por lo tanto, OS no parece jugar un papel después del momento muy temprano de la irradiación. Sin embargo, las consecuencias del OS (daños en el ADN, muerte celular e inducción de la senescencia celular) son cruciales en la RN.
Sistema renina-angiotensina-aldosterona
El sistema renina-angiotensina-aldosterona (RAAS) consiste en enzimas y sus sustratos peptídicos e involucra múltiples órganos. RAAS es un importante regulador de la presión arterial y electrolitos. La renina se produce en los riñones. Escinde el angiotensinógeno del hígado en angiotensina I (AT I), que luego se convierte en angiotensina II (AT-II) por la enzima convertidora de angiotensina (ACE), que se origina en los pulmones. Sin embargo, todos los componentes individuales del SRAA están presentes dentro de los riñones y se denominan SRAA intrarrenales. La activación intrarrenal del SRAA desempeña un papel fundamental en las enfermedades renales, especialmente en la hipertensión renal [97].
La inhibición de RAAS con captopril mitigó RN en un ensayo controlado aleatorizado en pacientes después de 14 Gy TBI en 9 fracciones con protección renal que produjo una dosis total de 9,8 Gy en preparación para BMT. Se administró captopril o placebo después del injerto del huésped y mejoró la TFG a 1 año y la supervivencia general del paciente [76]. La inhibición de RAAS fue beneficiosa en modelos animales de RN (dosis única de 10 Gy TBI en ratas, aplicación de 177Lu-DOTATATE en ratones) [77–79]. La mitigación por inhibición de RAAS fue más efectiva en experimentos con animales que en pacientes después de un BMT. La explicación más probable es que en los pacientes con TCE no sea el único agente nefrotóxico en el proceso de TMO. La quimioterapia, la infección y los medicamentos antiinfecciosos contribuyen a la ERC después de un BMT, y la inhibición de RAAS no mitiga todas las formas de lesión renal.
La inhibición de RAAS también es beneficiosa en las lesiones por radiación en los pulmones [98] y el cerebro [99]. Estos hallazgos plantean urgentemente la pregunta de si RAAS juega un papel mecánico en RN después de RT. Hasta el momento, no existe evidencia sólida para la inducción de RAAS- en RN. Cohen et al. no mostró ninguna activación de SRAA con actividad de renina normal, niveles de proteína de renina normales y valores normales de AT-II sérica e intrarrenal después de 17 Gy TBI en 6 fracciones [82]. La unión al receptor AT-II de la membrana celular renal se observó igualmente en ratas después de una LCT con 18,8 Gy o 20,5 Gy administrados en seis fracciones durante 3 días y en el grupo de control [81]. La aldosterona es un componente periférico del sistema RAAS involucrado en varios tipos de lesiones renales [100]. En un estudio no se mostró aumento de la aldosterona después de una dosis única de 10 Gy de TBI en ratas y el antagonista de la aldosterona, la espironolactona, no mitigó la RN [79]. Sin embargo, otro grupo encontró que la espironolactona mitiga la RN después de la irradiación interna con partículas alfa en ratones [101]. Parece que, al igual que el bloqueo de AT II, los antagonistas de la aldosterona pueden mitigar la RN, aunque la aldosterona en sí misma no está regulada al alza.
El efecto claramente beneficioso de la inhibición de RAAS sin un aumento medible de la actividad de RAAS sugiere que la actividad normal de RAAS es dañina en sujetos irradiados o que los sistemas opuestos a RAAS como el óxido nítrico (NO) disminuyen después de la irradiación [79]. Hay evidencia de reducción de NO en RN en ratas después de 17 Gy TBI en 6 fracciones durante 3 días, y RN podría mitigarse con captopril [102]. En general, la inhibición de RAAS estabiliza el progreso de numerosas enfermedades renales de diferentes etiologías. Su efecto nefroprotector está mediado por la reducción de la presión intraglomerular y, por lo tanto, la reducción de la proteinuria con un daño tubulointersticial consecutivo menor [103]. En conclusión, la inhibición de RAAS podría tener un efecto protector al reducir la presión intraglomerular, la fibrosis renal y equilibrar la reducción de NO en RN. El bloqueo de RAAS es, por lo tanto, una estrategia muy prometedora para la terapia con RN.
Senescencia celular
La senescencia celular (CS) es la combinación de la detención del ciclo celular, la supresión de las vías apoptóticas, una alta actividad metabólica y un fenotipo secretor asociado a la senescencia (SASP). SASP incluye una mayor secreción de IL-1, IL-6, IL-8, factor de crecimiento del tejido conectivo, factor de crecimiento transformante, factor de crecimiento del endotelio vascular y TNF- [104, 105]. Si bien es parte del proceso de envejecimiento cronológico normal, caracterizado por el desgaste de los telómeros, la senescencia prematura es inducida por factores de estrés, como la radiación ionizante directa o indirectamente por OS [106, 107]. En el cerebro [108], el corazón [109] y los pulmones [98], la CS contribuye al daño orgánico inducido por la radiación. En la ERC de etiologías distintas a la NRC, el CS también es un mecanismo patológico sugerido [60]. En RN experimental con dosis única de 18 Gy en ratas, se ha demostrado CS en células endoteliales glomerulares y en podocitos de ratas, lo que subraya el impacto de CS en RN. La lesión endotelial glomerular fue dominante, lo que resultó en un aumento de la microangiopatía trombótica, el colapso de los glomérulos y una disminución del número de células endoteliales en la RN experimental. Las células renales demostraron un aumento de los marcadores de senescencia celular (p53, p21, p16), detención del ciclo celular y tenían un SASP con una mayor secreción de IL-6. La secreción de TNF-, IL-8 y VEGF-A no aumentó significativamente. En este modelo experimental de RN [83] se encontró daño glomerular y deterioro de la función renal. Así, la senescencia celular parece estar activada en RN.
infamación
La inflamación se ha propuesto como un mecanismo para la RN porque está presente en otras lesiones por radiación, como la lesión gastrointestinal por radiación [110] y la neumonitis por radiación [25]. Además, la inflamación mecánica vincula la lesión de las células renales y la ERC. Las células tubulares necróticas liberan patrones moleculares asociados al daño (DAMP) y desencadenan la secreción de citocinas y quimiocinas proinflamatorias en células residentes en tejidos y leucocitos reclutados [111]. Los macrófagos, por ejemplo, producen citoquinas como TNF- e IL-6. Estas respuestas informa-obligatorias conducen a una muerte celular aún mayor y alimentan un círculo vicioso de muerte celular e inflamación [67], seguido de una disminución de la función renal y el inicio de la fibrosis renal [112]. Sin embargo, solo hay pocos datos sobre la inflamación activa en RN. Se descubrió que las citocinas proinflamatorias, como TNF-, IL-1 e interferón-, son los principales reguladores aguas arriba de las transcripciones reguladas al alza en ratones después de la admisión de 177Lu-octreotato [84]. Los niveles de expresión de TNF-aumentaron y se correlacionaron con la actividad metabólica detectada en [18F]-FDG-PET-CT en minicerdos tibetanos después de una dosis única de TBI de 2, 5, 8, 11 y 14 Gy [85]. Otras pruebas de la implicación de la inflamación en la RN derivan de la observación de que montelukast fue capaz de mitigar la RN en ratones después de una dosis única de TBI de 3 Gy de forma dependiente de la dosis [69]. Montelukast tiene efectos antiinflamatorios mediante la inhibición de la activación del factor nuclear κB y la reducción de citocinas antiinflamatorias, como TNF- e IL-6 [113].
Por el contrario, hay estudios recientes realizados en macacos rhesus, que demuestran que la inflamación juega un papel menor o nulo en la RN. Van Kleef et al. investigó la RN crónica en macacos mediante análisis histológico de 6 a 8 años después de una dosis única de irradiación de 4,5 a 8,5 Gy o dos fracciones de 5 Gy. En comparación con los controles de la misma edad, no hubo diferencias significativas en la infiltración de leucocitos en el riñón y solo un número ligeramente mayor de macrófagos estaban presentes en la corteza renal [57]. Sin embargo, después de un período de tiempo tan largo, es de esperar que la inflamación ya se haya detenido y la fibrosis se haya hecho cargo. Parker et al. macacos expuestos a irradiación corporal parcial a 10, 11 o 12 Gy con un 5 por ciento de protección de la médula ósea. La infiltración de células inflamatorias o el aumento de las poblaciones de macrófagos no fueron características histológicas destacadas aproximadamente 100 días después de la irradiación [56]. Muy recientemente, Cohen et al. no mostró inflamación celular relevante en los riñones 180 días después de la irradiación corporal parcial de 10 Gy en macacos con un 5 por ciento de preservación de la médula ósea o un 2,5 por ciento de preservación de la médula ósea. La inflamación celular casi nunca superó el 1 por ciento del área del parénquima renal [87]. La estimulación de los linajes hematopoyéticos con factor estimulante de granulocitos no cambió la infiltración de leucocitos y no tuvo efectos adversos ni beneficiosos en la RN experimental. Cuando se probó en conejos irradiados, el potente agente antiinflamatorio prednisolona afectó negativamente la supervivencia de 6 semanas y 9 meses [86]. Aunque sería posible que la inflamación no celular pero mediada por citocinas desempeñe un papel en la RN, parece poco probable, ya que las células que ejecutan la inflamación mediada por citocinas no estaban presentes. Actualmente falta descartar por completo el papel de los macrófagos en el análisis funcional de RN de estas poblaciones, ya que se sabe que los macrófagos residentes en tejidos contribuyen a la enfermedad renal [114].
En resumen, los datos actuales sugieren que la inflamación, a diferencia de otros órganos, no es un mecanismo patológico importante para la RN y la búsqueda de opciones de tratamiento debe concentrarse en otras vías.
disfunción vascular
La disfunción endotelial y la hemodinámica alterada son características conocidas de la toxicidad renal inducida por la radiación [88]. Los ácidos epoxieicosatrienoicos (EET) son producidos en el endotelio por las enzimas epoxigenasas CYP. Los EET derivan del ácido araquidónico y se ha demostrado que protegen los riñones en varios modelos de patologías renales [89, 90]. La irradiación experimental conduce a una disminución de las epoxigenasas renales CYP y de los niveles urinarios de EET, a daño endotelial y vascular con disfunción arteriolar aferente y respuestas autorreguladoras alteradas en el riñón. Los análogos de Eet se administraron diariamente desde el día 2 hasta las 12 semanas en ratas después de una dosis única de 11 Gy TBI. Se mejoró la función arteriolar aferente, se mitigó la hipertensión y se redujo la apoptosis renal a través de la vía Fas/FasL [91]. Por lo tanto, los análogos de EET parecen mitigar la RN por mecanismos distintos al OS y la inflamación y, por lo tanto, pueden ser prometedores para futuras terapias.
Fibrosis
La fibrosis renal es la formación de cicatrices en el parénquima. Es una forma patológica de cicatrización normal de heridas con activación y migración de miofibroblastos, depósito de matriz extracelular y remodelación renal. La fibrosis es la vía final común para casi todas las etiologías de la ERC. Los mecanismos que conducen a la fibrosis pueden ser útiles para la reparación de tejidos en lesiones agudas; sin embargo, cuando ocurren de manera persistente en la ERC, conducen a un tejido funcional y provocan una disminución de la función renal [23]. Los mi- fibroblastos son la fuente principal de la matriz extracelular. El colágeno I es la proteína de matriz más común en la fibrosis renal, pero también se encuentran los tipos II, IV, V y XV [115]. El factor de crecimiento transformante beta (TGF-) estimula la diferenciación de miofibroblastos en la fibrosis renal [116].
Otros estímulos importantes para la activación de los miofibroblastos y la fibrosis renal son el sistema inmunitario innato y adaptativo [112]. Solo hay pocos datos histológicos y mecanicistas sobre la fibrosis en la RN crónica. Sin embargo, los datos disponibles apoyan la hipótesis de que la fibrosis está presente en RN. En macacos, la fibrosis renal se mostró aproximadamente 100 días después de 10, 11 o 12 Gy TBI con una protección de la médula ósea del 5 por ciento. Todos los hallazgos ocurrieron globalmente en todo el riñón, incluida la corteza y la médula. En el momento de la necropsia, el TGF- estaba igualmente aumentado en los riñones irradiados y en los controles, lo que resultó sorprendente dada la extensa fibrosis que siguió a la RT. Esos hallazgos sugieren un efecto independiente de TGF- -sobre la fibrosis renal. La fibrosis renal estuvo presente principalmente en los animales que sobrevivieron más tiempo, lo que sugiere que se trata de un efecto a largo plazo, como se conoce en otras formas de lesión renal [56]. El bloqueo de RAAS con inhibidores de la ECA y análogos de EET redujo el depósito de matriz extracelular y la fibrosis renal y resultó beneficioso en la RN experimental.

Conclusión
Aunque existen datos sobre los mecanismos patogénicos moleculares y celulares en la toxicidad renal inducida por radiación, son escasos. Hasta la fecha, la señalización precisa y los mecanismos patogénicos no se conocen por completo. Hay algunos datos de pacientes, pero la mayoría proviene de modelos experimentales (principalmente ratas y primates no humanos). Los esquemas de aplicación y las dosis de radiación ionizante varían, lo que complica aún más la comparabilidad. En muchos aspectos, la RN tiene características comunes con la lesión renal aguda que se transforma en enfermedad renal crónica. El estímulo agudo en la RN es la radiación ionizante y la etapa final común es la fibrosis renal con atrofia de órganos y disminución de la función renal. Se propuso que el estrés oxidativo y la inflamación son mecanismos patogénicos relevantes en la fase latente, pero no existe evidencia sólida para ninguno de ellos.
El sistema renina-angiotensina-aldosterona parece ser un candidato prometedor. Los inhibidores de RAAS mitigan la progresión de RN en pacientes y en modelos experimentales. La disfunción vascular renal está presente en la RN y puede ser atenuada por los ácidos epoxieicosatrienoicos. Se demostró que la senescencia celular estaba presente en RN experimental. Debido a que la fibrosis es la etapa final de la RN, el bloqueo del depósito de matriz extracelular puede ser un objetivo prometedor para futuras terapias. Todavía faltan biomarcadores para diagnosticar y evaluar la progresión y la gravedad de la RN y es necesario identificarlos. Pueden indicar nuevas vías para futuras investigaciones y objetivos terapéuticos en RN.
Referencias
1. Wild CP, Espina C, Bauld L, Bonanni B, Brenner H, Brown K, et al. Prevención del cáncer Europa. Mol Oncol. 2019;13(3):528–34.
2. Bray F, Ferlay J, Soerjomataram I, Siegel RL, Torre LA, Jemal A. Estadísticas globales de cáncer 2018: estimaciones de GLOBOCAN de incidencia y mortalidad en todo el mundo para 36 cánceres en 185 países. CA Cáncer J Clin. 2018;68(6):394–424.
3. Bristow RG, Alexander B, Baumann M, Bratman SV, Brown JM, Camphausen K, et al. Combinación de radioterapia de precisión con orientación molecular y agentes inmunomoduladores: una guía de la Sociedad Estadounidense de Oncología Radioterápica. Lanceta Oncol. 2018;19(5):e240–51.
4. Cunha JAM, Flynn R, Belanger C, Callaghan C, Kim Y, Jia X, et al. Direcciones futuras de la braquiterapia. Semin Radiat Oncol. 2020;30(1):94–106.
5. Erbas B, Tuncel M. Evaluación de la función renal durante la terapia con radionúclidos del receptor de péptidos. Semin Nucl Med. 2016;46(5):462–78.
6. Orth M, Lauber K, Niyazi M, Friedl AA, Li M, Maihofer C, et al. Conceptos actuales en oncología radioterápica clínica. Radiat Environ Biophys. 2014;53(1):1–29.
7. De Ruysscher D, Niedermann G, Burnet NG, Siva S, Lee AWM, Hegi‑ Johnson F. Radiotherapytoxicity. Imprimadores Nat Rev Dis. 2019;5(1):13.
8. de Crevoisier R, Chauvet B, Barillot I, Lafond C, Mahe M, Delpon G. Radioterapia guiada por imágenes. Cáncer Radiother. 2016;20(Suplemento):S27‑35.
9. Teoh M, Clark CH, Wood K, Whitaker S, Nisbet A. Terapia de arco modulado volumétrico: una revisión de la literatura actual y el uso clínico en la práctica. Br J Radiol. 2011;84(1007):967–96.
10. Gregoire V, Guckenberger M, Haustermans K, Lagendijk JJW, Menard C, Potter R, et al. Orientación por imagen en radioterapia para la mejor cura del cáncer. Mol Oncol. 2020;14(7):1470–91.
11. Corradini S, Alongi F, Andratschke N, Belka C, Boldrini L, Cellini F, et al. MR: orientación en la realidad clínica: desafíos actuales del tratamiento y perspectivas futuras. Radiat Oncol. 2019;14(1):92.
12. Kugele M, Mannerberg A, Norring Bekke S, Alkner S, Berg L, Mahmood F, et al. La radioterapia guiada por superficie (SGRT) mejora la precisión de la configuración del paciente con cáncer de mama. J Appl Clin Med Phys. 2019;20(9):61–8.
13. Langendijk JA, Lambin P, De Ruysscher D, Widder J, Bos M, Verheij M. Selección de pacientes para radioterapia con protones con el objetivo de reducir los efectos secundarios: el enfoque basado en modelos. Radiother Oncol. 2013;107(3):267–73.
14. Durante M, Orecchia R, Loefer JS. Terapia de partículas cargadas en cáncer: usos clínicos y perspectivas futuras. Nat Rev Clin Oncol. 2017;14(8):483–95.
15. Paix A, Antoni D, Waissi W, Ledoux MP, Bilger K, Fornecker L, et al. Irradiación corporal total en regímenes de acondicionamiento de trasplante alogénico de médula ósea: una revisión. Crit Rev Oncol Hematol. 2018;123:138–48.
16. Schaue D, McBride WH. Oportunidades y desafíos de la radioterapia para el tratamiento del cáncer. Nat Rev Clin Oncol. 2015;12(9):527–40.
17. Wei J, Wang B, Wang H, Meng L, Zhao Q, Li X, et al. Daño tisular normal inducido por radiación: estrés oxidativo y mecanismos epigenéticos. Oxid Med Cell Longev. 2019;2019:3010342.
18. Lord CJ, Ashworth A. La respuesta al daño del ADN y la terapia del cáncer. Naturaleza. 2012;481(7381):287–94.
19. Goldstein M, Kastan MB. La respuesta al daño del ADN: implicaciones para las respuestas tumorales a la radiación y la quimioterapia. Annu Rev Med. 2015;66:129–43.
20. Mahamud O, So J, Chua MLK, Bristow RG. Dirigirse a la reparación del ADN para la radioterapia de precisión: equilibrar la proporción terapéutica. Curr Probl Cáncer. 2017;41(4):265–72.
