El inhibidor del factor prolil hidroxilasa oral inducible por hipoxia Enarodustat contrarresta las alteraciones en el metabolismo energético renal en las primeras etapas de la enfermedad renal diabética
Mar 02, 2022
Contacto: emily.li@wecistanche.com
Introducción
División de Nefrología y Endocrinología, Facultad de Medicina de la Universidad de Tokio, Tokio, Japón; Beca de Investigación para Jóvenes Científicos, Sociedad Japonesa para la Promoción de la Ciencia, Tokio, Japón; Laboratorios de Investigaciones Biológicas y Farmacológicas,
Instituto Central de Investigación Farmacéutica, Japan Tobacco Inc., Takatsuki, Japón; Departamento de Farmacología de Sistemas, Facultad de Medicina de la Universidad de Tokio, Tokio, Japón; Laboratorio de Biología Sintética, Centro RIKEN para la Investigación de Dinámica de Biosistemas, Suita, Japón; y el Centro Internacional de Investigación de Neurointeligencia WPI, Institutos de Estudios Avanzados de la Universidad de Tokio (UTIAS), Universidad de Tokio, Tokio, Japón.
Los inhibidores de la prolil hidroxilasa del factor inducible por hipoxia (HIF), también conocidos como estabilizadores del HIF, aumentan la producción endógena de eritropoyetina y sirven como nuevos agentes terapéuticos contra la anemia encrónicoriñónenfermedad. HIFinduce la expresión de varios genes relacionados con el metabolismo energético como respuesta adaptativa a la hipoxia. Sin embargo, sigue siendo oscuro cómo la reprogramación metabólica del tejido interno por la estabilización de HIF afecta la fisiopatología deriñón enfermedades. Estudios previos sugieren que los trastornos metabólicos sistémicos, como la hiperglucemia y la dislipidemia, provocan alteraciones del metabolismo renal, lo que lleva a una disfunción renal, incluida la enfermedad renal diabética. Aquí, analizamos los efectos de enarodustat (JTZ-951), un estabilizador oral de HIF, sobre el metabolismo energético renal en las primeras etapas de la enfermedad renal diabética, utilizando ratas diabéticas inducidas por estreptozotocina y ratones diabéticos inducidos por aloxano. El análisis del transcriptoma reveló que enarodustat contrarresta las alteraciones en el metabolismo renal diabético. El análisis del transcriptoma mostró que los metabolismos de ácidos grasos y aminoácidos estaban regulados al alza en el tejido renal diabético y regulados a la baja por enarodustat, mientras que el metabolismo de la glucosa estaba regulado al alza. Estos cambios simétricos fueron confirmados por análisis de metaboloma. Mientras que la glucólisis y los metabolitos del ciclo del ácido tricarboxílico se acumularon y los aminoácidos se redujeron en el tejido renal de los animales diabéticos, estos trastornos metabólicos se mitigaron con enarodustat. Además, la enarodusta aumentó la proporción de glutatión a disulfuro de glutatión y alivió el estrés oxidativo en el tejido renal de los animales diabéticos. Así, la estabilización del HIF contrarresta las alteraciones en el metabolismo energético renal que se producen en pacientes incipientes.diabéticoriñónenfermedad.

Cistanche es muy bueno para la función renal
Declaración de traducción
Los inhibidores de la prolil hidroxilasa del factor inducible por hipoxia (HIF) (también conocidos como estabilizadores de HIF) aumentan la producción de eritropoyetina endógena y sirven como nuevos agentes terapéuticos contra la anemia encrónicoriñónenfermedad. Nuestros análisis de transcriptoma y metaboloma del tejido renal en modelos diabéticos de rata y ratón han revelado que enarodustat (JTZ-951), un estabilizador oral de HIF, contrarresta las alteraciones del metabolismo energético renal en las primeras etapas de la enfermedad renal diabética. Los resultados proporcionan datos importantes para extrapolar los efectos de los estabilizadores de HIF sobre el metabolismo energético renal en entornos clínicos, aunque se necesitan más estudios para aclarar cómo esta reprogramación del metabolismo renal por los estabilizadores de HIF afecta la progresión de la enfermedad.diabéticoriñónenfermedad.
La introducción
Los inhibidores de la prolil hidroxilasa del factor inducible por hipoxia (HIF) aumentan la producción endógena de eritropoyetina y sirven como nuevos agentes terapéuticos contra la anemia en pacientes crónicos.riñónenfermedad. Las células están dotadas de un mecanismo defensivo frente a la hipoxia, y el HIF es un regulador maestro de esta defensa. Los riñones están fisiológicamente expuestos a la hipoxia, y la hipoxia crónica se reconoce como una vía común final que conduce a la enfermedad renal en etapa terminal. Teniendo en cuenta que HIF induce la expresión de varios genes relacionados con las respuestas de hipoxia, los estabilizadores de HIF podrían tener efectos pleiotrópicos en la progresión de lariñónenfermedadesasí como la mejora de la anemia en pacientes crónicosriñónenfermedad. Curiosamente, el HIF induce la expresión de genes glucolíticos y de la piruvato deshidrogenasa cinasa, que impide que la piruvato deshidrogenasa use piruvato para alimentar el ciclo del ácido tricarboxílico mitocondrial (TCA).6,7 Esta reprogramación metabólica del ciclo TCA a la glucólisis reprime el consumo de oxígeno y es fundamental para la adaptación de las células expuestas a ambientes hipóxicos. Sin embargo, sigue siendo oscuro cómo la reprogramación metabólica del tejido renal por la estabilización HIF afecta la fisiopatología deriñón enfermedades. La enfermedad renal diabética (DKD, por sus siglas en inglés) es la causa principal de la enfermedad renal en etapa terminal. Los trastornos metabólicos sistémicos, como la hiperglucemia y la dislipidemia, provocan alteraciones del metabolismo renal, lo que lleva a una disfunción renal, incluida la ND. Estudios previos han demostrado un aumento del flujo metabólico y la acumulación de glucosa y metabolitos del ciclo TCA en el tejido cortical renal diabético, lo que podría estar relacionado con la disfunción mitocondrial y la progresión de la DKD. Presumimos que los estabilizadores de HIF podrían revertir las alteraciones del metabolismo en el tejido cortical renal diabético, considerando que HIF, como respuesta adaptativa a la hipoxia, reduce el flujo metabólico en las células para reprimir el consumo de oxígeno. Por lo tanto, utilizando análisis de transcriptoma y metaboloma, realizamos un estudio de prueba de concepto para comprender de manera integral cómo el enarodustat (JTZ-951), un estabilizador oral de HIF, afecta las alteraciones del metabolismo renal que ocurren en las primeras etapas de la ND.
RESULTADOS: Enarodustat induce la reprogramación metabólica del ciclo TCA a la glucólisis en las células del túbulo proximal renal
Como la corteza renal se compone principalmente de túbulos proximales, primero examinamos los efectos de enarodustat en el flujo metabólico de las células del túbulo proximal renal in vitro. En primer lugar, se realizaron la prueba de estrés Mito (Agilent Technologies, Inc., Santa Clara, CA) y el ensayo de velocidad glucolítica (Agilent) en células HK-2 cultivadas, una línea de células epiteliales del túbulo proximal humano (Figura 1a). Enarodustat redujo significativamente la respiración mitocondrial (ciclo TCA) y aumentó la glucólisis basal, lo que indica una reprogramación metabólica del ciclo TCA a la glucólisis (Figura 1; Figura complementaria S1). También realizamos un experimento con ARN de interferencia pequeño (siRNA) para HIF-1 (Figura 2; Figura complementaria S2). La eliminación de HIF-1 por siRNA invirtió las alteraciones metabólicas (respiración basal, respiración máxima, capacidad respiratoria adicional y producción de trifosfato de adenosina [ATP]) inducidas por enarodustat, lo que demostró que la reprogramación metabólica se produjo principalmente a través de HIF-1 estabilización (Figura 2; Figura complementaria S2). La actividad de la piruvato deshidrogenasa, un factor importante para que las células usen piruvato para alimentar el ciclo de TCA, también se redujo con enarodustat (Figura 2f), lo que era compatible con las observaciones publicadas anteriormente.


Antecedentes de ratas diabéticas inducidas por estreptozotocina
A partir de los resultados de los experimentos in vitro, planteamos la hipótesis de que los estabilizadores de HIF podrían aliviar las alteraciones del metabolismo en el tejido cortical renal diabético a través de la reprogramación metabólica del ciclo TCA a la glucólisis. Primero elegimos ratas diabéticas inducidas por estreptozotocina (STZ) como modelo para el experimento de prueba de concepto para probar la hipótesis mencionada anteriormente. En este modelo, la diabetes se induce rápidamente, lo que nos permite observar los efectos netos de la diabetes y los estabilizadores de HIF en el metabolismo energético del tejido renal en un corto período de tiempo. El protocolo de estudio y los datos básicos de los experimentos en ratas diabéticas inducidas por STZ se muestran en la Figura 3a. Dividimos las ratas en 3 grupos: grupo A (falso), grupo B (DKD) y grupo C (DKD + enarodustat). Los niveles de glucosa en plasma sanguíneo, hemoglobina glicosilada HbA1c, triglicéridos y colesterol total en el día 14 aumentaron significativamente en los grupos diabéticos en comparación con el grupo A, mientras que no hubo diferencias significativas entre los grupos B y C (Figura 3d-g). Aunque los niveles de creatinina plasmática no fueron diferentes entre los grupos, la excreción urinaria de albúmina aumentó significativamente y la glomerulomegalia fue notoria en el grupo B en comparación con el grupo A, y enarodustat tendió a revertir estos cambios (Figura 4). Los niveles de nitrógeno ureico en sangre fueron más altos en los grupos de diabéticos, lo que refleja la deshidratación debida a la diabetes. En resumen, los riñones de ratas tratadas con STZ en nuestro estudio representan las primeras etapas de DKD. Se realizaron análisis de transcriptoma y metaboloma usando el tejido cortical renal de estas ratas.

Análisis transcriptómico del tejido cortical renal
Los resultados del análisis del transcriptoma del tejido cortical renal se muestran en las Figuras 5 y 6. El análisis de componentes principales y el análisis de agrupamiento jerárquico indicaron que los grupos A, B y C se separaron en diferentes grupos, respectivamente (Figura 5a yb). Los genes expresados diferencialmente se seleccionaron mediante │log2 fold-change (FC) │ Mayor o igual que 0.5 y valor Q < 0.05.="" la="" ontología="" génica="" y="" los="" análisis="" de="" vías="" canónicas="" revelaron="" que="" los="" genes="" relacionados="" con="" el="" metabolismo="" de="" los="" ácidos="" grasos="" estaban="" regulados="" al="" alza="" en="" el="" grupo="" b="" en="" comparación="" con="" el="" grupo="" a.="" por="" el="" contrario,="" los="" genes="" relacionados="" con="" el="" metabolismo="" de="" la="" glucosa="" y="" la="" respuesta="" a="" la="" hipoxia,="" incluida="" la="" red="" hif-1,="" estaban="" regulados="" al="" alza="" en="" el="" grupo="" c="" en="" comparación="" con="" el="" grupo="" b="" (figura="" 5c="" y="" d).="" también="" realizamos="" un="" análisis="" de="" enriquecimiento="" de="" conjuntos="" de="" genes="" (gsea)="" utilizando="" los="" datos="" transcriptómicos="" (figura="" 6,="" tablas="" 1="" y="" 2).="" los="" conjuntos="" de="" genes="" del="" metabolismo="" de="" ácidos="" grasos="" y="" aminoácidos="" aumentaron="" en="" el="" grupo="" b="" en="" comparación="" con="" el="" grupo="" a="" (figura="" 6).="" por="" el="" contrario,="" estos="" conjuntos="" de="" genes="" estaban="" regulados="" a="" la="" baja,="" y="" los="" conjuntos="" de="" genes="" del="" metabolismo="" de="" la="" glucosa="" estaban="" regulados="" al="" alza="" en="" el="" grupo="" c="" en="" comparación="" con="" el="" grupo="" b,="" lo="" que="" demuestra="" que="" enarodustat="" revirtió="" las="" alteraciones="" del="" metabolismo="" inducidas="" por="" la="" diabetes="" (figura="" 6).="" además,="" los="" conjuntos="" de="" genes="" del="" ciclo="" tca="" se="" regularon="" a="" la="" baja="" en="" el="" grupo="" c="" en="" comparación="" con="" el="" grupo="" b="" (tabla="" 2),="" lo="" que="" es="" compatible="" con="" la="" noción="" de="" reprogramación="" metabólica="" inducida="" por="" enarodustat="" en="" los="" túbulos="" proximales="" observados="" en="" nuestro="" estudio="" in="" vitro.="" en="" resumen,="" enarodustat="" contrarrestó="" las="" alteraciones="" del="" metabolismo="" renal="" diabético="" desde="" el="" punto="" de="" vista="">


Análisis del metaboloma del tejido cortical renal
Medimos las concentraciones absolutas de 116 metabolitos relacionados con la energía en el tejido cortical renal de ratas (n =4, para cada grupo) seleccionadas al azar de cada grupo (Tabla complementaria S1; Figura complementaria S3). Se realizó un análisis discriminante de mínimos cuadrados parciales (PLS-DA) para evaluar la importancia de la discriminación de clase (Figura 7). Realizamos un análisis de enriquecimiento de conjuntos de metabolitos (MSEA) utilizando los metabolitos con una puntuación de importancia variable en proyección (VIP) de PLS-DA de $ 1. Diferencias en el metabolismo de aminoácidos, como glicina, serina, metionina, aspartato, glutamato, arginina, prolina, y b-alanina entre los grupos A y B. También se observaron diferencias en el metabolismo de los aminoácidos entre los grupos B y C. Además, los procesos del metabolismo de la glucosa, como la glucólisis y la gluconeogénesis, mostraron tendencias diferentes entre los grupos B y C (Figura 7).


Visualización de datos de transcriptoma y metaboloma en el mapa de rutas metabólicas de energía
Visualizamos los datos del transcriptoma y el metaboloma para una comprensión integral de las alteraciones del metabolismo energético (Figura 8). Se encontró que los metabolitos del ciclo de la glucólisis y del TCA se acumulaban en el grupo B en comparación con el grupo A, lo que podría deberse a la entrada excesiva de glucosa y la regulación positiva del metabolismo de los ácidos grasos en la DKD. La concentración de aminoácidos se redujo en el grupo B en comparación con el grupo A, lo que refleja la regulación positiva del metabolismo de los aminoácidos (Figura 8a). Por el contrario, la acumulación de metabolitos de la glucólisis fue aliviada por enarodustat, debido al flujo facilitado de la glucólisis. Enarodustat también revirtió los cambios inducidos por la diabetes en los metabolitos y aminoácidos del ciclo TCA (Figura 8b). Además, el enarodustat alivió la acumulación de disulfuro de glutatión (GSSG) en el tejido renal diabético y, por lo tanto, mostró una mayor proporción de glutatión/GSSG, lo que sugirió que el enarodustat alivió el estrés oxidativo en la DKD (Figura 8a yb). La reducción del estrés oxidativo fue confirmada por los niveles del marcador de peroxidación lipídica malondialdehído en el tejido cortical renal: enarodustat revirtió la acumulación de malondialdehído en el tejido cortical renal diabético (Figura complementaria S4). En resumen, la integración de los datos del transcriptoma y el metaboloma ha demostrado que enarodustat contrarresta las alteraciones del metabolismo energético renal que se producen en las primeras etapas de la ND.


Alteraciones simétricas del metabolismo (diabetes vs. enarodustat) se confirman en un modelo alternativo
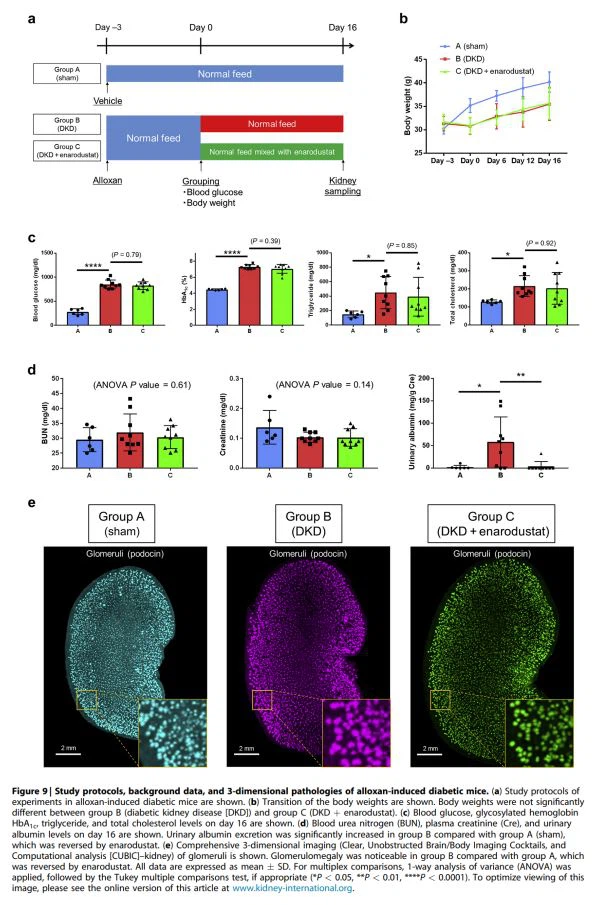
Realizamos un análisis del transcriptoma en ratones diabéticos inducidos por aloxano, otro modelo animal de diabetes, para confirmar nuestros hallazgos en el modelo de rata. Los protocolos de estudio y los datos de fondo para el modelo de ratón se muestran en la Figura 9. La excreción de albúmina urinaria aumentó significativamente en el grupo B en comparación con el grupo A, que se revirtió con enarodustat (Figura 9d). Además, aplicamos un análisis 3-dimensional completo (Cócteles de imágenes cerebrales/corporales claros y sin obstrucciones, y análisis computacional [CUBIC]–riñón)16 para visualizar los glomérulos en el riñón. La glomerulomegalia fue notable en el grupo B en comparación con el grupo A, que fue revertida por enarodustat (Figura 9e). El análisis del transcriptoma del tejido renal en ratones diabéticos inducidos con aloxano mostró alteraciones metabólicas simétricas (diabetes frente a enarodustat) de la misma manera que en el modelo de rata diabética inducida por STZ (Figura 10): el metabolismo de los ácidos grasos aumentó debido a la diabetes, mientras que la glucosa el metabolismo fue regulado por enarodustat. Además, el metabolismo de los aminoácidos se regulaba al alza por la diabetes y a la baja por el enarodustat. Por lo tanto, enarodustat contrarrestó las alteraciones del metabolismo energético renal que se producen en las primeras etapas de la DKD en el modelo de ratón diabético inducido por aloxano, así como en el modelo de rata diabética inducida por STZ.

DISCUSIÓN
En este estudio, hemos demostrado que enarodustat (JTZ-951), un estabilizador oral de HIF, contrarresta las alteraciones del metabolismo energético renal que se producen en las primeras etapas de la DKD en modelos de diabetes en ratas y ratones. Los análisis del transcriptoma y del metaboloma han mostrado alteraciones metabólicas simétricas en el tejido renal (diabetes versus enarodustat): los metabolismos de ácidos grasos y aminoácidos aumentaron en DKD, mientras que enarodustat reguló a la baja estas vías y, además, reguló al alza el metabolismo de la glucosa (figuras 5-10).
No se ha dilucidado completamente si la estabilización de HIF tiene efectos protectores sobre la fisiopatología de la ND o no. Estudios previos han demostrado que el tejido renal diabético está expuesto a la hipoxia17 y la expresión de HIF en el tejido renal diabético es insuficiente para responder a sus condiciones hipóxicas, que en parte es causada por el estrés oxidativo.18 La estabilización de HIF con cloruro de cobalto mejoró el estado de estrés oxidativo y redujo la proteinuria y daño tubulointersticial en la DKD inducida por STZ.19 Los resultados del estudio en animales también indicaron que la estabilización de HIF protegió contra el desarrollo de obesidad,20 mejoró la sensibilidad a la insulina,20 y redujo los niveles de colesterol sérico.21 Estos resultados sugieren los efectos protectores de la estabilización de HIF en el desarrollo de DKD. Por el contrario, se informó que la estabilización suprafisiológica de HIF por deleción de von Hippel-Lindau induce fibrosis renal.22 El papel de la estabilización de HIF en la progresión de DKD puede depender del contexto dados los efectos pleiotrópicos de HIF y la existencia de variados fenotipos de DKD. El objetivo de este estudio fue aclarar los efectos netos de la estabilización HIF sobre el metabolismo energético en el riñón diabético. Informes anteriores han indicado que en la DKD se producen alteraciones del metabolismo energético. Sas et al.10 demostraron un aumento del flujo metabólico energético y la acumulación de metabolitos de glucosa en el tejido cortical renal diabético, lo que podría estar relacionado con la disfunción mitocondrial. You et al.23 informaron que el fumarato, un metabolito del ciclo de los ATC, se acumulaba en el tejido renal diabético y contribuía directamente a la progresión de la ND. Anteriormente, hemos demostrado que los metabolitos del ciclo TCA se acumulan en el tejido renal diabético, lo que se revierte mediante la inhibición del cotransportador de sodio-glucosa 2 o la restricción calórica. estaban regulados al alza en pacientes diabéticos tipo 1 sin DKD en comparación con pacientes con DKD. La activación de PKM2 revirtió la acumulación de metabolitos de la glucólisis y restauró la función mitocondrial, en parte al aumentar el flujo glucolítico.24,25 Estos informes anteriores sugieren que la acumulación de metabolitos del ciclo de la glucólisis y del TCA podría afectar la progresión de la ND, que puede mitigarse mediante la glucólisis facilitada, incluida la PKM2. activación. En nuestro estudio, la estabilización del HIF con enarodustat revirtió las alteraciones del metabolismo energético y mitigó la acumulación de metabolitos del ciclo de la glucólisis y del TCA en el tejido cortical renal diabético (Figura 8). La expresión de enzimas glucolíticas, incluida PKM2, también se reguló positivamente con enarodustat (Figura complementaria S4B). Además, enarodustat alivió la acumulación de GSSG y aumentó la relación glutatión/GSSG, lo que sugiere que enarodustat alivió el estrés oxidativo en la DKD (Figura 8). Esta reducción del estrés oxidativo inducida por enarodustat también se confirmó mediante cambios en los niveles de malondialdehído en el tejido cortical renal (Figura complementaria S4A). Estos resultados sugieren que la estabilización de HIF debería tener funciones protectoras en la fisiopatología de la DKD al menos desde las perspectivas metabólicas. Es cierto que no podemos examinar si la reprogramación metabólica por la estabilización de HIF tiene efectos directos sobre la progresión de la DKD, porque puede ser imposible discernir los efectos netos de las alteraciones del metabolismo en el resultado renal debido al papel pleiotrópico de HIF. Sin embargo, en nuestro estudio, la excreción urinaria de albúmina leve y las anomalías patológicas renales (glomerulomegalia y engrosamiento de la membrana basal glomerular) inducidas por la diabetes fueron mitigadas por enarodustat, en asociación con la normalización del metabolismo energético renal. Extrajimos los genes cuyos cambios de expresión se correlacionaron con los niveles de albúmina urinaria (257 sondas; 232 genes) de los datos de micromatrices en el modelo de ratón diabético inducido por aloxano y realizamos un análisis de enriquecimiento de la vía (Figura complementaria S5). Como resultado, las vías relacionadas con la membrana mitocondrial y el transporte respiratorio de electrones se regulan al alza en relación con los niveles de albúmina urinaria, lo que indica que la carga mitocondrial está estrechamente relacionada con la excreción de albúmina urinaria. Por lo tanto, existe la posibilidad de que la normalización metabólica del tejido renal diabético por los estabilizadores HIF pueda reducir la carga mitocondrial y mitigar la progresión de la ND. Nuestros datos sugieren la fisiopatología de la DKD desde las perspectivas metabólicas de la siguiente manera: la hiperglucemia crea una demanda de energía para la reabsorción de glucosa en los túbulos proximales renales; por lo tanto, el ciclo de TCA en las mitocondrias se activa a la fuerza para satisfacer la demanda de energía en las primeras etapas de DKD (regulación positiva del metabolismo de ácidos grasos y aminoácidos). Y los estabilizadores de HIF podrían mitigar esta carga mitocondrial mediante la reprogramación metabólica del ciclo TCA a la glucólisis (regulación a la baja del metabolismo de ácidos grasos y aminoácidos y regulación al alza de la glucólisis), lo que podría tener funciones protectoras contra la progresión de la ND. Se necesitan más estudios que incluyan ómica unicelular para aclarar cómo la carga mitocondrial en el tejido renal afecta directamente la fisiopatología de la ND. Otra pregunta interesante es si los estabilizadores de HIF afectan directamente la absorción de glucosa en los túbulos proximales. Nuestros datos in vitro mostraron que el enarodustat reduce significativamente la producción de ATP a través de la reprogramación metabólica del ciclo TCA a la glucólisis (Figuras 1 y 2). Teniendo en cuenta que se requiere ATP para la reabsorción de glucosa por el cotransportador de sodio-glucosa 2, primero planteamos la hipótesis de que el enarodustat podría inactivar la reabsorción de glucosa. Sin embargo, los niveles de glucosa en orina no fueron significativamente diferentes entre el grupo B y el grupo C en ambos modelos animales (Figura complementaria S6). Probablemente, la reducción en la producción de ATP por enarodustat es mucho más leve en una situación fisiológica en comparación con su efecto in vitro; por lo tanto, la estabilización de HIF no afecta la absorción de glucosa a través del cotransportador de sodio-glucosa 2, al menos en nuestros experimentos con animales. Nuestro estudio tuvo 2 limitaciones. Primero, utilizamos ratas diabéticas inducidas por STZ y ratones diabéticos inducidos por aloxano como modelos de DKD en etapa temprana y observamos los efectos a corto plazo de las condiciones diabéticas. Sin embargo, en el entorno clínico, los estabilizadores de HIF se administrarían a pacientes con anemia en etapa avanzada de DKD. Se necesitan más estudios para comprender el efecto de la estabilización de HIF sobre las alteraciones del metabolismo renal en la etapa tardía de la ND. En segundo lugar, el estudio carecía de poder estadístico suficiente con respecto a la dispersión de las concentraciones de metabolitos en los datos del metaboloma, mientras que los datos del transcriptoma tenían un poder estadístico lo suficientemente grande como para aclarar la imagen completa del metabolismo energético. Debido a que no muchos metabolitos mostraron una diferencia significativa entre los grupos, realizamos PLS-DA y seleccionamos los metabolitos con una puntuación VIP de PLS-DA mayor o igual a 1 para MSEA. Aunque es difícil realizar una verificación cruzada de un cambio metabólico usando solo datos de metabolómica, los resultados del análisis del metaboloma fueron compatibles con los datos transcriptómicos (Figuras 7 y 8), lo que brinda apoyo adicional para los efectos observados de las alteraciones del transcriptoma en el metabolismo energético renal. En conclusión, enarodustat (JTZ-951), un estabilizador oral de HIF, contrarresta las alteraciones del metabolismo energético renal en las primeras etapas de la ND. Nuestro estudio sugiere que la estabilización de HIF puede servir como una intervención potencial que se dirige al metabolismo energético renal desregulado en DKD.

MÉTODOS
Prueba de estrés Mito y ensayo de tasa glucolítica
Se sembraron células HK-2 en una microplaca de 96-pocillos a una densidad de 1 * 104células/pocillo. Al día siguiente, el flujo metabólico se midió en tiempo real con el analizador Seahorse XFe96 (Agilent) utilizando el kit de prueba de estrés Mito (103015-100; Agilent) o el kit de ensayo de índice glicolítico (103344- 100; Agilent). Las concentraciones de glucosa, piruvato y glutamina en los medios de cultivo fueron de 10 mmol/l, 1 mmol/l y 2 mmol/l, respectivamente.
transfección de ARNip
La eliminación de HIF-1 fue realizada por Stealth RNAi para HIF1A humano (HSS104774 [n.º 1] y HSS104775 [n.º 2]; Thermo Fisher Scientific, Waltham, MA). Stealth RNAi siRNA Negative Control Med GC Duplex #2 (12935112; Thermo Fisher Scientific) se utilizó como control negativo.
transferencia occidental
Los anticuerpos primarios utilizados para la tinción fueron el anticuerpo anti-HIF humano-1 (policlonal de conejo, 1:500; Novus Biologicals, Littleton, CO) y el anticuerpo anti-actina humana (policlonal de conejo, 1:1000; Sigma-Aldrich, St. . Louis, MO). Un anticuerpo secundario fue el anticuerpo IgG anti-conejo de cabra conjugado con peroxidasa de rábano picante (170-6515, 1:5000; Bio-Rad Laboratories, Hercules, CA).
experimentos con animales
Se obtuvieron ratas Crl: CD (Sprague Dawley) y ratones Crl: CD1 (Instituto de Investigación del Cáncer) de Charles River Laboratories Japan Inc. (Yokohama, Japón). Todos los experimentos fueron aprobados por la Junta de Revisión Institucional de la Universidad de Tokio (número de aprobación P17-110). Todos los procedimientos con animales se realizaron de acuerdo con las pautas de los Institutos Nacionales de Salud (Guía para el cuidado y uso de animales de laboratorio). Los protocolos de estudio se muestran en las Figuras 3 y 9.
Análisis transcriptómico
El ARN total del tejido de la corteza renal se aisló utilizando el kit de minipreparación de ARN total de mamíferos GenElute (RTN7{{10}}; Sigma-Aldrich). El ARN total (100 ng) se marcó con el kit de etiquetado de amplificador rápido de entrada baja (Agilent) y luego se hibridó con SurePrint G3 Rat GE v2 8x60K Microarray (para la rata; Agilent) y SurePrint G3 Mouse GE v{{7 }}x60K Microarray (para ratón), respectivamente. Todos los experimentos de micromatrices fueron realizados por DNA Chip Research Inc. (Tokio, Japón). Los datos sin procesar se procesaron con el paquete R limma en Bioconductor (http://www.bioconductor.org/) para realizar la corrección de fondo y la normalización de datos mediante el método de normalización de cuantiles. Los efectos por lotes fueron eliminados por ComBat (Bioconductor) en el experimento con ratas. Los genes expresados diferencialmente se determinaron mediante │log2 FC│ Mayor o igual a 0,5 y valor Q < 0,05.="" los="" análisis="" de="" ontología="" génica="" y="" vía="" canónica="" se="" realizaron="" utilizando="" basespace="" correlation="" engine="" (illumina,="" san="" diego,="" ca).="" los="" datos="" de="" micromatrices="" se="" han="" depositado="" en="" el="" ómnibus="" de="" expresión="" génica="" del="" centro="" nacional="" de="" información="" biotecnológica="" como="" serie="" gse131221="" (rata)="" y="" gse139317="">
Análisis de enriquecimiento de conjuntos de genes
GSEA es un método computacional que determina si un conjunto de genes definido a priori muestra diferencias estadísticamente significativas y concordantes entre 2 estados biológicos. GSEA se realizó utilizando GSEA v.3.0 (Broad Institute, Cambridge, MA). Las vías con una tasa de descubrimiento falso < 0.25="" se="" consideraron="">

Análisis del metaboloma
Las mediciones de metaboloma fueron realizadas por Human Metabolome Technologies Inc. (Tsuruoka, Japón). Las concentraciones de metabolitos se calcularon mediante la normalización del área del pico de cada metabolito con respecto al área del estándar interno y mediante el uso de curvas estándar, que se obtuvieron a partir de calibraciones de 3-puntos. Consulte también los métodos complementarios.
Análisis de enriquecimiento de conjuntos de metabolitos
El análisis de los datos de metabolómica se realizó utilizando la plataforma web integrada MetaboAnalyst 4.0. Se realizó PLS-DA y se calcularon las puntuaciones VIP asociadas. Los metabolitos con puntaje VIP de PLS-DA mayor o igual a 1 se usaron para el MSEA.
Cuantificación de áreas glomerulares en patologías renales
Tomamos aleatoriamente 3 fotografías patológicas de la imagen de tinción de Schiff con ácido peryódico de cada muestra y medimos cada área glomerular respectivamente usando Fiji (una distribución de ImageJ; Institutos Nacionales de Salud, Bethesda, MD).
CUBIC-riñón
Se realizaron imágenes 3-dimensionales completas de los glomérulos en el tejido renal utilizando CUBIC de acuerdo con nuestros artículos anteriores. En resumen, los riñones de ratón fijados se sumergieron en CUBIC-L para la eliminación de lípidos y luego se sometieron a tinción inmunofluorescente. Finalmente, el índice de refracción fue igualado por la colocación de las muestras en CUBIC-R plus. Se adquirieron imágenes tridimensionales integrales de riñones transparentes con microscopía de fluorescencia de hoja de luz hecha a la medida (MVX10-LS; Olympus, Tokio, Japón). El anticuerpo principal utilizado para la tinción fue el anticuerpo anti-podocina (policlonal de conejo, 1:100, P0372; Sigma-Aldrich). El anticuerpo secundario era Alexa Flour 555- IgG anti-conejo de burro conjugado (1:100, A-31572; Invitrogen, Thermo Fisher Scientific).
análisis estadístico
Para las comparaciones múltiples, se aplicó el análisis de varianza {{0}}way seguido de las pruebas post hoc de comparaciones múltiples de Tukey, si correspondía. Todos los análisis estadísticos se realizaron con el software GraphPad Prism 7 (GraphPad Software, San Diego, CA). P < 0,05="" se="" consideró="" estadísticamente="" significativo.="" los="" datos="" se="" presentan="" como="" la="" media="" ±="">
DIVULGACIÓN
MN ha recibido honorarios, honorarios por asesoramiento o financiación para investigación de KyowaHakko-Kirin, Akebia, Astellas, Chugai, GlaxoSmithKline, Japan Tobacco Inc. (JT), Torii, Tanabe-Mitsubishi, Daiichi-Sankyo, Takeda, Ono, Bayer, Boehringer Ingelheim y Alexión. TT ha recibido una beca de investigación de JT. Enarodustat (JTZ-951) fue proporcionado por JT, Tokio, Japón. EAS y HRU son coinventores de patentes propiedad de RIKEN. Parte de este estudio se realizó en colaboración con Olympus Corporation y un tipo de software respaldado por Bitplane. El otro autor declaró que no había intereses contrapuestos.
EXPRESIONES DE GRATITUD
Agradecemos al Dr. Shuhei Yao y al Dr. Shinji Tanaka por sus valiosos debates. También agradecemos al Dr. Tsuyoshi Inoue, al Dr. Satoru Fukuda y a la Sra. Kahoru Amitani por su apoyo técnico. Este trabajo se llevó a cabo parcialmente con el apoyo del Centro de Ciencias de Isótopos de la Universidad de Tokio. Este trabajo fue apoyado por Grant-in-Aid for Japan Society for the Promotion of Science (JSPS) Research Fellow (JSPS KAKENHI grant 19J11928 to SH), Grant-in-Aid for Scientific Research (B) (JSPS KAKENHI grant 18H02824 to MN ), subvención para la investigación científica (C) (subvención JSPS KAKENHI 17K09688 a TT) y subvención para la investigación científica en áreas innovadoras (subvención KAKENHI 26111003 a MN).

