La 'otra' gran complicación: cómo la enfermedad renal crónica influye en los riesgos y los resultados del cáncer Ⅱ
Jan 25, 2024
Factores de enfermedad
Condiciones genéticas.
La enfermedad de Von Hippel-Lindau (VHL) es una enfermedad genética rara con un patrón de herencia autosómico dominante, caracterizada por mutaciones en el gen supresor de tumores VHL. Esto lleva atumor anormaly crecimiento de quistes que pueden ser benignos y/o malignos y, en particular, aumentan el riesgo de carcinoma de células renales de células claras. La resección del carcinoma de células renales (recurrente) en la enfermedad de VHL a menudo conduce aERC progresivay/o enfermedad renal terminal que requieraterapia de reemplazo renal.
La esclerosis tuberosa es otra afección rara, autosómica dominante, causada por mutaciones inactivadoras encomplejo de esclerosis tuberosa(TSC) genes supresores de tumores TSC1 o TSC2 [31].Angiomiolipomas renalesse desarrollan en la mayoría de los pacientes con esclerosis tuberosa. Una proporción menor de pacientes desarrollará una gran cantidad de quistes renales y, más raramente, carcinoma de células renales. En última instancia, cualquiera de estos crecimientos anormales puede provocar insuficiencia renal.
La hematopoyesis clonal es un fenómeno relacionado con la edad caracterizado por mutaciones somáticas en las células madre hematopoyéticas que conducen a la expansión clonal de leucocitos mutantes. Las personas con evidencia de hematopoyesis clonal tienen un riesgo sustancialmente mayor de cáncer hematológico [32] (junto con enfermedades cardiovasculares y muerte prematura). Más recientemente, la hematopoyesis clonal mieloide se asocia causalmente con ladesarrollo de ERC(definido por efectos) [33] y aumenta el riesgo de resultados adversos (enfermedad cardiovascular, insuficiencia renal, ycánceres mieloides) en personas con ERC [33].
Lesión renal aguda, cualcausa ERCy es más común enERC preexistente, puede promover el desarrollo del carcinoma papilar de células renales al estimular el daño del ADN y los procesos de reparación, desencadenando la proliferación de células progenitoras renales y la mitosis aberrante y, por lo tanto, impulsando la tumorigénesis [34].

HAGA CLIC AQUÍ PARA OBTENER EXTRACTO DE CISTANCHE ORGÁNICO NATURAL CON 25% DE EQUINACOSIDO Y 9% DE ACTEÓSIDO PARA LA FUNCIÓN RENAL
Trastornos inflamatorios e inmunológicos.
El trastorno glomerular más notorio es la glomerulonefritis membranosa, en la que entre el 5 y el 20% de los pacientes tienen cáncer. Sin embargo, se han descrito varias otras glomerulonefritis en asociación con neoplasias malignas de órganos sólidos, más comúnmente enfermedad de cambios mínimos y glomerulonefritis mesangial-proliferativa, pero también incluyen nefropatía por inmunoglobulina A, glomeruloesclerosis focal y segmentaria, glomerulonefritis en media luna, incluida la enfermedad antimembrana basal glomerular (GBM). y vasculitis asociadas con anticuerpos anticitoplasma de neutrófilos (ANCA) y microangiopatías trombóticas [35].
La ERC, la albuminuria y el cáncer se asocian con inflamación. La cistatina C se expresa de forma ubicua y se filtra libremente en el glomérulo, funcionando como marcador de filtración glomerular. Como la cistatina C no se ve afectada por la edad, el sexo y la masa muscular, puede ser un marcador más sensible de cambios tempranos en la función renal en comparación con la creatinina sérica. Sin embargo, la cistatina C también puede estar elevada en estados inflamatorios, incluidos algunos cánceres. La cistatina C es un importante inhibidor endógeno de las enzimas reguladoras implicadas en la tumorigénesis, incluidas las cisteína proteasas y el factor de crecimiento tisular (TGF-), pero se ha implicado como promotor [36] y como supresor [37, 38] de la progresión de la enfermedad. en ciertos subtipos de cáncer. No está claro hasta qué punto la cistatina C como marcador tanto de inflamación como de filtración glomerular se confunde con la presencia de cáncer. Hasta donde sabemos, ningún estudio ha investigado esto específicamente. Una discusión adicional sobre este tema está más allá del alcance de esta revisión, pero esto puede explicar parcialmente las asociaciones más fuertes observadas entre eGFRcys y el riesgo de cáncer específico del sitio.
Infecciones. Las infecciones, y en particular los virus, pueden causar directamente cáncer y enfermedad renal, incluido el virus de Epstein-Barr, el citomegalovirus, el virus del papiloma humano, el virus linfotrópico de células T humanas y la hepatitis B y C. El virus de la inmunodeficiencia humana puede causar cáncer y enfermedad renal por sí solo. o exacerbar el efecto cancerígeno de la coinfección con otros virus. Esto explica en parte el aumento sustancial del riesgo de cáncer, donde los efectos de la inmunosupresión parecen aumentar el riesgo de cáncer asociado con la infección, y el riesgo de cáncer incidente puede atenuarse mediante la retirada de la inmunosupresión [39].
Sesgo de detección. Es posible que se notifique con mayor frecuencia una mayor incidencia de algunos cánceres relacionados con el riñón, como el de próstata y algunos cánceres hematológicos, entre las personas con ERC. Los pacientes con ERC que reciben atención especializada tienen interacciones más frecuentes con proveedores de atención médica donde se realizan pruebas de "detección" con orina para detectar hematuria mediante tira reactiva de orina, análisis de sangre para detectar discrasias de células plasmáticas y/o investigación de síntomas urinarios como parte del estudio clínico de rutina. Alternativamente, la enfermedad renal se puede detectar mientras se realiza una investigación para un diagnóstico de cáncer no relacionado.
Reforzando la preocupación sobre el sesgo de detección y/o la causalidad inversa, un estudio informa una disipación del riesgo asociado con la ERC y subtipos de cáncer específicos, incluidos los cánceres de próstata y hematológicos, después de un período de observación de 12 meses [7]. Sin embargo, análisis históricos en otras poblaciones no han mostrado una atenuación significativa de la asociación entre la TFGe [16] o la albuminuria [16, 19] y el riesgo de cáncer, lo que sugiere que puede haber una asociación genuina más allá de la capacidad de detectar el cáncer presintomático.

Factores de tratamiento
Los tratamientos para enfermedades renales pueden causar cáncer.
Las opciones médicas utilizadas en el tratamiento de la ERC y afecciones asociadas pueden provocar el desarrollo de cáncer. El ejemplo obvio es la ciclofosfamida, utilizada en el tratamiento de la glomerulonefritis (como la nefropatía membranosa) y los trastornos hematológicos (incluidos el linfoma y el mieloma), que se asocia con el desarrollo de enfermedades malignas, en particular cáncer de vejiga. Los agentes estimulantes de la eritropoyesis, utilizados en el tratamiento de la anemia renal, pueden exacerbar los cánceres preexistentes [40]. La inmunosupresión para la glomerulonefritis inflamatoria o inmune, o después de un trasplante de riñón, aumenta el riesgo de ciertos cánceres, en particular, entre otros, los provocados por infecciones (especialmente virus) [41].
Los tratamientos contra el cáncer pueden causar enfermedad renal. El fármaco de quimioterapia original a base de platino, el cisplatino, se introdujo en la década de 1970 y fue un tratamiento muy eficaz contra varias neoplasias malignas de órganos sólidos, incluidos los cánceres de testículo, ovario, pulmón, cuello uterino y vejiga. Sin embargo, en realidad se excreta y es altamente nefrotóxico, provocando una disminución de la filtración glomerular (de forma dosis dependiente) a las pocas horas de su administración [42]. La hidratación intravenosa puede mitigar el riesgo de nefrotoxicidad inducida por cisplatino y ahora se considera un cotratamiento esencial, pero el cisplatino se evita de manera rutinaria en pacientes con ERC preexistente (estadios G3 a G5). En comparación, el carboplatino presenta una nefrotoxicidad muy baja y puede seleccionarse como tratamiento alternativo en personas con ERC moderada.
Muchos antimetabolitos, utilizados en el tratamiento de diversos tipos de cáncer, se excretan realmente, al menos en parte. En dosis más altas, el metotrexato puede asociarse con precipitación intratubular, lo que produce lesión renal aguda y disminución de la TFG [43]. Generalmente se recomiendan reducciones de dosis en personas con ERC preexistente G3-G5 o en diálisis. Pequeños estudios sugieren que puede haber una nefrotoxicidad similar, dependiente de la dosis, asociada con la terapia con pemetrexed (utilizado en el tratamiento del cáncer de pulmón), particularmente cuando los pacientes reciben un tratamiento prolongado de 10 ciclos o más [44].
El agente alquilante ifosfamida es sustancialmente más nefrotóxico que su primo, la ciclofosfamida, aunque la evidencia de esto proviene principalmente de la literatura pediátrica. La ifosfamida normalmente causa disfunción tubular o, en algunos casos, puede provocar una reducción (generalmente leve) de la TFG [45], aunque los efectos a largo plazo son inciertos. El riesgo de efectos secundarios renales aumenta con dosis más altas y exposición acumulativa, coadministración con cisplatino y en pacientes con enfermedad renal preexistente.
Los avances más recientes en el tratamiento han sido posibles gracias a una mejor comprensión de la biología del cáncer y su microentorno inmunológico, lo que ha llevado a nuevas terapias basadas en el sistema inmunológico con mejoras notables en los resultados de los pacientes [46, 47]. El uso de estos nuevos agentes inmunitarios continúa creciendo, y se utilizan cada vez en etapas más tempranas de la enfermedad [48]. En consecuencia, seguiremos siendo testigos de un cambio de los agentes quimioterapéuticos citotóxicos tradicionales a terapias dirigidas e inmunoterapias. Con este entorno cambiante de la terapia contra el cáncer, el espectro de efectos secundarios adversos seguirá diversificándose. Este puede ser el caso, especialmente cuando estos nuevos agentes anticancerígenos se utilizan en combinación con quimioterapias convencionales.
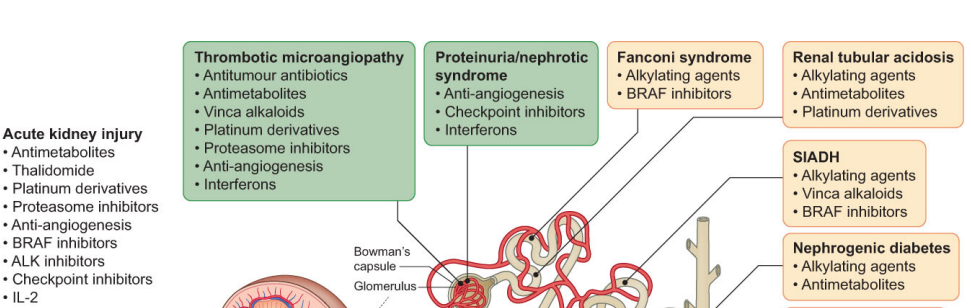
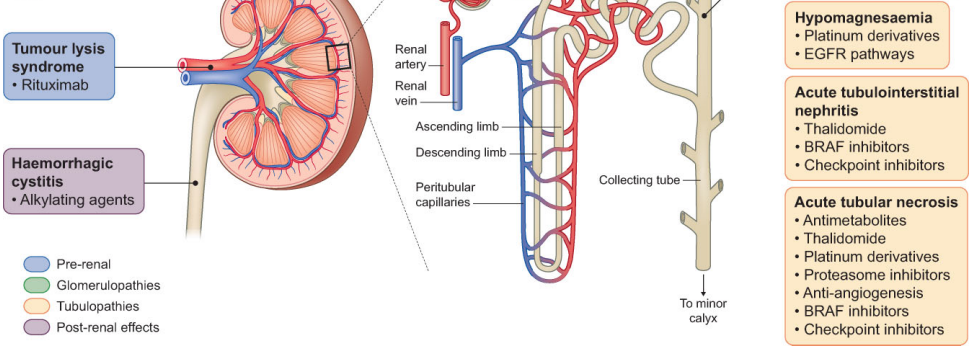
El uso de terapias sistémicas contra el cáncer (SACT) que en realidad no se excretan (por ejemplo, inhibidores de puntos de control inmunitarios; ICI) no previene por completo los efectos secundarios renales no deseados [49]. SACT puede afectar cualquier segmento de la nefrona y provocar manifestaciones clínicas que incluyen proteinuria, hipertensión, alteraciones electrolíticas, glomerulopatía, nefritis intersticial aguda o crónica y episodios repetidos de lesión tubular aguda que provocan ERC [50]. Además, los pacientes, incluso con ERC leve, pueden tener una excreción y metabolismo reducidos de SACT, lo que potencia el riesgo de toxicidad sistémica, incluso cuando el fármaco se excreta mínimamente [51]. Esto potencialmente limita la dosis o la duración de SACT que se puede administrar a pacientes con ERC. Por lo tanto, sigue siendo importante ser consciente de los posibles efectos secundarios de los agentes oncológicos para intentar identificar a los pacientes con mayor riesgo y permitir la prevención o el tratamiento temprano de la lesión renal para evitar un deterioro funcional grave y permanente. Si ya se ha establecido una lesión grave, es primordial brindar el apoyo adecuado para mejorar la atención a esta población con cáncer. En la Figura 2 se ilustra un resumen de los efectos secundarios renales del SACT común.
El uso de terapias sistémicas contra el cáncer (SACT) que en realidad no se excretan (por ejemplo, inhibidores de puntos de control inmunitarios; ICI) no previene por completo los efectos secundarios renales no deseados [49]. SACT puede afectar cualquier segmento de la nefrona y provocar manifestaciones clínicas que incluyen proteinuria, hipertensión, alteraciones electrolíticas, glomerulopatía, nefritis intersticial aguda o crónica y episodios repetidos de lesión tubular aguda que provocan ERC [50]. Además, los pacientes, incluso con ERC leve, pueden tener una excreción y metabolismo reducidos de SACT, lo que potencia el riesgo de toxicidad sistémica, incluso cuando el fármaco se excreta mínimamente [51]. Esto potencialmente limita la dosis o la duración de SACT que se puede administrar a pacientes con ERC. Por lo tanto, sigue siendo importante ser consciente de los posibles efectos secundarios de los agentes oncológicos para intentar identificar a los pacientes con mayor riesgo y permitir la prevención o el tratamiento temprano de la lesión renal para evitar un deterioro funcional grave y permanente. Si ya se ha establecido una lesión grave, es primordial brindar el apoyo adecuado para mejorar la atención a esta población con cáncer. En la Figura 2 se ilustra un resumen de los efectos secundarios renales del SACT común.
Alrededor de un tercio de los cánceres malignos se tratan con SACT, aunque la evidencia de ensayos sobre el uso de fármacos específicos en personas con ERC suele ser escasa. En una búsqueda dirigida, Kitchlu et al. [54] evaluaron ensayos controlados aleatorios realizados en los cinco cánceres de órganos sólidos más comunes (vejiga, mama, colorrectal, pulmón y próstata) de una selección de seis revistas médicas y de oncología de alto impacto desde 2012 hasta 2017 inclusive. De los 310 ensayos (292 889 pacientes) identificados, el 85 % excluyó específicamente a los pacientes con marcadores de ERC. Los criterios de exclusión variaron, pero incluyeron creatinina sérica elevada por encima de los límites normales (49% de los ensayos), aclaramiento de creatinina reducido (umbral más alto<60 mL/min; 44%), reduced eGFR (highest threshold <60 mL/min/1.73 m2; 5%), proteinuria (12% of trials), unspecified CKD (16% of trials)and/or multiple exclusion criteria for CKD (34% of trials). This report did not comment on the number of potential participants who were screened and then excluded from clinical cancer trials based on CKD. Acknowledging that as many as half of patients with cancer may have evidence of CKD at diagnosis [17], it is likely that participants in clinical cancer trials are not representative of the patients who require treatment for cancer in the 'real world'. Furthermore, the majority of SACT is licensed without safety information in patients with moderate-to-severe CKD, and almost none report safety information in patients on dialysis [51].

Dificultades de dosificación.
La estimación precisa de la TFG en personas con cáncer es esencial para garantizar la dosificación óptima de las quimioterapias citotóxicas tradicionales y las SACT más nuevas. Existen algunas preocupaciones sobre el uso de eGFR entre personas a las que se les ha diagnosticado cáncer, particularmente en lo que respecta a la dosificación de los medicamentos. Las consecuencias de una estimación inexacta de la TFG incluyen la exposición de algunos pacientes a una mayor toxicidad de los medicamentos, mientras que a otros pacientes se les pueden negar tratamientos (o dosis adecuadas de tratamientos) que son seguros.
El cisplatino se evita habitualmente en personas con eGFR<60 mL/min/1.73 m2. Although carboplatin is better tolerated and can be used in people with moderate CKD, it is purely really excreted, and dosing decisions are based on eGFR at the time of administration (using Calvert's formula). In people with cancer, GFR is generally overestimated by Cockcroft and Gault creatinine clearance and the CKD Epidemiology Collaboration, whereas GFR is generally underestimated by MDRD (although body surface area adjustment may improve accuracy) [55]. Compared with measured GFR, CamGFR- a model developed and validated in patients with cancer- is more accurate than other published creatinine-based models and improves the precision of carboplatin dosing to within clinically acceptable limits [56].
Se necesita más evidencia para respaldar las decisiones de dosificación y asesorar sobre la eficacia del tratamiento y la toxicidad de SACT en pacientes con ERC preexistente. Además, se pueden recomendar medidas de eGFR diferentes para las decisiones de dosificación de medicamentos que para el seguimiento de la ERC o la evaluación del riesgo de cáncer.

PREDICCIÓN DEL RIESGO DE CÁNCER
En cuanto a las enfermedades cardiovasculares, se han desarrollado y validado una variedad de herramientas de predicción de riesgos para ayudar en la predicción del cáncer tanto en presencia de escenarios clínicos sugerentes como en individuos asintomáticos [57].
Las herramientas de evaluación de riesgos se diseñaron para 15 subtipos de cáncer y muestran rangos de valor predictivo positivo (VPP) basados en los síntomas del paciente. Las pautas del Instituto Nacional para la Excelencia en la Salud y la Atención (NICE) recomiendan la derivación para una investigación adicional con un VPP del 3% o superior. La herramienta de evaluación del riesgo de cáncer de vejiga incorpora "creatinina sérica elevada"; sin embargo, a pesar de los repetidos estudios que muestran una asociación entre la TFGe, la albuminuria y/o un diagnóstico categórico de ERC, las medidas de la función renal no se incorporan en las herramientas de evaluación de riesgos de pulmón, riñón, linfoma de Hodgkin y mieloma múltiple. Además, no se consideró la inclusión de medidas de función renal en QCancer, diseñado para estimar el riesgo de cáncer no diagnosticado en todos los subtipos, en función de los factores de riesgo existentes y/o los síntomas actuales en hombres [58] y mujeres [59].
Hemos ilustrado que la eGFRcr se asocia de manera inconsistente con el riesgo de cáncer en general, mientras que la eGFRcys puede estar más estrechamente asociada con el riesgo de cáncer. A diferencia de la creatinina sérica, la cistatina C no está influenciada por la edad, el sexo, la masa muscular o el origen étnico, y demuestra una relación lineal negativa con el riesgo cardiovascular [13, 14] y de cáncer [16] por debajo de 90 ml/min/1,73 m2. Por el contrario, la TFGe no se asocia con un mayor riesgo cardiovascular o de cáncer hasta que la TFGe cae por debajo de ~75 ml/min/1,73 m2 y tiene una relación en forma de U con el riesgo de enfermedad cardiovascular y cáncer [7, 13, 16].
Al incorporar medidas más sensibles del riesgo de cáncer relevantes para la ERC, como la eGFRcys y la albuminuria, en las herramientas de predicción del riesgo de cáncer, el VPP de los síntomas de presentación en el contexto de la ERC puede elevarse por encima del umbral para una mayor investigación, fomentando la derivación, el diagnóstico y la atención más tempranos. tratamiento. La utilidad de la detección no dirigida del cáncer en personas con enfermedades crónicas (incluida la ERC) es controvertida, debido a las incertidumbres en torno a la rentabilidad, la precisión y la seguridad, particularmente en un grupo con mayor riesgo de sufrir enfermedades no cancerosas y muerte. Sin embargo, se podrían desarrollar herramientas de predicción del riesgo de cáncer específicamente para personas con ERC para capturar el perfil de riesgo elevado observado en algunos, pero no en todos, los subtipos de cáncer. Estas herramientas pueden permitir entonces realizar pruebas de detección dirigidas a aquellas personas con mayor riesgo de padecer cánceres específicos.

RELEVANCIA Y TRABAJO FUTURO
Resumimos la relevancia para el nefrólogo de la relación entre la ERC y el cáncer en la Tabla 1. Hemos hecho algunas sugerencias para trabajos futuros para avanzar en nuestra comprensión deincidencia de cáncer, tratamiento y resultados enpersonas con ERCen la Tabla 2.
CONCLUSIONES
La incidencia y la mortalidad por cáncer son mayores, aunque específicas del sitio, en personas con ERC. Este riesgo no se reconoce lo suficiente: los marcadores de función renal como la TFGe y la albuminuria no se reconocen en las calculadoras de riesgo de cáncer (por ejemplo, herramientas de evaluación de tasas y QCancer). El riesgo de cáncer no se detecta de manera consistente hasta que la ERC está más avanzada, quizás confundido por el hecho de que una eGFRcr más baja y el cáncer se observan con mayor frecuencia en personas mayores. Marcadores lineales y más sensibles de filtración glomerular como la cistatina C detectan una asociación con un mayor riesgo de incidencia y mortalidad por cáncer en una etapa más temprana. Un uso más generalizado de eGFRcys puede mejorar la estratificación del riesgo; sin embargo, existen datos contradictorios sobre su precisión en comparación con la función renal medida en pacientes diagnosticados con cáncer, y es posible que se requieran métodos alternativos para la dosificación de medicamentos basados en eGFR. La mayor incidencia y muerte asociadas con el cáncer en la ERC probablemente esté relacionada con una combinación de factores del paciente, la enfermedad y el tratamiento. Una comprensión más clara de los mecanismos ayudará a diseñar estrategias para reducir el riesgo de cáncer entre las personas con ERC.

DECLARACION DE CONFLICTO DE INTERES
Fuera de los trabajos presentados, JSL informa honorarios personales de Pfizer, AstraZeneca y Bristol-Myers Squibb; PBM informa honorarios personales y/o apoyo no financiero de Vifor, Napp, Pharmacosmos, AstraZeneca, Astellas y Novartis, y subvenciones de Boehringer Ingelheim; NNL informa honorarios personales y apoyo no financiero de Roche, Pfizer, Novartis, AstraZeneca, Pharmacosmos y Vifor Pharma, y subvenciones de Roche Diagnostics, AstraZeneca y Boehringer (todos pagados a la Universidad de Glasgow, su institución empleadora). RJJ informa apoyo a la investigación de Clovis, Astellas, Exelixis, AstraZeneca y Roche, y honorarios de Clovis, Astellas, AstraZeneca, Roche, Ipsen, Bristol-Myers Squibb, Pfizer, Merck Serono, Merck Sharp Dohme, Janssen, Bayer y Novartis.
REFERENCIAS
1. Tu H, Wen CP, Tsai SPet al.Riesgo de cáncer asociado con enfermedades crónicas y marcadores de enfermedades: estudio de cohorte prospectivo.BMJ2018; 360:k134. doi: 10.1136/bmj.k134
2. Weng PH, Hung KY, Huang HLet al.Mortalidad específica del cáncer en la enfermedad renal crónica: seguimiento longitudinal de una gran cohorte.Clin J Am Soc Nephrol2011; 6: 1121–1128
3. Lowrance WT, Ordoñez J, Udaltsova Net al.ERC y el riesgo de cáncer incidente.J Am Soc Nephrol2014; 25: 2327–2334
4. Liu L, Zhu M, Meng Qet al.Asociación entre la función renal y el riesgo de cáncer: resultados del Estudio Longitudinal de Salud y Jubilación de China (CHARLS).J Cáncer2020; 11: 6429–6436
5. Mok Y, Matsushita K, Ballew SH,et al.Función renal, proteinuria e incidencia de cáncer: el estudio coreano del corazón.Soy J enfermedad renal2017; 70: 512– 521
6. Ishii T, Fujimaru T, Nakano Eet al.Asociación entre enfermedad renal crónica y mortalidad en cáncer en estadio IV.Int J Clin Oncol2020; 25: 1587– 1595
7. Xu H, Matsushita K, Su Get al.Tasa de filtración glomerular estimada y riesgo de cáncer.Clin J Am Soc Nephrol2019; 14: 530–539
8. Iff S, Craig JC, Turner Ret al.Reducción de la TFG estimada y de la mortalidad por cáncer.Soy J enfermedad renal2014; 63: 23–30
9. Park S, Lee S, Kim Yet al.Riesgo de cáncer en la enfermedad renal crónica previa a la diálisis: un estudio poblacional a nivel nacional con un grupo de control emparejado.Clínica de Res. Renal2019; 38: 60–70
10. Wong G, Staplin N, Emberson Jet al.Enfermedad renal crónica y riesgo de cáncer: un metanálisis de datos de pacientes individuales de 32.057 participantes de seis estudios prospectivos.Cáncer de BMC2016; 16: 488
11. Christensson A, Savage C, Sjoberg DDet al.Asociación de cáncer con función renal moderadamente deteriorada al inicio del estudio en un estudio grande, representativo,Cohorte poblacional seguida durante hasta 30 años.Cáncer Internacional J2013; 133: 1452–1458







