Las cepas probióticas viables y muertas por calor mejoran la inmunidad oral al elevar la concentración de IgA en la mucosa oral
Sep 11, 2023
Abstracto
La inmunidad de la mucosa oral-nasal juega un papel crucial en la protección del cuerpo contra la invasión bacteriana y viral. Se han utilizado productos probióticos seguros para mejorar la inmunidad humana y la salud bucal. En este estudio, verificamos los efectos beneficiosos de las tabletas mixtas de probióticos viables, que consisten en Lactobacillus salivarius subsp. salicinius AP-32, Bifdobacterium animalis subsp. lactis CP-9 y Lactobacillus paracasei ET-66, y tabletas de probióticos inactivados por calor, que consisten en L. salivarius subsp. salicinius AP-32 y L. paracasei ET-66, sobre la inmunidad oral entre 45 participantes sanos. Los participantes se dividieron aleatoriamente en grupos de probióticos viables, probióticos muertos por calor y placebo. La administración del tratamiento tuvo una duración de 4 semanas. Se recolectaron muestras de saliva en las semanas 0, 2, 4 y 6, y se midieron las poblaciones de Lactobacillus, Bifidobacterium y Streptococcus mutans y la concentración de IgA. Las concentraciones de IgA y los niveles de TGF-beta e IL-10 en células PBMC se cuantificaron mediante el método ELISA. Los resultados mostraron que los niveles de IgA salival aumentaron significativamente con la administración tanto de los viables (119,30 ± 12,63 %, ***P<0.001) and heat-killed (116.78±12.28%, ***P<0.001) probiotics for 4 weeks. Among three probiotic strains, AP-32 would effectively increase the levels of TGF-beta and IL-10 in PBMCs. The oral pathogen Streptococcus mutans was significantly reduced on viable probiotic tablet administration (49.60±31.01%, ***P<0.001). The in vitro antibacterial test confirmed that viable probiotics effectively limited the survival rate of oral pathogens. Thus, this clinical pilot study demonstrated that oral probiotic tablets both in viable form or heat-killed form could exert beneficial effects on oral immunity via IL-10, TGB-beta mediated IgA secretion. The effective dosage of viable probiotic content in the oral tablet was 109 CFUs/g and the heat-killed oral tablet was 1× 1010 cells/g.

Beneficios del suplemento cistanche: aumentar la inmunidad.
Introducción
La mucosa oral-nasal, la puerta de entrada para contactar con los antígenos inhalados, es la primera línea de defensa del sistema inmunológico humano [1, 2]. Por lo general, los virus o bacterias patógenos invaden las superficies mucosas de la cavidad buconasal luchando contra el sistema inmunológico local y la microbiota sana [3]. La inflamación y los síntomas, como tos, dolor de garganta, secreción nasal y fiebre, se desarrollan debido a las respuestas inmunitarias contra virus y bacterias patógenos invasivos [4]. Además, la inmunoglobulina A (IgA) es el principal factor inmunológico de la saliva y regula la homeostasis de la microbiota oral [5]. Varios estudios han informado sobre la capacidad de la IgA secretora para proteger al cuerpo de infecciones por patógenos virales, incluidos el virus respiratorio sincitial [6], el rotavirus [7] y el virus de la influenza [7]. La IgA secretora actúa protegiendo los epitelios mucosos. Nicolás Millet et al. Descubrieron que la IgA mucosa puede prevenir la disbiosis comensal de Candida albicans en la cavidad bucal [8]. También previene la agregación del patógeno oral Streptococcus mutans, que causa la placa dental [9].
Además, los investigadores descubrieron que la microbiota oral y sus metabolitos pueden influir localmente en la inmunidad de la barrera oral [10]. Estudios anteriores demostraron la eficacia de los probióticos para elevar la concentración de IgA en la mucosa oral [11]. Ericson et al. demostraron que el chicle que contenía Lactobacillus reuteri participaba en la respuesta inmune adaptativa de sujetos sanos al aumentar los niveles de IgA salival [12]. En humanos, las citoquinas inmunes TGF-beta e IL-10 están correlacionadas con la producción de IgA [13].
Sin embargo, aún no está claro si la microbiota oral elevó los niveles secretores de IgA a través de las citocinas TGF-beta e IL-10. Además, los patógenos orales incluyen S. mutans, P. gingivalis y F. nucleatum subsp. El polimorfismo y A. actinomycetemcomitans mostraron una alta correlación con la enfermedad periodontal y el mal aliento [14]. Los productos probióticos podrían ser una posible terapia alternativa a la periodontitis al inhibir los patógenos orales Fusobacterium nucleatum, pero Porphyromonas gingivalis y Aggregatibacter actinomycetemcomitans no mostraron una disminución significativa [15]. La suplementación con probióticos también puede prevenir infecciones patógenas [16]. Se ha informado que especies clave de la microbiota limitan el crecimiento de Streptococcus pneumoniae patógeno [17]. Por lo tanto, mantener un ecosistema microbiano equilibrado mediante la absorción de cepas probióticas puede ser una forma alternativa de regular la inmunidad bucal y mejorar la salud bucal. Hallazgos anteriores sobre la inhibición de patógenos orales por cepas probióticas han revelado que Lactobacillus salivarius subsp. salicinius AP-32, Bifdobacterium animalis subsp. lactis CP-9 y Lactobacillus paracasei ET-66 ejercen excelentes efectos antibacterianos in vitro; sin embargo, no por el mecanismo de aumento de los niveles de H2O2 [18]. Las principales estrategias de las cepas probióticas para limitar el crecimiento de patógenos orales fueron la coagregación de patógenos por vía oral, la producción de biosurfactantes, el cambio del entorno bucal y la generación de sustancias antimicrobianas [19]. Además, un estudio in vitro demostró que L. salicinius AP-32 mediaba la expresión de citocinas inflamatorias [interleucina (IL)-8, IL-10] en células epiteliales humanas [20]. Por lo tanto, en este estudio, verificamos si las tabletas mixtas de probióticos viables, que consisten en L. salivarius subsp. salicinius AP-32, B. animalis subsp. lactis CP-9 y L. paracasei ET-66, y tabletas de probióticos inactivados por calor, que consisten en L. salivarius subsp. Salicinius AP-32 y L. paracasei ET-66, mejoraron la función inmune a través de TGF-beta, IL-10 o elevaron el nivel de concentración de IgA salival. Se probó la función antibacteriana de la absorción del producto probiótico en la cavidad bucal.

Beneficios del suplemento cistanche: cómo fortalecer el sistema inmunológico
Haga clic aquí para ver los productos Cistanche Enhance Immunity
【Pregunte por más】 Correo electrónico:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
Material y métodos
Participantes
En total, se reclutó a 45 participantes sanos de entre 20 y 40 años y se dividieron aleatoriamente en tres subgrupos: los grupos de tableta oral de probiótico viable, tableta oral de probiótico muerto por calor y grupo de placebo. Cada grupo estuvo formado por 15 participantes. Se excluyeron los participantes con hábitos de fumar y comer nueces de betel. Se asignaron tabletas orales de forma ciega a los participantes. Todos los participantes tomaron las tabletas orales tres veces al día (mañana, mediodía y noche) durante 4 semanas. Se recolectaron muestras de saliva (2 ml) para medir la concentración de IgA y las poblaciones de microorganismos en las semanas 0, 2, 4 y 6. Se obtuvo el consentimiento informado de todos los participantes incluidos en este estudio. El protocolo fue aprobado por la Junta de Revisión Institucional de la Universidad Médica Chung Shan, Taiwán (CS19052).
Tabletas orales probióticas viables
La tableta oral de probióticos viables (1 g) contenía tres cepas de probióticos viables, L. salivarius subsp. salicinius AP-32, B. animalis subsp. lactis CP-9 y L. paracasei ET-66. Mezclamos 0.01 g de 1011 unidades de formación de colonias (UFC) de un solo probiótico en la tableta oral. Cada cepa de probiótico se midió alrededor de 0,33 * 109 UFC/g. El contenido total de probióticos en la tableta oral fue de 109 colonias UFC/g. La dosis activa de la tableta oral probiótica fue la siguiente en trabajos publicados anteriormente [18]. Todas las cepas probióticas se obtuvieron del laboratorio de Biofag Biotech Co., Ltd. (Tainan, Taiwán). L. salivarius subsp. salicinius AP-32 se aisló de un intestino humano sano y se depositó en el Instituto de Investigación y Desarrollo de la Industria Alimentaria de Taiwán (ID: BCRC 910437) y en la Universidad de Wuhan, China (ID: CCTCC-M2011127); B. animalis subsp. Se aisló CP láctico-9 de leche materna humana sana y se depositó en el Instituto de Investigación y Desarrollo de la Industria Alimentaria de Taiwán (ID: BCRC 910645) y en la Universidad de Wuhan (ID: CCTCC-M2014588); L. paracasei ET-66 se aisló de leche materna humana sana y se depositó en el Instituto de Investigación y Desarrollo de la Industria Alimentaria, Taiwán (ID: BCRC 910753) y en el Centro General de Colección de Cultivos Microbiológicos de China, Beijing, China (ID: CGMCC{ {22}}). Lactobacilo. salivarius subsp. salicinius AP-32 y L. paracasei ET-66 se cultivaron en placas de agar de Man, Rogosa y Sharpe (MRS) (110,660, Merck, Darmstadt, Alemania) y se incubaron en condiciones anaeróbicas facultativas a 37 grados. durante 48h. B. animalis subsp. Lactis CP-9 se cultivó en agar MRS suplementado con cisteína al 0,05% y se incubó anaeróbicamente a 37 grados durante 48 h. Se realizó un recuento de colonias para cuantificar las UFC bacterianas después de cultivar cepas probióticas [18].

planta cistanche que aumenta el sistema inmunológico
Tabletas orales probióticas muertas por calor
Las tabletas orales probióticas muertas por calor (1 g) consistían en L. salivarius subsp. salicinius AP-32 y L. paracasei ET-66. Las cepas viables se cultivaron e incubaron, como se describió anteriormente. Luego, AP-32 y ET-66 se inactivaron incubando las cepas viables en medio MRS a 100 grados durante 1 h. El contenido de probióticos en la tableta oral fue de 1 × 1010 células/g. La dosis activa de las tabletas orales probióticas muertas por calor se realizó siguiendo pruebas in vitro publicadas previamente [11]. Todos los procedimientos experimentales se realizaron en el laboratorio de Biofag Biotech Co., Ltd. (Tainan, Taiwán).
Medición de las poblaciones de Lactobacillus y Bifidobacterium en muestras de saliva
Se recolectaron muestras de saliva (2 ml) de cada participante en las semanas 0, 2, 4 y 6. Las muestras de saliva (100 µL) se diluyeron en serie y se agregaron a MRS. platos. Para medir las poblaciones de Lactobacillus, se cultivó Lactobacillus y se incubó en placas de agar MRS en condiciones anaeróbicas facultativas a 37 grados durante 48 h. Para medir las poblaciones de Bifdobacterium, Bifdobacterium se cultivó y se incubó anaeróbicamente en agar MRS suplementado con 0.05 % de cisteína a 37 grados durante 48 h. Se realizó el recuento de colonias para cuantificar las UFC bacterianas después de cultivar cepas probióticas. Las tasas de población de Lactobacillus y Bifidobacterium se normalizaron al número de población de probióticos en la Semana 0. La tasa de población de Lactobacillus y Bifidobacterium recolectada en la Semana 0 se consideró del 100 %. El método experimental siguió trabajos publicados previamente [18].
Medición de la concentración de IgA en la mucosa oral
Se recolectaron muestras de saliva (2 ml) de cada participante en las semanas 0, 2, 4 y 6 y se mantuvieron a 20 grados. Se utilizó el kit ELISA IgA Human Uncoated (n.º de catálogo 88-50600-88; Invitrogen, Thermo Fisher Scientific, San José, CA, EE. UU.) para analizar la concentración de IgA. En primer lugar, cubrimos una placa de pocillos con anticuerpos anti-IgA humana. Se añadió IgA salival presente en la muestra o estándar al micropocillo y luego se añadió anticuerpo anti-IgA humana conjugado con HRP a temperatura ambiente durante 1 h. Pipetear sustrato TMB a cada pocillo durante 30 min. Finalmente, se midió la concertación de IgA en un espectrofotómetro a 450 nm. Todo el procedimiento experimental se realizó por triplicado, según las instrucciones del fabricante. La tasa de concentración de IgA recogida en la semana 0 se consideró del 100 %. El método experimental siguió trabajos publicados previamente [18].

cistanche tubulosa-mejora el sistema inmunológico
Medición de la concentración de TGF-Beta e IL-10 en PBMC
La prueba de la elevación inducida por probióticos de los niveles de TGF-beta e IL-10 después del estudio anterior [20]. Las células mononucleares de sangre periférica (PBMC) se obtuvieron de muestras de sangre de donantes sanos (Tainan Blood Center, Taiwan Blood Services Foundation). Se centrifugó la sangre completa a través de un gradiente de Ficoll-Hypaque (Pharmacia, Suecia) y se eluyó la fracción de densidad ligera de la interfaz del 42,5%-50%. Sembrando 4 * 105 células PBMC extraídas de células en 100 µl de RPMI-1640 con FBS al 1% (Sigma Chemical Co., St. Louis, MO, EE. UU.) en cada pocillo de placas de 96 pocillos. Luego agregue 5 * 105 ufc/20 µl de tratamiento probiótico a cada pocillo sembrado de PBMC (células: cepas probióticas=1:10). Los controles positivos agregaron 10 µg/ml de fitohemaglutinina (PHA) (Sigma-Aldrich, Munich, Alemania) a pocillos sembrados con PBMC para la producción de TGF-, IL-10 respectivamente [21]. Cocultivo de probióticos con PBMC durante 48 h. Medición del sobrenadante que contiene citoquinas IL-10 y TGF- mediante análisis de ensayo inmunoabsorbente ligado a enzimas (ELISA) (Thermo Scientific, Carlsbad, CA, EE. UU.). Todos los experimentos se midieron y siguieron el protocolo comercial al menos por triplicado.
Evaluación de la función antibacteriana en la cavidad bucal.
Streptococcus mutans es una amenaza común para la salud bucal, que causa caries dental al formar peste o biopelícula [22]. Se recogieron muestras de Streptococcus mutans de los hisopos, mediante los cuales recolectamos S. mutans en la parte supragingival, las encías y la mucosa oral, en las semanas 0, 2, 4 y 6. S. mutans se mantuvo en tríptico caldo de soja (TSB, 5 ml) suplementado con 50% de glicerol. El medio de S. mutans se diluyó en serie y se añadió a la placa de agar Mitis Salivarius-Bacitracina (MSBA, 0.2 U/mL), que se incubó a 37 grados durante 2 días. Finalmente, se contó el número de colonias de S. mutans en cada muestra participante para calcular las tasas de supervivencia patógena; la tasa de supervivencia de S. mutans recolectada en la semana 0 se consideró del 100 %. El método experimental siguió trabajos publicados previamente [18].
Actividad antibacteriana in vitro de las tabletas orales
Oral tablets (1 g) that contained viable (AP-32, CP-9, and ET-66; > 109 CFUs) and heat-killed (AP-32 and ET-66,>Se disolvieron 1010 UFC) cepas probióticas en TSB y medio de infusión cerebro-corazón, respectivamente, para obtener una concentración final de 0,1 g/ml. Sólo se utilizó el medio para el grupo blanco, mientras que se disolvieron comprimidos (1 g) sin ningún componente probiótico en los medios respectivos para el grupo placebo. Luego, se introdujeron patógenos orales (106 UFC) en las soluciones de las tabletas y se incubaron conjuntamente a 37 grados durante 2 (S. mutans) o 3 (Porphyromonas gingivalis, Fusobacterium nucleatum subsp. polymorphum y Aggregatibacter actinomy cetemcomitans) d. Los patógenos se obtuvieron del BCRC. La tasa de inhibición de patógenos orales (%) se calculó de la siguiente manera: (control de UFC en blanco – grupo experimental de UFC)/control de UFC en blanco. El método experimental siguió pruebas publicadas previamente [11].
Análisis estadístico
Se utilizó el software GraphPad Prism para el análisis estadístico de los resultados de la prueba t de dos colas. Los datos se presentaron como la desviación estándar media (DE) o la media de los resultados de dos o tres experimentos independientes. Las diferencias estadísticas se consideraron significativas en el valor de P.<0.05.
Resultados
Las tabletas de probióticos aumentaron la población de bifidobacterias en la cavidad bucal
La población de Bifidobacterium se mantuvo establemente elevada en la cavidad bucal después de la administración de tabletas de probióticos. Las poblaciones bacterianas después de los tratamientos se normalizaron con las poblaciones bacterianas antes de los tratamientos (tasa de población %=UFC postratamiento/UFC previa al tratamiento). En el grupo de probióticos viables, la tasa de población aumentó significativamente a 244,14 ± 164,96 % en la Semana 2 (**P<0.01, Fig. 1a) and 438.41±308.58 at Week 4 (***P<0.001), compared to Week 0. The Bifidobacterium population rate remained high at Week 6 (no administration of viable probiotic tablets for 2 weeks after Week 4, 550.16±448.19%, ***P<0.001), compared to Week 0. The Bifidobacterium population number was significantly different between the viable probiotic and placebo groups at Week 6 (**P<0.01). In the heat-killed probiotic group, the Bifidobacterium population was increased at Weeks 2 (149.92±60.47%, **P<0.01) and 4 (199.87±148.64%, *P<0.05), but was decreased at Week 6 after administration of the heat-killed probiotic tablets was stopped for 2 weeks (182.98±163.73%, Fig. 1a).
Las tabletas de probióticos aumentaron la población de lactobacillus en la cavidad bucal
El cambio en la población oral de Lactobacillus debido a la administración de tabletas de probióticos reveló un patrón similar al seguido por el cambio en la población oral de Bifidobacterium. Las poblaciones bacterianas después de los tratamientos se normalizaron con las poblaciones bacterianas antes de los tratamientos. En el grupo de probióticos viables, la tasa de población de Lactobacillus aumentó significativamente a 447,74 ± 337,89 % en la Semana 2 (**P<0.01, Fig. 1b) and 982.27±726.66% at Week 4 (***P<0.001), compared to Week 0. The Lactobacillus population rate was higher at Week 6 (no administration of viable probiotic tablets for 2 weeks after Week 4, 727.57±539.76%, ***P<0.001) than at Week 0. The Lactobacillus population number was significantly different between the viable probiotic and placebo groups at Week 6 (***P<0.001). In the heat-killed probiotic group, the Lactobacillus population was increased at Weeks 2 (256.66±183.78%, **P<0.01) and 4 (312.85 ± 279.71%, *P < 0.05). Additionally, the Lactobacillus number remained but showed no significant difference at Week 6 after the administration of heat-killed probiotics was stopped for 2 weeks (208.00±199.50%, Fig. 1b).
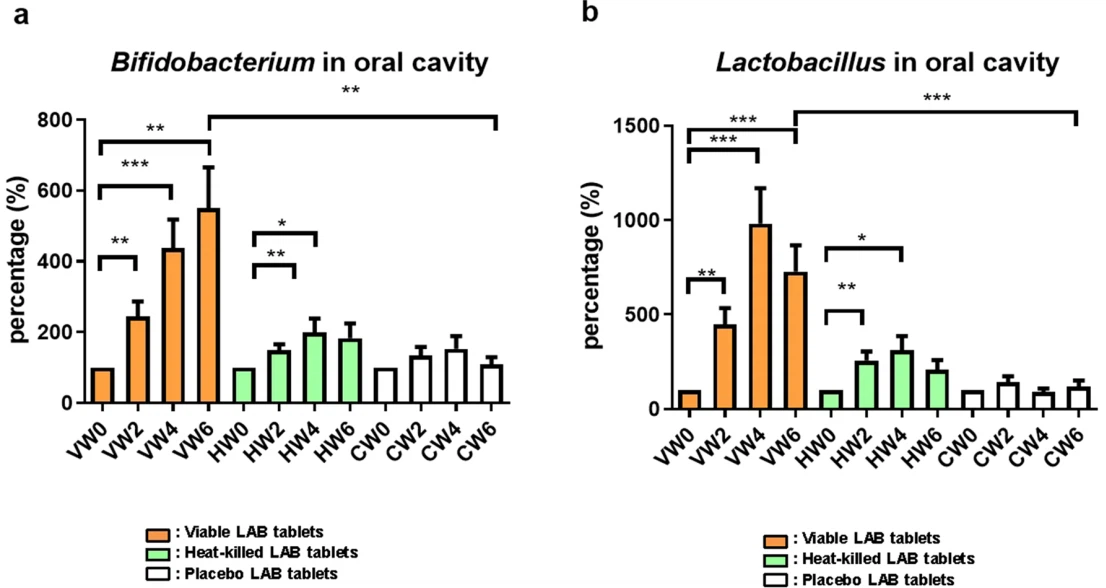
Fig. 1 a Medición de poblaciones de Bifidobacterium en las superficies de la mucosa oral. V tabletas probióticas viables; H tabletas probióticas inactivadas muertas por calor; C comprimidos de placebo (control); y bacterias lácticas LAB. Se realizaron la recolección y análisis de muestras de saliva en las semanas 0, 2, 4 y 6. Los datos se presentaron como desviación estándar media (DE). Se utilizó una prueba t de dos colas para analizar las diferencias estadísticas. Las significancias estadísticas se marcaron con *P<0.05, **P<0.01, ***P<0.001. b Measurement of Lactobacillus populations on the oral mucosal surfaces. V viable probiotic tablets; H heat-killed inactivated probiotic tablets; C placebo tablets (control); and LAB lactic acid bacteria. Collection and analysis of salivary samples at Weeks 0, 2, 4, and 6 were performed. Data were presented as the mean standard deviation (SD). A two-tailed t-test was used to analyze statistical differences. Statistical significances were marked with *P<0.05, **P<0.01, ***P<0.001
Las tabletas de probióticos que contienen AP‑32, ET‑66 y CP‑9 elevaron significativamente la concentración de IgA en la mucosa oral
Como se ha demostrado que el consumo de tabletas de probióticos (viables o muertas por calor) eleva los niveles de Bifidobacterium y Lactobacillus en la cavidad bucal, analizamos más a fondo los cambios en la concentración de IgA en la saliva, que ocurrieron debido a la ingesta de productos probióticos. Los niveles de IgA después de los tratamientos se normalizaron con los niveles de IgA antes de los tratamientos. En el grupo de probióticos viables, la concentración de IgA en saliva aumentó ligeramente a 103,24 ± 8,10% en la Semana 2 (Fig. 2) y 104,81 ± 13,26 en la Semana 4, pero sin diferencias estadísticamente significativas. Sin embargo, la concentración de IgA en saliva en el grupo de probióticos viables, en comparación con el grupo de placebo, aumentó significativamente a 119,30 ± 12,63% en la Semana 6 (sin administración de tabletas de probióticos viables durante 2 semanas después de la Semana 4), en comparación con la Semana 0 ( ***PAG<0.001). Furthermore, in the heat-killed probiotic group, the salivary IgA concentration was slightly increased at Weeks 2 (102.51± 7.20%) and 4 (104.35 ± 10.27%). The saliva IgA concentration was increased at Week 6 (116.78 ± 12.28%, ***P < 0.001, Fig. 2), compared to Week 0.
Las cepas viables aumentaron los niveles de IL-10 y TGF-Beta en PBMC
El control positivo de 10 µg/ml de fitohemaglutinina (PHA) elevó con éxito los niveles de IL-10 (58,2 ± 7,9 pg/ml, ***P < 0,001, Fig. 3a) y TGF- (53,4±8 pg/ml, ***P<0.001, Fig. 3b) in PBMCs by comparing to the negative control (PBMCs treated with medium only). Viable strains of CP-9, AP-32 and ET-66 signifcantly increased the levels of IL-10 in PBMCs to 84.2±9 pg/ml (***P<0.001, ##P<0.01), 303.1±170.9 pg/ml (*P<0.05, ##P<0.01) and 98.2±17.5 pg/ml (***P<0.01, ##P<0.01), respectively. Symbol *indicated a significant difference by comparing to the medium-treated control; symbol #indicated a significant difference by comparing to the PHA control (Fig. 3a). Besides, viable strains of CP-9, AP-32, and ET-66 significantly increased the levels of TGF-beta in PBMCs to 23.2 ± 4.7 pg/ml (***P < 0.001), 130.9 ± 16 pg/ ml (***P < 0.001, ###P < 0.001) and 31.4 ± 5.5 pg/ml (***P<0.01), respectively (Fig. 3b).

Fig. 2 Concentración de inmunoglobulina A (IgA) en las muestras de saliva. V tabletas probióticas viables; H tabletas probióticas inactivadas muertas por calor; C comprimidos de placebo (control); y bacterias lácticas LAB. Se realizaron la recolección y análisis de muestras de saliva en las semanas 0, 2, 4 y 6. Los datos se presentaron como desviación estándar media (DE). Se utilizó una prueba t de dos colas para analizar las diferencias estadísticas. Estadístico
Las tabletas probióticas que contienen AP‑32, ET‑66 y CP‑9 prohibieron la población de S. mutans en la saliva
Las poblaciones elevadas de Bifidobacterium y Lactobacillus y el aumento de la concentración de IgA en la saliva podrían contribuir a la lucha contra los microorganismos patógenos orales. En el experimento posterior, probamos la alteración en la población del patógeno oral S. mutans debido a la intervención probiótica. Las poblaciones bacterianas después de los tratamientos se normalizaron con las poblaciones bacterianas antes de los tratamientos. En el grupo de probióticos viables, la población de S. mutans se redujo significativamente en las Semanas 2 (53,55 ± 31,60 %, ***P<0.001), 4 (49.60±31.01%, ***P<0.001), and 6 (55.19±42.72%, **P<0.01, Fig. 4). At week 6, S. mutans was significantly inhibited in the viable probiotic group (55.19±42.72%, ***P<0.001), compared to in the placebo group. Furthermore, in the heat-killed probiotic group, the S. mutans population was slightly decreased at Week 2 (85.81±49.87%) and significantly reduced at Week 4 (58.35 ± 33.17%, ***P<0.001). The S. mutans population level in the heat-killed probiotic group (202.81±167.99%) reverted to that in the placebo group (225.05±127.01%) at Week 6 (no administration of heat-killed probiotic tablets for 2 weeks from Week 4) (Fig. 4).
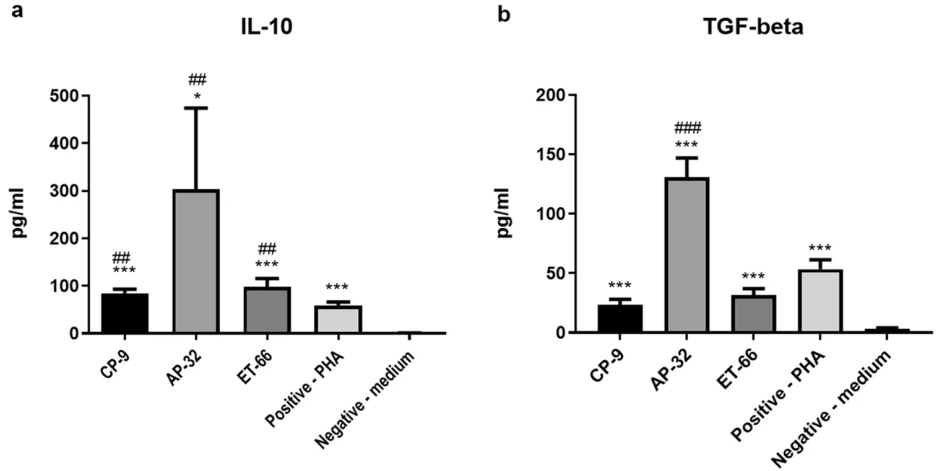
Fig. 3 Las cepas viables aumentaron los niveles de IL-10 y TGF-beta en las PBMC. El nivel de IL-10 y b TGF-beta en PBMC se probó mediante el tratamiento de cepas probióticas. Agregar 5 * 105 ufc/20 µl de cepas viables de CP-9, AP-32 y ET-66 a PMBC de 10 µg/ml. Se utilizó fitohemaglutinina (PHA) como control positivo. El control negativo fueron PBMC tratadas únicamente con medio RMPI-1640. Se realizaron pruebas por triplicado. Los datos se presentaron como desviación estándar media (DE). Se utilizó una prueba t de dos colas para analizar las diferencias estadísticas. Las significancias estadísticas se marcaron con P<0.05, P<0.01, P<0.001. The symbol *indicated a significant difference by comparing to the medium-treated control; symbol #indicated significant difference by comparing to the PHA control
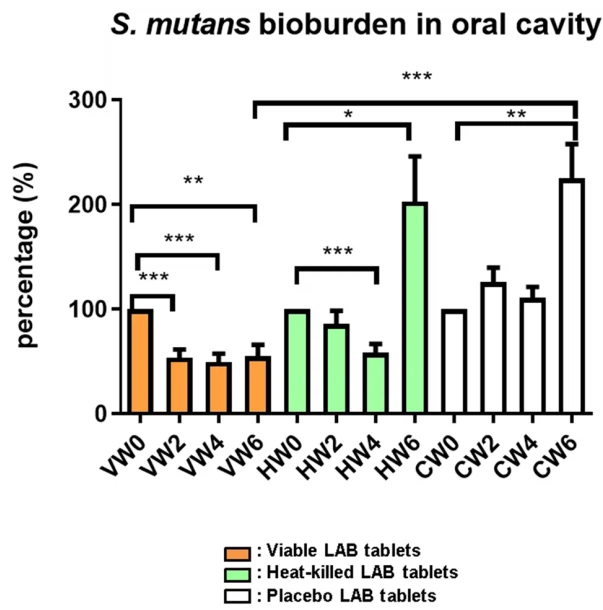
Fig. 4 Medición de poblaciones patógenas de Streptococcus mutans en las superficies de la mucosa oral. V tabletas probióticas viables; H tabletas probióticas inactivadas muertas por calor; C comprimidos de placebo (control); y bacterias lácticas LAB. Se realizaron la recolección y análisis de muestras de saliva en las semanas 0, 2, 4 y 6. Los datos se presentaron como desviación estándar media (DE). Se utilizó una prueba t de dos colas para analizar las diferencias estadísticas. Las significancias estadísticas se marcaron con *P<0.05, **P<0.01, ***P<0.001
Confirmación de la capacidad de las tabletas de probióticos para inhibir el crecimiento de patógenos orales mediante una prueba in vitro
El estudio in vitro reveló que las tabletas de probióticos viables inhibieron significativamente la tasa de supervivencia de los patógenos orales (Fig. 5a). Las poblaciones bacterianas después de los tratamientos se normalizaron con las poblaciones bacterianas antes de los tratamientos. La tasa de supervivencia de S. mutans, P. gingivalis, F. nucleatum y A. actinomy cetemcomitans en el grupo de probióticos viables, en comparación con el grupo de placebo, disminuyó al 4,23 % (***P < 0 .001, placebo=91%), 8,64% (***P < 0,001, placebo=89%), 5,77% (**P<0.01, placebo=98%), and 6.23% (**P<0.01, placebo=87%), respectively. However, the heat-killed probiotic tablet exerted weaker antibacterial effects than the viable probiotic tablet (Fig. 5b). The survival rate of S. mutans, P. gingivalis, F. nucleatum, and A. antinomy cetemcomitans in the heat-killed probiotic group, compared to in the placebo group, was slightly decreased without statistical significance (82%, placebo=91%), significantly reduced to 53% (*P<0.05, placebo=89%), not inhibited (96.88%, placebo=98%), and significantly reduced to 80% (**P<0.01, placebo=87%), respectively.
Discusión
En comparación con el grupo de placebo, las poblaciones orales de Lactobacillus y Bifidobacterium aumentarían significativamente al alimentar con tabletas de probióticos viables o tabletas de probióticos muertos por calor durante 4 semanas. Además, los números de Lactobacillus y Bifidobacterium se mantuvieron en niveles significativamente altos durante 2 semanas después de la suspensión del consumo de probióticos viables (Fig. 1a y b). De manera similar, Camila Casuccio Almeida et al. demostró que una administración de cuatro semanas de un tratamiento probiótico podría persistir y mejorar los síntomas en pacientes intolerantes a la lactosa durante al menos 3 meses después de suspender el consumo de probióticos [23]. Sin embargo, en el futuro se deberá evaluar el efecto persistente de los probióticos en tratamientos a largo plazo. Además, la concentración de IgA en la saliva aumentó significativamente con la administración de tabletas de probióticos viables y muertas por calor. Tanto el grupo de probióticos muertos por calor como el de probióticos viables elevaron la IgA salival mediante la administración de tabletas orales durante 4 semanas, pero sin mostrar diferencias estadísticas con respecto al placebo. La concentración de IgA en los grupos de probióticos viables y muertos por calor mostró un aumento significativo en la semana 6. Sin embargo, el mecanismo de elevación de IgA después de suspender la administración de probióticos durante 2 semanas debe investigarse más a fondo (Fig. 2) Braathen et al. informaron resultados similares sobre el papel inmunomodulador de las cepas probióticas en la cavidad bucal [24]. Además, se ha informado que las cepas probióticas aumentan significativamente la concentración de IgA fecal en cerdas y lechones [25]. Sin embargo, los estudios sobre el alivio de los síntomas de IgA en las infecciones de las vías respiratorias superiores siguen siendo insuficientes. El mecanismo molecular detallado de inhibición y prevención de infecciones de las vías respiratorias superiores mediante cepas probióticas CP-9, AP-32 y ET-66 podría investigarse en estudios futuros. En el presente estudio, las cepas viables CP-9, AP-32 y ET-66 elevarían el nivel de IL-10 y TFG-beta en células PBMC. AP-32 mostró una capacidad efectiva para aumentar IL-10 y TFG-beta en PBMC al compararlos con el control positivo de PHA (Fig. 3a y b). Se presumió que las cepas viables CP-9, AP-32 y ET-66 podrían inducir IL-10 y TFG-beta secretoras de células B para aumentar los niveles de IgA salival. Sin embargo, la correlación entre IL-10 salival, TFG-beta e IgA salival debe probarse más a fondo [26]. Además, aún no está claro si los probióticos destruidos por calor elevaron la IgA mediante la inducción de IL-10 y TFG-beta. Una prueba in vitro indicó que la AP-32 muerta por calor promovía la secreción de interferón e IL-12p70 y disminuía los niveles de IL-13 [27]. Por lo tanto, en este estudio clínico, se analizó la capacidad de las cepas probióticas CP-9, AP-32 y ET-66 y de AP-32 y ET-66 muertas por calor. Se validaron aún más cepas para inhibir bacterias patógenas en la cavidad bucal (Fig. 4). Las pastillas probióticas viables presentaron una mejor capacidad antipatogénica que las pastillas muertas por calor mediante la secreción de ácidos orgánicos, péptidos antimicrobianos [28], exopolisacáridos (EPS) [29] y bacteriocinas [30] (Fig. 5a y b). Los componentes antimicrobianos funcionales producidos por cepas probióticas viables deberían detectarse mediante cromatografía líquida de alta resolución (HPLC) y cromatografía líquida (LC)-espectrometría de masas en el futuro [31]. Se ha informado que los probióticos destruidos por calor poseían ventajas clave de los probióticos viables, pero sin ciertas preocupaciones de seguridad de las cepas probióticas viables [32]. Sin embargo, los componentes antimicrobianos de los probióticos muertos por calor deben verificarse más a fondo.
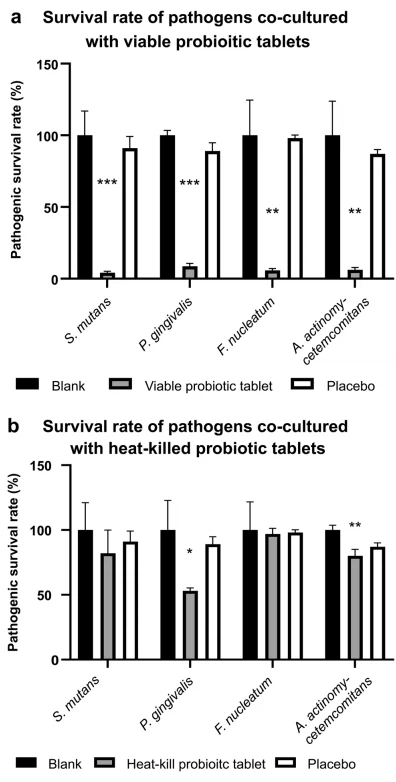
Fig. 5 Confirmación de la capacidad de las tabletas de probióticos para inhibir el crecimiento de patógenos orales mediante una prueba in vitro. Se validó la capacidad de las tabletas de probióticos viables y muertas por calor para inhibir la tasa de supervivencia de patógenos orales, incluidos Streptococcus mutans, Porphyromonas gingivalis, Fusobacterium nucleatum y Aggregatibacter actinomycetemcomitans. Grupo en blanco, sólo mediano; grupo placebo, comprimidos (1 g) sin ningún componente probiótico. Se realizaron pruebas por triplicado. Los datos se presentaron como desviación estándar media (DE). Se utilizó una prueba t de dos colas para analizar las diferencias estadísticas. Las significancias estadísticas se marcaron con *P<0.05, **P<0.01, ***P<0.001
Conclusión
Comprimidos probióticos viables mixtos, compuestos de L. salivarius subsp. salicinius AP-32, B. animalis subsp. CP láctico-9 y L. paracasei ET-66, y probióticos muertos por calor, incluido L. salivarius subsp. salicinius AP-32 y L. paracasei ET-66, ejercieron sus funciones beneficiosas elevando las poblaciones orales de Lactobacillus y Bifdobacterium, reduciendo S. mutans en la cavidad bucal y aumentando la concentración de IgA salival en participantes sanos. Los resultados de las pruebas in vitro validaron que los probióticos viables inhibían eficazmente los patógenos orales, incluidos S. mutans, P. gingivalis y F. nucleatum subsp. polimorfismo y A. actinomycetemcomitans. La inmunidad de la mucosa oral-nasal es la primera línea de defensa contra los microorganismos invasores, y esto se ha convertido en una cuestión crucial. Por tanto, este estudio ofrecerá una estrategia alternativa (suplementación con probióticos) para mantener la inmunidad y la salud bucal.

Beneficios del suplemento cistanche: cómo fortalecer el sistema inmunológico
Referencias
1. Takaki H, Ichimiya S, Matsumoto M, Seya T (2018) Respuesta inmune de la mucosa en tejido linfoide asociado a la nariz tras la administración intranasal de adyuvantes. J Inmunidad innata 10(5–6):515–521
2. Wu RQ, Zhang DF, Tu E, Chen QM, Chen WJ (2014) El sistema inmunológico de la mucosa en la cavidad bucal: una orquesta de diversidad de células T. Int J Oral Sci 6 (3): 125-132
3. Man WH, de Steenhuijsen Piters WAA, Bogaert D (2017) La microbiota del tracto respiratorio: guardián de la salud respiratoria. Nat Rev Microbiol 15(5):259–270
4. Wald ER, Guerra N, Byers C (1991) Infecciones del tracto respiratorio superior en niños pequeños: duración y frecuencia de las complicaciones. Pediatría 87(2):129–133
5. Marcotte H, Lavoie MC (1998) Ecología microbiana oral y el papel de la inmunoglobulina A salival. Microbiol Mol Biol Rev 62(1):71–109
6. Weltzin R, Traina-Dorge V, Soike K, Zhang JY, Mack P, Soman G et al (1996) El anticuerpo IgA monoclonal intranasal contra el virus respiratorio sincitial protege a los monos rhesus contra la infección del tracto respiratorio superior e inferior. J Infectar Dis 174(2):256–261
7. Ruggeri FM, Johansen K, Basile G, Kraehenbuhl JP, Svensson L (1998) La inmunoglobulina A antirotavirus neutraliza el virus in vitro después de la transcitosis a través de células epiteliales y protege a los ratones infantiles de la diarrea. J virol 72(4):2708–2714
8. Millet N, Solis NV, Swidergall M (2020) La IgA mucosa previene la disbiosis comensal de Candida albicans en la cavidad bucal. Inmunol frontal 11:2448
9. Katz J, Harmon CC, Buckner GP, Richardson GJ, Russell MW, Michalek SM (1993) Respuestas protectoras de la inmunoglobulina A salival contra la infección por Streptococcus mutans después de la inmunización intranasal con el antígeno I/II de S. mutans acoplado a la subunidad B de la toxina del cólera . Infectar inmune 61(5):1964–1971
10. Moutsopoulos NM, Konkel JE (2018) Inmunidad específica de tejido en la barrera de la mucosa oral. Tendencias Immunol 39(4):276–287
11. Lin CW, Chen YT, Ho HH, Hsieh PS, Kuo YW, Lin JH, Liu CR, Huang YF, Chen CW, Hsu CH, Lin WY, Yang SF (2021) Los motores Lozengines con cepas probióticas mejoran la respuesta inmune y la salud oral . Enfermedad oral. https://doi.org/10.1111/odi.13854
12. Ericson D, Hamberg K, Bratthall G, Sinkiewicz-Enggren G, Ljunggren L (2013) Respuesta salival de IgA a bacterias probióticas y estreptococos mutans después del uso de chicle que contiene Lactobacillus reuteri. Patog Dis 68(3):82–87
13. Defrance T, Vanbervliet B, Briere F, Durand I, Rousset F, Banchereau J (1992) La interleucina 10 y el factor de crecimiento transformante beta cooperan para inducir que las células B humanas vírgenes activadas con anti-CD40- secreten inmunoglobulina A. J Exp Med. 175(3):671–682
14. Papone V, Verolo C, Zafaroni L, Batlle A, Capo C, Bueno L et al (2015) Detección y prevalencia de patógenos periodontales en una población uruguaya con periodontitis crónica mediante metodología convencional y metagenómica. Odontoestomatologia 17(25):23–32
15. Butera A, Gallo S, Maiorani C, Molino D, Chiesa A, Preda C, Scribante A (2021) Alternativa probiótica a la clorhexidina en terapia periodontal: evaluación de parámetros clínicos y microbiológicos. Microorganismos 9(1):69
16. Wang Y, Li X, Ge T, Xiao Y, Liao Y, Cui Y et al (2016) Probióticos para la prevención y el tratamiento de infecciones del tracto respiratorio en niños: una revisión sistemática y metanálisis de ensayos controlados aleatorios. Medicina 95(31):e4509. https://doi.org/10.1097/MD.0000000000004509
17. Laufer AS, Metlay JP, Gent JF, Fennie KP, Kong Y, Pettigrew MM (2011) Comunidades microbianas del tracto respiratorio superior y otitis media en niños. mBio 2(1):e00245-10. https://doi.org/10. 1128/mBi.00245-10
18. Chen YT, Hsieh PS, Ho HH, Hsieh SH, Kuo YW, Yang SF, Lin CW (2020) Actividad antibacteriana de cepas probióticas viables y muertas por calor contra patógenos orales. Lett Appl Microbiol 70(4):310–317
19. Bonifait L, Chandad F, Grenier D (2009) Probióticos para la salud bucal: ¿mito o realidad? Asociación J Can Dent 75(8):585–90
20. Hsieh PS, An Y, Tsai YC, Chen YC, Chuang CJ, Zeng CT, King AE (2013) Potencial de las cepas probióticas para modular las respuestas inflamatorias de las células epiteliales e inmunes in vitro. Nuevo Microbiol 36(2):167–179
21. Elrefaei M, Burke CM, Baker CA, Jones NG, Bousheri S, Bangsberg DR, Cao H (2009) La producción de TGF e IL-10 por células T CD8+ específicas del VIH está regulada por CTLA{ {5}} señalización en células T CD4+. Más UNO 4(12):e8194
22. Ranganathan V, Akhila CH (2019) Streptococcus mutans: ¿se ha convertido en el principal autor de las manifestaciones orales? J. Microbiol Exp. 7(4):207–213
23. Almeida CC, Lorena SLS, Pavan CR, Akasaka HMI, Mesquita MA (2012) Los efectos beneficiosos del consumo a largo plazo de una combinación de probióticos de Lactobacillus casei Shirota y Bifidobacterium breve Yakult pueden persistir después de la suspensión del tratamiento en pacientes intolerantes a la lactosa. Práctica de Nutr Clin 27(2):247–251
24. Braathen G, Ingildsen V, Twetman S, Ericson D, Jørgensen MR (2017) La presencia de Lactobacillus reuteri en la saliva coincide con una mayor IgA salival en adultos jóvenes después de la ingesta de pastillas probióticas. Microbios beneficiosos 8(1):17–22
25. Scharek L, Guth J, Filter M, Schmidt MFG (2007) Impacto de las bacterias probióticas Enterococcus faecium NCIMB 10415 (SF68) y Bacillus cereus var. a usted NCIMB 40112 sobre el desarrollo de IgG sérica e IgA fecal de cerdas y sus lechones. Arch Anim Nutr 61(4):223–234
26. Ebrahimpour-Koujan S, Milajerdi A, Larijani B, Esmaillzadeh A (2020) Efectos de los probióticos sobre las citocinas e inmunoglobulinas salivales: una revisión sistemática y un metanálisis de ensayos clínicos. Representante científico 10(1):1–11
27. Ou CC, Lin SL, Tsai JJ, Lin MY (2011) Las bacterias del ácido láctico muertas por calor mejoran el potencial inmunomodulador al desviar la respuesta inmune hacia la polarización Th1. J Ciencia de los alimentos 76(5):M260–M267. https://doi.org/10.1111/j.1750-3841.2011. 02161.x
28. Nair MS, Amalaradjou MA, Venkitanarayanan K (2017) Propiedades antivirulentas de los probióticos en la lucha contra la patogénesis microbiana. Adv Appl Microbiol 98:1–29
29. Wu MH, Pan TM, Wu YJ, Chang SJ, Chang MS, Hu CY (2010) Actividades de exopolisacáridos de bifidobacterias probióticas: efectos inmunomoduladores (en macrófagos J774A. 1) y propiedades antimicrobianas. Int J Microbiol alimentario 144(1):104–110
30. Barefoot SF, Klaenhammer TR (1983) Detección y actividad de la lactacina B, una bacteriocina producida por Lactobacillus acidophilus. Appl Environ Microbiol 45(6):1808–1815
31. Kim PI, Sohng JK, Sung C, Joo HS, Kim EM, Yamaguchi T, Kim BG (2010) Caracterización e identificación de la estructura de un péptido antimicrobiano, homínido, producido por Staphylococcus hominis MBBL 2–9. Biochem Biophys Res Commun 399(2):133–138
32. Piqué N, Berlanga M, Miñana-Galbis D (2019) Beneficios para la salud de los probióticos muertos por calor (tyndallizados): una descripción general. Int. J Mol Sci 20(10):2534






