El perfil inmunológico longitudinal revela epítopos dominantes que median la inmunidad humoral a largo plazo en individuos convalecientes de COVID-19
Sep 12, 2023
Fondo: El coronavirus 2 del síndrome respiratorio agudo severo (SARS-CoV-2) es un coronavirus altamente patógeno y contagioso que causó una pandemia mundial con 5,2 millones de muertes hasta la fecha. Quedan por dilucidar las cuestiones relativas a las características serológicas de la inmunidad a largo plazo, especialmente los epítopos dominantes que median respuestas duraderas de anticuerpos después de la infección por SARS-CoV-2.
Objetivo: Nuestro objetivo era analizar la cinética y la longevidad de las respuestas inmunitarias en pacientes con enfermedad por coronavirus 2019 (COVID-19), así como los epítopos responsables de la inmunidad humoral sostenida a largo plazo contra el SARS-CoV-2.
Métodos: Evaluamos la dinámica inmune del SARS-CoV-2 hasta 180 a 220 días después del inicio de la enfermedad en 31 personas que experimentaron predominantemente síntomas moderados de COVID-19, luego realizamos un perfil proteómico de los epítopos dominantes responsables de respuestas inmunes humorales persistentes.
Resultados: El análisis longitudinal reveló anticuerpos sostenidos específicos de la proteína de pico del SARS-CoV-2 y anticuerpos neutralizantes en pacientes con COVID-19, junto con una activación de la producción de citocinas en las primeras etapas después de la infección por SARS-CoV-2. Se demostró que los epítopos altamente reactivos que eran capaces de mediar respuestas de anticuerpos a largo plazo estaban ubicados en las proteínas Spike y ORF1ab. Se asignaron epítopos clave de la proteína de pico del SARS-CoV-2 al dominio N-terminal de la subunidad S1 y la subunidad S2, con diversos grados de homología de secuencia entre los coronavirus humanos endémicos y una alta identidad de secuencia entre los primeros brotes del SARS-CoV. CoV-2 (Wuhan-Hu- 1) y variantes circulantes actuales.

Beneficios del suplemento cistanche: cómo fortalecer el sistema inmunológico
Conclusión: La infección por SARS-CoV-2 induce inmunidad humoral persistente en personas convalecientes de COVID-19 al atacar los epítopos dominantes ubicados en la espiga y las proteínas ORF1ab que median las respuestas inmunitarias a largo plazo. Nuestros hallazgos proporcionan un camino para ayudar al diseño racional de vacunas y al desarrollo de diagnóstico. (J Allergy Clin Immunol 2022;149:1225-41.)
Palabras clave:
SARS-CoV-2, COVID-19, respuesta inmune a largo plazo, inmunidad humoral, micromatriz de péptidos proteoma completo, epítopo dominante
El síndrome respiratorio agudo severo coronavirus 2 (SARS-CoV- 2), el patógeno causante de la actual pandemia de enfermedad por coronavirus 2019 (COVID-19), pertenece al género Betacoronavirus, que incluye otros 2 humanos altamente patógenos conocidos. coronavirus: los coronavirus del síndrome respiratorio agudo severo (SARS) y del síndrome respiratorio de Oriente Medio (MERS).1 Desde la aparición del primer caso registrado a finales de diciembre de 2019, la infección por SARS-CoV-2 ha provocado más de 263 millones casos confirmados y 5,2 millones de muertes en todo el mundo hasta noviembre de 2021, lo que afecta a 220 países y regiones en los 5 continentes.2 Después de la infección, las presentaciones clínicas varían ampliamente, incluidas infecciones asintomáticas, síntomas leves o moderados o incluso neumonía grave potencialmente mortal.3 A pesar de Debido a la disponibilidad de múltiples tipos de vacunas, muchos países todavía luchan por contener nuevas oleadas de infecciones, y están surgiendo variantes del virus que parecen exhibir una mayor transmisibilidad y resistencia a las respuestas inmunitarias antivirales. Una respuesta inmune humoral eficaz mediada por anticuerpos neutralizantes debería poseer una inmunidad adaptativa poderosa e indispensable para bloquear la infección y eliminar los patógenos virales. Después de la infección por SARS-CoV-2, se observó una tasa alta (más del 90 %) de seroconversión robusta entre las personas infectadas entre 7 y 14 días después del inicio de la enfermedad.4-6 La producción de antígenos específicos IgA, IgG, y la IgM que reconoce la proteína de pico (S) y la proteína de la nucleocápside (N) del SARS-CoV-2 fue detectable durante la fase aguda de la enfermedad y la etapa inicial de convalecencia.4,5,7 La magnitud de los anticuerpos neutralizantes pareció asociarse con la edad, la infección sintomática y la gravedad de la enfermedad. Los pacientes de edad avanzada y las personas que presentan síntomas graves de COVID-19 tienden a desarrollar niveles más altos de anticuerpos neutralizantes.4,8-10 Varios estudios sobre la longevidad de las respuestas de los anticuerpos han revelado que, a pesar de una pérdida de reactividad del suero/plasma al virus antígenos y disminución de los títulos de anticuerpos neutralizantes con el tiempo en algunos casos sintomáticos de COVID-19, se observó un nivel sostenido de inmunidad humoral general a largo plazo durante un máximo de 8 a 12 meses después de la infección en personas convalecientes de COVID-19 .10-13 Además, el número de células B de memoria específicas del antígeno SARS-CoV-2 se mantuvo estable durante al menos 6 a 12 meses,12,13 junto con la selección y acumulación continuas de clones de células B que expresan anticuerpos neutralizantes,12,14 que indican el mantenimiento de una inmunidad humoral persistente después de la infección por SARSCoV-2.

Beneficios del suplemento cistanche: aumentar la inmunidad.
Los anticuerpos neutralizantes desempeñan un papel fundamental en las defensas del huésped contra la infección viral. Se ha identificado un panel de anticuerpos monoclonales muy potentes del SARS-CoV-2,15-17 dirigidos principalmente a epítopos ubicados en el dominio de unión al receptor de la proteína S que se ensambla en trímeros en la superficie del virión y facilita la entrada del virus. y fusión al acoplarse al receptor 2 de la enzima convertidora de angiotensina.18 Otras regiones de la proteína S, incluido el dominio N-terminal (NTD) de la subunidad S1 y la subunidad S2, también contienen epítopos inmunogénicos que son capaces de inducir anticuerpos neutralizantes.16 ,19,20 Además de la neutralización, los anticuerpos del SARS-CoV-2 pueden conferir protección in vivo a través de funciones efectoras mediadas por Fc, como la fagocitosis dependiente de anticuerpos desencadenada por células asesinas naturales y la citotoxicidad dependiente de anticuerpos por monocitos o macrófagos. 21,22 Además de combatir las infecciones virales, los anticuerpos generados por infección natural o vacunación pueden facilitar la patogénesis del virus, ya sea mediante una mayor activación de la inflamación o una mayor infectividad del virus a través de la formación de complejos inmunes antígeno/anticuerpo o mediante funciones dependientes de Fc,23-25 aunque no se ha observado una infección viral mejorada en el contexto del SARS-CoV-2 in vivo. Estas funciones divergentes de las respuestas de los anticuerpos requieren una caracterización sistemática de los epítopos del SARSCoV-2, así como las propiedades de los anticuerpos de larga duración dirigidos a los epítopos neutralizantes o no neutralizantes. A pesar de los avances recientes sobre la cinética y la duración de las respuestas de los anticuerpos después de la infección por SARS-CoV-2, el análisis longitudinal sobre los epítopos prominentes que sustentan las respuestas inmunes humorales a largo plazo aún es limitado. Estudios anteriores han perfilado epítopos de la respuesta de anticuerpos en individuos infectados con COVID-19 utilizando principalmente ensayos basados en ELISA,26,27 enfoques basados en visualización de fagos o bacterias,28-31 y tecnologías basadas en microarrays.30,{{ 38}} Se han identificado varios epítopos inmunodominantes de la proteína S del SARS-CoV-2; las regiones detectadas con mayor frecuencia se mapearon cerca o abarcando el péptido de fusión (FP) de la subunidad S2, la segunda heptada se repite dentro de la subunidad S2 y en el dominio C-terminal de la subunidad S1.26,28-30, 32,33 Además, el examen serológico también reveló epítopos ubicados en otras proteínas del proteoma del SARS-CoV-2, incluida la proteína N, la proteína de membrana (M) y ORF1ab, ORF3a y ORF7a.28-30 34,35 Aunque estudios anteriores han proporcionado información importante sobre los epítopos antigénicos, estos estudios se han centrado en gran medida en el perfil de epítopos de los pacientes con COVID-19 en la fase de convalecencia temprana. Aún no se han dilucidado los epítopos exactos que median las respuestas duraderas de anticuerpos específicos del SARS-CoV-2, así como la dinámica del reconocimiento de los epítopos. En este caso, para obtener una comprensión más profunda de la cinética y la longevidad de las respuestas inmunes humorales en pacientes con COVID-19, especialmente los epítopos responsables de la inmunidad sostenida a largo plazo contra el SARS-CoV-2, realizamos un análisis longitudinal integral. del perfil inmunológico en 31 pacientes con COVID-19 hasta 180 a 220 días después de la aparición de los síntomas. Basándonos en la evaluación de los anticuerpos neutralizantes y de unión al antígeno, así como de los niveles de citoquinas séricas, identificamos además un panel de epítopos ubicados en las proteínas ORF1ab, S y N del SARSCoV-2 que media las respuestas inmunitarias humorales persistentes utilizando un péptido. micromatriz que abarca el proteoma completo del SARS-CoV-2. Nuestros resultados arrojan luz sobre las características de la inmunidad a largo plazo para superar la infección viral y ayudarán a informar el diseño racional de vacunas y el desarrollo de herramientas de diagnóstico serológico mejoradas.

MÉTODOS
Participantes del estudio y recolección de muestras.
Para evaluar longitudinalmente la cinética de las respuestas inmunitarias dirigidas por el SARS-CoV-2, se recogieron 101 muestras de suero de 31 personas infectadas por el SARS-CoV-2 que ingresaron en el Tercer Hospital de Nantong afiliado a la Universidad de Nantong (Nantong , China) entre enero y marzo de 2020. A todos los pacientes se les diagnosticó infección confirmada por SARS-CoV-2 mediante pruebas de PCR cuantitativa de transcripción inversa; la gravedad de la enfermedad se definió como COVID leve a moderada (no grave) o grave-19 según la versión 7 del Protocolo de diagnóstico y tratamiento para la neumonía por el nuevo coronavirus publicado por la Comisión Nacional de Salud de la República Popular China.36 Se dio seguimiento a los pacientes longitudinalmente durante 4 a 8 meses después de la recuperación de la infección aguda. Se recolectaron muestras de sangre de manera longitudinal de 4 a 219 días después del inicio de los síntomas para 20 pacientes entre 31 participantes del estudio (mediana de 4,5 muestras por individuo, con un rango de 2 a 8), mientras que se realizó un muestreo en un solo momento para cada uno de los otros 11 individuos que se encontraban en una fase de convalecencia tardía de la enfermedad (días 122 a 214 después del inicio de la enfermedad). En consecuencia, también se incluyeron como grupo de control sueros (n 5 20) de donantes sanos de la misma edad y sexo. Ningún participante del estudio tenía una infección previa documentada con SARS o MERS.
El estudio fue aprobado por el comité de ética del Tercer Hospital de Nantong afiliado a la Universidad de Nantong (aprobación EL2020006). Se obtuvo el consentimiento informado por escrito de cada uno de los participantes del estudio. El suero se separó de la sangre periférica en tubos de gel de suero mediante centrifugación, se formaron alícuotas y se almacenaron a 280 °C antes de su uso.
Líneas celulares
Se cultivaron células HEK293T y Huh7 en medio Eagle modificado por Dulbecco (Gibco; Thermo Fisher Scientific, Waltham, Mass) suplementado con suero bovino fetal inactivado por calor al 10% (Gibco), penicilina 100 U/ml (Gibco) y 100 mg/ml. mL de estreptomicina (Gibco) a 378C con 5% de CO2.

Beneficios de cistanche para hombres: fortalece el sistema inmunológico.
Haga clic aquí para ver los productos Cistanche Enhance Immunity
【Pregunte por más】 Correo electrónico:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
Detección de anticuerpos IgG mediante ELISA
Los niveles de anticuerpos IgG de unión a antígeno en muestras de suero humano se determinaron mediante ELISA. Se recubrieron previamente placas ELISA de noventa y seis pocillos (Corning, Corning, NY) con proteína de la nucleocápside del SARS-CoV-2 (Sino Biological, Beijing, China, número de catálogo 40588-V08B). , 50 ng por pocillo) o proteína de pico (Sino Biological, 40589-V08B1, 100 ng por pocillo), proteína de pico de SARS-CoV (Sino Biological, 40634-V08B, 100 ng por pozo), o proteína de pico MERS-CoV (Sino Biological, 40069-V08B, 50 ng por pozo) durante la noche a 48 ° C. Después de bloquear con leche desnatada al 5 % en solución salina tamponada con fosfato (PBS) que contiene Tween 20 al 0,05 % (PBS-T) durante 2 horas a 378 °C, 3-veces muestras de suero inactivadas por calor diluidas en serie a una dilución inicial de 1 :200 se añadieron a placas prerrevestidas durante 2 horas a 378°C. Los pocillos se lavaron 3 veces entre cada paso con PBS-T. Las reacciones se visualizaron mediante incubación con anticuerpo anti-IgG humano conjugado con peroxidasa de rábano picante (Abcam, Cambridge, Reino Unido, dilución 1:100, 000) durante 1 hora a 378 °C, seguido de la adición de sustrato de tetrametilbencidina (Life Technologies, Carlsbad). , California). Las reacciones en desarrollo se detuvieron con 2 moles de H2SO4 y se midió la absorbancia a 450 nm con la longitud de onda de corrección establecida en 630 nm (OD450 2 OD630). Para calcular el título de criterio de valoración de los anticuerpos de unión, los datos se linealizaron trazando el log10 de las diluciones de suero versus los valores de densidad óptica (OD) corregidos (OD450 2 OD630) dentro de la porción lineal de la curva (y 5 kx 1 b , r2 > 0,99) y la dilución de suero a la que se calculó el valor de DO ajustado (OD450 2OD630) 5 0 para dar un título de criterio de valoración. Los anticuerpos IgG específicos de antígeno en ratones inmunizados con péptidos se evaluaron mediante ELISA basado en péptidos. Brevemente, se recubrieron placas de ELISA de 96- pocillos (Thermo Fisher Scientific) con 1 mg por pocillo de 4 péptidos mixtos (péptidos 318, 356, 510 y 530) en tampón carbonato (pH 9,6) durante la noche a 48 °C. Después del bloqueo con PBS-T que contenía un 5 % de leche descremada, los pocillos se incubaron con muestras de suero diluidas a 1:40 durante 1 hora a 378 °C. Posteriormente, las placas se lavaron e incubaron con anticuerpo IgG anti-ratón conjugado con peroxidasa de rábano picante (Abcam). Las reacciones se visualizaron con sustrato de tetrametilbencidina (Life Technologies) y se midió la absorbancia a 450 nm después de detener las reacciones con 2 moles de H2SO4.
Producción y titulación de pseudovirus.
El gen con codones optimizados que codifica la proteína de pico del SARS-CoV-2 (NC_045512) o del SARS-CoV (AY291315.1) con deleción de 19 aa C-terminal, o MERS-CoV (JX{{10 }}) la proteína de pico truncada con 16 aa C-terminal se clonó en el vector pcDNA3.1(1), respectivamente. Se cotransfectaron células HEK 293T cultivadas en una placa de cultivo de tejidos de 100 mm con 1 mg de un plásmido que codifica la proteína de pico y 15 mg de una columna vertebral deficiente en env que expresa luciferasa (pNL4-3.luc.RE) utilizando polietilenimina (Polysciences , Warrington, Pensilvania). Los sobrenadantes de cultivos celulares que contenían pseudovirus se recogieron 48 horas después de la transfección, se filtraron y se almacenaron a 280 °C en alícuotas. Para la determinación de los títulos de virus (dosis infecciosa del 50 % en cultivo de tejidos), se agregaron diluciones en serie de pseudovirus a 1 3 104 células Huh7 presembradas en 96-placas de pocillos. Después de 12 horas de infección, el medio que contenía el virus se reemplazó por un medio de crecimiento nuevo y las células se cultivaron durante 48 horas más. La actividad luciferasa de la lisis celular se midió con el sistema de ensayo Steady-Glo Luciferase (Promega, Madison, Wisc) usando un lector de microplacas (BioTek Instruments, Winooski, Vt), y se consideraron los pocillos que producían unidades de luminiscencia relativas superiores a 10 veces el valor de fondo promedio. positivo.
pseudoviensayo de neutralización rus
Muestras de suero inactivadas por calor de pacientes con COVID-19 o donantes sanos se diluyeron 2-veces en serie y se incubaron con 200 pseudovirus a una dosis infecciosa del 50 % en cultivo de tejidos durante 1 hora a 378 °C. Luego, las mezclas se aplicaron para infectar células Huh7 presembradas en placas de pocillos 96- por duplicado. Los pocillos se rellenaron con medio de crecimiento nuevo 12 horas después de la infección y la actividad luciferasa de las células se determinó 48 horas después. Los títulos de neutralización del 50 % (NT50) contra los pseudovirus SARS-CoV-2 y SARS-CoV se calcularon mediante regresión no lineal utilizando el software GraphPad Prism 8.0 (GraphPad Software, La Jolla, California); y el NT50 del pseudovirus MERS-CoV se definió como la dilución más alta de suero que resultó en una reducción del 50% de las unidades relativas de luminiscencia en comparación con el control del virus sin aplicar muestras de suero.
Detección de citocinas basada en microarrays de proteínas
La medición cuantitativa de múltiples citocinas (IL-1a, IL-1b, IL- 4, IL-6, IL-8, IL-10 , IL-13, MCP-1, IFN-g y TNF-a) en muestras de suero se realizó utilizando una matriz ELISA multiplex (RayBiotech, Peachtree Corners, Ga) de acuerdo con el protocolo del fabricante. Brevemente, se bloquearon portaobjetos de vidrio prerrevestidos con anticuerpos específicos de citoquinas con diluyente de muestra a temperatura ambiente durante 30 minutos, seguido de la adición de 60 ml de muestras de suero diluidas 2- veces o diluciones estándar de citoquinas. Después de una incubación durante la noche a 48 ° C, los portaobjetos se lavaron 5 veces y se tiñeron con 80 ml de cóctel de anticuerpos de detección biotinilados y luego estreptavidina conjugada con colorante equivalente a Cy3 a temperatura ambiente durante 1 hora. La intensidad de la fluorescencia se detectó mediante el escáner de microarrays InnoScan 300 (Innopsys, Chicago, Ill) a 532 nm y los datos se analizaron mediante el software Q-Analyzer (RayBiotech).
Síntesis de péptidos y conjugación con albúmina sérica bovina.
GL Biochem (Shanghai, China) sintetizó un total de 515 péptidos (15 aa de longitud, superpuestos por 11 aa) que cubren el proteoma del SARS-CoV-2 basándose en la secuencia de aminoácidos del SARS-CoV. -2 cepa Wuhan-Hu-1. Los péptidos se conjugaron con albúmina sérica bovina (BSA) utilizando el reticulante Sulfo-SMCC (Thermo Fisher Scientific) según las instrucciones del fabricante. Brevemente, se añadió Sulfo-SMCC en un exceso molar de 30- veces a BSA, seguido de diálisis a PBS. Posteriormente, se añadió el péptido que contenía cisteína en una proporción de 1:1 (peso/peso), se incubó durante 2 horas y se dializó adicionalmente con PBS para eliminar los péptidos libres.
Fabricación de microarrays de péptidos.
Para preparar el microarray de péptidos, péptidos del SARS-CoV-2, así como el control negativo (BSA) y los controles positivos (anticuerpos anti-IgG humano y anti-IgM humano; Sigma-Aldrich, St Louis, Mo) , se inmovilizaron en portaobjetos de sustrato PATH (Grace Bio-Labs, Bend, Ore) por triplicado utilizando una impresora Super Marathon (Arrayjet, Edimburgo, Escocia, Reino Unido). Luego, las micromatrices de péptidos se conservaron a 280 ° C para su uso posterior.

cistanche tubulosa-mejora el sistema inmunológico
Mapeo de epítopos basado en microarrays
El análisis de suero basado en microarrays se realizó como Li et al,37 con modificaciones menores. Para crear cámaras individuales para subconjuntos idénticos, se montó una junta de goma de cámara 14- en cada portaobjetos de microarrays de péptidos. Las matrices de portaobjetos se calentaron a temperatura ambiente antes de su uso y luego se bloquearon con BSA al 3% en PBS-T durante 3 horas. Las muestras de suero de pacientes con COVID-19 o los sueros combinados de 20 donantes sanos (grupo de control) se diluyeron a 1:200 en PBS-T para la mayoría de las muestras y luego se incubaron con cada subconjunto durante 2 horas a 48C. Las matrices se lavaron con PBS-T y se incubaron con IgG antihumana de cabra conjugada con Cy3- y IgM antihumana de burro conjugada con Alexa Fluor 647 (Jackson ImmunoResearch Laboratories, West Grove, Pensilvania) a una dilución de 1:1000. cada uno durante 1 hora a temperatura ambiente. Después de la incubación, las matrices se lavaron con PBS-T y luego se secaron completamente mediante centrifugación a temperatura ambiente. Posteriormente, las matrices se escanearon utilizando un escáner de microarrays LuxScan 10K-A (CapitalBio, Beijing, China), y los datos de intensidad de fluorescencia de FL se obtuvieron y analizaron mediante el software GenePix Pro 6.0 (Molecular Devices, Sunnyvale, California).
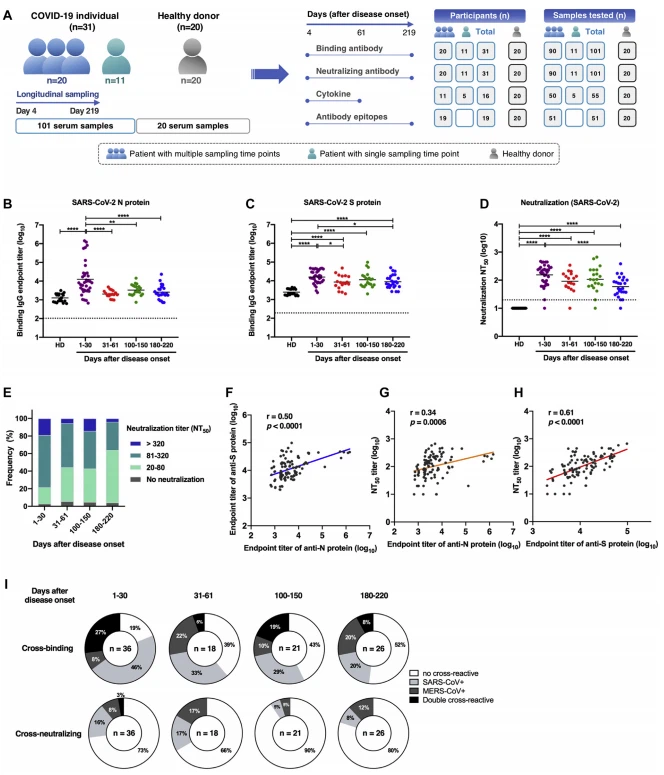
FIG 1. Dinámica longitudinal de las respuestas de anticuerpos en pacientes con COVID-19. Un esquema del diseño del estudio. En el estudio se inscribieron un total de 31 personas infectadas con SARS-CoV-2 y 20 donantes sanos. La recolección de muestras de suero se realizó longitudinalmente en múltiples momentos para 20 pacientes entre 31 individuos infectados por SARS-CoV-2, mientras que el muestreo se realizó en un solo momento para los otros 11 pacientes. Se enumera el número de participantes y muestras de suero utilizadas en varios ensayos. B y C. Se analizaron mediante ELISA un total de 101 muestras de suero de 31 pacientes con COVID-19 para detectar anticuerpos IgG que se unen a la proteína N (B) y la proteína S (C) del SARS-CoV-2 en diferentes momentos. después del inicio de los síntomas (días 1-30, n 5 37; días 31-61, n 5 18; días 100-150, n 5 21; días {{21 }}, n 5 25). Se incluyeron muestras de suero de 20 donantes sanos como grupo de control. D, NT50 contra pseudovirus SARS-CoV-2 a lo largo del tiempo se calculó mediante regresión no lineal. E, Se presenta la distribución de la actividad neutralizante del suero en pacientes con COVID-19 en los momentos indicados después del inicio de la enfermedad. Las muestras con un título de NT50 inferior a 20 se definieron como no neutralizantes.
Análisis de datos de microarrays de péptidos.
Los datos de IgG e IgM se analizaron respectivamente. La intensidad de la señal de cada punto se definió como el primer plano menos el fondo y se promediaron los puntos triples para cada péptido. El valor límite para la respuesta peptídica positiva de las muestras de COVID-19 se estableció en el doble de la intensidad de la señal del control de donante sano. Los péptidos con tasas positivas superiores al 80 % entre las muestras analizadas en los 3 momentos de muestreo (días 10-60, 100-150 y 180-220 después del inicio de la enfermedad) se definieron como péptidos dominantes y persistentes y péptidos con una frecuencia de respuesta positiva superior al 60% en todos los 3-puntos temporales se consideró subdominante y persistente. Se calculó la intensidad de señal promedio de cada péptido en 3 grupos de puntos de tiempo de muestreo; También se seleccionaron péptidos que mostraban una alta intensidad de señal (por encima de la media 1 DE de intensidades de señal de todas las muestras analizadas). El procesamiento y análisis de datos se realizaron mediante el software R v3.6.3 (https://www.r-project.org/), y se evaluaron cambios significativos en la intensidad de la señal entre diferentes grupos de puntos de tiempo de muestreo según Limma. Las diferencias con p < 0,05 se consideraron estadísticamente significativas.
Inmunización del ratón
Se adquirieron ratones hembra BALB/c de 6 a 8 semanas de Beijing Vitalstar Biotechnology (Beijing, China). Todos los ratones se alojaron en instalaciones específicas libres de patógenos y el estudio con animales fue aprobado por el Comité Institucional de Cuidado y Uso de Animales de la Universidad Médica de Tianjin (Tianjin, China). Para la inmunización, a grupos de ratones (n 5 5) se les inyectó por vía intramuscular 25 mg por dosis de cada péptido (péptidos 318, 356, 510 y 530 respectivamente) mezclados con 50 mg de alumbre (InvivoGen, San Diego, California). y 10 mg de adyuvantes CpG, y se reforzaron dos veces con 50 mg por dosis de péptidos en presencia de adyuvantes en intervalos de 2-semanas. La vacunación con adyuvantes solos sirvió como control negativo. Se recogieron sueros de ratones inmunizados el día 10 o el día 14 después de la segunda y tercera inmunizaciones.
Análisis estadísticos y estructurales.
Todos los gráficos fueron trazados por GraphPad Prism. Las comparaciones estadísticas entre los grupos de las figuras 1, 2 y 4 se realizaron mediante ANOVA de vía con comparación múltiple de Tukey. Las correlaciones que se muestran en la Fig. 1, Fig. E9 y Fig. E10 en el repositorio en línea disponible en www.jacionline.org se determinaron mediante análisis de correlación de Pearson. Las diferencias con p < 0,05 se consideraron estadísticamente significativas. Las estructuras de la proteína de pico del SARS-CoV-2 (Protein Data Bank [PDB; http://www.wwpdb.org/] ID: 6VXX y PDB ID: 6ZGI) y el dominio de dimerización del SARS-CoV{{ 13}} se utilizó la proteína de la nucleocápside (PDB ID: 6YUN) para diseccionar los detalles estructurales de los epítopos identificados ubicados en la proteína de pico y el dominio de dimerización de la proteína de la nucleocápside. La alineación de secuencias y el análisis de homología entre varios coronavirus humanos se realizaron mediante el algoritmo Clustal W en el software MEGA v10.1.6.
RESULTADOS
La infección por SARS-CoV-2 induce una unión sostenida específica del antígeno y anticuerpos neutralizantes
Para evaluar longitudinalmente las respuestas de anticuerpos después de la infección por SARS-CoV-2, se recolectaron 101 muestras de suero de 31 personas con infección por SARS-CoV-2 confirmada por PCR (Fig. 1, A). Los participantes del estudio incluyeron 26 pacientes con COVID moderado-19, 1 con presentación asintomática, 2 con enfermedad leve y 2 con síntomas graves (consulte la Tabla E1 en el repositorio en línea disponible en www.jacionline.org). Los pacientes inscritos en este estudio tenían edades comprendidas entre 17 y 66 años (edad media, 45 años), con una distribución aproximadamente igual de hombres (51,6%) y mujeres (48,4%). Los síntomas más comunes entre los participantes del estudio incluyeron fiebre (83,9%), tos (67,7%), mialgia (22,6%) y escalofríos (22,6%), con una duración media de la enfermedad de 15 días. Se recogieron un total de 90 muestras de suero de 20 pacientes con COVID-19 durante la hospitalización y el alta después de la recuperación en múltiples momentos hasta 219 días después del inicio de los síntomas (Fig. 1, A y consulte la Tabla E2 en el repositorio en línea). El muestreo de los otros 11 participantes se realizó en un único momento durante la convalecencia tardía (días 122 a 214 después del inicio de los síntomas). Además, se incluyeron como grupo de control muestras de 20 donantes sanos con distribución coincidente por edad y sexo (Tabla E1). Los anticuerpos IgG específicos de antígeno en muestras de suero se cuantificaron mediante ELISA precubierto con proteína N o proteína S del SARS-CoV-2. En comparación con los donantes sanos, se desarrollaron anticuerpos IgG anti-N y anti-S en pacientes con COVID-19 dentro de los 30 días posteriores al inicio de los síntomas, con una media geométrica del título final de 4,10 (log10 anti-N IgG) y 4.20 (log10 anti-S IgG) (Fig. 1, B y C; y consulte la Tabla E3 en el repositorio en línea en www.jacionline.org; Fig. E1, A y B; y Fig. E2), de acuerdo con observaciones previas de que la seroconversión ocurre entre 1 y 2 semanas después de la infección por SARS-CoV-2.5,38 Posteriormente, los títulos de anticuerpos de unión a antígeno disminuyeron en diversos grados con el tiempo. Se observó una disminución rápida y espectacular de los niveles de anticuerpos anti-N IgG en pacientes con COVID-19, mientras que los niveles más altos de títulos de anti-S IgG se mantuvieron hasta 180 a 220 días después del inicio de la enfermedad en comparación con los donantes sanos (Fig. 1, B). , y C). El análisis de correlación reveló una correlación significativa entre los títulos de IgG anti-N log10 y los títulos de IgG anti-S (r 5 0.50 y P < 0,001; Fig. 1, F). Además de cuantificar los anticuerpos de unión, la dinámica de los anticuerpos neutralizantes funcionales en individuos con COVID-19 se determinó adicionalmente utilizando SARS-CoV pseudotipado-2. Más del 95% de las muestras de suero de pacientes (35/37) recolectadas entre 4 y 30 días después del inicio de los síntomas tuvieron actividades neutralizantes sólidas contra el SARS-CoV-2, y una gran proporción de muestras exhibieron (NT50 80-320 moderadas). ) a una fuerte actividad neutralizante (NT50 > 320) (Fig. 1, D y E). Es de destacar que se recogieron 2 muestras con títulos neutralizantes bajos o nulos (NT50 en una dilución sérica mínima de 1:20) en un período temprano después de la infección viral (el día 4 y el día 11 después del inicio de los síntomas) antes de provocar anticuerpos neutralizantes potentes (Fig. 1, D y Figura E1, C). A pesar de la disminución de los niveles de anticuerpos neutralizantes del SARS-CoV-2 en pacientes con COVID-19 con el tiempo, la mayoría de las muestras de suero de los pacientes (24/25) obtenidas entre 180 y 220 días después de la aparición de los síntomas mantuvieron una positividad para la neutralización contra el SARS-CoV. CoV-2, con una disminución de 2,8-veces en los títulos de NT50 medios geométricos (Fig. 1, D y E; Tabla E3; Fig. E3). Como se esperaba, en comparación con los anticuerpos anti-N IgG, se identificó una correlación más fuerte entre los títulos de IgG de unión al SARS-CoV-2 S y los títulos de anticuerpos neutralizantes (r 5 0.61 y P < 0,001; Fig. 1 , G y H), lo que coincide con los hallazgos de que la proteína S del SARS-CoV-2 es el principal objetivo de los anticuerpos neutralizantes. La proteína S del SARS-CoV-2 comparte una alta similitud de secuencia con el SARS-CoV altamente virulento (76 % de identidad de secuencia) y muestra una baja homología de secuencia con MERS-CoV (34 % de identidad de secuencia). Se ha informado de reactividad cruzada serológica entre coronavirus;8,10,28,29 sin embargo, los datos sobre la evaluación de seguimiento longitudinal de la reactividad cruzada de anticuerpos contra el SARS-CoV-2 hacia otros coronavirus siguen siendo limitados. Determinamos anticuerpos de unión cruzada y neutralización cruzada en sueros longitudinales de individuos infectados con SARS-CoV-2. Los resultados mostraron que más del 80 % de las muestras de suero de los pacientes se unieron a las proteínas S del SARS-CoV y/o MERS-CoV dentro del mes posterior al inicio de los síntomas, y el 27 % de las muestras exhibieron doble reactividad cruzada (Fig. 1, I). La reactividad a la proteína S del SARS-CoV tuvo una proporción mayor (73%) que la del MERS-CoV (35%) entre las muestras analizadas en un período temprano (1-30 días después del inicio de la enfermedad) (Fig. 1, I). Los anticuerpos de doble unión cruzada y de unión cruzada contra el SARS-CoV mostraron una disminución gradual con el tiempo, con solo un 8% de muestras de doble unión cruzada y un 20% de muestras de SARS-CoV de unión cruzada simple entre 180 y 220 días después del inicio de la enfermedad (Fig. 1). , I; en el repositorio en línea disponible en www.jacionline.org, ver Fig E4, A; Fig E5, A; y Fig E6 en el repositorio en línea de este artículo en www.jacionline.org). Curiosamente, la positividad de los anticuerpos reactivos a la proteína MERS-CoV S se mantuvo relativamente constante a lo largo del tiempo (Fig. 1, I). A diferencia de la alta capacidad de unión cruzada, solo una pequeña cantidad de muestras de suero de pacientes neutralizaron cruzadamente los pseudovirus del SARS-CoV y/o MERS-CoV (Fig. 1, I; Fig. E4, B; Fig. E5, B; y consulte la Fig. E7 en la Repositorio en línea). Aproximadamente el 27 % de las muestras recolectadas entre 1 y 30 días después del inicio de los síntomas presentaron actividad de neutralización cruzada, y este número se redujo al 20 % entre 180 y 220 días, con cambios más dramáticos en la actividad de neutralización cruzada del SARS-CoV (Fig. 1, I). ). Una mayor proporción de muestras neutralizaron cruzadamente el SARSCoV que el MERS-CoV dentro de los 30 días posteriores al inicio de la enfermedad. Vale la pena señalar que a pesar de proporciones similares de muestras que muestran neutralización cruzada de SARS-CoV y MERS-CoV, los valores de NT50 para MERS-CoV fueron mucho más bajos que los del SARSCoV entre las muestras de suero que fueron positivas para la neutralización cruzada (Fig. E4, B; Figura E5, B; Figura E7).

planta cistanche que aumenta el sistema inmunológico
La infección por SARS-CoV-2 provoca la activación de la producción de citoquinas
Para caracterizar exhaustivamente los cambios inmunológicos después de la infección por SARS-CoV-2, evaluamos más a fondo los cambios en la dinámica de los niveles de citoquinas en el suero de pacientes con COVID-19. Se utilizaron cincuenta y cinco muestras de suero longitudinales que se recolectaron dentro de los primeros 2 meses posteriores al inicio de los síntomas para la detección de la producción de citocinas mediante microarrays basados en proteínas. Se observaron niveles séricos elevados de múltiples citocinas durante el primer mes de la enfermedad, incluidas IL-1a (proinflamatoria), IL-6 (proininflamatoria) e IL-10 (antiinflamatoria). ), que se han relacionado con el síndrome de liberación de citocinas en casos graves de COVID-19,39,40, así como con IFN-g (tipo TH1) e IL-4 (tipo TH2) (Fig. 2, A, y Fig E8 en el repositorio en línea disponible en www.jacionline.org). Específicamente, los niveles séricos de IL-6, IL-10 e IFN-g aumentaron dentro de los 15 días posteriores al inicio de los síntomas en los pacientes y disminuyeron en fases posteriores, mientras que la liberación de IL-1 Se demostró que a e IL-4 aumentaban notablemente durante 16 a 30 días desde el inicio de la enfermedad y descendían rápidamente a la normalidad después (Fig. 2, A). El análisis de correlación indicó una asociación lineal débil o nula entre las respuestas de anticuerpos específicos de antígeno y la producción de citoquinas después de la infección por SARS-CoV-2, aunque se observó una significación estadística entre los niveles de IL-10 y SARS-CoV{{ 34}} Anticuerpo de unión a proteína N (r 5 0.321 y P < .05), entre la producción de IL-1b y anticuerpo de unión a proteína S (r 5 20.335 y P<.05), and between TNF-a and S protein binding antibody levels (r 5 20.335 and P <.05; see Fig E9 in the Online Repository). To allow direct visualization and comparison among patient samples across multiple cytokine responses over time, we constructed a heat map showing fold changes in cytokine release relative to the healthy donor control group (Fig 2, B). Consistent with our findings presented above, elevated serum cytokine levels after SARS-CoV-2 infection were predominantly observed during the acute phase and an early period of convalescence (within 30 days after disease onset) (Fig 2, A and B). Among cytokines tested, proinflammatory IL-6 exhibited the most robust response, with a 4.9-fold increase and a 2.9-fold increase on average for samples collected during 1 to 15 days and 16 to 30 after onset of symptoms, respectively (Fig 2, B). Of note, 1 serum sample (sample Pt-S22, collected on day 18 after disease onset) obtained from a COVID–19–infected individual with moderate disease, exhibited a marked increase in the production of multiple proinflammatory cytokines, including IL-1a, IL-1b, IL-6, and TNF-a (Fig 2, B). Additionally, hyperproduction of cytokines including IL- 1a, IL-4, IL-6, IL-10, IL-13, and IFN-g was also detected in 1 sample (sample Pt-S11, collected at day 15 after disease onset) collected from a severe case of COVID-19; presumably, these are associated with disease severity and outcome (Fig 2, B). These results indicate broad inflammatory activation and changes over time involving the concomitant release of proinflammatory and anti-inflammatory cytokines as well as TH1-type and TH2-type cytokines in COVID-19 patients.
El mapeo de epítopos de todo el proteoma identifica epítopos dominantes que median respuestas inmunes humorales persistentes en pacientes con COVID-19
Para caracterizar mejor las características distintivas de la inmunidad humoral al SARS-CoV-2 a lo largo del tiempo, aplicamos un mapeo de epítopos de todo el proteoma utilizando micromatrices basadas en péptidos. Se generó una biblioteca de péptidos que cubría el proteoma del SARS-CoV-2 y se inmovilizó en portaobjetos, en los que cada péptido tenía 15 aa de longitud con una superposición de 11 aa. Un total de 51 muestras de suero longitudinales de 19 pacientes con enfermedades asintomáticas (n 5 1) o leves (n 5 2) a moderadas (n 5 15) o graves (n 5 1 ) Se probaron infecciones por SARS-CoV-2 (Tabla I). Para lograr números de muestreo, intervalos y puntos de tiempo relativamente equilibrados, se recolectaron muestras secuencialmente en 2 o 3 puntos de tiempo de cada participante con COVID-19, entre 16 y 219 días después de la aparición de los síntomas. La mayoría de los pacientes (18/19) generaron anticuerpos neutralizantes después de la infección viral, excepto el único individuo con infección asintomática (Tabla I). Según los diferentes momentos de muestreo, las muestras se dividieron en 3 grupos: días 10-60 (n 5 18), días 100-150 (n 5 18) y días {{28 }} (n5 15). Se realizó una evaluación longitudinal de los perfiles de epítopos del virus en pacientes con COVID-19 para los anticuerpos IgG e IgM séricos, y se utilizó una combinación de sueros de 20 donantes sanos como control negativo. Utilizando la micromatriz de proteoma SARS-CoV-2, se determinó y analizó la cinética de las respuestas de los anticuerpos de unión a péptidos para (1) la intensidad de la señal de unión y (2) el porcentaje de muestras reactivas positivas (tasa positiva) para cada péptido. . Con base en el valor de corte para una respuesta de unión a péptido positiva, que se estableció como el doble de la intensidad de la señal del control negativo, identificamos un total de 460 péptidos positivos para IgG y 479 péptidos positivos para IgM que fueron reactivos con al menos 1 paciente. muestra de suero. Los números de péptidos positivos y la distribución de las respuestas en diferentes marcos de lectura abiertos (ORF) del SARS-CoV-2 fueron relativamente estables entre los diferentes grupos de muestreo, con una tendencia a una ligera disminución en los números de péptidos positivos a lo largo del tiempo (Fig. 3, A). La mayor reactividad se identificó en la poliproteína replicasa ORF1ab, que es el ORF más grande y abarca más de dos tercios de todo el genoma (Fig. 3, A). Curiosamente, observamos grados de correlación de moderados a fuertes entre las respuestas positivas de unión a péptidos y los niveles de citocinas séricas poco después de la infección por SARS-CoV-2 (días 10-60 después del inicio de la enfermedad; consulte la figura E10 en el repositorio en línea en www.jacionline.org). Se demostró que el número de péptidos de unión positivos para IgM está asociado con los niveles séricos de IL-6 e IL-10; Asimismo, la intensidad de señal promedio de los péptidos reactivos totales y la de los péptidos de unión a ORF1ab para IgM presentaron asociaciones positivas con la producción de IL-6 e IFN-g en muestras de suero. Estos datos sugieren que los cambios en los niveles de citocinas después de la infección por SARS-CoV-2 pueden influir en la magnitud y amplitud de los epítopos reconocidos por las respuestas humorales específicas de antígenos. Basándonos en la identificación de epítopos positivos, seleccionamos además los epítopos más comunes que permanecieron consistentemente reactivos en más del 80% de las muestras de COVID-19 entre cada uno de los 3 grupos de muestreo (denominados epítopos dominantes y persistentes). Los resultados revelaron que estos epítopos altamente dominantes capaces de mediar respuestas inmunes humorales a largo plazo estaban ubicados en la poliproteína ORF1ab y la proteína S del SARS-CoV-2, con más epítopos reconocidos por los anticuerpos IgM (n 5 33) que Anticuerpos IgG (n 5 10) (Figura 3, B y Tabla II; consulte las Figuras E11 y E12 en el repositorio en línea en www.jacionline.org). La poliproteína ORF1ab poseía el número máximo de epítopos dominantes que median respuestas a largo plazo, y los epítopos estaban ampliamente distribuidos en las regiones de proteínas no estructurales (nbsp) 2-5, nbsp 8-10, nbsp 12-14, y nbsp 16 (Tabla II). En particular, identificamos un epítopo inmunodominante, 2073 (ORF1ab, aa 5801-5815), que podría ser reconocido por anticuerpos IgG e IgM del 100% de los pacientes con COVID-19, independientemente de los puntos temporales de muestreo de suero (Fig. 3, B y Tabla II; consulte las Figuras E13 y E14 en el Repositorio en línea). Este péptido altamente reactivo se encuentra dentro de la región helicasa (nsp 13) de la poliproteína ORF1ab, que es esencial para desenrollar los moldes de ARN bicatenario durante la replicación del SARS-CoV-2.41 Entre los péptidos seleccionados de ORF1ab, dos péptidos inmunodominantes con las intensidades de señal promedio más altas reconocidas por los anticuerpos IgG, el número 1985 (ORF1ab, aa 5449-5463) y el número 2073 (ORF1ab, aa 5801-5815), están ubicados en nsp 13. Para las respuestas de IgM, el péptido 685 (ORF1ab, aa 249-263) en nsp 2 y el péptido 1985 (ORF1ab, aa 5449-5463) en nsp 13 presentaron las intensidades de unión más robustas (Fig. 3, B). Teniendo en cuenta la variación en las señales de referencia (sueros combinados de donantes sanos) para diferentes péptidos (Fig. 3, B), calculamos además los cambios en las intensidades de las señales con respecto a cada péptido clave, en relación con el grupo de control sano. Los resultados mostraron que el péptido 2073 (unión a IgG) y el péptido 1985 (unión a IgM) ubicados en la región nsp 13 mantuvieron las intensidades de unión del péptido superior (cambio en veces) entre los sueros de pacientes recolectados hasta 180 a 220 días (Fig. E13 y Fig. E14).

FIG 2. Cinética de producción de citocinas en pacientes con COVID-19. A, Los niveles de producción de citoquinas en 55 muestras de suero recolectadas de 16 pacientes con COVID-19 durante la fase aguda y una etapa temprana de convalecencia se detectaron mediante ELISA basado en microarrays de proteínas (días 1-15, n 5 11; días 16-30, n 5 26; días 31-61, n 5 18; donantes sanos, n 5 20). Cada punto representa una muestra de suero individual; Las líneas de puntos indican el límite de detección. La significancia estadística se determinó mediante ANOVA de 1-vías con comparaciones múltiples de Tukey. *P < 0,05, **P < 0,01 y ****P < 0,0001. B, Cambio en veces de cada nivel de producción de citoquinas en pacientes con COVID-19 que se muestra en (A) en comparación con los valores medios de 20 muestras de donantes sanos. Cada columna indica una muestra de suero distinta recolectada en los momentos indicados después del inicio de los síntomas; cada fila representa 1 citoquina individual analizada.
TABLA I. Características de los pacientes con COVID-19 y cohortes de muestra en el mapeo de epítopos

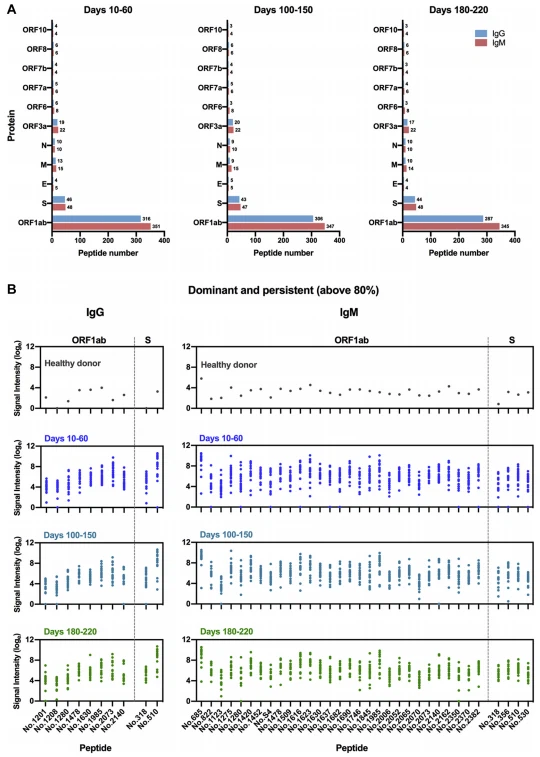
FIG 3. Reconocimiento de IgM e IgG de epítopos dominantes que contribuyen a las respuestas de anticuerpos a largo plazo en individuos infectados por SARS-CoV-2. Análisis longitudinal del reconocimiento sérico de epítopos en 19 individuos con COVID-19 utilizando una micromatriz de péptidos que cubre el proteoma del SARS-CoV-2. El valor de corte para la respuesta positiva de la unión de péptidos en muestras de pacientes (n 5 51) se estableció como el doble de la intensidad de la señal de los sueros combinados de 20 donantes sanos. A, Recuentos de péptidos y distribución de péptidos de unión positivos que fueron detectables en 1 o más muestras recolectadas en 10-60 días (n 5 18), 100-150 días (n 5 18), y 180- 220 días (n 5 15) después del inicio de la enfermedad. Los números indican el total de epítopos IgG e IgM identificados de cada ORF. B, Intensidades de señal de epítopos de IgG e IgM dominantes y persistentes (eje x) que fueron reactivos de manera sostenible en más del 80 % de las muestras dentro de los 3 puntos de tiempo de muestreo. Cada punto indica los sueros combinados de donantes sanos (arriba) o una muestra de suero de paciente distinta recogida en los momentos indicados después de la aparición de los síntomas. E, proteína de la envoltura.
TABLE II. Epitopes with >Tasa positiva del 80% en los 3 puntos de tiempo de muestreo

Los epítopos dominantes y persistentes de la proteína S del SARS-CoV-2 se encuentran en las subunidades NTD y S2
Se identificaron un total de 4 epítopos dominantes y persistentes de la proteína S del SARSCoV-2: péptido 318 (S, aa 45-59) y péptido 356 (S, aa 197-211), que se ubican dentro de la región NTD; el péptido 510 (S, aa 813-827), que cubre el sitio de escisión S2' y partes de la FP de la subunidad S2, y el péptido 530 (S, aa 893-907), que se encuentra en la región de conexión entre FP y la región de repetición de la primera heptada de la subunidad S2 (Fig. 3, B y Tabla II). Entre estos péptidos clave de la proteína S que seleccionamos, el péptido 318, ubicado en el NTD de la proteína S, poseía la intensidad de unión más robusta (cambio de veces en relación con el control; Fig. E13 y Fig. E14). Los análisis estructurales revelaron que estos epítopos están completamente expuestos en la superficie de la proteína S monomérica; sin embargo, algunos residuos de epítopos de los péptidos 318, 356 y 530 están ocultos bajo la superficie de la proteína S trimérica (Fig. 4, A y B), lo que sugiere que tanto el monómero S como las estructuras del trímero son reconocidos eficientemente por el sistema inmunológico del huésped bajo ciertas condiciones. circunstancias. Para ser específicos, 2 segmentos de bucle del péptido 318 (aa 45-46 y aa 56-59) están expuestos en la proteína S trimérica, con la cadena b central enterrada en el interior; y la mayoría de los residuos del péptido 356 son accesibles en la superficie, incluida una cadena b central (aa 203-209) y un segmento de bucle (aa 210-211). El péptido 510 contiene un sitio de escisión S2' y una hélice central de FP, los cuales están completamente presentados en la superficie de la proteína S; Los residuos del péptido 530 son en su mayoría crípticos, con solo una pequeña fracción del bucle (aa 893-895) expuesta en la proteína S trimérica (Fig. 4, C). El análisis de homología de secuencia entre 7 coronavirus humanos comunes reveló que 2 epítopos ubicados en la subunidad S2 (péptidos 510 y 530) comparten una alta identidad de secuencia con otros coronavirus, lo que sugiere una reactividad cruzada serológica dirigida a estos epítopos entre los coronavirus humanos (Fig. 4, D). La secuencia del péptido 318 mostró una gran similitud con el SARSCoV, mientras que se mostró un bajo nivel de homología de secuencia para el péptido 356 entre los coronavirus, lo que sugiere respuestas de anticuerpos específicas del SARS-CoV-2 dirigidas a esta región (Fig. 4, D). Teniendo en cuenta las nuevas variantes emergentes y circulantes del SARS-CoV-2 a nivel mundial, realizamos además un alineamiento de secuencias con respecto a los epítopos clave de la proteína S entre las primeras cepas del SARS-CoV-2 (Wuhan-Hu{{52} }) y 5 variantes de preocupación (Alfa, Beta, Gamma, Delta y Omicron), así como 2 variantes de interés (Lambda y Mu), según la clasificación de variantes de virus de la Organización Mundial de la Salud (actualizada el 30 de noviembre de 2021). ). Los resultados mostraron que las secuencias de estos epítopos dominantes y persistentes son casi idénticas entre las variantes analizadas, excepto por una única mutación N211I identificada en la nueva variante Omicron (Fig. 4, E). Estos datos indican que los anticuerpos generados por las primeras cepas de SARS-CoV-2 pueden reconocer consistentemente las variantes circulantes actuales y que estos epítopos dominantes pueden ser capaces de mediar respuestas de anticuerpos sostenidas a largo plazo en la infección por SARS-CoV-2 variantes. Para determinar más a fondo las características inmunológicas de los epítopos identificados en la proteína S y para investigar más a fondo el valor potencial de estos epítopos de proteína S como candidatos a vacunas peptídicas, realizamos un estudio de inmunización en ratones utilizando péptidos seleccionados. Se inocularon ratones BALB/c 3 veces con cada péptido en presencia de alumbre y adyuvantes CpG (Fig. 4, F). Entre los 4 péptidos seleccionados, la vacunación con el péptido 356 provocó anticuerpos específicos de antígeno después de la segunda y tercera dosis (Fig. 4, G). Los resultados del ensayo de neutralización sérica revelaron que la inmunización con péptidos lineales no generó niveles significativos de anticuerpos neutralizantes contra el SARS-CoV-2 (Fig. 4, H), lo que sugiere que estos péptidos lineales funcionan mal para inducir respuestas robustas de anticuerpos neutralizantes.
La proteína N del SARS-CoV-2 carece de la mayoría de los epítopos reactivos que median respuestas de anticuerpos duraderas después de una infección viral
Varios estudios han dilucidado la potente antigenicidad de la proteína N del SARS-CoV-2.4,11,12 Sin embargo, no pudimos identificar los epítopos dominantes y persistentes ubicados en la proteína N según los criterios de selección actuales. (tasa positiva superior al 80 % en los 3 puntos de tiempo de muestreo). Para la evaluación longitudinal de los perfiles de epítopos de la proteína N en individuos con COVID-19, llevamos a cabo una segunda ronda de detección de epítopos que se basó en datos obtenidos del microarray de péptidos para la selección de epítopos subdominantes que mantuvieron consistentemente reactividad positiva. en más del 60% de las muestras de COVID-19 para cada uno de los 3 puntos de tiempo de muestreo (denominados epítopos subdominantes y persistentes). Se identificaron un total de 4 epítopos subdominantes y persistentes de la proteína N del SARS-CoV-2, entre los cuales el péptido 2455 (N, aa 213-227) presentó reactividad a anticuerpos tanto IgG como IgM en COVID{{16 }} pacientes, con niveles relativamente más altos de intensidad de señal (Fig. 5, A y B, y consulte la Tabla E4 en el repositorio en línea en www.jacionline.org). Los 2 péptidos superpuestos, el péptido 2455 (N, aa 213-227) y el péptido 2456 (N, aa 217-231), están ubicados en la región conectora rica en Ser/Arg entre el dominio de unión al ARN N-terminal. y dominio de dimerización C-terminal de la proteína N. El péptido 2482 (N, aa 321-335) y el péptido 2491 (N, aa 357-371) están ubicados total o parcialmente dentro del dominio de dimerización de la proteína N (Tabla E4). Debido a la falta de estructuras 3-D con respecto a la conformación intacta de la proteína N, solo realizamos análisis estructurales de 2 epítopos identificados en la estructura dimérica del dominio de dimerización C-terminal. Los residuos del péptido 2482 forman cadenas 2 b que están dispuestas de manera antiparalela en las interfaces de dimerización, mientras que aa 357-364 del péptido 2491 forman estructuras basadas en hélices que se ubican en los extremos opuestos del dímero (Fig. 5, C). . La alineación de secuencias entre las primeras variantes del SARS-CoV-2 (cepa Wuhan-Hu-1) y 7 variantes emergentes reveló además que las secuencias de estos epítopos subdominantes y persistentes en la proteína N son casi idénticas entre las variantes circulantes actuales, con una una única sustitución G215C del péptido 2455 que se produce en la variante Delta y una única mutación G214C del péptido 2455 identificada en la variante Lambda, lo que sugiere que los anticuerpos dirigidos a estos péptidos reconocen potencialmente el antígeno de las variantes emergentes del SARS-CoV-2 (Fig. 5, D ).

FIG 4. Epítopos dominantes de la proteína de pico del SARS-CoV-2 en términos de mediación de respuestas inmunitarias humorales duraderas. A y B, Ubicaciones de los epítopos dominantes y persistentes en las estructuras 3-D de la proteína S monomérica (A) y trimérica (B) (PDB ID: 6VXX). Los epítopos están resaltados en verde (péptido 356, aa 197-211), rojo (péptido 318, aa 45-59), azul (péptido 510, aa 813-827) y morado (péptido 530, aa 893-907), respectivamente. Los tres monómeros S en conformación cerrada se representan en gris, rosa y cian, respectivamente. C, Análisis detallado de la estructura de los epítopos dominantes en la proteína S del SARS-CoV-2 en el estado cerrado del trímero S (PDB ID: 6VXX). D, Alineación de secuencia de epítopos identificados entre los coronavirus humanos comunes. Los residuos de epítopos que se conservan entre el SARS-CoV-2 y otros coronavirus humanos están sombreados en gris. E, Análisis de conservación de epítopos del SARS-CoV-2 temprano (cepa Wuhan-Hu-1) y 7 variantes emergentes. Los puntos negros representan residuos idénticos entre la cepa Wuhan-Hu-1 y la indicada.

FIG 5. Los epítopos subdominantes ubicados en la proteína de la nucleocápside del SARS-CoV-2 son capaces de mediar respuestas de anticuerpos persistentes. A, frecuencias de reconocimiento de IgG e IgM de péptidos subdominantes (duraderamente reactivos en más del 60 % de las muestras) entre muestras de suero de pacientes recolectadas en múltiples momentos después del inicio de la enfermedad. B, Cinética de intensidad de señal de epítopos subdominantes identificados a lo largo del tiempo. Cada punto representa una muestra de suero distinta obtenida de pacientes con COVID-19 en los momentos indicados después de la aparición de los síntomas. Las líneas horizontales de puntos indican los valores límite de respuesta positiva para cada péptido. C, análisis detallado de la estructura de epítopos en el dominio de dimerización C-terminal de la proteína N (PDB ID: 6YUN). Los epítopos están etiquetados en azul (péptido 2482, aa 321-335) y marrón (péptido 2491, aa 357-364). Las dos estructuras monoméricas se representan en gris y cian, respectivamente. D, Análisis de alineación de secuencia de los epítopos de proteína N identificados entre el SARS-CoV-2 temprano (cepa Wuhan-Hu-1) y 7 variantes emergentes. Los puntos negros indican secuencias idénticas entre la cepa Wuhan-Hu-1 y la variante indicada. Los cambios en la secuencia de aminoácidos están resaltados en rojo.

FIG 6. Epítopos del revestimiento con alta intensidad de unión y frecuencias reactivas decrecientes con el tiempo, reconocidos por individuos infectados por SARS-CoV-2. A y B, análisis longitudinal y distribución de péptidos identificados que muestran una alta intensidad de señal de unión (por encima de la media de 1 DE de intensidades de señal de todas las muestras analizadas) pero una tasa positiva decreciente con el tiempo. La frecuencia de reconocimiento (A) y la intensidad de la señal (B) de los epítopos se trazaron con 3 puntos de tiempo de muestreo después del inicio de los síntomas. Cada punto en (B) representa una muestra de suero de un paciente individual recolectada en los momentos indicados después del inicio de los síntomas; Las líneas horizontales de puntos indican los valores límite de positividad para cada péptido. El análisis de significación estadística se realizó con base en el software Limma of R v3.6.3. *P < 0,05 y **P < 0,01. C, Comparaciones de ubicación y secuencia de 2 epítopos adyacentes, el péptido 510 (dominante y persistente) y el péptido 511 (alta intensidad de señal y positividad decreciente con el tiempo), en la estructura de la proteína S del SARS-CoV-2 (PDB ID: 6ZGI) . Las regiones superpuestas entre los 2 epítopos están resaltadas en verde; Las secuencias únicas están etiquetadas en rojo y azul.
El análisis serológico longitudinal identifica epítopos con alta intensidad de señal pero reactividad decreciente con el tiempo
Además de los epítopos altamente reactivos seleccionados que son responsables de las respuestas inmunes humorales sostenidas mencionadas anteriormente, identificamos y caracterizamos además un panel de 9 péptidos positivos que mostraron intensidades de unión robustas (por encima de la media de 1 DE de intensidades de señal de todas las muestras analizadas) con una tendencia de disminución de la reactividad (cambios en la tasa positiva por encima del 20%) entre muestras de suero de pacientes con COVID-19 a lo largo del tiempo, de acuerdo con una tendencia general de disminución de las respuestas inmunitarias humorales. Estos epítopos están ubicados dentro de los 3 antígenos dominantes: proteínas ORF1ab, S y N (Fig. 6, A; y consulte la Tabla E5 en el repositorio en línea en www.jacionline.org). Además, se observaron reducciones significativas en las intensidades de señal de 4 péptidos de las proteínas ORF1ab (péptidos 784-IgG, 1617-IgM y 1986-IgM) y N (péptido 2457-IgG). entre muestras de un período inicial de puntos de tiempo de muestreo (días 10-60 después del inicio de la enfermedad) y la fase posterior de puntos de tiempo de muestreo (días 100-150 o días 180-220 después del inicio de los síntomas) (Fig. 6 , B). En particular, a pesar de superponerse en gran medida entre sí, 2 péptidos de la proteína S, el péptido 510 (dominante y persistente; Fig. 3, B) y el péptido 511 (alta intensidad de señal y tasa positiva decreciente con el tiempo; Fig. 6, A) exhibieron diferentes patrones de reactividad entre muestras de suero de pacientes a lo largo del tiempo. El análisis de secuencia y ubicación indicó que el péptido 510 contiene un sitio de escisión S2' y aminoácidos adicionales de 813-SKRS-816, mientras que el péptido 511 está completamente dentro del FP con 828-LADA{{29 extendida }} residuos que están completamente expuestos en la superficie de la proteína S trimérica (Fig. 6, C). Estos resultados revelaron nuevas características de los epítopos que, en última instancia, pueden contribuir a una inmunidad humoral más duradera y más fuerte contra el SARS-CoV-2.
DISCUSIÓN
Una caracterización sistemática de las respuestas inmunitarias a largo plazo a la infección por SARS-CoV-2 es fundamental para el desarrollo de mejores diagnósticos, intervenciones terapéuticas eficaces y vacunas. En el estudio actual, realizamos un análisis longitudinal integral de pacientes con COVID-19 durante un seguimiento de 180 a 220 días, que mostró respuestas inmunes humorales persistentes y producción activada de citocinas después de la infección viral.
Significativamente, al aprovechar la micromatriz basada en péptidos que abarca el proteoma del SARS-CoV-2, revelamos aún más la cinética del reconocimiento de epítopos e identificamos un panel de epítopos dominantes capaces de mediar en la inmunidad humoral a largo plazo. Los hallazgos que informamos aquí sobre la longevidad de las respuestas inmunes humorales después de la infección por SARS-CoV-2 confirman algunos datos previamente publicados5,10,12,13,42, pero los amplían mediante la realización de perfiles serológicos profundos y la detección de epítopos utilizando muestras de suero longitudinales. de personas con COVID-19 a través del enfoque de microarrays de todo el proteoma. En este estudio, identificamos 4 epítopos dominantes (péptidos 318, 356, 510 y 530) dentro de la proteína S del SARS-CoV-2 que era capaz de reaccionar de manera persistente con más del 80 % de los pacientes con COVID-19 muestras analizadas, hasta 180 a 220 días después de la aparición de los síntomas. El péptido 510 (S, aa 813-827), que comprende el sitio de escisión S2 y la FP de la subunidad S2, se ha identificado comúnmente en estudios previos de otros grupos.26,28,32-34 Los análisis funcionales indicaron anticuerpos apuntar a esta región puede exhibir una potencia de neutralización limitada contra el SARS-CoV-226,33 a pesar de estar altamente expuesto en la superficie de la proteína S (Fig. 4, AC). En el caso del péptido 530 (S, aa 893-907), que está situado entre la FP y la región de repetición de la primera heptada de la subunidad S2, los residuos generalmente están enterrados dentro de la estructura trimérica de la proteína S, lo que la convierte en de difícil acceso a través de anticuerpos neutralizantes robustos contra el SARS-CoV-2 (Fig. 4, AC). Además, también se seleccionaron dos péptidos dirigidos por S1-NTD que podrían mediar respuestas de anticuerpos a largo plazo del SARS-CoV-2. Los análisis relacionados con la secuencia y la ubicación del péptido indicaron que los residuos de estos 2 péptidos, el péptido 318 (S, aa 45-59) y el péptido 356 (S, aa 197-211), están muy cerca de los epítopos reconocidos. por anticuerpos que mejoran la infección23,25, pero aparte de los sitios clave de anticuerpos neutralizantes altamente potentes dirigidos a NTD de la subunidad S1,16,19,43, lo que sugiere la posibilidad de reconocimiento de epítopos por parte de anticuerpos no neutralizantes hacia estos 2 péptidos identificados. Además de los detalles mencionados anteriormente, la inmunización de ratones con péptidos seleccionados indicó además la baja eficacia de estos péptidos lineales con dominio de unión sin receptor para inducir respuestas robustas de anticuerpos neutralizantes (Fig. 4, G). En conjunto, estos datos sugieren que los epítopos lineales dominantes que median las respuestas inmunitarias humorales a largo plazo en la infección por SARS-CoV-2 probablemente inducen anticuerpos con potencia neutralizante limitada o nula. Una comprensión más completa del panorama de epítopos de los anticuerpos contra el SARS-CoV-2, especialmente los epítopos dirigidos a la proteína S, proporciona nuevos conocimientos sobre la disección funcional de los anticuerpos, lo que facilita aún más el diseño de vacunas innovadoras y racionales. Los anticuerpos neutralizantes confieren protección para eliminar las infecciones virales, mientras que los anticuerpos no neutralizantes pueden desempeñar un papel beneficioso, neutral o incluso perjudicial durante la eliminación del virus. Los anticuerpos no neutralizantes brindan protección adicional in vivo a través de una variedad de funciones efectoras mediadas por Fc en el contexto de la fagocitosis dependiente de anticuerpos y la citotoxicidad dependiente de anticuerpos. Por el contrario, algunos estudios han propuesto la posibilidad de un papel patogénico de los anticuerpos no neutralizantes en la infección por coronavirus. Estudios anteriores que utilizaron múltiples tipos de vacunas candidatas para el SARS-CoV y el MERS-CoV observaron una inmunopatología mejorada en animales pequeños y primates no humanos vacunados después de la exposición al virus.24,44-50 Más recientemente, estudios de 2 grupos informaron que las vacunas no neutralizantes Los anticuerpos dirigidos a los NTD de la proteína S del SARS-CoV-2 fueron capaces de mejorar la infección viral in vitro mediante mecanismos independientes del receptor Fcg,23,25 aunque se ha demostrado que los anticuerpos potenciadores de la infección administrados pasivamente en modelos animales protegen contra el SARS. -Infección por CoV-2 in vivo. Teniendo en cuenta las funciones controvertidas de los anticuerpos durante la infección por coronavirus, se requieren más investigaciones para validar el papel potencial de los anticuerpos en el reconocimiento de estos epítopos dominantes y persistentes en la lucha contra la infección viral in vivo. La siguiente etapa del diseño racional de una vacuna contra el SARS-CoV-2 podría concebirse generando anticuerpos neutralizantes muy potentes y anticuerpos protectores no neutralizantes, junto con una reducción de la presentación de epítopos que potencian la infección o epítopos inmunodominantes que no tienen efectos benéficos. Aunque varios estudios previos solo se han centrado en la proteína S del SARS-CoV-2 con el objetivo de delinear las funciones de los anticuerpos con respecto a la neutralización, realizamos un mapeo integral de epítopos de todo el proteoma e identificamos un panel de epítopos dentro de la poliproteína ORF1ab que fue reconocido consistentemente por una alta proporción de muestras de suero de pacientes a lo largo del tiempo. Aunque estos péptidos dirigidos a ORF1ab distribuidos en las múltiples proteínas no estructurales pueden no provocar anticuerpos funcionales dirigidos al virión del SARS-CoV-2, podrían ser aplicables como herramienta de diagnóstico para ayudar a diferenciar la infección natural de la vacunación. Con el creciente número de receptores de vacunas en todo el mundo, las pruebas serológicas actuales basadas en la proteína S y la proteína N enfrentan desafíos como enfoque eficaz para ayudar a las pruebas moleculares para la detección de la infección por SARS-CoV-2, y también para la determinación del estado inmunológico después de una infección viral. Al aprovechar los péptidos más comunes y persistentemente reactivos dentro del ORF1ab entre las personas infectadas con COVID, el diagnóstico serológico de la infección natural se llevará a cabo sin tener en cuenta el estado de vacunación que involucra la proteína S basada en el dominio de unión al receptor. vacunas basadas en virus inactivados y basadas en virus. Se necesitan estudios futuros para evaluar la reactividad, sensibilidad y especificidad de los péptidos ORF1ab identificados en cohortes más grandes que incluyan tanto a individuos infectados por SARSCoV-2 como a los receptores de la vacuna. Además, será necesaria una evaluación adicional de la eficacia de la detección mediante múltiples estrategias de combinación de péptidos para superar la menor sensibilidad de los péptidos en comparación con la proteína de longitud completa y la posible reactividad cruzada entre los coronavirus humanos comunes. Las principales limitaciones de nuestro estudio son las relativamente pocas muestras obtenidas de una cohorte de pacientes pequeña y la mayoría de los participantes experimentaron enfermedades de COVID no graves. Esto puede limitar algunas de nuestras conclusiones con respecto a la frecuencia de respuesta positiva y la magnitud de las respuestas inmunes, que pueden variar según la gravedad de la enfermedad. Sin embargo, los datos presentados en este estudio proporcionan información valiosa sobre la cinética de las respuestas inmunitarias a lo largo del tiempo después de la infección por SARS-CoV-2 y las características de los epítopos dominantes capaces de mediar la inmunidad humoral sostenida en personas con COVID-19. En conjunto, estos hallazgos ofrecen una comprensión más profunda de la longevidad de la inmunidad natural inducida por una infección viral y tienen amplias implicaciones para estrategias de vacunación innovadoras y mejores enfoques de diagnóstico.
REFERENCIAS
1. Lu R, Zhao X, Li J, Niu P, Yang B, Wu H, et al. Caracterización genómica y epidemiología del nuevo coronavirus de 2019: implicaciones para los orígenes del virus y la unión al receptor. Lanceta 2020;395:565-74.
2. Organización Mundial de la Salud (OMS). Panel de control del coronavirus (COVID-19) de la OMS, 2021. Disponible en: https://COVID19.who.int/. Consultado el 30 de noviembre de 2021.
3. Wu Z, McGoogan JM. Características y lecciones importantes del brote de enfermedad por coronavirus de 2019 (COVID-19) en China: resumen de un informe de 72314 casos del Centro Chino para el Control y la Prevención de Enfermedades. JAMA 2020;323:1239-42.
4. Rydyznski Moderbacher C, Ramirez SI, Dan JM, Grifoni A, Hastie KM, Weiskopf D, et al. Inmunidad adaptativa específica de antígeno al SARS-CoV-2 en COVID agudo-19 y asociaciones con la edad y la gravedad de la enfermedad. Celda 2020;183:996-1012.e19.
5. Wu J, Liang B, Chen C, Wang H, Fang Y, Shen S, et al. La infección por SARS-CoV-2 induce respuestas inmunes humorales sostenidas en pacientes convalecientes después de COVID sintomático-19. Nat Commun 2021;12:1813.
6. Long QX, Liu BZ, Deng HJ, Wu GC, Deng K, Chen YK, et al. Respuestas de anticuerpos al SARS-CoV-2 en pacientes con COVID-19. Nat Med 2020;26:845-8.
7. Sterlin D, Mathian A, Miyara M, Mohr A, Anna F, Claer L, et al. La IgA domina la respuesta temprana de anticuerpos neutralizantes al SARS-CoV-2. Sci Transl Med 2021;13: eabd2223.
8. Zhang J, Wu Q, Liu Z, Wang Q, Wu J, Hu Y, et al. Respuestas de células T foliculares auxiliares circulantes específicas de picos y respuestas de anticuerpos de neutralización cruzada en individuos convalecientes de COVID-19. Nat Microbiol 2021;6:51-8.
9. Wang P, Liu L, Nair MS, Yin MT, Luo Y, Wang Q, et al. Las respuestas de anticuerpos neutralizantes del SARS-CoV-2 son más sólidas en pacientes con enfermedad grave. Microbios emergentes infectan 2020;9:2091-3.
10. Vanshylla K, Di Cristanziano V, Kleipass F, Dewald F, Schommers P, Gieselmann L, et al. Cinética y correlatos de la respuesta de anticuerpos neutralizantes a la infección por SARSCoV-2 en humanos. Microbio huésped celular 2021;29:917-29.e4.
11. Xiang T, Liang B, Fang Y, Lu S, Li S, Wang H, et al. Disminución de los niveles de anticuerpos neutralizantes contra el SARS-CoV-2 en pacientes convalecientes de COVID-19 un año después de la aparición de los síntomas. Frente Inmunol 2021;12:708523.
12. Wang Z, Muecksch F, Schaefer-Babajew D, Finkin S, Viant C, Gaebler C, et al. Amplitud neutralizante naturalmente mejorada contra el SARS-CoV-2 un año después de la infección. Naturaleza 2021;595:426-31.
13. Dan JM, Mateus J, Kato Y, Hastie KM, Yu ED, Faliti CE, et al. Memoria inmunológica al SARS-CoV-2 evaluada hasta 8 meses después de la infección. Ciencia 2021;371:eabf4063.
14. Sokal A, Chappert P, Barba-Spaeth G, Roeser A, Fourati S, Azzaoui I, et al. Maduración y persistencia de la respuesta de las células B de memoria anti-SARS-CoV-2. Celda 2021; 184:1201-13.e14. 15. Ju B, Zhang Q, Ge J, Wang R, Sun J, Ge X, et al. Anticuerpos neutralizantes humanos provocados por la infección por SARS-CoV-2. Naturaleza 2020;584:115-9.
16. Liu L, Wang P, Nair MS, Yu J, Rapp M, Wang Q, et al. Potentes anticuerpos neutralizantes contra múltiples epítopos en el pico de SARS-CoV-2. Naturaleza 2020;584:450-6.
17. Zost SJ, Gilchuk P, Caso JB, Binshtein E, Chen RE, Nkolola JP, et al. Anticuerpos humanos potentemente neutralizantes y protectores contra el SARS-CoV-2. Naturaleza 2020; 584:443-9.
18. Xu C, Wang Y, Liu C, Zhang C, Han W, Hong X, et al. Dinámica conformacional de la glicoproteína de pico trimérica del SARS-CoV-2 en complejo con el receptor ACE2 revelada por crio-EM. Ciencia avanzada 2021;7:eabe5575.
19. McCallum M, De Marco A, Lempp FA, Tortorici MA, Pinto D, Walls AC, et al. El mapeo antigénico del dominio N-terminal revela un sitio de vulnerabilidad para el SARSCoV-2. Celda 2021;184:2332-47.e16.
20. Sauer MM, Tortorici MA, Park YJ, Walls AC, Homad L, Acton OJ, et al. Base estructural para una amplia neutralización del coronavirus. Nat Struct Mol Biol 2021;28:478-86.
21. Tortorici MA, Beltramello M, Lempp FA, Pinto D, Dang HV, Rosen LE, et al. Los anticuerpos humanos ultrapotentes protegen contra el desafío del SARS-CoV-2 a través de múltiples mecanismos. Ciencia 2020;370:950-7.
22. Pinto D, Park YJ, Beltramello M, Walls AC, Tortorici MA, Bianchi S, et al. Neutralización cruzada del SARS-CoV-2 mediante un anticuerpo monoclonal humano contra el SARS-CoV. Naturaleza 2020;583:290-5.
23. Liu Y, Soh WT, Kishikawa JI, Hirose M, Nakayama EE, Li S, et al. Un sitio que mejora la infectividad en la proteína de pico del SARS-CoV-2 al que se dirigen los anticuerpos. Celda 2021; 184:3452-66.e18.
24. Liu L, Wei Q, Lin Q, Fang J, Wang H, Kwok H, et al. La IgG anti-pico causa una lesión pulmonar aguda grave al distorsionar las respuestas de los macrófagos durante la infección aguda por SARS-CoV. JCI Insight 2019;4:e123158.
25. Li D, Edwards RJ, Manne K, Martinez DR, Schäfer A, Alam SM, et al. Funciones in vitro e in vivo de los anticuerpos potenciadores y neutralizantes de la infección por SARS-CoV-2. Celda 2021;184:4203-19.e32. 26. Poh CM, Carissimo G, Wang B, Amrun SN, Lee CY, Chee RS, et al. Dos epítopos lineales en la proteína de pico del SARS-CoV-2 provocan anticuerpos neutralizantes en pacientes con COVID-19. Nat Commun 2020;11:2806.
27. Zhang BZ, Hu YF, Chen LL, Yau T, Tong YG, Hu JC, et al. Extracción de epítopos en la proteína de pico del SARS-CoV-2 de pacientes con COVID-19. Resolución celular 2020;30:702-4.
28. Stoddard CI, Galloway J, Chu HY, Shipley MM, Sung K, Itell HL, et al. El perfil de epítopo revela firmas vinculantes de la respuesta inmune del SARS-CoV-2 en infecciones naturales y reactividad cruzada con CoV humanos endémicos. Representante celular 2021;35: 109164.
29. Shrock E, Fujimura E, Kula T, Timms RT, Lee IH, Leng Y, et al. El perfil de epítopos virales de pacientes con COVID-19 revela reactividad cruzada y correlaciones de gravedad. Ciencia 2020;370:eabd4250.
30. Zamecnik CR, Rajan JV, Yamauchi KA, Mann SA, Loudermilk RP, Sowa GM, et al. ReScan, un sistema de diagnóstico múltiple, analiza sueros humanos en busca de antígenos del SARS-CoV-2- 2. Cell Rep Med 2020;1:100123.
31. Haynes WA, Kamath K, Bozekowski J, Baum-Jones E, Campbell M, Casanovas Massana A, et al. Mapeo de epítopos de alta resolución y caracterización de anticuerpos contra el SARS-CoV-2 en grandes cohortes de sujetos con COVID-19. Común Biol 2021;4:1317.
32. Li Y, Lai DY, Lei Q, Xu ZW, Wang F, Hou H, et al. Evaluación sistemática de las respuestas de IgG a los péptidos derivados de la proteína de pico del SARS-CoV-2 para el seguimiento de pacientes con COVID-19. Cell Mol Immunol 2021;18:621-31.
33. Li Y, Ma ML, Lei Q, Wang F, Hong W, Lai DY, et al. Panorama de epítopos lineales de la proteína de pico del SARS-CoV-2 construido a partir de 1051 pacientes con COVID-19. Representante celular 2021;34:108915.
34. Wang H, Wu X, Zhang X, Hou X, Liang T, Wang D, et al. Micromatriz de proteoma SARS-CoV-2 para mapear las interacciones de los anticuerpos COVID-19 con resolución de aminoácidos. ACS Cent Ciencia 2020;6:2238-49.
35. Yi Z, Ling Y, Zhang X, Chen J, Hu K, Wang Y, et al. Mapeo funcional de epítopos lineales de células B del SARS-CoV-2 en población convaleciente de COVID-19. Los microbios emergentes infectan 2020;9:1988-96.
36. Comisión Nacional de Salud y Administración Nacional de Medicina Tradicional China. Protocolo de diagnóstico y tratamiento para la neumonía por nuevo coronavirus (versión de prueba 7). Chin Med J (inglés) 2020;133:1087-95; https://doi.org/10.1097/CM9.0000000000000819.
37. Li Y, Li CQ, Guo SJ, Guo W, Jiang HW, Li HC, et al. El perfil longitudinal del repertorio de autoanticuerpos séricos identifica biomarcadores asociados a la cirugía en el adenocarcinoma de pulmón. EBioMedicina 2020;53:102674.
38. Zhao J, Yuan Q, Wang H, Liu W, Liao X, Su Y, et al. Respuestas de anticuerpos al SARSCoV-2 en pacientes con la nueva enfermedad por coronavirus 2019. Clin Infect Dis 2020;71: 2027-34.
39. Lucas C, Wong P, Klein J, Castro TBR, Silva J, Sundaram M, et al. Los análisis longitudinales revelan fallos inmunológicos en la COVID grave-19. Naturaleza 2020;584: 463-9.
40. Moore JB, junio CH. Síndrome de liberación de citoquinas en COVID grave-19. Ciencia 2020;368:473-4.
41. Chen J, Malone B, Llewellyn E, Grasso M, Shelton PMM, Olinares PDB, et al. Base estructural para el acoplamiento helicasa-polimerasa en el complejo de replicación-transcripción del SARS-CoV-2. Celda 2020;182:1560-73.e13.
42. Wajnberg A, Amanat F, Firpo A, Altman DR, Bailey MJ, Mansour M, et al. Los fuertes anticuerpos neutralizantes contra la infección por SARS-CoV-2 persisten durante meses. Ciencia 2020; 370:1227-30.
43. Chi X, Yan R, Zhang J, Zhang G, Zhang Y, Hao M, et al. Un anticuerpo humano neutralizante se une al dominio N-terminal de la proteína de pico del SARS-CoV-2. Ciencia 2020;369:650-5.
44. Tseng CT, Sbrana E, Iwata-Yoshikawa N, Newman PC, Garron T, Atmar RL, et al. La inmunización con vacunas contra el coronavirus del SARS conduce a una inmunopatología pulmonar al enfrentarse al virus del SARS. PLoS One 2012;7:e35421.
45. Bolles M, Deming D, Long K, Agnihotram S, Whitmore A, Ferris M, et al. Una vacuna contra el coronavirus del síndrome respiratorio agudo grave con doble inactivación proporciona una protección incompleta en ratones e induce una mayor respuesta pulmonar proinflamatoria eosinófila tras la exposición. J Virol 2011;85:12201-15.
46. Weingartl H, Czub M, Czub S, Neufeld J, Marszal P, Gren J, et al. La inmunización con la vacuna recombinante del virus vaccinia modificado basada en Ankara contra el síndrome respiratorio agudo grave se asocia con un aumento de la hepatitis en los hurones. J Virol 2004;78:12672-6.
47. Yasui F, Kai C, Kitabatake M, Inoue S, Yoneda M, Yokochi S, et al. La inmunización previa con la proteína de la nucleocápside del coronavirus asociada al síndrome respiratorio agudo severo (SARS) (SARS-CoV) causa neumonía grave en ratones infectados con SARS-CoV. J Immunol 2008;181:6337-48.
48. Deming D, Sheahan T, Heise M, Yount B, Davis N, Sims A, et al. Eficacia de la vacuna en ratones senescentes desafiados con variantes epidémicas y zoonóticas recombinantes portadoras de SARS-CoV. PLoS Med 2006;3:e525.
49. Wang Q, Zhang L, Kuwahara K, Li L, Liu Z, Li T, et al. Los epítopos inmunodominantes del coronavirus del SARS en humanos provocaron efectos tanto potenciadores como neutralizantes sobre la infección en primates no humanos. ACS Infect Dis 2016;2: 361-76.
50. Agrawal AS, Tao X, Algaissi A, Garron T, Narayanan K, Peng BH, et al. La inmunización con la vacuna inactivada contra el coronavirus del síndrome respiratorio de Oriente Medio conduce a una inmunopatología pulmonar al exponerse a un virus vivo. Hum Vaccin Immunother 2016;12:2351-6.
