Predecir el papel del LncRNA en el envejecimiento renal según la secuenciación de ARN Ⅱ
Jan 26, 2024
Correlación de lncRNA Gm43360 y sus posibles ARNm objetivo
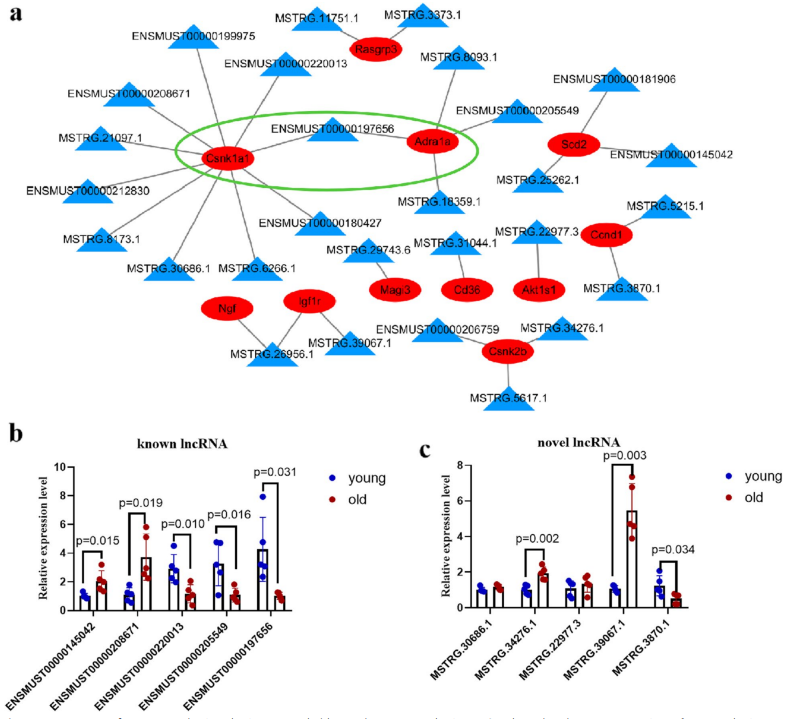
Se seleccionó LncRNA Gm43360 para el estudio porque conectaba dos redes de coexpresión de lncRNA-mRNA. El nivel de expresión de Adra1a se correlacionó positivamente (rho=0.8650, p=0.026) con el de Gm43360, Csnk1a1 (caseína quinasa 1A1) se correlacionó negativamente (rho{{12 }}.8084, p=0.0084) (Fig. 5a). Para verificar aún más la correlación de lncRNA Gm43360 y sus posibles ARNm objetivo Adra1a y Csnk1a1, en este estudio se diseñó un plásmido de sobreexpresión de lncRNA Gm43360. La expresión de Csnk1a1 disminuyó como se esperaba y la expresión de Adra1a también disminuyó, pero no de manera significativa. A continuación, eliminamos el lncRNA Gm43360 mediante siRNA para detectar si la expresión de sus ARNm objetivo se vio afectada. Como se esperaba, Csnk1a1 aumentó en las células desactivadas de lncRNA Gm43360 en relación con el grupo de control negativo de siRNA (Fig. 5b). Diez, detectamos el papel del lncRNA Gm43360 en el ciclo celular. Los resultados del kit de recuento de células -8 (CCK-8) mostraron que el lncRNA Gm43360 promovió la viabilidad celular (Fig. 5c). Los resultados mostraron que el lncRNA Gm43360 aumentó el porcentaje de células en fase S y disminuyó el porcentaje de células en fase G1 en comparación con el control negativo (Fig. 5d). Las proteínas p53 y p21 estaban implicadas en la regulación del ciclo celular y, por tanto, eran marcas del envejecimiento celular. Los niveles de expresión de p53 y p21 disminuyeron significativamente en el grupo de sobreexpresión en relación con el grupo de control. Los niveles de expresión de p53 y p21 aumentaron significativamente en el grupo de ARNip en relación con el grupo de control de ARNip (Fig. 5e). La sobreexpresión de lncRNA Gm43360 disminuyó el número de células SA- -gal positivas y las células -gal positivas aumentaron en el grupo de transfectado Gm43360 (Fig. 5f). En conjunto, estos resultados indicaron que el lncRNA Gm43360 inhibió la senescencia de las células epiteliales tubulares renales alinhibiendo la expresión de Csnk1a1.

HAGA CLIC AQUÍ PARA OBTENER EXTRACTO DE CISTANCHE ORGÁNICO NATURAL CON 25% DE EQUINACOSIDO Y 9% DE ACTEÓSIDO PARA LA FUNCIÓN RENAL
Discusión
En este estudio, evaluamos los datos de expresión de ARNm de riñones de ratones jóvenes y viejos y realizamos análisis de bioinformación que revelaron las funciones de los ARNm expresados de forma aberrante. Observamos 347 ARNm regulados positivamente y 355 ARNm regulados negativamente, así como 130 lncRNA regulados positivamente y 91 lncRNA regulados negativamente enRiñones de ratón viejos comparados con riñones de ratón jóvenes. Además, se demostró que estos ARNm están involucrados en vías relacionadas con el envejecimiento, comofosforilación oxidativa, la vía de señalización AMPK, la vía de señalización Wnt, la vía de señalización Rap1 y las enfermedades relacionadas con la edad, que demostraron las funciones de los ARNm expresados diferencialmente en la patogénesis del envejecimiento renal.
El largo ARN no codificante NEAT1 es un factor protector en la progresión de la fibrosis renal en las células epiteliales tubulares renales [21]. Casualmente, en nuestros resultados de secuenciación, el lncRNA NEAT1 se expresó en niveles más bajos en los riñones de ratones ancianos que en ratones jóvenes, lo que concuerda con hallazgos anteriores. LincRNA-Gm4419 acelera la inflamación y la fibrosis mediante mecanismos mediados por el inflamasoma NF-kB/NLRP3 en la nefropatía diabética [22]. En nuestros resultados de secuenciación, también encontramos que la expresión de Gm4419 era mayor en los riñones de ratones viejos que en ratones jóvenes, pero no hubo una diferencia significativa. LncRNA Gm43360 se encuentra en el cromosoma 5 (Chr5: 122494022–122,494,908, 2887 pb). Según el UCSC Genome Browser, Gm43360 se encuentra en el intrón del gen codificador de proteínas Atp2a2. Sin embargo, hasta la fecha no ha habido informes sobre la participación del lncRNA Gm43360 en enfermedades. En este estudio, la eliminación del lncRNA Gm43360 promovió la senescencia de las células epiteliales tubulares renales. Además, identificamos muchos lncRNA expresados diferencialmente en los resultados de la secuenciación y los investigamos.
Los LncRNA se clasificaron en regulación cis o transregulación según los mecanismos reguladores de lncRNA. Los lncRNA que actúan en cis podrían influir en la expresión de genes vecinos al depender de elementos que actúan en cis, como promotores, potenciadores y secuencias reguladoras, que son distancias entre los lncRNA y los mRNA de menos de 100 kb. Los lncRNA de acción trans se refieren a los lncRNA que abandonan el sitio de transfección y operan en sitios distantes (es decir, la distancia entre los lncRNA y los mRNA es de más de 100 kb) [23]. El lncRNA MAAT aumenta la expresión del gen vecino Mbnl1 a través de un módulo regulador cis [24]. El lncRNA Pnky desempeña un papel como regulador de acción trans en el desarrollo cortical [25]. En este estudio, hubo una relación transrreguladora entre el lncRNA Gm43360 y Csnk1a1. Csnk1a1 es un gen supresor de tumores [26] que codifica una proteína que participa en el ciclo celular y el proceso de división celular [27]. La regulación negativa de Csnk1a1 induceinflamatoria asociada a la senescenciarespuesta con detención del crecimiento en tumores colorrectales [26]. Csnk1a1 se reguló a la baja cuando Gm43360 se reguló al alza; por lo tanto, es probable que el lncRNA Gm43360 participe enenvejecimiento renalporregulando la expresión de Csnk1a1.

Conclusiones
Nuestra investigación de la red de coexpresión lncRNA-mRNA enenvejecimiento renalreveló que un lncRNA, lncRNA Gm43360, puede desempeñar un papel protector en el envejecimiento renal y amplió nuestra comprensión de los mecanismos implicados enenvejecimiento renal

Materiales y métodos
Muestras Se compraron ratones C57BL/6J machos jóvenes ({0}}meses) y viejos (24-meses) en el Centro Experimental de Animales de la Universidad de Xiamen y se criaron en un entorno estándar. Todos los ratones tuvieron libre acceso a comida y agua. Los ratones se aclimataron a las nuevas instalaciones durante un mes antes de ser sacrificados. Los ratones fueron anestesiados con uretano mediante inyección intraperitoneal a una dosis de 750 mg/kg antes de la recolección de la muestra. Se sacrificaron ratones jóvenes y viejos el mismo día.Riñón residual de ratónSe utilizó tejido para la secuenciación en cada ensayo. RNA-seq e histopatología se realizaron enriñones separadosdesde el mismo ratón. Se recogió tejido de riñón de ratones. Un riñón se sumergió inmediatamente en formalina tamponada neutra al 10 % para la posterior inclusión de la sección, y el otro riñón se dividió en varios tejidos y se colocó inmediatamente en nitrógeno líquido y luego se almacenó a -80 grado. El estudio contó con el apoyo del Comité de Ética del Primer Hospital Afiliado de la Universidad Xi'an Jiaotong (Shaanxi, China) (No. 2018-G-164). Todos los métodos se llevaron a cabo según las pautas y regulaciones de ética animal. Este estudio se llevó a cabo de conformidad con las directrices ARRIVE.
histopatología renal
Se fijaron muestras de tejido renal de ratones jóvenes y viejos en una solución de paraformaldehído al 10% durante la noche. Diez de las secciones se deshidrataron, se incluyeron en parafina y se seccionaron con un espesor de 4- µm. La tinción PAS y tricromática de Masson se realizaron utilizando protocolos estándar. La cámara capturó las imágenes y se midió el área positiva para la tinción. El área para las imágenes de la cámara de histopatología se calculó con Image-Pro Plus 6.0.
Tinción SA‑‑gal
La actividad de SA{{0}}gal se analizó utilizando un kit de tinción de SA- -gal (Cell Signaling Technology #9860) de acuerdo con el protocolo del fabricante. Se midió el área de tinción positiva y se calcularon las células positivas para SA- -gal utilizando Image-Pro Plus 6.0.
Construcción y secuenciación de bibliotecas de extracción de ARN.
Samples (each 5 mice in young and old mice) were used for lncRNA and mRNA expression analyses. Young mice were numbered 3M1, 3M2, 3M3, 3M4, and 3M5, and old mice were numbered 24M1, 24M2, 24M3, 24M4, and 24M5. Total RNA was extracted using Trizol reagent (thermofsher, 15,596,018) following the manufacturer's instruction. The total RNA quantity and purity were analyzed of Bioanalyzer 2100 and RNA 6000 Nano LabChip Kit (Agilent, CA, USA, 5067−1511), and high-quality RNA samples with RIN number>7.0 se utilizaron para construir una biblioteca de secuenciación. Después de la extracción del ARN total, el ARNm se purificó a partir del ARN total (5 ug) utilizando Dynabeads Oligo (dT) (Thermo Fisher, CA, EE. UU.) con dos rondas de purificación. Después de la purificación, el ARNm se dividió en fragmentos cortos utilizando cationes divalentes a altas temperaturas (Módulo de fragmentación de ARN de magnesio (NEB, cat. e6150, EE. UU.) a 94 grados 5-7 min). Luego, los fragmentos de ARN escindidos se transcribieron de forma inversa para obtener el ADNc mediante la transcriptasa inversa SuperScript™ II (Invitrogen, cat. 1.896.649, EE. UU.), que luego se usaron para sintetizar ADN de segunda cadena marcados con U con ADN polimerasa I de E. coli ( NEB, cat.m0209, EE. UU.), RNasa H (NEB, cat.m0297, EE. UU.) y solución dUTP (Termo Fisher, cat.R0133, EE. UU.). Luego se añadió una base A a los extremos romos de cada hebra, preparándolos para la ligación a los adaptadores indexados. Cada adaptador contenía un saliente de base T para ligar el adaptador al ADN fragmentado con cola A. Se ligaron adaptadores de doble índice a los fragmentos y la selección del tamaño se realizó con perlas AMPureXP. Después del tratamiento con enzima UDG termolábil (NEB, cat.m0280, EE. UU.) de los ADN de segunda cadena marcados con U, los productos ligados se amplificaron con PCR mediante las siguientes condiciones: desnaturalización inicial a 95 grados durante 3 minutos; 8 ciclos de desnaturalización a 98 grados durante 15 s, recocido a 60 grados durante 15 s y extensión a 72 grados durante 30 s; y luego extensión final a 72 grados durante 5 min. La longitud media del inserto para las bibliotecas de ADNc finales fue de 300 ± 50 pb. Finalmente, realizamos la secuenciación de extremos emparejados de 2 × 150 pb (PE150) en un Illumina Novaseq™ 6000 (LC-Bio Technology CO., Ltd., Hangzhou, China) de acuerdo con el protocolo del fabricante [28].

Análisis bioinformático Secuencia y filtrado de lecturas limpias
Una biblioteca de ADNc construida mediante tecnología a partir del ARN combinado demuestras de riñónde ratones se secuenció y se ejecutó con la plataforma de secuencia Illumina NovaseqTM 6000. Utilizando el enfoque de secuenciación de ARN de extremos emparejados de Illumina, secuenciamos el transcriptoma, generando un total de millones de lecturas de extremos emparejados de 2 × 150 pb. Las lecturas obtenidas de las máquinas de secuenciación incluyen lecturas sin procesar que contienen adaptadores o bases de baja calidad que afectarán el siguiente ensamblaje y análisis. Por lo tanto, para obtener lecturas limpias de alta calidad, Cutadapt [29] filtró aún más las lecturas (https://cutadapt.readthedocs.io/en/stable/, versión:cutadapt-1.9). Los parámetros fueron los siguientes:
1) eliminar lecturas que contienen adaptadores;
2) eliminar lecturas que contienen poliA y poli;
3) eliminar lecturas que contengan más del 5% de nucleótidos desconocidos (N);
4) eliminar lecturas de baja calidad que contengan más del 20 % de bases de baja calidad (valor Q inferior o igual a 20).
La calidad de diez secuencias se verificó utilizando FastQC [30] (http://www.bioinformatics.babraham.ac.uk/projects/fastqc/, 0.11.9). incluido el contenido Q20, Q30 y GC de los datos limpios. Después de eso, se produjo un total de G pb de lecturas limpias de extremos emparejados. Los datos de secuencia sin procesar se enviaron a los conjuntos de datos NCBI Gene Expression Omnibus (GEO) con número de acceso GSE154223.
El genoma/anotación de referencia fue Mus_musculus.GRCm38. La fuente y la versión de la anotación genética utilizada para los análisis fue Ensembl_v88.

Asamblea de transcripciones
En primer lugar, se utilizó Cutadapt [29] para eliminar las lecturas que contenían contaminación del adaptador, bases de baja calidad y bases indeterminadas. La calidad de diez secuencias se alimentó con FastQC (http://www.bioinformatics.Babra ham.ac.uk/projects/fastqc/). Usamos Bowtie2 [31] e Hisat2 [32] para mapear lecturas en el genoma del ratón. Las lecturas mapeadas de cada muestra se ensamblaron utilizando StringTie [33]. Diez, todas las transcripciones demuestras de riñónse fusionaron para reconstruir un transcriptoma completo utilizando scripts Perl. Después de generar el transcriptoma final, se utilizaron StringTie [33] y edgeR [34] para estimar los niveles de expresión de todas las transcripciones.
Identificación de ARNnc
En primer lugar, se descartaron las transcripciones que se superponían con ARNm conocidos y las transcripciones de menos de 200 pb. Luego utilizamos CPC [35] y CNCI [36] para predecir transcripciones con potencial de codificación. Todas las transcripciones con puntuación CPC<-1 and CNCI score<0 were removed. The remaining transcripts were considered as lncRNAs.
Análisis de genes de análisis expresados diferencialmente (DGE)
StringTie [33] was used to perform expression levels for mRNAs and lncRNAs by calculating FPKM [37]. Genes differential expression analysis was performed by DESeq2 software between two different groups (and by edgeR between two samples) [34, 38]. The genes with the parameter of q value below 0.6 and absolute fold change>2 se consideraron genes expresados diferencialmente.
Predicción de genes diana y análisis funcional de lncRNA
Para explorar la función de los lncRNA, predijimos los genes objetivo cis de los lncRNA. Los LncRNA pueden desempeñar un papel cis al actuar sobre genes diana vecinos. En este estudio, los genes codificantes en 100,000 en sentido ascendente y descendente se seleccionaron mediante script Perl. Luego, mostramos un análisis funcional de los genes objetivo de los lncRNA utilizando los scripts BLAST2GO [39]. El enlace de comandos completo al dominio público era Jie-Li/README.md en main · dandan-li/Jie-Li (github.com).

Categorías de ontología genética (GO) y análisis de la Enciclopedia de genes y genomas de Kioto (KEGG)
El análisis bioinformático para la secuenciación de ARN se realizó utilizando las herramientas OmicStudio (http://www.omicsudio.cn/tool). Se utilizaron el análisis de enriquecimiento funcional de la ontología genética (GO) y el análisis de enriquecimiento de la Enciclopedia de genes y genomas de Kyoto (KEGG) [37–39] para analizar las funciones biológicas de los genes diana predichos. El análisis GO aclara los principales procesos biológicos a través de tres aspectos: composición celular, funciones moleculares y procesos biológicos (http://www.geneontology.org/). El análisis primero coloca todos los genes expresados diferencialmente y los genes de fondo en la base de datos GO. Se mapea cada elemento, se calcula el número de genes en cada elemento y se utiliza la distribución hipergeométrica para realizar pruebas de hipótesis para obtener el valor P del resultado de enriquecimiento. Cuanto menor sea el valor P, más significativo será el resultado del enriquecimiento. KEGG es un recurso de base de datos que analiza los ARNm expresados diferencialmente mediante biología genética para explorar vías importantes relacionadas con genes diana (https://www.genome.jp/kegg/). Los resultados se expresan mediante valores p; cuanto menor sea el valor p, más significativo será el resultado del enriquecimiento.
QRT–PCR
Se utilizó GAPDH como control endógeno. Luego, se calcularon los niveles de expresión relativos de genes desconocidos. Todos los cebadores fueron diseñados y sintetizados específicamente para este experimento. Se han comercializado cebadores para GAPDH. La especificidad de los cebadores Adra1a y Csnk1a1 se identificó mediante el pico único de la curva de fusión.
Construir una red de coexpresión de ARNm-lncRNA
La transregulación se basó en la investigación y luego se calculó la energía trans. Cuanto menor era la energía trans, mayor era la posibilidad de unión. Luego, también se calculó el coeficiente de correlación de ARNm-ARNc. La red mRNA-lncRNA se construyó eligiendo un coeficiente de correlación de Spearman superior a 0.9. La red de coexpresión de ARNm-lncRNA se construyó utilizando el software Cytoscape (v3.7.1).
Cultivo de células
Se cultivaron células epiteliales tubulares proximales renales de ratón (MRPT-EpiC) en medio de células epiteliales-animal (EpiCM-a, Cat. #4131) que contenía suero bovino fetal al 2% (FBS, Cat. #0010) y suplemento de crecimiento de células epiteliales-animal. (EpiCGS-a, Cat. #4182) sin antibióticos en una incubadora humidificada a 37 grados y 5% de CO2. El medio de cultivo se cambió cada 2-3 días. Las células en la fase de crecimiento logarítmico se subcultivaron cuando el crecimiento alcanzó el 90%. La suspensión de células digeridas con tripsina se sembró en 6-placas de pocillos con 2*104 -5*104 células en cada pocillo. Las células utilizadas para la transfección estaban todas entre las generaciones 2 y 5.
Construcción de plásmidos y transfección celular.
GeneChem (Shanghai, China) construyó el plásmido de sobreexpresión lncRNA Gm43360. La columna vertebral del plásmido era GV658 y el promotor de CMV impulsó la expresión del ARNc. La secuencia de nucleótidos clonada se proporciona en el material complementario. Para la eliminación de lncRNA Gm43360, tres lncRNA ENS DEBEN 00000197656-apuntar a los ARNip (lncRNA Gm43360- siRNA1, 5'-CCUUCACUCCAGCUGGUAATT-3'; lncRNA Gm43360-siRNA2, 5'-CCCUGUCACUCA UGAAGUUTT-3'; y lncRNA Gm43360-siRNA3, 5'-GGUCAAAUAACUCAAUGGTT-3') se diseñaron y sintetizaron en GenePharma (Shanghai, China). Según el protocolo del fabricante, las células se transfectaron con 2500 ng de plásmido o 100 pmol de ARNip con 6 µl de reactivo de transfección Lipofectamine™ 2000 (Invitrogen, EE. UU.) por pocillo. Los niveles de expresión de ARN y proteínas se detectaron 48 h después de la transfección y cada experimento se repitió al menos tres veces. Se utilizó PCR cuantitativa en tiempo real para validar la eficiencia de la sobreexpresión y eliminación del lncRNA Gm43360.
Análisis de Western Blot
Las células cultivadas se lavaron con PBS enfriado con hielo, se agregaron 120 µl de tampón RIPA (Heart, China) y se agregaron inhibidor de proteasa y PMSF (Heart, China) durante 30 minutos en hielo. Después de recolectar las células en diferentes tubos de microcentrífuga, se cuantificó la concentración de proteínas. Se añadió tampón de carga a cada muestra y luego se hirvió durante 7 minutos. Se separaron treinta microgramos de la muestra con SDS-PAGE al 12% (Beyotime, China) y se electrotransfirieron a membranas de PVDF (Thermo Fisher, EE. UU.). Luego, las membranas se bloquearon con leche al 5%. Las membranas se incubaron con anticuerpos primarios específicos: anti-p21 (1:1000, Abcam, ab109199), anti-p53 (1:1000, Proteintech, 10442-1-AP) y anti-GAPDH (1:3000, Profintech). , 60004-1-Ig) durante la noche a 4 grados. Después de lavar con TBST, las membranas se incubaron con un anticuerpo secundario durante 1 hora a temperatura ambiente. Las bandas de proteínas se observaron utilizando un kit de quimioluminiscencia (Millipore, EE. UU.). La expresión de GAPDH se utilizó para normalizar los niveles de proteína.
Ensayo de proliferación celular.
La capacidad de proliferación celular se determinó mediante el ensayo del kit de recuento celular-8 (CCK-8). Cuarenta y ocho horas después de la transfección, se agregaron a cada pocillo 90 µl de medio nuevo y 10 µl de solución CCK-8 (Beyotime, C0042). Las células se incubaron durante 1 a 4 h a 37 grados en CO2 al 5% y se midieron a 450 nm con un lector de microplacas universal (Bio-Tek, EE. UU.).
Análisis de citometría de flujo.
Las células se sembraron en placas de 6-pocillos el día antes de la transfección. Cuarenta y ocho horas después de la transfección, las células se tripsinizaron y se centrifugaron a 1000 rpm durante 5 minutos. Luego, las células se fijaron en etanol al 70% a 4 grados durante al menos 4 h. Después de la centrifugación, se añadió a las células una solución de tinción con ARNasa A y yoduro de propidio (PI), y luego las células se incubaron durante 30 minutos a temperatura ambiente en la oscuridad. Las células teñidas con Te se analizaron utilizando un ACEA NovoCyte (Biosciences, EE. UU.).
análisis estadístico
Los datos de medición según la distribución normal se presentan como media ± DE. La diferencia entre los dos grupos diferentes se determinó mediante pruebas t de Student no pareadas de dos colas, y un valor de p < 0.05 se consideró estadísticamente significativo. Todos los cálculos se realizaron utilizando GraphPad Prism 8 (GraphPad Software, Inc., EE. UU.).
Referencias
1. Docherty MH, O'Sullivan ED, Bonventre JV, Ferenbach DA. Senescencia celular en el riñón. J. Am Soc Nephrol. 2019;30(5):726–36.
2. Partridge L, Deelen J, Slagboom PE. Afrontar los desafíos globales del envejecimiento. Naturaleza. 2018;561(7721):45–56.
3. Panorámica JX. LncRNA H19 promueve la aterosclerosis al regular las vías de señalización de MAPK y NF-kB. Eur Rev Med Pharmacol Sci. 2017;21(2):322–8.
4. Wasson CW, Abignano G, Hermes H, Malaab M, Ross RL, Jimenez SA, Chang HY, Feghali-Bostwick CA, Del Galdo F. El ARN largo no codificante HOTAIR impulsa la activación de miofibroblastos dependiente de EZH2-en enfermedades sistémicas. esclerosis a través de la activación de NOTCH dependiente de miARN 34a. Ann Enfermedad reumática. 2020;79(4):507–17.
5. Luo J, Wang K, Yeh S, Sun Y, Liang L, Xiao Y, Xu W, Niu Y, Cheng L, Maity SN, et al. LncRNA-p21 altera la diferenciación neuroendocrina del cáncer de próstata inducida por antiandrógeno enzalutamida mediante la modulación de la señalización EZH2/STAT3. Comuna Nacional. 2019;10(1):2571.
6. Wang Y, Yang L, Chen T, Liu X, Guo Y, Zhu Q, Tong X, Yang W, Xu Q, Huang D, et al. Un nuevo lncRNA MCM3AP-AS1 promueve el crecimiento del carcinoma hepatocelular al apuntar al eje miR-194-5p/FOXA1. Cáncer de Mol. 2019;18(1):28.
7. Wu YY, Kuo HC. Roles funcionales y redes de ARN no codificantes en la patogénesis de enfermedades neurodegenerativas. J Biomed Ciencias. 2020;27(1):49.
8. Li Z, Wang Z. Envejecimiento del riñón y enfermedades relacionadas con el envejecimiento. Experimento avanzado Med Biol. 2018;1086:169–87.
9. Wang X, Vrtiska TJ, Avula RT, Walters LR, Chakkera HA, Kremers WK, Lerman LO, Rule AD. La edad, la función renal y los factores de riesgo se asocian de manera diferente con los volúmenes corticales y medulares del riñón. Riñón Int. 2014;85(3):677–85.
10. Lin Q, Hou S, Dai Y, Jiang N, Lin Y. LncRNA HOTAIR se dirige a miR-126-5p para promover la progresión de la enfermedad de Parkinson a través de RAB3IP. Bioquímica. 2019;400(9):1217–28.
Servicio de apoyo de Wecistanche: el mayor exportador de cistanche de China:
Correo electrónico:wallence.suen@wecistanche.com
Whatsapp/Tel:+86 15292862950
Compre para obtener más detalles de especificaciones:
https://www.xjcistanche.com/cistanche-shop







