Dirigirse al cáncer de próstata avanzado con inmunoterapia de células T con receptor de antígeno quimérico STEAP1 e inmunoterapia con IL-12 localizada en tumor
Sep 18, 2023
Seis antígenos epiteliales transmembrana de la próstata 1 (STEAP1) es un antígeno de superficie celular para la terapia dirigida en el cáncer de próstata. Aquí, informamos la amplia expresión de STEAP1 en relación con el antígeno de membrana específico de la próstata (PSMA) en cánceres de próstata metastásicos letales y el desarrollo de una terapia de células T con receptor de antígeno quimérico (CAR) dirigida por STEAP1-. Las células T CAR STEAP1 demuestran reactividad en baja densidad de antígeno, actividad antitumoral en modelos de cáncer de próstata metastásico y seguridad en un modelo de ratón knock-in humano STEAP1. El escape del antígeno STEAP1 es un mecanismo recurrente de resistencia al tratamiento y se asocia con una disminución del procesamiento y la presentación del antígeno tumoral. La aplicación de la terapia con interleucina-12 (IL-12) localizada en el tumor en forma de una proteína de fusión del dominio de unión a colágeno (CBD)-IL-12 combinada con la terapia con células T con CAR STEAP1 mejora eficacia antitumoral al remodelar el microambiente tumoral inmunológicamente frío del cáncer de próstata y combatir el escape del antígeno STEAP1 mediante la participación de la inmunidad del huésped y la propagación del epítopo.

Planta de hierba china cistanche-Antitumoral
Metastatic prostate cancer represents an incurable disease responsible for over 33,000 deaths per year in the United States1. Prostate cancer is critically reliant on androgen receptor (AR) signaling and thus the suppression of gonadal androgen production through surgical or chemical castration (androgen deprivation therapy) has been a mainstay of treatment for advanced disease. However, metastatic prostate cancer inevitably develops resistance to androgen deprivation therapy and enters a stage called metastatic castration-resistant prostate cancer (mCRPC). mCRPC is currently incurable and is considered the end stage of the disease and is associated with a median overall survival of three years2. In the past decade, multiple therapies including an inhibitor of extragonadal androgen synthesis (abiraterone acetate)3, second-generation AR antagonists (enzalutamide)4, radioactive isotope (radium-223)5, and a prostate-specific membrane antigen (PSMA)-specific radioligand therapy (lutetium Lu 177 via votide tetraxetan)6 have been approved for mCRPC. Each of these agents extends survival on average by several months but long-term remissions are rare. Strategies to reprogram the immune system to combat prostate cancer first gained traction with the clinical approval of the dendritic cell vaccine sipuleucel-T for asymptomatic mCRPC7. More recently, several types of immunotherapies including immune checkpoint inhibitors, a DNA cancer vaccine, antibody-drug conjugates (ADC), T cell engaging bispecific antibodies (T-BsAb), and chimeric antigen receptor (CAR) T cell therapies have been under active clinical investigation8,9. CARs are synthetic receptors that leverage the potency, expansion, and memory of T cells and can be engineered against virtually any tumor-associated cell surface antigen. The adoptive transfer of CAR T cells has rapidly become an established treatment for hematologic malignancies with exceptional response rates leading to six clinical approvals in the last five years10. In contrast, CAR T cell therapies targeting solid tumors have lagged due to additional challenges related to the lack of bona fide tumor-specific antigens, inhospitable tumor microenvironments, and poor trafficking, persistence, and expansion of CAR T cells11. Despite the challenges observed in driving effective immune responses toward solid tumors, recent early-phase clinical trials investigating CAR T cell therapies targeting PSMA in mCRPC have reported safety and evidence of significant biochemical and radiographic responses12,13. These preliminary results serve to embolden efforts to develop and optimize new CAR T cell therapies for prostate cancer. While PSMA is the preeminent target for therapeutic and diagnostic development in prostate cancer, recent work indicates that PSMA expression may be quite heterogeneous in mCRPC14. Tumor antigen heterogeneity, especially in the context of single antigen-targeted CAR T cell therapies for solid tumors like prostate cancer, is an important barrier to therapeutic efficacy15. Thus, identifying cell surface antigens with broad and relatively homogeneous expression in prostate cancer is imperative. In addition, very few if any tumor-associated antigens demonstrate tumor-restricted expression—most also exhibit low-level expression in normal tissues that could represent liabilities for CAR T cell therapies due to on-target off-tumor toxicities which can lead to devastating consequences including death16. We previously performed integrated transcriptomic and cell surface proteomic profiling of human prostate adenocarcinoma cell lines and identified six transmembrane epithelial antigens of the prostate 1 (STEAP1) as one of the most highly enriched cell surface antigens17. STEAP1 was first described over two decades ago18 and was recognized as being highly expressed in prostate cancer. STEAP1 is strongly expressed in >El 80% de los mCRPC tienen afectación ósea o de los ganglios linfáticos19, el 62% de los sarcomas de Ewing20 y muchos otros tipos de cáncer21. STEAP1 pertenece a la familia STEAP de metaloreductasas que pueden formar homotrímeros o heterotrímeros con otras proteínas STEAP22. STEAP1 tiene un papel funcional establecido en la promoción de la proliferación, invasión y transición epitelial a mesenquimal de células cancerosas–26.

Beneficios de la cistanche tubulosa-Antitumoral
Además, STEAP1 demuestra una expresión limitada en tejido normal27, lo que lo convierte en un objetivo muy atractivo para la terapia contra el cáncer. Se han desarrollado múltiples agentes inmunoterapéuticos para atacar STEAP1, pero ninguno está clínicamente aprobado. Se descubrió que el ADC vandor tuzumab ved otin (DSTP3086S), que consiste en un anticuerpo IgG1 anti-STEAP1 humanizado unido a monometil auristatina E, tiene un perfil de seguridad aceptable en un ensayo clínico de fase I en mCRPC, pero se observaron pocas respuestas tumorales objetivas28. Actualmente se está evaluando un T-BsAb que incorpora dos dominios de unión al antígeno (Fab) del fragmento anti-STEAP1, un fragmento variable de cadena única (scFv) anti-CD3 y un dominio de fragmento cristalizable (Fc) diseñado para carecer de función efectora llamado AMG 509. en un ensayo clínico de fase I (NCT04221542) en mCRPC29. También se informó recientemente que el T-BsAb bivalente dual asimétrico llamado BC261 demuestra una potente actividad antitumoral en múltiples modelos preclínicos de cáncer de próstata y sarcoma de Ewing30. Además, se ha demostrado que un receptor de células T (TCR) restringido al antígeno leucocitario humano (HLA) de clase I específico para un péptido STEAP1 inhibe el crecimiento local y metastásico del sarcoma de Ewing en un modelo preclínico de xenoinjerto después de la transferencia adoptiva de células T transgénicas31. En este estudio, realizamos un análisis comparativo de la expresión relativa de STEAP1 y PSMA en mCRPC letal para investigar la utilidad de apuntar a STEAP1 en la era actual de la teranóstica de PSMA. Diseñamos y seleccionamos CAR STEAP1 de segunda generación para la activación de células T específicas de antígeno y la citólisis de células diana para generar un candidato principal para una mayor caracterización. Determinamos la especificidad del epítopo funcional de las células T con CAR STEAP1 y perfilamos la expansión y el inmunofenotipo de los productos de células T con CAR STEAP1 de múltiples donantes. Luego establecimos la potencia y la seguridad preliminar de la terapia con células T con CAR STEAP1 en modelos preclínicos relevantes de cáncer de próstata, pero observamos la pérdida recurrente de la expresión del antígeno STEAP1 como mecanismo de resistencia al tratamiento. Para superar este problema, evaluamos la administración concomitante de CBD-IL-12, que remodela el microambiente tumoral inmunosupresor del cáncer de próstata y activa la inmunidad endógena para ampliar las respuestas antitumorales. En conjunto, estos estudios proporcionan una sólida justificación para la traducción clínica de la terapia con células T con CAR STEAP1 a hombres con mCRPC y guían estrategias para superar los posibles mecanismos de resistencia terapéutica.

Beneficios de la cistanche tubulosa-Antitumoral
Resultados
STEAP1 se expresa ampliamente en tejidos mCRPC refractarios al tratamiento
We first set out to determine the pattern and extent of STEAP1 expression relative to PSMA in advanced metastatic prostate cancer. We performed immunohistochemical (IHC) staining on a duplicate set of tissue microarrays consisting of 121 metastatic tumors (each with up to three cores represented) collected from 44 men with lethal mCRPC patients collected by rapid autopsy between the years 2010 and 2017 through the University of Washington Tumor Acquisition Necropsy Program32 (Fig. 1a). Plasma membrane staining for STEAP1 and PSMA in each tissue was scored by a research pathologist and semiquantitative H-scores were determined based on the staining intensity (Supple mentary Fig. 1a) multiplied by the percentage of cancer cells staining at each intensity (Supplementary Fig. 1b). By implementing a minimal staining threshold with an H-score cut-off of 30, we found that 87.7% of evaluable matched mCRPC tissues (100 of 114) demonstrated staining for STEAP1 compared to only 60.5% (69 of 114) for PSMA (Fig. 1b). In addition, 28.1% of mCRPC tissues (32 of 114) showed STEAP1 but not PSMA staining (Fig. 1b, c) whereas only 0.9% (one of 114) exhibited PSMA but not STEAP1 staining. Based on these results, we used a linear mixed statistical model to determine that the odds of non-zero (H-score >La tinción {{0}}) fue 22-veces (IC del 95 % 6-173) mayor para STEAP1 que para PSMA y las probabilidades de una puntuación H mayor o igual a 3{{ 27}} son 84-veces (IC del 95 % 30-317) mayores para STEAP1 que para PSMA. La puntuación H media de STEAP1 en hueso (193; IC del 95 %: 171 a 215) fue significativamente mayor que en las metástasis en los ganglios linfáticos (diferencia −48; IC del 95 %: −21 a −76; p < 0.001) y significativamente mayor que en las metástasis viscerales (diferencia −59; IC del 95%: −42 a −77; p <0,001). No hubo diferencias significativas entre la puntuación H media de STEAP1 en las metástasis a los ganglios linfáticos en comparación con las metástasis viscerales (diferencia 11; IC del 95%: −16 a 39; p=0.4) (Figura complementaria 1c). También observamos varios casos con expresión heterogénea de PSMA dentro de los núcleos (Fig. 1d), lo que es consistente con un informe reciente de heterogeneidad de PSMA intratumoral en biopsias de mCRPC14. El análisis a nivel de paciente utilizando un umbral medio de puntuación H mayor o igual a 30 y la prueba de McNemar reveló que el 95 % de los pacientes evaluables (42 de 44) tenían tumores con expresión de STEAP1, mientras que el 68 % (30 de 44) eran positivos para PSMA. (Figura complementaria 1d). Para estudiar los patrones de heterogeneidad entre pacientes e intrapaciente asociados con la expresión de STEAP1 y PSMA, utilizamos las puntuaciones H de STEAP1 y PSMA para evaluar las puntuaciones de diversidad hipergeométrica, Simpson y Shannon. Observamos dos patrones de expresión de STEAP1 (Fig. 1e) con un 68% (30/44) de pacientes que mostraron expresión de STEAP1 en todos los sitios metastásicos (STEAP1 alto) y un 32% (14/44) de pacientes que mostraron sitios metastásicos con y sin expresión de STEAP1. (STEAP1 heterogéneo). No se identificaron pacientes en los que todos los tejidos metastásicos carecieran de expresión de STEAP1. Un análisis similar para la expresión de PSMA en la misma cohorte reveló un 45 % (20/44) de pacientes con alta expresión de PSMA, un 32 % (14/44) con expresión heterogénea de PSMA y un 23 % (10/44) sin expresión de PSMA. Según la subclasificación molecular de los tejidos de mCRPC utilizando AR y la expresión del marcador neuroendocrino sinaptofisina (SYP) evaluada por IHC, la mayoría de los pacientes con expresión alta o heterogénea de STEAP1 y PSMA tenían cáncer de próstata AR positivo (AR+/SYP- o AR+/SYP+), mientras que aquellos sin expresión de PSMA tenía cáncer de próstata AR-nulo (AR-/SYP+ o AR-/SYP-). Identificamos una correlación positiva entre la expresión de STEAP1 y AR (p <0,001) mediante un modelo mixto lineal ajustado con efecto aleatorio en los casos representados en la micromatriz de tejido (Figuras complementarias 2a, b), lo que se esperaba dado que STEAP1 es un andrógeno. -gen regulado33,34. Por el contrario, se apreció una tendencia negativa entre la expresión de STEAP1 y SYP (Figura complementaria 2c). Estos hallazgos sugieren que, al igual que PSMA35, la expresión de STEAP1 puede perderse con la transdiferenciación neuroendocrina del cáncer de próstata.

Fig. 1 | Comparative analysis of STEAP1 and PSMA in lethal, metastatic castration-resistant prostate cancer (mCRPC). a Characteristics of the mCRPC tissues represented on University of Washington Tissue Acquisition Necropsy Tissue Microarray 92 (UW TAN TMA92). b Contingency table showing the frequency of mCRPC tissues with STEAP1 or PSMA IHC staining above or below an H-score threshold of 30. Micrographs of select mCRPC tissues after STEAP1 and PSMA IHC staining to highlight the (c) absence of PSMA but the presence of STEAP1 expression and (d) intratumoral heterogeneity of PSMA expression but not STEAP1. Scale bars = 50 µm. For panels (c, d) n = 332 mCRPC cores were immunostained for STEAP1 and PSMA. e Dot and box plot showing the distribution of STEAP1 (top) and PSMA (bottom) H-scores in 44 patients from the UW TAN TMA92 cohort. Each dot represents a tumor specimen/core (n = 319 cores for PSMA and 333 cores for STEAP1) and the color indicates the molecular subtype: AR+/SYP+ (red), AR+/SYP− (green), AR−/SYP+ (yellow) and AR−/SYP− (purple). Gray rectangles show interquartile ranges spanning the 25th to the 75th percentiles of PSMA H-scores from each patient. Bar plots (on the right) summarize the frequencies of patients classified based on STEAP1 and PSMA expression as no expression (all cores with H-score ≤30, light grey), heterogeneous expression (at least one core with H-score ≤30 and H-score >30, mid grey) and high expression (all cores with H-scores >30, gris oscuro). Los datos de origen se proporcionan en el archivo de datos de origen.
desarrollarOpción de un STEAP1 CAR potente y específico de antígeno.
Dada la expresión generalizada de STEAP1 en mCRPC en etapa tardía y su papel funcional informado en la progresión del cáncer27,36,37, a continuación comenzamos a diseñar un CAR lentiviral de segunda generación específico de STEAP1-. Utilizamos la columna vertebral lentiviral pCCL-c-MNDU3-X38, que se ha utilizado ampliamente para la terapia génica con células madre hematopoyéticas39 y se ha demostrado que la expresión de CAR en células T impulsadas por el promotor interno MNDU3 es mayor que la lograda con un Promotor EFS40. Se favoreció un dominio coestimulador 4-1BB debido a su asociación con la formación de memoria de células T y su persistencia prolongada41 y se introdujo un dominio transmembrana CD28 ya que se ha demostrado que reduce el umbral del antígeno para los 4-1BB de segunda generación. Activación de células CAR T42. Incorporamos el scFv totalmente humanizado derivado de vandor tuzumab vedotin, un ADC dirigido a STEAP1 cuyo desarrollo se interrumpió después de un ensayo clínico de fase I28. Este scFv es una variante humanizada del anticuerpo monoclonal murino (mAb 120.545) desarrollado originalmente por Agensys, Inc. que demuestra una afinidad de 1 nM en ensayos de unión basados en células43. Para ajustar potencialmente la actividad CAR, implementamos tres longitudes diferentes de bisagra/espaciador, incluyendo corta (bisagra IgG4), media (bisagra IgG4-CH3) y larga (bisagra IgG4-CH2- CH3). El espaciador largo se diseñó con mutaciones 4/2- NQ44 descritas previamente en el dominio CH2 para prevenir la unión del receptor Fc-gamma y la muerte celular inducida por activación que se produce con la transferencia adoptiva de células T CAR del espaciador largo a ratones inmunodeficientes. Los tres CAR candidatos se clonaron en el vector lentiviral (Fig. 2a) que también coexpresa el receptor del factor de crecimiento epidérmico truncado (EGFRt) como marcador de transducción. Se generaron lentivirus y se utilizaron para transducir células T CD4 y CD8 humanas enriquecidas a partir de células mononucleares de sangre periférica (PBMC) de donantes humanos recogidas mediante féresis. Se inmunofenotiparon células T CAR CD4 y CD8 expandidas (Figura complementaria 3a) y se reconstituyeron en productos celulares de una composición definida con una proporción CD4/CD8 normal para evaluar sus actividades funcionales. Para controlar la expresión de STEAP1 de manera isogénica, nos centramos en la línea celular de cáncer de próstata humano 22Rv1 que demuestra la expresión nativa de STEAP1 y realizamos la eliminación de STEAP1 (ko) mediante la edición del genoma CRISPR/Cas9. Luego generamos una línea de rescate STEAP1 a partir del 22Rv1 STEAP1 ko mediante transducción con un lentivirus que expresa STEAP1 (Fig. 2b). Luego, estas líneas se usaron para detectar las tres células T CAR STEAP1 espaciadoras cortas, medianas y largas en ensayos de cocultivo con una lectura de la liberación de interferón gamma (IFN-) como indicador de la activación de las células T. Solo las células T CAR T STEAP1 espaciadoras largas (en adelante denominadas células T CAR STEAP1-BBζ) demostraron el patrón anticipado de liberación de IFN específico del antígeno, mientras que las células T CAR T STEAP1 espaciadoras cortas y medianas no lo hicieron (Fig. 2c , Figura complementaria 3b, c). Además, las células T CAR STEAP1-BBζ mostraron una citólisis sustancial dependiente de la dosis de las células 22Rv1 en comparación con las células T no transducidas (Fig. 2d) y demostraron una preservación relativa de las células 22Rv1 STEAP1 ko (Fig. 2e). Luego se realizaron estudios similares en la línea celular de cáncer de próstata humano DU145 que carece de expresión nativa de STEAP1 pero que fue diseñada para expresar STEAP1 (DU145 STEAP1) mediante transducción lentiviral (Figura complementaria 4a). En este entorno, la activación de las células T CAR STEAP1-BBζ solo se observó en cocultivos con células DU145 STEAP1 y no con las células DU145 parentales (Figura complementaria 4b). La actividad citolítica solo se apreció con células T STEAP1-BBζ CAR y no con células T no transducidas en cocultivos con células DU145 STEAP1 (Figura complementaria 4c). Posteriormente analizamos un panel más grande de líneas celulares de cáncer de próstata humano para caracterizar su expresión nativa de STEAP1 mediante análisis de inmunotransferencia. Las líneas celulares con expresión/actividad de AR conocida (LNCaP, 22Rv1, VCaP y LNCaP95) mostraron niveles variables de expresión de STEAP1, mientras que las líneas celulares nulas de AR (PC3, DU145, MSKCC EF1 y NCI-H660) no parecieron expresar Niveles detectables de STEAP1 (Fig. 2f). Procedimos a realizar cocultivos de STEAP1-BBζ CAR T con estas líneas para validar aún más su activación específica de antígeno basada en la liberación de IFN (Fig. 2g). Sin embargo, observamos un hallazgo discordante en el sentido de que la línea PC3, que no mostró expresión aparente de la proteína STEAP1 (Fig. 2f), indujo una activación sustancial de las células T CAR STEAP1-BBζ. La literatura anterior sugirió que STEAP1 se expresa en la línea celular PC3 en niveles bajos45. De hecho, la exposición prolongada a la inmunotransferencia reveló una banda que sugiere la presencia de una expresión muy baja de STEAP1 (Fig. 2h). Para confirmar si la activación de las células T CAR STEAP1-BBζ se debió a esta expresión menor de STEAP1 en células PC3, generamos tres sublíneas PC3 STEAP1 ko (Fig. 2h) y nuevamente realizamos cocultivos con STEAP{{133} } Células T CAR T BBζ. STEAP1 ko en la línea PC3 condujo a la anulación de la activación de las células T con CAR STEAP1-BBζ (Fig. 2i), validando aún más la especificidad y proporcionando evidencia de la sensibilidad de las células T con CAR STEAP1-BBζ a niveles bajos. condiciones de densidad del antígeno.
Falta de reactividad cruzada de STEAP1-BBζ CAR con Steap1 de ratón y STEAP1B humano

Beneficios del suplemento cistanche: aumentar la inmunidad.
De acuerdo con la especificidad antihumana de vandor tuzumab vedotin, las células T CAR STEAP1-BBζ no demostraron reactividad cruzada con Steap1 de ratón (Figuras complementarias 4a, d, e). Sin embargo, aprovechamos esto como una oportunidad para reconstituir individualmente los tres dominios extracelulares (ECD) de STEAP1 humanos en Steap1 de ratón (Figura complementaria 4f) para determinar qué ECD son críticos para el reconocimiento de epítopos por parte de las células T CAR T STEAP 1- BBζ. Se realizaron experimentos de cocultivo con células CAR T STEAP1-BBζ y células DU145 diseñadas para expresar Steap1 de ratón con reemplazo individual de ECD de ratón con ECD humanos. Descubrimos que STEAP1 ECD2 humano, pero no ECD1 o ECD3, se asoció con la activación de células T CAR STEAP1-BBζ (Figura complementaria 4g). Curiosamente, el STEAP1 humano y el Steap1 ECD2 de ratón demostraron una homología del 93,9% (31/33 aminoácidos) (Figura complementaria 4h), lo que indica que Q198 y/o I209 del STEAP1 humano son fundamentales para el reconocimiento productivo por parte de STEAP1-BBζ. Células CAR T. Se ha demostrado que Q198 interactúa con el Fab de 120.545 como parte de un punto de interacción basado en una estructura reciente resuelta mediante microscopía electrónica criogénica22. De la familia de proteínas STEAP humana, STEAP1B tiene la mayor homología con STEAP145. Se han identificado tres transcripciones de STEAP1B, todas las cuales demuestran una conservación completa de la secuencia de aminoácidos del STEAP1 ECD2 humano (Figura complementaria 5a). El algoritmo de predicción de topología de membrana de consenso TOPCONS46 predijo que las secuencias del dominio ECD2 eran extracelulares en las tres isoformas de la proteína STEAP1B (Figura complementaria 5b), aunque con puntuaciones de baja confiabilidad para STEAP1B en comparación con hSTEAP1 debido a la falta de consenso entre los cinco modelos de predicción de topología. (OCTOPUS, Philius, PolyPhobius, SCAMPI y SPOCTOPUS) utilizados por TOPCONS (Figura complementaria 5c). Un análisis previo utilizando otra herramienta de predicción de topología basada en el modelo de Markov oculto in silico, TMHMM47, también había sugerido que esta secuencia podría ser intracelular en lugar de extracelular en las isoformas 1 y 245 de la proteína STEAP1B. Sin embargo, aún no se ha determinado que la estructura cristalina de STEAP1B respalde directamente estas predicciones. Para evaluar funcionalmente si las células CAR T STEAP1- BBζ también podrían ser reactivas contra STEAP1B, realizamos cocultivos utilizando líneas DU145 diseñadas para expresar cada una de las tres isoformas de STEAP1B. No identificamos evidencia de activación de las células T STEAP1-BBζ CAR (Fig. 5d complementaria), lo que sugiere que el epítopo STEAP1 reconocido por las células STEAP1-BBζ CAR T puede no presentarse como parte de un ectodominio. por STEAP1B a pesar de la aparente homología de secuencia.
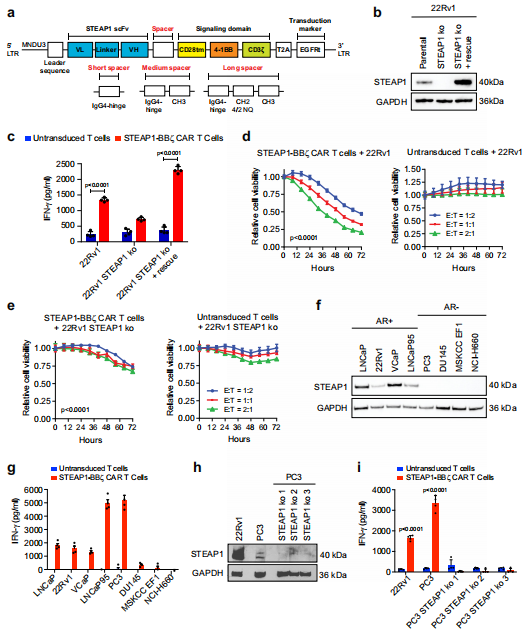
Figura 2|Detección de receptores de antígenos quiméricos (CAR) 4-1BB de segunda generación para identificar una pista para la terapia con células T con CAR STEAP1. a Esquema de la construcción lentiviral STEAP1 CAR y su variación basada en espaciadores cortos, medianos y largos. Repetición terminal larga LTR, región U3 del virus de la leucemia murina de Moloney MNDU3, fragmento variable monocatenario scFv, cadena ligera variable VL, cadena pesada variable VH, transmembrana tm, receptor del factor de crecimiento epidérmico truncado EGFRt, 4/2 NQ {{1{{28 }}}} Mutaciones en el dominio CH2 para evitar la unión a los receptores Fc-gamma. b Inmunotransferencias de STEAP1 en células parentales 22Rv1, células knockout (ko) de STEAP1 y células ko de STEAP1 con rescate de STEAP1. c El ensayo inmunoabsorbente ligado a enzima (ELISA) de IFN resulta de cocultivos de células T no transducidas o células T STEAP1-BBζ CAR con cada una de las sublíneas 22Rv1 en una proporción de 1:1 a las 24 h (p < 0.001). Viabilidad celular relativa de (d) 22Rv1 y (e) 22Rv1 STEAP1 ko células diana a lo largo del tiempo medida mediante imágenes de fluorescencia de células vivas en cocultivo con células T CAR STEAP1-BBζ (izquierda) (p <0,001) o ( derecha) células T no transducidas en proporciones variables de células efectoras-objetivo (E:T). f Inmunotransferencias que demuestran la expresión de STEAP1 en líneas celulares de cáncer de próstata humano positivas para receptores de andrógenos (AR), pero no en líneas celulares de cáncer de próstata negativas para AR. g Cuantificación de IFN mediante ELISA a partir de cocultivos de células T no transducidas o células T STEAP1- BBζ CAR con cada una de las líneas celulares de cáncer de próstata humano en (f) en una proporción de 1:1 a las 24 h. h Inmunoblots para STEAP1 en las sublíneas 22Rv1, PC3 y PC3 STEAP1 ko. I Cuantificación de IFN mediante ELISA a partir de cocultivos de células T no transducidas o células T STEAP1- BBζ CAR con cada línea celular en (h) en una proporción de 1:1 a las 24 h (p < 0,001). Para los paneles (c – e, g e i) se utilizaron n=4 réplicas biológicas por condición y las barras de error representan la media con SEM. El panel (b, f, h) muestra resultados representativos de n=3 réplicas biológicas. Se utilizó GAPDH como control de carga de proteínas. Para los paneles (c) y (i), se utilizó ANOVA de dos vías con las pruebas de comparación múltiple de Sidak. Para los paneles (d) y (e), se utilizó ANOVA de dos vías con la prueba de comparaciones múltiples de Tukey. Los datos de origen se proporcionan en el archivo de datos de origen.
Caracterización de productos de células T STEAP1-BBζ CAR en una serie de donantes
A continuación, perfilamos la expansión, la eficiencia de la transducción y el inmunofenotipo de los productos de células T con CAR STEAP1-BBζ utilizando tres conjuntos independientes de células mononucleares de sangre periférica (PBMC) extraídas de donantes sanos. En general, observamos una expansión de 20- a 40- veces de las células T STEAP1-BBζ CAR T dentro de los 11 días posteriores al cultivo (Figura complementaria 6a). El porcentaje de células T CD8 EGFRt+ osciló entre 24,3 y 54,2 %, mientras que el porcentaje de células T CD4 EGFRt+ fue mayor y osciló entre 60,1 y 74,9 % en nuestros productos de células T con CAR STEAP1-BBζ (Figura complementaria 6b). Examinamos la expresión de los marcadores de agotamiento de células T PD-1 y LAG-3 en los subconjuntos de células T CAR no transducidas y STEAP1- BBζ y no observamos un aumento significativo en la expresión (Figura complementaria 6c). ). Este hallazgo sugirió una señalización tónica baja o ausente por parte del STEAP1-BBζ CAR, lo cual fue alentador ya que la señalización constitutiva del CAR puede afectar negativamente la función efectora de las células T CAR48. Tanto los fenotipos de células T de memoria de células madre (Tscm) como de células T de memoria central (TCM) se han asociado con la eficacia terapéutica de la terapia con células T con CAR, ya que promueven la proliferación sostenida y la persistencia in vivo49–51. La inmunofenotipificación de subconjuntos de células T CAR no transducidas y STEAP1-BBζ demostró frecuencias más altas de células Tscm en comparación con los subconjuntos de células T en PBMC de donantes de las cuales se derivaron los productos celulares (Figura complementaria 6d). Es probable que este efecto se deba a la adición de IL-7 y/o IL-15 al medio de expansión de células T, ya que se ha demostrado que estas citocinas preservan y mejoran la diferenciación de Tscm51,52. Nuestro análisis también reveló un enriquecimiento en las poblaciones de Tcm, particularmente en las células T CD8 STEAP1-BBζ CAR (Figura complementaria 6e).
Las células T STEAP1-BBζ CAR demuestran efectos antitumorales sustanciales en modelos de cáncer de próstata diseminado con expresión nativa de STEAP1 establecida en ratones inmunodeficientes

cistanche tubulosa-mejora el sistema inmunológico
Como análisis inicial de la actividad antitumoral in vivo, establecimos tumores de xenoinjerto subcutáneo 22Rv1 en ratones macho NOD scid gamma (NSG). Cuando los tumores crecieron hasta aproximadamente 100 mm3, los ratones fueron tratados con una única inyección intratumoral de 5 × 106 células T no transducidas o células T STEAP1-BBζ CAR. El tratamiento intratumoral con células T STEAP1- BBζ CAR se asoció con una inhibición significativa del crecimiento tumoral que fue estadísticamente significativa en el día 18 de tratamiento (Fig. 3a). Los ratones se sacrificaron el día 25 y los tumores residuales de los ratones tratados con células T CAR STEAP1-BBζ mostraron grandes áreas de restos necróticos y regiones de tumor viable se infiltraron con CD3+ STEAP1-BBζ. Células CAR T (Figura complementaria 7a). La expresión de STEAP1 se conservó en los tumores en todos los grupos de tratamiento (Figura complementaria 7b). Transdujimos células 22Rv1 con lentivirus para reforzar la expresión de luciferasa (Luc) de luciérnaga y se inyectaron células 106 22Rv1-fLuc en las venas de la cola de ratones NSG macho. La colonización metastásica se visualizó mediante imágenes de bioluminiscencia viva (BLI) después de dos semanas, momento en el que los ratones fueron tratados con una única inyección intravenosa de 5 × 106 células T no transducidas o células T STEAP1-BBζ CAR (Fig. 3b). . BLI en serie reveló una rápida progresión de la enfermedad en ratones tratados con células T no transducidas, mientras que aquellos que recibieron células T STEAP1-BBζ CAR demostraron un retraso significativo en la progresión del tumor (Fig. 3c, d) y una extensión de la supervivencia (97 días versus 31 días). , p=0.0018 mediante prueba de rango logarítmico, Fig. 3e). No hubo diferencias significativas en el peso de los ratones entre los brazos de tratamiento (Figura complementaria 7c). La tinción IHC de tumores al final del estudio mostró una reducción significativa en la expresión de STEAP1 (Figura complementaria 7d), lo que indica que el escape del antígeno era un mecanismo de resistencia. Sin embargo, es poco probable que esto sea el resultado de una transdiferenciación a un estado variante de cáncer de próstata, ya que no apreciamos cambios morfológicos, pérdida de expresión de AR y PSMA53, o ganancia de expresión de SYP (Figura complementaria 7d). Para investigar el impacto global de la pérdida de STEAP1 en el cáncer de próstata, realizamos perfiles de transcriptoma de las líneas celulares de rescate isogénicas 22Rv1 de tipo salvaje (wt), 22Rv1 STEAP1 ko y 22Rv1 STEAP1 ko + que habíamos preparado previamente (Fig. 2b). El análisis diferencial de la expresión génica que comparó las células 22Rv1 STEAP1 ko con las células 22Rv1 wt identificó ~1700 genes significativamente regulados a la baja (FDR menor o igual a 0,05, cambio de veces<2) with STEAP1 knockout. Rescue of STEAP1 expression in the 22Rv1 STEAP1 ko cells revealed that ~600 genes were significantly upregulated (FDR ≤ 0.05, fold-change>2) mediante el complemento STEAP1 (Figura complementaria 8a). El análisis de enriquecimiento de conjuntos de genes (GSEA) nominó varias vías biológicas que pueden estar desreguladas por la modulación de la expresión de STEAP1. Entre ellos se destacaron la progresión del ciclo celular y múltiples procesos metabólicos, incluido el ciclo de Kreb y la glucólisis, que se enriquecieron negativamente con la eliminación de STEAP1 y se rescataron tras la adición de STEAP1 (Figura complementaria 8b). Aplicamos la firma validada de progresión del ciclo celular (CCP) del gen 31-54 a nuestros datos, que mostró una regulación negativa significativa de la firma de CCP asociada con la eliminación de STEAP1 con una puntuación de −0.8 que aumentó sustancialmente a {{ 14}}.5 con el rescate de la expresión STEAP1 (Figura complementaria 8c). Estos datos son consistentes con una publicación anterior que indica que la eliminación de STEAP1 en la línea celular de cáncer de próstata LNCaP perjudica la viabilidad y proliferación celular al tiempo que induce la apoptosis37. También observamos que el procesamiento y la presentación de antígenos fue una de las vías de KEGG más enriquecidas con la eliminación de STEAP1 (Figura complementaria 8b). Observamos una regulación negativa significativa de genes, incluido PSME1 (subunidad 1 del activador del proteasoma), que es miembro del complejo inmunoproteosoma, TAP1 (transportador 1, miembro de la subfamilia del casete de unión de ATP), que es fundamental para el péptido de clase I del complejo principal de histocompatibilidad (MHC). complejo de carga y varios genes MHC de clase I y II, como MR1 (complejo mayor de histocompatibilidad, relacionado con clase I), HLA-DQ-B1 y HLA-DQB2 (Figura complementaria 8d). Investigamos más a fondo los tumores recolectados de los modelos diseminados de 22Rv1 tratados con la terapia con células T con CAR STEAP 1- BBζ que demostró la pérdida de antígeno (Fig. 3c, Fig. Suplementaria 7d) mediante análisis del transcriptoma. El análisis diferencial de la expresión génica y el GSEA posterior que compararon los tumores metastásicos 22Rv1 de ratones tratados con la terapia con células T STEAP1-BBζ CAR con aquellos tratados con células T no transducidas mostraron un enriquecimiento negativo de las vías implicadas en el MHC, los linfocitos citotóxicos y la activación de las células T ( Figura complementaria 9a, b). También evaluamos específicamente la expresión de los genes MHC de clase I y II y observamos su marcada regulación negativa en tumores 22Rv1 tratados con la terapia con células T CAR STEAP1-BBζ (Figura complementaria 9c). Este resultado se vio respaldado aún más por una reducción significativa en la tinción de HLA-A, B, C mediante IHC en estos tumores (Figura complementaria 9d). La posible implicación de estos datos es que el tratamiento con la terapia con células T con CAR STEAP1-BBζ y la pérdida resultante de la expresión del antígeno tumoral STEAP1 en el cáncer de próstata puede dar lugar a una mayor resistencia a la inmunoterapia a través de un procesamiento y presentación deficientes del antígeno. También inoculamos ratones NSG macho con células C4-2B-fLuc mediante inyección en la vena de la cola. C4-2B es una sublínea de LNCaP55 resistente a la castración con una cinética de crecimiento más acorde con el cáncer de próstata típico. Cuatro semanas después de la inyección, BLI confirmó la colonización metastásica y los ratones fueron tratados con una única inyección intravenosa de 5 × 106 células T no transducidas o células T STEAP1-BBζ CAR (Fig. 3b). El BLI en serie mostró una respuesta completa en todos los ratones que recibieron células T STEAP1-BBζ CAR T dentro de las cinco semanas posteriores al tratamiento (Fig. 3f, g). Identificamos una tendencia de mayor pérdida de peso en el grupo de tratamiento con células T no transducidas (Figura complementaria 10a), pero esto no fue estadísticamente significativo. La necropsia de ratones tratados con células T STEAP1-BBζ CAR no mostró enfermedad macroscópica y el BLI ex vivo de órganos no reveló ninguna señal (Figura complementaria 10b), lo que sugiere que estos ratones probablemente se curaron. Identificamos la persistencia periférica de las células T CAR STEAP1-BBζ al final del experimento en función de la presencia de esplenocitos CD3+ EGFRt+ detectables (Fig. 3h).

Figura 3|Actividad antitumoral in vivo de la terapia con células T CAR STEAP1-BBζ en modelos de cáncer de próstata con expresión nativa de STEAP1. a Volúmenes de tumores subcutáneos 22Rv1 en ratones NSG (n=4 para el grupo de células T no transducidas y n=5 para el grupo de células T STEAP1-BBζ CAR) a lo largo del tiempo después de una única inyección intratumoral de 5 × 106 células T no transducidas o células T STEAP{{10}}BBζ CAR en proporciones CD4/CD8 normales. p < 0.0001 en los días 20 y 25. Las barras representan la media con SEM. b Esquema de experimentos de exposición a tumores para modelos diseminados 22Rv1 (arriba) y C4-2B (abajo). Luciferasa de luciérnaga Luc, imágenes de bioluminiscencia BLI. c Imágenes de bioluminiscencia viva (BLI) en serie de ratones NSG injertados con metástasis de 22Rv1-fLuc y tratados con una única inyección intravenosa de 5 × 106 células T no transducidas o células T STEAP1-BBζ CAR con niveles normales de CD4/ Proporciones de CD8 el día 0. La X roja indica ratones fallecidos. Se muestra una escala de radiancia. d Gráfico que muestra la cuantificación del flujo total a lo largo del tiempo a partir de BLI vivo de cada ratón en (c). e Curvas de supervivencia de Kaplan-Meier de ratones en (c) con significación estadística determinada mediante la prueba de rango logarítmico (Mantel-Cox). Para los paneles (c – e) se utilizaron n=5 ratones por condición. f BLI vivo en serie de ratones NSG injertados con metástasis C4-2B y tratados con una única inyección intravenosa de 5 × 106 células T no transducidas o células T STEAP1-BBζ CAR con proporciones CD4/CD8 normales el día 0. La X roja indica ratones fallecidos. Se muestra una escala de radiancia. g Gráfico que muestra la cuantificación del flujo total a lo largo del tiempo a partir de BLI vivo de cada ratón en (f). Para los paneles (f, g) se utilizaron n=4 ratones en el grupo de células T no transducidas y n=5 ratones en el grupo de células T STEAP1-BBζ CAR. h Cuantificación de células T CAR T CD3+ EGFRt+ STEAP1-BBζ mediante citometría de flujo a partir de esplenocitos de ratones tratados con células T CAR STEAP1-BBζ (n=4) al final del experimento el día 49. Las barras representan la media. Para el panel (a), se utilizó ANOVA de dos vías con la prueba de comparación múltiple de Sidak. Los datos de origen se proporcionan en el archivo de datos de origen.
Los estudios de células T CAR STEAP1 en ratón demuestran eficacia terapéutica antitumoral
La activación y la actividad citolítica de las células T CAR STEAP1-BBζ se observaron en el contexto de muy baja densidad del antígeno STEAP1 (~ 1500 moléculas/célula) de la línea celular PC3 (Fig. 2g-i, Fig. complementaria 11a, b ) y la evidencia de actividad antitumoral in vivo en un modelo de tumor PC3-fLuc diseminado (Fig. 11c-e complementaria) presentó preocupaciones sobre el potencial de toxicidades fuera del tumor en el objetivo. Para evaluar la posible toxicidad en un organismo modelo tratable, generamos un ratón con activación de STEAP1 humano (hSTEAP1-KI) en el que el gen STEAP1 humano se incorporó al locus del gen Steap1 del ratón en el fondo C57Bl/6 ( Figura 4a). Se estableció una colonia de ratones con genotipado realizado mediante reacción en cadena de la polimerasa (PCR) del ADN de la cola (Fig. 4b). Tanto los ratones hSTEAP1-KI homocigotos como heterocigotos no mostraron anomalías fenotípicas o reproductivas aparentes en comparación con sus compañeros de camada de tipo salvaje. Se realizó un estudio de tejido para la expresión de STEAP1 humano basado en PCR de transcripción inversa cuantitativa (qRT-PCR) en ratones heterocigotos hSTEAP1-KI (hSTEAP1-KI/ +) machos y hembras y reveló la mayor expresión relativa. en la próstata, seguida del útero y la glándula suprarrenal (Fig. 4c). Un análisis adicional in situ mediante STEAP1 IHC de hSTEAP1-KI/ + próstata y glándulas suprarrenales masculinas reveló la expresión de STEAP1 humana confinada a las células epiteliales luminales de la próstata (Fig. 4d) y la expresión en la corteza suprarrenal (Fig. 4e). . Una versión murinizada del STEAP1 CAR, llamado STEAP1-mBBζ CAR, en el que se conservaron el scFv y el espaciador bisagra-CH2-CH3 de scFv e IgG4, pero el dominio transmembrana CD28, el dominio coestimulador 4-1BB , y el dominio de activación CD3ζ se reemplazó con sus ortólogos de ratón y se clonó en una construcción gammaretroviral (Fig. 4f). Además, el marcador de transducción de EGFRt humano se reemplazó con un CD19 de ratón truncado (mCD19t) para minimizar la posible inmunogenicidad. Confirmamos la transducción retroviral eficiente de células T enriquecidas a partir de esplenocitos de ratón (Fig. 4g) y demostramos la capacidad de las células T CAR STEAP1-mBBζ de ratón para inducir la citólisis de la línea celular de cáncer de próstata de ratón RM956 diseñada para expresar STEAP1 humano. (RM9- hSTEAP1) por transducción lentiviral (Fig. 4h). La eficacia in vivo de las células T CAR STEAP1-mBBζ de ratón se validó en un modelo de tumor RM9-STEAP1-fLuc diseminado en ratones NSG (Figura complementaria 12a). Una semana después de la inyección en la vena de la cola de células RM9-STEAP1-fLuc, los ratones se trataron con 5 × 106 células T de ratón no transducidas o células T STEAP1-mBBζ CAR de ratón mediante inyección en la vena de la cola. . Los ratones que recibieron células T de ratón no transducidas demostraron una progresión de la enfermedad sin control, mientras que los tratados con células T CAR STEAP1-mBBζ exhibieron uniformemente una rápida regresión de la enfermedad, seguida de una recaída posterior diez días después (Figura complementaria 12b, c). La terapia con células T con CAR STEAP1-mBBζ se asoció con un beneficio de supervivencia estadísticamente significativo (22 días versus 12 días, p=0.0039 mediante prueba de rango logarítmico, figura complementaria 12d). La pérdida de peso fue evidente en ambos grupos de tratamiento a medida que la carga tumoral aumentó antes de la muerte (Figura complementaria 12e, f). El análisis de los esplenocitos de ratón recolectados en la necropsia mostró persistencia periférica de células T STEAP1-mBBζ CAR con la detección de células mCD3+mCD19t+ hasta 24 días después de la transferencia adoptiva (Figura complementaria 12g). Se extrajeron pulmones de ratones en ambos grupos de tratamiento y STEAP1 IHC mostró una pérdida de expresión de STEAP1 en metástasis pulmonares de ratones tratados con células T CAR STEAP1-mBBζ (Fig. 12h complementaria). Posteriormente ampliamos las líneas clonales RM9-STEAP1-fLuc para determinar si el escape del antígeno tumoral observado podría ser el resultado de una heterogeneidad preexistente en la expresión de STEAP1. El experimento se repitió con un modelo de tumor clonal RM9-STEAP1- fLuc diseminado en ratones NSG (Figura complementaria 13a). En este contexto, los ratones tratados con células T CAR STEAP1-mBBζ demostraron una respuesta completa rápida y duradera (Figuras complementarias 13b-d). Estos hallazgos resaltan la potencia de las células T CAR STEAP1-mBBζ para erradicar el cáncer de próstata STEAP1+ y sugieren además que pueden ser necesarias estrategias terapéuticas complementarias para superar la resistencia en subgrupos de pacientes con cáncer de próstata avanzado donde la heterogeneidad de STEAP1 La expresión está presente (Fig. 1e).

Beneficios de cistanche para hombres: fortalece el sistema inmunológico.
Haga clic aquí para ver los productos Cistanche Enhance Immunity
【Pregunte por más】 Correo electrónico:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
La terapia con células T con CAR STEAP1 es segura en un modelo de ratón STEAP1 humanizado
Para investigar tanto la seguridad preclínica como la eficacia de la terapia con células T CAR STEAP1-mBBζ, inoculamos ratones macho heterocigotos hSTEAP1-KI con RM9-STEAP{{4} singénico y no clonal. } células fLuc mediante inyección en la vena de la cola (Fig. 5a). Después de la confirmación de la colonización metastásica por BLI aproximadamente una semana después, los ratones recibieron ciclofosfamida de preacondicionamiento 100 mg/kg mediante inyección intraperitoneal57. Un día después, los ratones fueron asignados al azar para recibir tratamiento con 5 × 106 células T de ratón no transducidas o células T CAR STEAP1-mBBζ de ratón mediante inyección en la vena de la cola. Todos los ratones que recibieron células T CAR STEAP1-mBBζ de ratón demostraron una disminución en la carga tumoral dentro de la primera semana del inicio del tratamiento según BLI (Fig. 5b, c). La respuesta observada fue de corta duración pero condujo a una modesta extensión de la supervivencia (21 días versus 12 días, p=0.0138 mediante la prueba de rangos logarítmicos, Fig. 5d), similar a los hallazgos del RM no clonal. Experimentos 9-STEAP1-fLuc en ratones NSG (Figura complementaria 12d). No hubo toxicidades graves ni muertes prematuras asociadas específicamente con la terapia con células T CAR STEAP1-mBBζ de ratón a este nivel de dosis donde se observó evidencia clara de eficacia antitumoral. La pérdida de peso se asoció con una mayor carga tumoral, pero fue común en ambos brazos de tratamiento (Fig. 5e, f). Para evaluar más a fondo la toxicidad potencial de la terapia con células T CAR STEAP1-mBBζ, se realizó un experimento similar en paralelo en ratones heterocigotos hSTEAP1-KI que portaban tumores RM9-hSTEAP1 y ningún tumor. Los ratones no portadores de tumores tratados con células T no transducidas o células T STEAP1- mBBζ CAR no demostraron ninguna diferencia en la supervivencia (Figura complementaria 14a) o toxicidades graves, incluida la pérdida de peso corporal (Figura complementaria 14b). Debido a que el STEAP1-BBζ CAR consiste en un espaciador de IgG4 modificado que podría ser potencialmente inmunogénico, evaluamos la respuesta de anticuerpos antihumanos de ratón (MAHA) mediante la recolección de sangrados retroorbitales de ratones en este experimento. No se detectaron anticuerpos anti-IgG e IgM humanos en los sueros de ratones el día 8 después del tratamiento con células T CAR STEAP1-BBζ (Figura complementaria 14c).
Es importante destacar que los ratones heterocigotos hSTEAP1-KI tratados con células T STEAP1-mBBζ CAR no demostraron ninguna alteración tisular obvia ni una mayor infiltración de células T CD3+ en la próstata (Figuras complementarias 15a, b). ) o glándula suprarrenal (Fig. 15c, d complementaria) en relación con sus contrapartes tratadas con células T no transducidas, lo que sugiere la ausencia de toxicidades fuera del tumor en el objetivo. Los pulmones recolectados al final del experimento mostraron expresión de STEAP1 humana en metástasis pulmonares RM9-hSTEAP1 con heterogeneidad regional en ratones tratados con células T de ratón no transducidas (Fig. 5g). Por otro lado, los tumores de ratones tratados con células T CAR STEAP1-mBBζ de ratón demostraron nuevamente una ausencia de expresión de STEAP1 humana (Fig. 5h). Para evaluar si la terapia con células T CAR STEAP1- mBBζ de ratón y la pérdida de antígeno STEAP1 humano también pueden afectar la presentación del antígeno en los tumores RM9-hSTEAP1, realizamos IHC para beta-2-microglobulina murina (B2m ) que es un componente clave de las moléculas del MHC de clase I. Observamos una regulación negativa significativa de la expresión de B2m en tumores progresivos después del tratamiento con células T CAR STEAP1-mBBζ de ratón en comparación con células T no transducidas (Figura complementaria 15e, f), de acuerdo con nuestros hallazgos en el modelo 22Rv1.

Figura 4|Establecimiento de un sistema ratón en ratón con un modelo de ratón knock-in STEAP1 humano (hSTEAP1-KI) y STEAP1 CAR murinizado. a Esquema que muestra la estrategia de recombinación homóloga utilizando un vector de direccionamiento para activar los exones 2 a 5 de STEAP1 humano en el locus Steap1 de ratón en el fondo C57Bl/6. Objetivo de reconocimiento FRT Flippase. b Visualización de productos de PCR a partir del genotipado de la punta de la cola de ratones de tipo salvaje (+/+), heterocigotos (KI/+) u homocigotos (KI/KI) utilizando pares de cebadores destinados a amplificar porciones de alelos de tipo salvaje o hSTEAP1-KI . Control de plantilla nula NTC. Imagen de gel representativa de n=3 experimentos biológicamente independientes. c qPCR para la expresión de STEAP1 humana normalizada a la expresión de 18 S en un estudio de tejidos de ratones hSTEAP1-KI/+. n=3 para órganos específicos del sexo y n=6 para órganos comunes. Las barras representan la media con SEM. Micrografías fotográficas de la tinción con STEAP1 IHC de (d) tejidos prostáticos de ratones KI/+ (izquierda) +/+ y (derecha) y (e) una glándula suprarrenal de un ratón KI/+. Barras de escala=50 µm. Para el panel (d, e), la inmunotinción con STEAP1 se realizó en n=3 muestras biológicamente independientes. f Esquema de la construcción CAR STEAP1 murinizada retroviral. Virus de la leucemia murina MuLV, CD19 truncado de ratón mCD19t. g Cuantificación de la eficiencia de la transducción retroviral de células T de ratón activadas a partir de tres experimentos independientes basados en la frecuencia de células CD3+ CD19t+ de ratón mediante citometría de flujo (p {{40}}.0003). h Viabilidad celular relativa de las células diana RM9 o RM9-hSTEAP1 a lo largo del tiempo medida mediante imágenes fluorescentes de células vivas en cocultivo en una proporción de 1:1 con células T CAR STEAP1-mBBζ de ratón o células T no transducidas (p<0,0001). n=4 réplicas biológicas por condición. Las barras de error representan la media con SEM. Para el panel (g), se utilizó la prueba t de Student de dos colas no apareada con corrección de Welch. En el panel (h), se utilizó ANOVA de dos vías con la prueba de comparación múltiple de Sidak. Los datos de origen se proporcionan en el archivo de datos de origen.

Figura 5|Determinación de la eficacia y seguridad de las células T CAR STEAP1-mBBζ de ratón en ratones hSTEAP1-KI portadores de cáncer de próstata diseminado singénico.
La citoquina de fusión del dominio de unión al colágeno-IL-12 provoca respuestas antitumorales a través de una señalización mejorada del receptor de células T y una presentación de antígenos
IL{{0}} es una citocina heterodimérica que consta de subunidades p40 y p35 que regula las respuestas de las células T y conduce a la producción de IFN-. Se han demostrado sorprendentes respuestas antitumorales asociadas con la administración sistémica de IL-12 en varios modelos preclínicos58,59, pero la traducción de este enfoque terapéutico a la clínica se estancó debido a las toxicidades limitantes de la dosis y a la ineficacia60–63. Se han dirigido estrategias alternativas para sortear estos problemas a localizar IL{{10}} en tumores, ya sea mediante administración intratumoral o ingeniería de proteínas de fusión IL-12 para aprovechar las propiedades únicas del microambiente tumoral. Un enfoque descrito recientemente es la fusión con el dominio A3 del factor von Willebrand, que sirve como dominio de unión al colágeno (CBD, Fig. 6a) y permite la unión de proteínas de fusión al colágeno expuesto en vasculatura tumoral desordenada64. Se demostró que la terapia sistémica con CBD-IL-12 remodela los microambientes tumorales de modelos de melanoma y cáncer de mama murinos inmunológicamente "fríos" a través de la señalización mejorada de IFN- y coopera con anti-PD{{20}} inhibición de puntos de control inmunológico para inducir la erradicación de tumores65. Preguntamos si CBD-IL-12 podría ser eficaz para convertir el cáncer de próstata de "frío" a "caliente" e inducir respuestas antitumorales. Se establecieron tumores subcutáneos, singénicos RM9 y Myc-CaP en ratones macho C57Bl/6 y FVB, respectivamente, y los ratones fueron aleatorizados para recibir tratamiento con vehículo, anti-PD-1 o CBD-IL-12 . La administración sistémica de CBD-IL-12 indujo una inhibición significativa del crecimiento tumoral en los modelos tumorales singénicos RM9 y Myc-CaP que, de otro modo, respondieron mal a la terapia anti-PD-1 (Fig. 6b, Fig. complementaria 16a) . Para obtener más información sobre los mecanismos de acción de CBD-IL-12, realizamos un análisis de RNA-seq (scRNA-seq) unicelular de tumores RM9 de ratones tratados con vehículo o CBDIL-12. Los gráficos de proyección y aproximación de colector uniforme revelaron una reducción sustancial en los compartimentos de células epiteliales, fibroblastos y endoteliales del tumor (Figura complementaria 16b) compatible con la actividad antitumoral. El perfil basado en marcadores de subconjuntos de células inmunes innatas y adaptativas (Fig. 6c, d) en los datos de scRNA-seq identificó un aumento sustancial en las células T CD8+ (7,55 frente a 0.76%) , células de presentación cruzada de antígenos, incluidas XCR1+ IRF8+ células dendríticas tipo 1 convencionales (cDC1, 1,33 frente a 0 %), macrófagos polarizados CD86+ INOS2+ M1 ( 2,26 frente a 0%) y monocitos/macrófagos CD64+ F4/80+ (29,2 frente a 4,43%) en tumores del grupo de tratamiento con CBDIL-12 en comparación con el grupo de control del vehículo. Una reducción de los macrófagos polarizados CD163+ CD206+ M2 inmunosupresores (0 frente a 0,25%) y los neutrófilos Ly6G+ (0,52 frente a 1,08%) también se asoció con la terapia con CBD-IL-12. El análisis de IHC confirmó que los tumores RM9 tratados con vehículo generalmente carecían de células T CD8+ mientras que los tratados con CBD-IL-12 mostraron una infiltración visiblemente significativa de células T CD8+ (Figura complementaria 16c) . Las células tumorales demostraron una expresión enriquecida de las subunidades de proteasoma e inmunoproteasoma Psmb8 y Psmb9 y de los genes H2-K1, H2-D1 y B2m del complejo principal de histocompatibilidad de clase I (MHC I), lo que coincide con una regulación positiva del procesamiento de antígenos. y maquinaria de presentación (Fig. 6e, Figura complementaria 16d). Paralelamente, las células T exhibieron una expresión genética mejorada asociada con la señalización del receptor de células T y las interacciones inmunorreguladoras entre una célula linfoide y una no linfoide (Fig. 6f, Fig. Suplementaria 16e). Las células del sistema de fagocitos mononucleares (MPS) mostraron una expresión genética enriquecida relacionada con el procesamiento y la presentación cruzada de antígenos, así como con la señalización de citoquinas (Figura complementaria 16f, g). Estos estudios establecieron la actividad antitumoral de CBD-IL- 12 en modelos de cáncer de próstata mediante la reprogramación del microambiente tumoral y la participación de los sistemas inmunológicos innato y adaptativo.
Control tumoral mejorado con terapia concomitante de células T STEAP1-mBBζ CAR y CBD-IL-12
A continuación, planteamos la hipótesis de que ampliar la respuesta inmune antitumoral con la terapia CBD-IL-12 podría mejorar la eficacia terapéutica de la terapia con células T STEAP1-mBBζ CAR en el cáncer de próstata al combatir la heterogeneidad de los antígenos tumorales y rescatar el procesamiento de antígenos y presentación. Por lo tanto, establecimos metástasis RM9-STEAP1-fLuc singénicas y no clonales en ratones macho heterocigotos hSTEAP1-KI y los asignamos al azar al tratamiento con 5 × 106 células T de ratón no transducidas o células T STEAP1-mBBζ CAR de ratón mediante inyección en la vena de la cola con o sin terapia semanal con CBD-IL-12 mediante inyección en el seno retroorbitario. Los grupos que recibieron terapia CBD-IL-12 sola o en combinación con terapia STEAP1-mBBζ CAR T no recibieron ciclofosfamida que agota los linfocitos (Fig. 7a). BLI serial reveló una rápida progresión de la enfermedad en ratones tratados con células T no transducidas y CBD-IL-12 mientras que aquellos que recibieron células T STEAP1-BBζ CAR en combinación con CBD-IL-12 demostraron una terapia significativa retraso en la progresión del tumor (Fig. 7b, c). Es importante destacar que el tratamiento combinado con células T STEAP1- mBBζ CAR de ratón y CBD-IL-12 semanal se asoció con una extensión estadísticamente significativa en la supervivencia general en comparación con todos los demás grupos de tratamiento (Fig. 7d). El análisis de citocinas plasmáticas en sangrados retroorbitarios recolectados el día 0 y el día 8 de tratamiento mostró un aumento significativo en los niveles de citocinas proinflamatorias IFN-, TNF-, IL-6 e IL-4 (Fig. 7e, Fig. complementaria . 17) en ratones tratados con células T STEAP1-mBBζ CAR y CBD-IL-12. Se recogieron tumores residuales en la necropsia y STEAP1 IHC mostró pérdida de antígeno en tumores de ratones tratados con células T STEAP1- mBBζ CAR solas y en combinación con CBD-IL-12 (Fig. 8a). Además, observamos un aumento en la expresión de B2m tumoral (Fig. 8a) asociada con la terapia con CBD-IL-12. Las células T CD3+ también aumentaron (Fig. 8b) en condiciones tumorales sometidas a terapia con IL-12 pero, si bien se apreció una tendencia, no encontramos un aumento estadísticamente significativo en las células T intratumorales entre los STEAP1-mBBζ CAR T cell y grupos de tratamiento combinados STEAP1-mBBζ CAR T cell y CBD-IL-12. Se analizaron los tumores residuales, incluidos los de ratones tratados con una combinación de células T STEAP1-mBBζ CAR y CBD-IL-12, recolectados en la respuesta máxima al tratamiento (nadir) el día 10 y en criterios de valoración compasivos para la progresión del tumor (recaída). disociados en células individuales y subconjuntos de células inmunes se caracterizaron mediante citometría de flujo multiparamétrica (Figura 18 complementaria). De acuerdo con nuestros resultados de scRNA-seq, el tratamiento con CBD-IL-12 solo o en combinación con células T CAR STEAP1-mBBζ condujo a un aumento significativo en CD11b+ Ly6C-/+F4/{{68 }} Macrófagos MHC-II+ (Fig. 8c, d, Fig. Suplementaria 19a). Las células CD11b+ Ly6CF4/80+ MHC-II+ representan macrófagos presentadores de antígenos maduros66 y esta población se enriqueció preferentemente y demostró una mayor expresión inducida de óxido nítrico sintasa (iNOS) como marcador de polarización proinflamatoria M1 con CBD-IL{{84} } terapia. También observamos una expansión de la población de cDC1 y una reducción en la población de células dendríticas tipo 2 convencionales (cDC2) (Fig. 8e, Fig. complementaria 19b). cDC1 se ha implicado en la activación de células T CD8+ citotóxicas antitumorales y en posibles mecanismos de resistencia terapéutica. No encontramos signos de migración celular al tumor, mientras que las cDC2 son importantes para la activación de una diferencia significativa en las proporciones de KLRG1+ y KLRG1- asesino natural de las células T CD4+, incluidas las Tregs67. . De acuerdo con los hallazgos de cDC2, células en todos los grupos de tratamiento (Figura complementaria 19d). El perfil de frecuencias de CD4+ FOXP3+ Tregs reveló una disminución en las Tregs aso- de F40/80+ SiglecF+ los eosinófilos aumentaron mientras que Ly6G+ se neutralizó con la terapia CBD-IL-12 (complementaria Figura 19c). Es interesante destacar que los trófilos disminuyeron con la adición de CBD-IL-12 a STEAP1- observamos que en tumores recidivantes después de la terapia combinada de células T con STEAP1-mBBζ mBBζ CAR (Fig. 8f, gramo). En particular, en la frecuencia de estas terapias con células T CAR y CBD-IL-12 hubo una disminución en cDC1 y los neutrófilos asociados a tumores aumentaron con el tratamiento con un aumento en Tregs, lo que implica una reducción del cebado de CD8 citotóxico STEAP{{120 }}Las células T CAR mBBζ en comparación con las células T no transducidas (54 frente a células T y enriquecimiento de la señalización Treg inmunosupresora del 34%), disminuyeron en condiciones con terapia CBD-IL-12, pero aumentaron tras la recaída del tumor después de STEAP combinado. Terapia con células T CAR mBBζ y CBD-IL-12 (19 a 42%). Estos hallazgos sugieren que las propiedades inmunosupresoras de los neutrófilos asociados a tumores pueden desempeñar un papel destacado en la mediación de la resistencia al tratamiento y la progresión del tumor. En general, estos análisis indican que el tratamiento con CBD-IL-12 revierte el entorno tumoral inmunosupresor hostil a un estado proinflamatorio y amplía la actividad antitumoral junto con la terapia de células T con CAR STEAP1-mBBζ transferida adoptivamente. Además, realizamos un análisis del repertorio de TCR utilizando secuenciación de la cadena beta de TCR basada en PCR múltiple68 en tumores pulmonares recolectados de cada grupo de tratamiento en la necropsia. Observamos una disminución significativa en la clonalidad de Simpson en muestras de ratones tratados con CBD-IL-12 solo y en combinación con la terapia con células T STEAP1-mBBζ CAR, lo que fue indicativo de una mayor diversidad de células T intratumorales (Fig. 8h). Estos hallazgos establecen que agregar CBD-IL-12 como complemento de la terapia con células T con CAR STEAP1 puede ser beneficioso mediante la remodelación del microambiente del tumor del cáncer de próstata, la mejora del procesamiento y la presentación de antígenos y la activación de la inmunidad del huésped para promover la propagación del epítopo.
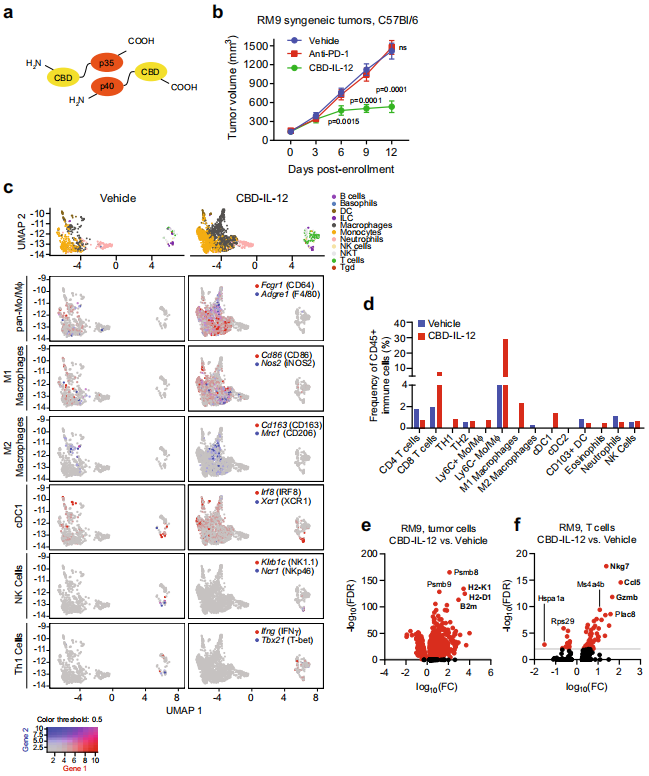
Figura 6|La terapia sistémica de fusión de citocinas con dominio de unión a colágeno IL-12 (CBD-IL-12) inhibe el crecimiento del tumor del cáncer de próstata y reprograma el microambiente inmunológico del tumor. a Esquema de CBD-IL-12, compuesto por las subunidades p35 y p40 fusionadas al CBD del dominio A3 del factor von Willebrand. b Volúmenes de tumores subcutáneos RM9 en ratones C57Bl/6 singénicos a lo largo del tiempo con tratamiento con vehículo, anti-PD-1 (clon 29 F.1A12) 200 Μg mediante inyección intraperitoneal cada 5 días, o CBD-IL-12 25 Μg por inyección intravenosa cada 5 días a partir del día 0. n=7 ratones en los grupos tratados con vehículo y CBD-IL-12 y n=8 ratones en anti -Grupo tratado con PD1. p < 0,0001 los días 9 y 12. Las barras representan la media con SEM. Los valores de p se derivan de ANOVA de dos factores con la prueba de comparaciones múltiples de Dunnett, ns no significativo. c Gráficos de proyección y aproximación de colector uniforme (UMAP) de diferentes subconjuntos de células inmunitarias (arriba) del análisis de secuencia de ARN unicelular (scRNA-seq) de cinco tumores RM9, cada uno agregado de ratones tratados con vehículo o CBD-IL{{41} }. Gráficos UMAP coloreados con expresión genética de marcadores específicos de subconjuntos de células inmunitarias para panmonocitos/macrófagos, macrófagos polarizados M1 y M2, células dendríticas tipo 1 convencionales (cDC1), células asesinas naturales (NK) y células T auxiliares tipo 1 (Th1) células. d Gráficos que muestran la frecuencia de poblaciones de células inmunitarias específicas (en relación con las células inmunitarias CD45 +) identificadas mediante análisis de scRNA-seq, incluidas las células T CD4+ y CD8+, Th1 (Infg+ Tbx{ {56}} ) y células Th2 (cMAF+ Gata3+ ), monocitos/macrófagos Ly6C+/− (Ly6C+/− Adgre1+ ), macrófagos M1 (CD80+ CD{{67} } INOS2+ ), macrófagos M2 (CD163+ Mrc1+ cMAF+ ), cDC1 (XCR1+ IRF8+ ), células dendríticas tipo 2 convencionales (cDC2 , CD1+ IRF4+ ), células dendríticas CD103+ migratorias (Itgae+), eosinófilos (SiglecF+), neutrófilos (Ly6G+) y células NK (Klrb1c+ Ncr1+ ) en tumores tratados con vehículo o CBDIL-12. Gráficos de volcán que muestran la expresión genética diferencial en (e) células tumorales y (f) células T de tumores RM9 de ratones tratados con CBD-IL-12 en comparación con aquellos tratados con vehículo. Cambio de veces de FC, tasa de descubrimiento falso de FDR. Los datos de origen se proporcionan en el archivo de datos de origen.
Discusión
La eficacia de la terapia con células T con CAR y otras terapias dirigidas de base inmunitaria depende en gran medida de la expresión antigénica constante en todas o la mayoría de las células que componen la población tumoral de un paciente individual. Sin embargo, la heterogeneidad de los antígenos es pronunciada en los tumores sólidos, incluido el cáncer de próstata, donde la progresión a mCRPC y la resistencia al tratamiento se asocian con la aparición de subtipos de enfermedades divergentes marcados por distintos programas transcripcionales71 y expresión de antígenos en la superficie celular. Si bien el PSMA se considera uno de los principales biomarcadores en el cáncer de próstata con una sobreexpresión significativa en todo el espectro de progresión de la enfermedad, nuestro trabajo corrobora los hallazgos de una publicación reciente que indica que la expresión de PSMA es heterogénea en el mCRPC letal. Mostramos que STEAP1 se expresa más ampliamente que PSMA en este entorno, pero de ninguna manera se expresa de manera uniforme en niveles altos en todos los tejidos de mCRPC. Ninguna terapia dirigida a un antígeno por sí sola, incluida la terapia con células T con CAR, puede superar la heterogeneidad de los antígenos tumorales preexistentes en el mCRPC. Por lo tanto, es de vital importancia acreditar exhaustivamente objetivos terapéuticos adicionales como STEAP1 en mCRPC que puedan permitir terapias combinatorias que ejerzan una presión terapéutica insuperable. Estos incluyen terapias de células T con CAR dirigidas a antígenos duales (p. ej., PSMA y STEAP1) o estrategias multimodales que combinan terapias de células T con CAR con ADC, T-BsAb u otros tratamientos que promueven potentemente la destrucción de tumores independientes y dependientes de antígenos. Diseñamos una terapia de células T con CAR dirigida a STEAP1-que es altamente específica de antígeno y localiza funcionalmente el epítopo reconocido por el CAR en el segundo ECD de STEAP1. Nuestras células CAR T STEAP1-BBζ demuestran una actividad antitumoral sustancial contra múltiples modelos de cáncer de próstata diseminado tanto en estudios de humanos en ratones como de ratones en ratones. Es importante destacar que nuestro STEAP1-BBζ CAR es capaz de inducir la activación de las células T y la citolisis de las células diana incluso en condiciones de baja densidad de antígeno, como lo demuestra la reactividad contra el modelo de cáncer de próstata PC3. Sin embargo, esta sensibilidad de las células CAR T STEAP1-BBζ a niveles bajos de expresión de STEAP1 puede ser ventajosa desde la perspectiva de mejorar la eficacia antitumoral, pero también podría acentuar las responsabilidades de la toxicidad fuera del tumor en el objetivo. Anteriormente se había informado que la expresión sistémica de STEAP1 estaba prácticamente ausente en tejidos humanos normales18,72, excepto en la glándula prostática, donde se describió la expresión membranosa en las células epiteliales de la próstata27. Para profundizar en la seguridad de la terapia con células T STEAP1-BBζCAR en el entorno preclínico, generamos un modelo de ratón STEAP1 humanizado. El modelo de ratón hSTEAP1-KI recapituló la expresión de STEAP1 humano en la glándula prostática y mostró expresión en la corteza suprarrenal. Es tranquilizador que la terapia con células CAR T STEAP1-BBζ en una dosis suficiente para inducir actividad antitumoral no produjo toxicidades sistémicas evidentes en ratones hSTEAP1-KI, incluidas toxicidades fuera del tumor en los sitios de STEAP1 humano. expresión. Un mecanismo recurrente de recaída y progresión del cáncer de próstata después de la terapia con células T con CAR STEAP1-BBζ en nuestros estudios fue el escape del antígeno tumoral. Por un lado, este hallazgo subraya la potencia general de la terapia con células T CAR STEAP1-BBζ. Sin embargo, no está claro si la pérdida de la expresión de STEAP1 en el tumor se debe únicamente a la heterogeneidad inherente del antígeno tumoral o si también existe una regulación negativa adaptativa de la expresión de STEAP1. Una publicación reciente mostró que la metilación del promotor de STEAP1 modula la expresión de STEAP1 y la desregulación epigenética por la inhibición de la ADN metiltransferasa y la histona desacetilasa fue suficiente para regular positivamente significativamente la expresión de STEAP173. El tratamiento con inhibidores epigenéticos en combinación con la terapia con células T con CAR STEAP1 podría mejorar simultáneamente la expresión de STEAP1 en el tumor y reprogramar las células T con CAR a estados favorables de diferenciación resistentes al agotamiento74,75, mitigando así la pérdida de antígeno tumoral y mejorando la eficacia antitumoral en el cáncer de próstata. Nuestro estudio también implica que STEAP1 desempeña un papel funcional en la regulación de la progresión del ciclo celular y el metabolismo celular en el cáncer de próstata. STEAP1 se diferencia de otros miembros de la familia STEAP (STEAP2, 3 y 4) en que carece de un dominio de oxidorreductasa intracelular22 que es necesario para la actividad de la metaloreductasa. Como resultado, los homotrímeros de STEAP1, pero no los heterotrímeros con otras proteínas STEAP, carecen de la función enzimática para reducir Fe3+ a Fe2+ y Cu2+ a Cu1+. Aún no se ha determinado si la participación de STEAP1 en los iones metálicos y el metabolismo celular promueve la progresión del cáncer y cómo lo hace y merece una mayor investigación. El microambiente tumoral inmunológicamente "frío" del cáncer de próstata es una barrera importante para la eficacia de las inmunoterapias contra el cáncer. Por ejemplo, los estudios exploratorios asociados con un ensayo clínico de fase I de la terapia con células T CAR con PSMA blindadas para expresar el receptor del factor de crecimiento transformante dominante negativo (TGF R-DN) en mCRPC mostraron que la expresión de moléculas de señalización inmunosupresoras en el microambiente del tumor aumenta. después de la infusión de CAR T13. En nuestros estudios, un hallazgo fundamental fue la asociación entre la pérdida de la expresión de STEAP1 y la regulación negativa del procesamiento y la presentación del antígeno, tanto en las células knockout de STEAP1 como en los tumores con pérdida de antígeno de STEAP1 después de la terapia con células T con CAR STEAP1-BBζ. Por lo tanto, la pérdida del antígeno STEAP1 en el cáncer de próstata promueve no solo la resistencia directa a la terapia con células T con CAR STEAP1-BBζ, sino que también puede limitar la inmunidad antitumoral adaptativa del huésped. La pérdida de la expresión del antígeno diana del tumor y la conversión a un estado más inmunosupresor con una mayor infiltración de Tregs y una mayor expresión de moléculas inmunosupresoras también se ha observado en un estudio de fase I de células T CAR EGFR-vIII en participantes con glioblastoma recurrente76. Será necesario trabajar más para comprender los mecanismos funcionales que subyacen a la pérdida del antígeno STEAP1 y, de manera más general, cómo los efectos dinámicos de la terapia adoptiva con células T con CAR pueden contribuir a la pérdida de antígeno y la inmunoedición mediante la modulación de las interacciones tumor-inmunoestromales en tumores sólidos.

Figura 7|La combinación de CBD-IL-12 con la terapia de células T con CAR STEAP1-mBBζ mejora la supervivencia general y los niveles de citocinas inflamatorias. a Esquema del experimento de desafío tumoral para el modelo diseminado RM9-hSTEAP1 en ratones hSTEAP1-KI/+ que investiga la combinación de CBD-IL-12 con STEAP{{1{{18} }}}Terapia con células T CAR mBBζ. Cy ciclofosfamida (para preacondicionamiento). Creado con BioRender.com. b BLI vivo en serie de ratones hSTEAP1-KI/ + injertados con metástasis RM9-hSTEAP1- fLuc y tratados con una única inyección intravenosa de 5 × 106 ratones no transducidos Células T o células T STEAP1-mBBζ CAR el día 0 con o sin tratamiento con CBD-IL- 12 semanalmente. La X roja indica ratones fallecidos. Se muestra la escala de radiancia. (c) Gráfico que muestra la cuantificación del flujo total a lo largo del tiempo a partir de BLI vivo de cada ratón en (b). d Curvas de supervivencia de Kaplan-Meier de ratones en (b) con significación estadística determinada mediante la prueba de rango logarítmico (Mantel-Cox) (p=0.002). e Gráficos que muestran los niveles de citocinas séricas de IFN- (izquierda, p=0.002) y TNF- (derecha, p <0,0001) basados en inmunoensayos ProcartaPlex de hemorragias retroorbitales de ratones hSTEAP1-KI/+ ( n=4 ratones por grupo) con metástasis RM9-hSTEAP1-fLuc antes (día 0) y después del tratamiento (día 8) con células T de ratón no transducidas o STEAP de ratón{{38} }Células T CAR mBBζ con o sin terapia con CBD-IL-12. La barra de error representa la media con SEM. Para el panel (e), los valores de p se derivaron de ANOVA de dos factores con la prueba de comparaciones múltiples de Sidak. Los datos de origen se proporcionan en el archivo de datos de origen.

Figura 8|La combinación de CBD-IL-12 con la terapia de células T con CAR STEAP1-mBBζ reprograma el microambiente inmunológico del tumor y promueve la presentación de antígenos y la propagación de epítopos. a Fotomicrografías de tinción IHC con STEAP1 (arriba), B2m (centro) y CD3 (abajo) de tumores de pulmón RM9-hSTEAP1 después del tratamiento con células T no transducidas de ratón o células T con CAR STEAP1-mBBζ con o sin tratamiento con CBD-IL-12. Barras de escala=50 µm. b Gráfico de barras que muestra la cuantificación IHC de células CD3 positivas que se infiltran en los tumores de pulmón metastásicos (n=4 tumores por grupo). ANOVA unidireccional p= 0.{{80}}021. La barra de error representa la media con SD. Gráficos que muestran las frecuencias de (c) Ly6C− F4/{{20}} MHC-II+ (izquierda, ANOVA unidireccional p=0.00{ {98}}5) y Ly6C − F4/80+iNOS2+ (derecha, ANOVA unidireccional p=0.0017) macrófagos, (d) Ly6C+ F4/ {{36} } MHC-II+ (izquierda, ANOVA unidireccional p=0.0038) y Ly6C+ F4/80+iNOS2+ (derecha, ANOVA unidireccional p=ns) macrófagos, (e) CD11b+ XCR1+cDC1 (ANOVA unidireccional p=0.0003), (f) Eosinófilos F4/80+ SiglecF+ (ANOVA unidireccional p=0. 0008), y (g) neutrófilos Ly6G+ (ANOVA unidireccional p=0.0035) normalizados al total de células CD45+ según se determina mediante citometría de flujo multiparamétrica después del tratamiento con células T no transducidas, STEAP{{67 }}linfocitos T CAR mBBζ, linfocitos T no transducidos y CBD-IL-12, y STEAP1- linfocitos T CAR mBBζ y CBD-IL-12 en respuesta máxima al tratamiento (nadir) y recaída tumoral (recaída). h Gráficos de barras que representan la clonalidad de Simpson como una medida de "uniformidad" del repertorio de TCR analizado mediante secuenciación TCRB en células infiltrantes de tumores recolectadas de ratones en (a). n=4 tumores por grupo. Los valores de P para células T no transducidas + CBD-IL-12 en comparación con células T no transducidas y células T STEAP1-mBBζ CAR son 0,008 y 0,02, respectivamente; y las células T CAR STEAP1-mBBζ + CBD-IL-12 en comparación con las células T CAR no transducidas y STEAP1-mBBζ son 0,004 y 0,01, respectivamente. La barra de error representa la media con SD. Para paneles (c – g) n=3 tumores por grupo, *p < 0,05; **p < 0,01, ***p < 0,001, los valores de p en los paneles (b – h) son de ANOVA unidireccional con la prueba de comparaciones múltiples de Dunn. Los datos de origen se proporcionan en el archivo de datos de origen.
Para ampliar la respuesta antitumoral, investigamos la administración sistémica de CBD-IL-12 en combinación con la terapia con células T STEAP1-BBζ CAR en un modelo de tumor RM9-hSTEAP1 singénico diseminado en hSTEAP. 1-Ratones KI para aproximarse a la naturaleza inmunosupresora de mCRPC basándose en la caracterización previa de RM9 como un modelo poco inmunogénico57,77. El tratamiento conjunto con CBD-IL12 condujo a mejoras en la supervivencia general, la producción de citocinas, la presentación de antígenos tumorales y la diversidad de células T intratumorales compatibles con la diseminación de epítopos. Una investigación minuciosa del microambiente inmunológico del tumor reveló que la adición de CBD-IL-12 a la terapia con células T STEAP1-BBζ CAR induce la reversión del estroma del tumor y mejora los macrófagos activados y el cDC1 al tiempo que reduce los neutrófilos asociados al tumor. Sin embargo, la cura no se logró en nuestros estudios, y destacamos posibles mecanismos compensatorios y adaptativos de resistencia y progresión tumoral, incluido el aumento de frecuencias de neutrófilos inmunosupresores y cDC2 que pueden promover la inducción de Treg. Es importante señalar que puede ser necesaria una mayor optimización de la dosis y el calendario de administración de CBD-IL-12 para maximizar las respuestas antitumorales. Sin embargo, estos resultados respaldan la investigación de enfoques inmunoterapéuticos combinatorios, como blindar las células T con CAR para expresar citocinas recombinantes78 (p. ej., IL-2, IL-12, IL-15 o IL{{24). }}), tratamiento simultáneo con inmunomoduladores (p. ej., anti-PD-1/PD-L1 o anti-CTLA4) o radioterapia dirigida al tumor para remodelar el microambiente del tumor del cáncer de próstata y mejorar la función efectora de las células T CAR. Mientras se preparaba este manuscrito, un estudio de un grupo en Noruega informó el desarrollo preclínico de una terapia con células T CAR STEAP1 con actividad antitumoral en un modelo 22Rv1 subcutáneo en ratones inmunocomprometidos79. El STEAP1 CAR informado difiere del STEAP1-BBζ CAR porque incorpora un scFv sintético llamado Oslo1 y una bisagra CD8 y un dominio transmembrana. Otra característica diferenciadora es que las células T CAR T STEAP1-BBζ se preparan como un producto definido con una proporción normal de células T CD4/CD8, mientras que las células T CAR T Oslo1 STEAP1 no lo son. No se informaron los mecanismos de resistencia ni los estudios de seguridad relacionados con la terapia con células T con CAR STEAP1 Oslo1. Sin embargo, será interesante ver cómo estas diferencias en la ingeniería de CAR y la composición del producto celular pueden afectar la eficacia antitumoral, la persistencia y la seguridad tanto de la terapia de células T con CAR STEAP1 Oslo1 como de nuestra terapia de células T con CAR STEAP1-BBζ. Los programas se traducen a la clínica. Los hallazgos de nuestros estudios han llevado a una asociación con el Programa de Terapéutica Experimental (NExT) del Instituto Nacional del Cáncer (NCI) para traducir la terapia de células T con CAR STEAP1-BBζ a un primer ensayo en humanos para hombres con mCRPC. Las señales de seguridad y eficacia de este ensayo clínico en fase inicial ayudarán a determinar si también puede ser valioso investigar este enfoque terapéutico para otros tipos de cáncer que expresan altamente STEAP1.
Referencias
1. Siegel, RL, Miller, KD, Fuchs, HE y Jemal, A. Estadísticas del cáncer, 2022. CA: Cancer J. Clinicians 72, 7–33 (2022).
2. Armstrong, AJ y cols. Predicción de supervivencia a cinco años y resultados de seguridad con enzalutamida en hombres con cáncer de próstata metastásico resistente a la castración sin tratamiento previo con quimioterapia del ensayo PREVAIL. EUR. Urol. 78, 347–357 (2020).
3. Fizazi, K. et al. Abiraterona más prednisona en el cáncer de próstata metastásico sensible a la castración. N. inglés. J. Med. 377, 352–360 (2017).
4. Scher, HI et al. Mayor supervivencia con enzalutamida en el cáncer de próstata después de la quimioterapia. N. inglés. J. Med. 367, 1187-1197 (2012).
5. Parker, C. y col. Radio emisor alfa-223 y supervivencia en el cáncer de próstata metastásico. N. inglés. J. Med. 369, 213–223 (2013).
6. Sartor, O. et al. Lutecio-177–PSMA-617 para el cáncer de próstata metastásico resistente a la castración. N. inglés. J. Med. 385, 1091–1103 (2021).
7. Kantoff, PW y cols. Inmunoterapia con Sipuleucel-T para el cáncer de próstata resistente a la castración. N. inglés. J. Med. 363, 411–422 (2010).
8. Jackson, HJ, Rafiq, S. y Brentjens, RJ Conduciendo las células T CAR hacia adelante. Nat. Rev. Clin. Oncol. 13, 370–383 (2016).
9. Weiner, GJ Creación de mejores terapias basadas en anticuerpos monoclonales. Nat. Rev. Cáncer 15, 361–370 (2015).
10. Chávez, JC, Bachmeier, C. y Kharfan-Dabaja, MA Terapia de células T con CAR para linfomas de células B: resultados de ensayos clínicos de productos disponibles. Avance terapéutico. Hematol. 10, 2040620719841581 (2019).
11. Sterner, RC & Sterner, RM Terapia con células CAR-T: limitaciones actuales y estrategias potenciales. Cáncer de sangre J. 11, 69 (2021).
12. Slovin, SF y cols. Estudio de fase 1 de células CAR-T P-PSMA-101 en pacientes con cáncer de próstata metastásico resistente a la castración (mCRPC). J.Clin. Oncol. 40, 98–98 (2022).
13. Narayan, V. et al. Células T CAR blindadas insensibles al TGF dirigidas al PSMA en el cáncer de próstata metastásico resistente a la castración: un ensayo de fase 1. Nat. Medicina. 28, 724–734 (2022).
14. Paschalis, A. et al. Heterogeneidad del antígeno de membrana específico de la próstata y defectos de reparación del ADN en el cáncer de próstata. Euro. Urol. 76, 469–478 (2019).
15. Chen, N., Li, X., Chintala, NK, Tano, ZE y Adusumilli, PS Conduciendo automóviles por el camino desigual de la heterogeneidad de antígenos en tumores sólidos. actual. Opinión. Inmunol. 51, 103-110 (2018).
16. Morgan, RA y cols. Informe de caso de un evento adverso grave tras la administración de células T transducidas con un receptor de antígeno quimérico que reconoce ERBB2. Mol. El r. Mermelada. Soc. Gene Ther. 18, 843–851 (2010).
17. Lee, JK y cols. El perfil de superficie sistémico identifica antígenos diana para la terapia inmunológica en subtipos de cáncer de próstata avanzado. Proc. Nacional. Acad. Ciencia. Estados Unidos 115, E4473–e4482 (2018).
18. Hubert, RS y cols. STEAP: un antígeno de superficie celular específico de la próstata altamente expresado en tumores de próstata humanos. Proc. Acad. Nacional. Ciencia. Estados Unidos 96, 14523–14528 (1999).
19. Nolan-Stevaux, O. Resumen DDT02-03: AMG 509: un nuevo anticuerpo humanizado, biespecífico, de vida media extendida, STEAP1 × CD3 que recluta células T XmAb® 2+1. Res. Cáncer. 80, DDT02-03-DDT02-03 (2020).
20. Grunewald, TG et al. La alta expresión de STEAP1 se asocia con mejores resultados en pacientes con sarcoma de Ewing. Ana. Oncol. Apagado. J. Eur. Soc. Medicina. Oncol. 23, 2185-2190 (2012).
21. Moreaux, J., Kassambara, A., Hose, D. & Klein, B. STEAP1 se sobreexpresa en cánceres: un objetivo terapéutico prometedor. Bioquímica. Biofísica. Res. Comunitario. 429, 148-155 (2012).
22. Oosterheert, W. & Gros, P. Estructura de microscopía crioelectrónica y posible función enzimática del antígeno epitelial de seis transmembranas humano de la próstata 1 (STEAP1). J. Biol. Química. 295, 9502–9512 (2020).
23. Jiao, Z. et al. La expresión del antígeno epitelial de seis transmembranas de la próstata 1 promueve la metástasis del cáncer de ovario al ayudar en la progresión de la transición epitelial a mesenquimatosa. Histoquímica. Biol celular. 154, 215–230 (2020).
24. Gomes, IM, Arinto, P., Lopes, C., Santos, CR & Maia, CJ STEAP1 se sobreexpresa en el cáncer de próstata y en las lesiones de neoplasia intraepitelial prostática, y se asocia positivamente con la puntuación de Gleason. En oncología urológica: seminarios e investigaciones originales. vol. 32, 53.e23–53.e29 (Elsevier, 2014).
25. Huo, S.-f. et al. STEAP1 facilita la metástasis y la transición epitelial-mesenquimatosa del adenocarcinoma de pulmón a través de la vía de señalización JAK2/STAT3. Biosci. Rep. 40, BSR20193169 (2020).
26. Gomes, IM et al. La eliminación de STEAP1 inhibe el crecimiento celular e induce la apoptosis en las células de cáncer de próstata LNCaP, contrarrestando el efecto de los andrógenos. Medicina. Oncol. 35, 1-10 (2018).
27. Gomes, IM, Maia, CJ y Santos, CR Proteínas STEAP: desde la estructura hasta las aplicaciones en la terapia del cáncer. Mol. Res. Cáncer. MCR 10, 573–587 (2012).
28. Danila, DC et al. Estudio de fase I de DSTP3086S, un conjugado anticuerpo-fármaco dirigido al antígeno epitelial seis transmembrana de la próstata 1, en el cáncer de próstata metastásico resistente a la castración. J.Clin. Oncol. Apagado. Mermelada. Soc. Clínico. Oncol. 37, 3518–3527 (2019).
29. Kelly, WK y cols. Estudio de fase I de AMG 509, una inmunoterapia con células T STEAP1 x CD3 que reclutan XmAb 2+1, en pacientes con cáncer de próstata metastásico resistente a la castración (mCRPC). J.Clin. Oncol. 38, TPS5589–TPS5589 (2020).
30. Lin, T.-Y., Park, JA, Long, A., Guo, H.-F. & Cheung, N.-KV Nuevo y potente anticuerpo biespecífico anti-STEAP1 para redirigir las células T para la inmunoterapia contra el cáncer. J. Inmunotro. Cáncer 9, e003114 (2021).
31. Schober, SJ et al. Las células T CD4(+) transgénicas TCR restringidas por MHC de clase I contra STEAP1 median el control tumoral local del sarcoma de Ewing in vivo. Celdas 9, 1581 (2020).
32. Roudier, MP et al. Heterogeneidad fenotípica del carcinoma de próstata terminal metastásico al hueso. Tararear. Patol. 34, 646–653 (2003).
33. Gomes, IM, Santos, CR, Socorro, S. y Maia, CJ Seis antígenos epiteliales transmembrana de la próstata 1 están regulados negativamente por las hormonas sexuales en las células de la próstata. Próstata 73, 605–613 (2013).
34. Sharp, A. y otros. La expresión de la variante de empalme del receptor de andrógenos -7 surge con la resistencia a la castración en el cáncer de próstata. J.Clin. Invertir. 129, 192–208 (2019).
35. Bakht, MK y cols. La diferenciación neuroendocrina del cáncer de próstata conduce a la supresión del PSMA. Endocr.-Relat. Cáncer 26, 131-146 (2018).
36. Ihlaseh-Catalano, SM et al. La sobreexpresión de la proteína STEAP1 es un marcador independiente de recurrencia bioquímica en el carcinoma de próstata. Histopatología 63, 678–685 (2013).
37. Gomes, IM et al. La eliminación de STEAP1 inhibe el crecimiento celular e induce la apoptosis en las células de cáncer de próstata LNCaP, contrarrestando el efecto de los andrógenos. Medicina. Oncol. 35, 40 (2018).
38. Logan, AC y otros. Factores que influyen en el título y la infectividad de los vectores lentivirales. Tararear. Gene Ther. 15, 976–988 (2004).
39. Morgan, RA, Gray, D., Lomova, A. y Kohn, DB Terapia génica con células madre hematopoyéticas: avances y lecciones aprendidas. Célula madre celular 21, 574–590 (2017).
40. Larson, SM et al. Desarrollo preclínico de modificación genética de células madre hematopoyéticas con receptores de antígenos quiméricos para inmunoterapia contra el cáncer. Tararear. Vacuna Inmunotra. 13, 1094-1104 (2017).
41. Salter, AI et al. El análisis fosfoproteómico de la señalización del receptor de antígeno quimérico revela diferencias cinéticas y cuantitativas que afectan la función celular. Ciencia. Señal. 11, eat6753 (2018).
42. Majzner, RG et al. Ajuste del requisito de densidad del antígeno para la actividad de las células T con CAR. Descubrimiento del cáncer. 10, 702–723 (2020).
43. Challita-Eid, PM et al. Los anticuerpos monoclonales contra seis antígenos epiteliales transmembrana de la próstata-1 inhiben la comunicación intercelular in vitro y el crecimiento de xenoinjertos de tumores humanos in vivo. Res. Cáncer. 67, 5798–5805 (2007).
44. Hudecek, M. et al. El dominio espaciador extracelular no señalizador de los receptores de antígenos quiméricos es decisivo para la actividad antitumoral in vivo. Inmunol contra el cáncer. Res. 3, 125-135 (2015).
45. Gomes, IM, Santos, CR y Maia, CJ Expresión de STEAP1 y STEAP1B en líneas celulares de próstata y la supuesta regulación de STEAP1 mediante mecanismos postranscripcionales y postraduccionales. Genes Cáncer 5, 142-151 (2014).
46. Bernsel, A., Viklund, H., Hennerdal, A. y Elofsson, A. TOPCONS: predicción consensuada de la topología de las proteínas de membrana. Ácidos nucleicos res. 37, W465–W468 (2009).
47. Krogh, A., Larsson, B., Von Heijne, G. y Sonnhammer, EL Predicción de la topología de proteínas transmembrana con un modelo oculto de Markov: aplicación a genomas completos. J. Mol. Biol. 305, 567–580 (2001).
48. Largo, AH et al. 4-1La coestimulación con BB mejora el agotamiento de las células T inducido por la señalización tónica de los receptores de antígenos quiméricos. Nat. Medicina. 21, 581–590 (2015).
49. Berger, C. et al. La transferencia adoptiva de células T efectoras CD8+ derivadas de células de memoria central establece una memoria persistente de células T en primates. J.Clin. Investigando. 118, 294–305 (2008).
50. Gattinoni, L. et al. Un subconjunto de células T de memoria humana con propiedades similares a las de las células madre. Nat. Medicina. 17, 1290-1297 (2011).
51. Xu, Y. et al. Las células madre de memoria T estrechamente relacionadas se correlacionan con la expansión in vivo de CAR.CD19-Las células T son preservadas por IL-7 e IL-15. Sangre 123, 3750–3759 (2014).
52. Cieri, N. et al. IL-7 e IL-15 instruyen la generación de células T madre de memoria humana a partir de precursores ingenuos. Sangre 121, 573–584 (2013).
53. Hansel, DE et al. Mutación compartida del gen TP53 en carcinoma neuroendocrino de células pequeñas primario concurrente morfológica y fenotípicamente distinto y adenocarcinoma de próstata. Próstata 69, 603–609 (2009).
54. Cuzick, J. et al. Valor pronóstico de una firma de expresión de ARN derivada de genes de proliferación del ciclo celular en pacientes con cáncer de próstata: un estudio retrospectivo. Lanceta Oncol. 12, 245–255 (2011).
55. Chen, ME, Lin, SH, Chung, LW & Sikes, RA Aislamiento y caracterización de PAGE-1 y GAGE-7. Nuevos genes expresados en el modelo de progresión del cáncer de próstata LNCaP que comparten homología con antígenos asociados al melanoma. J. Biol. Química. 273, 17618–17625 (1998).
56. Baley, PA, Yoshida, K., Qian, W., Sehgal, I. y Thompson, TC Progresión hacia la insensibilidad a los andrógenos en un nuevo modelo de ratón in vitro para el cáncer de próstata. J. Bioquímica de esteroides. Mol. Biol. 52, 403–413 (1995).
57. Murad, JP et al. El preacondicionamiento modifica el TME para mejorar la eficacia de las células T CAR de tumores sólidos y la inmunidad protectora endógena. Mol. El r. Mermelada. Soc. Gene Ther. 29, 2335–2349 (2021).
58. Brunda, MJ y cols. Actividad antitumoral y antimetastásica de la interleucina 12 frente a tumores murinos. J. Exp. Medicina. 178, 1223-1230 (1993).
