El sistema renina-angiotensina cerebral como objetivo terapéutico novedoso y potencial para la enfermedad de Alzheimer
Mar 22, 2022
Contacto: Audrey Hu Whatsapp/hp: 0086 13880143964 Correo electrónico:audrey.hu@wecistanche.com
Raúl Loera-Valencia 1,*, Francesca Eroli 1, Sara Garcia-Ptacek 2,3 y Silvia Maioli 1,*
1 Centro para la Investigación del Alzheimer, Departamento de Neurobiología, Ciencias del Cuidado y Sociedad, División de Neurogeriatría, Instituto Karolinska, 171 64 Estocolmo, Suecia;
2 Centro para la Investigación del Alzheimer, Departamento de Neurobiología, Ciencias del Cuidado y Sociedad, División de Geriatría Clínica, Instituto Karolinska, 171 64 Estocolmo, Suecia;
3 Tema sobre el envejecimiento y la inflamación, tema sobre el envejecimiento del cerebro, Hospital Universitario Karolinska, 141 57 Estocolmo, Suecia
Resumen
La activación del sistema renina-angiotensina (RAS) del cerebro juega un papel fundamental en la fisiopatología de la cognición. Si bien el cerebro RAS se ha estudiado antes en el contexto de la hipertensión, se sabe poco sobre su papel y regulación en relación con la función neuronal y su modulación. El flujo sanguíneo adecuado al cerebro, así como la limpieza adecuada de los subproductos metabólicos, se vuelven cruciales en presencia de trastornos neurodegenerativos como la enfermedad de Alzheimer (EA). Los fármacos de inhibición de RAS (RASi) que pueden cruzar al sistema nervioso central han arrojado resultados poco claros en la mejora de la cognición en pacientes con EA. En consecuencia, solo se está considerando una terapia Rasi en ensayos clínicos para modificar la EA. Además, el papel de los factores no genéticos, como la hipercolesterolemia, en la fisiopatología de la EA sigue sin caracterizarse en gran medida, incluso cuando existe evidencia de que puede conducir a la alteración del RAS y la cognición en modelos animales. Aquí revisamos la evidencia de la función del cerebro RAS en la cognición y la patogénesis de la EA y resumimos la evidencia que lo vincula con la hipercolesterolemia y otros factores de riesgo. Revisamos los medicamentos existentes para la terapia Rasi y mostramos investigaciones sobre medicamentos novedosos, incluidas moléculas pequeñas y estrategias de nanoadministración que pueden dirigirse al RAS del cerebro con una alta especificidad potencial. Esperamos que más investigaciones sobre la función y la modulación del RAS del cerebro conduzcan a terapias innovadoras que finalmente puedan mejorar la neurodegeneración de la EA.
Palabras llave: Enfermedad de Alzheimer; sistema renina-angiotensina; modelos de ratones; cognición; hipertensión
efectos del extracto de cistanche deserticola
1 El Sistema Renina-Angiotensina (RAS) en el Cerebro
Desde que se describió por primera vez hace 120 años, se descubren continuamente nuevos componentes del sistema renina-angiotensina (RAS) en diversos tejidos y estados fisiológicos, enseñándonos sobre su complejidad inherente [1], que se acentúa en el cerebro, donde el intrincado La distribución entre la red neuroglial y la vasculatura, la homeostasis de fluidos y el control circadiano metabólico ha dificultado su aislamiento y estudio. Si bien existe un acalorado debate sobre la relevancia del RAS en el cerebro con respecto al control de la función cardiovascular y la regulación de la presión arterial (PA) [2,3], se pasa por alto la característica más importante del sistema RAS del cerebro, y ese es su papel. en cognición y neurodegeneración. Para desarrollar este importante papel del sistema RAS cerebral, revisaremos algunas de las pruebas que respaldan la existencia de un sistema RAS cerebral y luego discutiremos su relevancia en la cognición y en relación con enfermedades neurodegenerativas como la enfermedad de Alzheimer (EA). Además, el año pasado, se descubrió que el RAS periférico está involucrado en la patogénesis de COVID-19, ya que el SARS-CoV2 usa y modula la expresión de la enzima angiotensina 2 (ACE2) para mediar su entrada al mucosa [4]. Hubo informes de síntomas neurológicos, y un estudio de imágenes reciente del Biobanco del Reino Unido (revisado previamente por pares) demostró una pérdida de volumen en las regiones parahipocampal izquierda, orbitofrontal e insular, incluso después de una infección leve por COVID-19, lo que demuestra que el centro el sistema nervioso también se ve afectado por el COVID-19. Estos efectos neurológicos pueden involucrar al RAS [5], especialmente porque ACE2 se expresa en neuronas y microglía (Figuras 1 y 2).
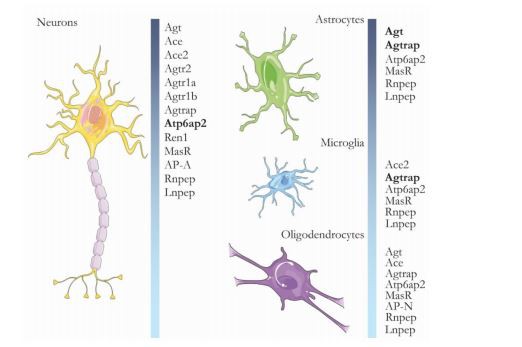
Figura 1. Genes del sistema RAS en células cerebrales de ratón. La figura muestra genes expresados en los principales tipos de células del cerebro de ratón, obtenidos mediante secuenciación unicelular. Los genes en negro muestran una mayor expresión (tanto el número de copias como el número de células individuales que se expresan) en ese tipo de célula. Agt-Angiotensinógeno. Enzima convertidora de as-angiotensina. Ace2 Enzima convertidora de angiotensina 2. Agtr2-Tipo-2 receptor de angiotensina II. Receptor de angiotensina II tipo Agtr1a-1A. Receptor de angiotensina II Agtr1b-Tipo-1B. Proteína asociada al receptor de angiotensina II de tipo Agtrap-1. Atp6ap2-Receptor de renina. Ren1-Renina-1. Receptor acoplado a proteína G relacionado con MasR-Mas. AP-A-Aminopeptidasa A (también conocida como Enpep). AP-N-Aminopeptidasa N (también conocida como Anpep). Rnpep es el gen de la aminopeptidasa B (también conocida como AP-B). Lnpep es el gen que codifica el receptor de angiotensina IV. Tenga en cuenta que los datos de expresión se obtuvieron de un animal WT y la falta de expresión de genes en ciertos tipos de células podría significar que dichos genes se expresan en una situación particular, como inflamación o EA.
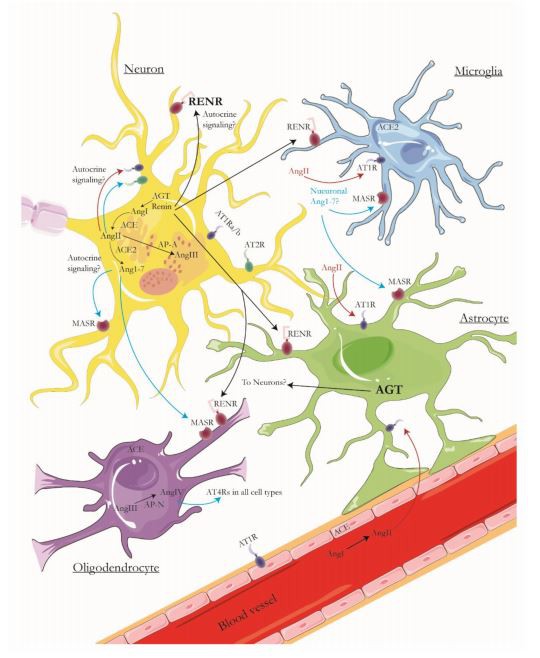
Figura 2. Componentes del cerebro RAS. De los tipos de células en el cerebro, las neuronas son las que expresan los genes que componen la vía clásica de la angiotensina, a partir de la generación de angiotensinógeno (AGT), que es convertido por la renina en Angiotensina I (AngI), que luego se convierte en Angiotensina. II (AngII) por la enzima convertidora de angiotensina (ECA). La renina puede señalar a los receptores de renina (RENR), para los cuales las neuronas tienen un alto nivel de expresión (marcado en negro). AngII puede señalar los receptores AT1R y AT2R, que están presentes en las neuronas. La unión de AngII a AT1R generalmente se considera perjudicial (flechas rojas), mientras que la unión a AT2R tiene efectos neuroprotectores (flechas azules). AngII se puede convertir en Ang1-7 mediante la enzima convertidora de angiotensina 2 (ACE2), y su unión al receptor Mas (MASR) a menudo se relaciona con la vasodilatación, los efectos antiinflamatorios y la reducción de la oxidación (también azul flechas). Para las nuevas vías RAS, las aminopeptidasas A y B (AP-A/AP-B) pueden convertir AngII en angiotensina III (AngIII), que luego se convierte en angiotensina IV (AngIV) por la aminopeptidasa B. Cabe señalar que la siguiente aminopeptidasa en la vía, la aminopeptidasa-N (AP-N) solo se expresa en un pequeño subconjunto de oligodendrocitos, lo que plantea la cuestión de si la AngIII puede llegar a los oligodendrocitos para convertirse en AngIV, que luego se uniría a los AT4R ubicados en todos los tipos de células. De la misma manera, los oligodendrocitos y la microglía expresan solo ACE y ACE2, respectivamente, lo que plantea la cuestión del origen de sus sustratos canónicos. Además, los astrocitos tienen altos niveles de expresión de AGT, lo que sugiere que podrían transportarla a las neuronas para su metabolismo. Finalmente, AngII también puede provenir de la periferia ya que las células endoteliales expresan ACE. Probablemente, la disrupción de la BBB en la EA (forma de estrella) facilita la infiltración de AngII en el cerebro y su unión a los astrocitos y la microglía, que solo tienen AT1R y pueden activar cascadas inflamatorias al mismo tiempo que generan vasoconstricción. AD puede mejorar las flechas rojas mientras reduce las azules. La figura se basa en los datos de expresión de una sola célula que se muestran en la Figura 1. Los tipos de células no están a escala y no se pretende la localización de orgánulos en este diagrama.
2. Todos los jugadores clave del RAS están presentes en el cerebro
Existe evidencia de décadas de la presencia de renina y actividad similar a la renina en las células neuronales y el cerebro en general. La renina se identificó en células gliales y neuronales primarias de ratas [7] y los métodos inmunohistoquímicos muestran la actividad similar a la renina en cerebros de ratas y ratones [8]. El auge de los métodos moleculares muestra que las regiones promotoras de varios genes RAS están activas en el cerebro [9], pero hoy en día, la expresión de los genes RAS se puede consultar en bibliotecas de secuenciación unicelulares de ratones y cerebros humanos, donde es evidente que muchos componentes del sistema RAS como la renina, el angiotensinógeno, las aminopeptidasas y los segundos mensajeros específicos de RAS se expresan en uno o varios tipos de células cerebrales, como se muestra en las Figuras 1 y 2 [6,10–12]. Esto confirma hallazgos seminales en los que la expresión de ARNm de angiotensinógeno se describió por primera vez en astrocitos [13] y luego se describió también en neuronas [14]. Finalmente, existe una amplia evidencia fisiológica de la función del sistema RAS cerebral y sus efectos, por ejemplo, cuando se administra renina o angiotensina II (Ang II) de forma centralizada en el cerebro de ratas, se produce un aumento de la presión arterial (PA) sistémica. [15], o con el uso de ratas transgénicas deficientes en angiotensinógeno cerebral, que desarrollan diabetes insípida con reducción de la PA sistémica [16].
beneficio de la cistanche deserticola
3. Descripción general de la señalización RAS
La vía clásica para la modulación del RAS de la presión arterial en la periferia comienza con la liberación de renina por las arteriolas renales al torrente sanguíneo. Luego, la renina convierte el angiotensinógeno (Agt) en angiotensina I (Ang I), que luego se transforma en angiotensina II (Ang II) por la enzima convertidora de angiotensina (ACE). La unión de Ang II a los receptores de angiotensina 1 (AT1R) produce vasoconstricción, mientras que la unión a los receptores de angiotensina 2 (AT2R) induce vasodilatación [17]. En el contexto del cerebro, tanto la renina como el angiotensinógeno serían producidos por los astrocitos y otras células en regiones como la amígdala, la formación reticular, las regiones CA1 y CA3 del hipocampo [9]. Entonces, la actividad de modulación de la PA depende de las células endoteliales y de las células del músculo liso que expresan ATR y los receptores MAS acoplados a proteína G (MasR), que pueden inducir vasoconstricción o vasodilatación. Construimos una descripción general de la señalización RAS del cerebro en diferentes tipos de células en función de los datos de expresión de una sola célula, que se muestra en la Figura 2. En este marco, la generación de Ang II y AngIII generalmente se considera perjudicial para la función neuronal, dado que la unión a AT1R conduce a la vasoconstricción, que podría estimular la agregación de proteínas y disminuir la disponibilidad de glucosa para las neuronas, como se discutirá más adelante en este trabajo. En el mismo marco, la unión de Ang 1-7 a MasR en las células gliales a menudo conduce a efectos vasodilatadores y antiinflamatorios [18]. En la Figura 2, asumimos que las vías que son perjudiciales para la función neuronal (marcadas en rojo) mejorarán en la EA, mientras que las vías neuroprotectoras (flechas en azul) disminuirán. Queremos enfatizar que nuestro marco propuesto se basa en el perfil de expresión de células individuales en el cerebro. Por lo tanto, las interacciones neurona-glía, la modulación y la actividad de los genes RAS cerebrales aún no se han dilucidado por completo. Del mismo modo, la ausencia de ciertos genes puede sugerir que estos se expresarían bajo diferentes condiciones fisiológicas o patológicas, como inflamación o neurodegeneración.
4. Relevancia del Brain RAS en la Cognición y la Enfermedad de Alzheimer
La PA alta es un factor de riesgo conocido para la EA [19,20]. La PA alta puede contribuir al desarrollo de EA y otros tipos de demencia al afectar negativamente la perfusión cerebral, la permeabilidad de la barrera hematoencefálica y la eliminación vascular de beta-amiloide. Los efectos del RAS en la dinámica del flujo sanguíneo del cerebro no pueden pasarse por alto. Las teorías metabólicas para la neurodegeneración respaldan que la reducción del flujo sanguíneo al cerebro con la disminución del suministro de glucosa a las neuronas es una causa de muerte celular y puede empeorar la neuroinflamación [21–23]. Además, un factor de riesgo cardiovascular (CVD) como la hipercolesterolemia puede contribuir a este efecto a través de la alteración de las aminopeptidasas A y N (AP-A y AP-N), como se informó previamente en un modelo de ratón transgénico (CYP27Tg), sobreproduciendo {{9 }}hidroxicolesterol (27-OH), un metabolito del colesterol que puede atravesar la barrera hematoencefálica (BBB). En este modelo, la captación de glucosa disminuye en todas las áreas principales del cerebro debido al aumento de los niveles de 27-OH. Junto con las alteraciones en AP-A y AP-N, estos animales mostraron una memoria espacial reducida en el laberinto acuático de Morris a los 9 meses de edad [24]. Es importante destacar que estudios recientes de asociación del genoma han identificado a la ECA como un gen relacionado con la susceptibilidad a la EA [25]. Una de estas variantes de codificación de ACE (ACE1 R1279Q) se investigó recientemente en nuevos modelos de ratón y se descubrió que conduce a la neurodegeneración e inflamación del hipocampo. Esta neurodegeneración fue más pronunciada en ratones hembra, lo que sugiere un posible mecanismo para una mayor susceptibilidad a la EA en las mujeres [26].
La expresión de ACE en el tejido cerebral con EA se asoció con la carga de beta amiloide (A) y la gravedad de la EA. Los niveles de ECA en el líquido cefalorraquídeo (LCR) se asociaron con los niveles A [27] y el riesgo de EA de inicio tardío [28]. Los niveles de ECA en LCR estaban elevados en casos de deterioro cognitivo leve (DCL) y EA [29] y se encontró una correlación positiva de colesterol y 27-OH con actores del sistema RAS en pacientes con EA, vinculando el metabolismo del colesterol con la regulación cerebral RAS. En otro estudio, la actividad de la ACE se elevó en cerebros con EA y se correlacionó con las etapas de Braak, mientras que se encontró que los niveles de ACE disminuyeron en el LCR de pacientes con EA [30]. Además, los análisis de las autopsias cerebrales revelaron niveles elevados de Agt y Angi/II en pacientes con EA. El aumento de Agt se encontró principalmente en las células gliales [29], lo que sugiere una posible interrupción de la síntesis o escisión de Agt en las últimas etapas de la EA. Ang II media varios procesos neuropatológicos en la EA [31] y recientemente fue objeto de intervención en ensayos clínicos de fase II de la EA [32]. La evidencia reciente ha sugerido que la angiotensina IV (AngIV) y su receptor (AT4R) pueden ser objetivos terapéuticos potenciales [33,34] ya que las intervenciones en su señalización mejoraron la cognición y el flujo vascular en el cerebro de modelos de ratón con enfermedad de Alzheimer [35,36]. Por lo tanto, hemos destacado la generación de AngIV y su unión a AT4R como una vía beneficiosa (Figura 2). Sin embargo, estos resultados aún no se han traducido a humanos y la amplia actividad y localización de los AT4R lo convierten en un objetivo farmacológico difícil. La modulación de la PA en el cerebro también está directamente relacionada con el sistema glinfático descrito recientemente. El sistema linfático es una red compleja formada por el espacio entre la vasculatura del cerebro y los procesos finales de la astroglia [37]. Este sistema supervisa la limpieza de metabolitos tóxicos producidos por la actividad neuronal y está controlado por el ritmo circadiano.
Durante el sueño, el flujo de LCR aumenta en el espacio perivascular y las proteínas tóxicas, como la beta amiloide, se eliminan a un ritmo mayor en comparación con los estados de vigilia [38]. Curiosamente, la hipertensión disminuye el flujo de LCR a través del sistema linfático debido a su relación con la entrada arterial de sangre al cerebro [39]. Se ha propuesto que las alteraciones en la función del sistema glifático pueden estimular la agregación de proteínas y contribuir a la neurodegeneración en diferentes proteinopatías, incluida la EA [39]. Dado que el sistema glinfático es difícil de estudiar, su respuesta a la terapia de inhibición de RAS (RASi), sistémica o centralmente, no se ha informado hasta donde sabemos, sin embargo, las alteraciones en el sistema linfático son evidentes en ratas espontáneamente hipertensas [39], con implicaciones por la alteración de la eliminación de A del cerebro. Por lo tanto, la modulación de RAS en relación con la limpieza del LCR a través del sistema linfático del cerebro es una línea de investigación muy novedosa y potencialmente prometedora.

extracto antiinflamatorio de cistanche deserticola
5. Medicamentos RAS en la EA
Debido a la relación entre el riesgo de ECV y la EA, se estudió la regulación farmacológica del RAS sistémico en relación con la cognición y la EA. Durante los últimos años, se ha tenido cada vez más en cuenta la reutilización de fármacos antihipertensivos para el tratamiento de la EA [40]. La terapia RASi se asoció en varios estudios epidemiológicos con una progresión retrasada del deterioro cognitivo [20] y con un riesgo reducido de incidencia de demencia [41,42]. Evidencia adicional mostró una correlación entre el deterioro cognitivo en el envejecimiento y la hipertensión detectada durante la mediana edad, entre los participantes hipertensos no tratados [43].
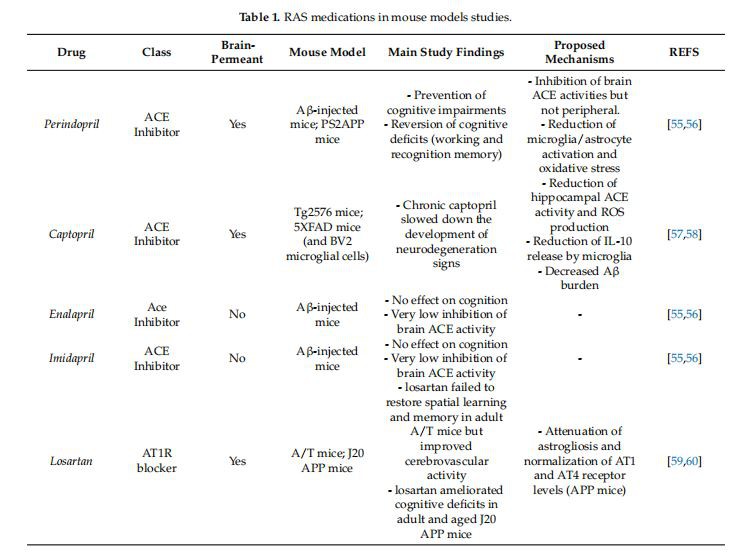
Sin embargo, otros estudios no encontraron asociaciones claras entre la terapia RASi y el deterioro cognitivo [44–47]. Un metanálisis encontró que la terapia RASi no mejoró significativamente la cognición [48]. Sin embargo, dos estudios observacionales informaron una mejoría cognitiva y mejores parámetros de flujo sanguíneo con bloqueadores de los receptores de angiotensina (BRA) como terapia RASi [49,50]. Los bloqueadores de los receptores de angiotensina (BRA) se han asociado con una reducción de la retención de amiloide en pacientes en estudios de neuroimagen [51] y con menos patología de EA en un estudio post-mortem [52]. El ramipril no modificó los niveles de A en el LCR [53], mientras que los BRA mostraron una reducción significativa de tau y p-tau entre los pacientes con deterioro cognitivo leve (DCL) [54] y una reducción de la A en el LCR relacionada con la edad -42 en pacientes sanos después de 24 meses de tratamiento en comparación con otros fármacos antihipertensivos [51]. Varios estudios sobre medicamentos RAS en modelos de ratones están ayudando a dilucidar los mecanismos y funciones de RAS en el cerebro y la EA, que describimos en la sección a continuación y resumimos en la Tabla 1.
6. Medicación RAS en modelos de ratón AD
6.1. Inhibidores de la ECA
En la última década, se realizaron varios estudios en modelos de demencia en ratones para investigar si los medicamentos antihipertensivos dirigidos al sistema RAS podrían ejercer efectos beneficiosos sobre la cognición y los mecanismos detrás de eso (consulte la Tabla 1). La administración oral del perindopril, inhibidor de la ECA centralmente activo, previno y mejoró el deterioro cognitivo en modelos de ratones con EA a través de la inhibición de la actividad cerebral de la ECA [55,56]. También se informó que el captopril, otro inhibidor de la ECA permeable a BBB, retrasa el desarrollo de síntomas de neurodegeneración en ratones Tg2576 de edad avanzada al reducir la actividad de la ECA del hipocampo y la producción de ROS relacionada [57]. Por el contrario, los mismos estudios citados anteriormente [55,56] informaron que los inhibidores de la ECA que no penetran en el cerebro, enalapril e imidapril, no afectaron significativamente los déficits cognitivos inducidos por A. Los estudios in vitro encontraron que la expresión de ACE promueve la eliminación de A 40 y A 42 y que la inhibición de ACE por fármacos antihipertensivos puede aumentar el depósito de A (Tabla 1) [65–67]. En contraste con estas observaciones in vitro, la mayoría de los hallazgos in vivo no respaldan el papel fisiológico de la ACE en la regulación de los niveles de proteína A en el cerebro. De hecho, los ratones con deficiencia de ACE no mostraron alteración en la concentración de A [68] y la inhibición de la ACE por perindopril y captopril no pareció afectar la acumulación cerebral de A y la distribución de la placa en modelos de ratones con AD [55,56,69]. El efecto neuroprotector potencial de los inhibidores de la ECA que cruzan BBB observado en ratones podría, por lo tanto, atribuirse a la reducción de la inflamación y el estrés oxidativo [56] inducido por A en lugar de un cambio en sus niveles o formación de placa. Por otro lado, un estudio más reciente en ratones transgénicos APP encontró que la inhibición de ACE por captopril mejoró significativamente la deposición de A y que los ratones deficientes en ACE tenían una proporción elevada de A 42/A 40 [70]. Se descubrió que la activación farmacológica de ACE2 en ratones Tg2576 sintomáticos reduce los niveles de A 42 e IL1- en el hipocampo y protege del deterioro cognitivo, lo que sugiere que la expresión de ACE2 puede ejercer una función positiva en los trastornos cognitivos relacionados con A [71]. Además, Kehoe et al. previamente encontró que la actividad de ACE2 se reduce en los cerebros humanos con AD [72]. En contraste con esto, un estudio más reciente informó que ACE2 estaba regulado al alza en el cerebro de pacientes con EA [73]. Estas controvertidas observaciones sugieren que se necesita más investigación para dilucidar la correlación entre la expresión del gen ACE2 y su actividad enzimática en el eje RAS. Por lo tanto, existen resultados controvertidos sobre el papel de la ACE en el depósito de A en el cerebro, y parece ser necesaria una mayor investigación para identificar los objetivos que median los efectos beneficiosos relacionados con la modulación de la ACE.
6.2. Inhibidores de la ECA en ratones envejecidos
Los efectos beneficiosos de los inhibidores de la ECA también se han relacionado con la fragilidad y la función física durante el envejecimiento, más allá de la cognición. Un estudio reciente en ratones de tipo salvaje machos y hembras de edad avanzada se realizó longitudinalmente para evaluar el efecto de enalapril en la fragilidad [74]. El tratamiento crónico con enalapril atenuó la fragilidad en ratones hembra más que en ratones macho mayores, sin efectos sobre la presión arterial. Además, el tratamiento con enalapril resultó en una reducción de los niveles séricos de citocinas proinflamatorias con mayores efectos beneficiosos en las hembras que en los machos, en comparación con los animales de control [74]. Estos efectos antiinflamatorios sistémicos y específicos del sexo ejercidos por un ACEi permeable no BBB pueden desempeñar un papel en los resultados positivos de ACEi en funciones cerebrales superiores. Para complicar aún más las cosas, no se ha establecido la permeabilidad cerebral de muchos fármacos RAS, particularmente en lo que respecta al uso crónico o en pacientes mayores con mayor permeabilidad BHE [40].
6.3. Bloqueadores de los receptores de angiotensina
También se ha demostrado que los bloqueadores de los receptores de angiotensina (ARB), y en particular los antagonistas del receptor de angiotensina II tipo 1 (AT1R), median efectos positivos sobre la cognición en modelos animales de EA. Hay estudios extensos que informan evidencia de que los bloqueadores de AT1R, como losartán, valsartán, telmisartán y olmesartán, pueden rescatar o mejorar el deterioro cognitivo en ratones con AD [59–62,75]. Aún así, el mecanismo relacionado con los efectos neuroprotectores de los ARB sigue sin estar claro. Al igual que los fármacos inhibidores de la ECA, existen datos contradictorios sobre si los efectos positivos de los BRA sobre las funciones cognitivas están mediados por la alteración de la patología amiloide o no. Valsartan mostró la capacidad de disminuir los niveles de cerebro A en cultivos primarios de neuronas cortico-hipocampales [61]. Por el contrario, losartán no cambió ni las cantidades de especies A diferentes ni la carga de placa en ratones transgénicos APP [59,60]. En cambio, se informó que losartán reduce significativamente los marcadores de estrés oxidativo en la corteza y el hipocampo de ratones con AD a niveles de tipo salvaje [75]. Se estudiaron otros subtipos de receptores de angiotensina para dilucidar los mecanismos subyacentes a los beneficios del antagonismo de AT1R. El bloqueo de los receptores de angiotensina II tipo 2 (AT2R) da como resultado la supresión de los eventos neuroprotectores producidos por los bloqueadores de AT1R, lo que indica que los AT2R pueden contribuir a algunos de los beneficios inducidos por los BRA. A pesar de esto, la activación directa de los AT2R no logró rescatar los síntomas y la neuropatología relacionados con la EA en ratones [75]. Esto sugiere que los AT2R desempeñan un papel en los efectos inducidos por los ARB, aunque el agonismo de los AT2R por sí solo puede no ser suficiente como tratamiento candidato para restaurar las deficiencias cognitivas de la EA. La función del receptor de angiotensina IV (AT4R) demostró ser necesaria para mantener la capacidad de losartán de rescatar el aprendizaje espacial y la memoria en animales APP jóvenes [35], lo que sugiere además la implicación de diferentes cascadas de angiotensina/receptor de angiotensina. Un estudio reciente en el mismo modelo de ratón APP encontró que la administración de angiotensina IV era capaz de restaurar los deterioros cognitivos relacionados con A, junto con una reducción del estrés oxidativo, independientemente de la patología A [36]. Esta observación fue respaldada por un aumento en la proliferación celular, el número de células recién nacidas y la arborización dendrítica de las neuronas del hipocampo en ratones con AD tratados con angiotensina IV. La mejora cognitiva también estuvo acompañada por la restauración de la función cerebrovascular. Estos hallazgos proponen a los BRA y, en particular, a los componentes de la cascada de angiotensina IV/AT4R, como objetivos terapéuticos prometedores para la prevención y el tratamiento de los déficits neuronales y vasculares relacionados con la EA [33,34].
6.4. Modulación de la neuroinflamación por medicamentos RAS
La creciente evidencia de los últimos años sugiere un papel de RAS en la neuroinflamación asociada con AD [76,77], proponiendo medicamentos RASi como neuroprotectores y, por lo tanto, agentes terapéuticos potenciales en trastornos cerebrales. En la última década, varios estudios en el modelo de ratón de demencia y EA indican la modulación de la activación glial como uno de los posibles mecanismos que median los efectos positivos de los inhibidores de RAS sobre la cognición.
Los inhibidores de la ECA perindopril y captopril pueden prevenir la activación de la microglía y los astrocitos en el hipocampo y la corteza de modelos de EA en ratones [56,58]. También se observó una reducción similar de la activación de la microglía en un modelo de ratón con enfermedad de Parkinson después del tratamiento crónico con captopril [78]. La participación de RAS en la actividad de la función glial dentro de AD se investigó más a fondo con la administración de ARB. Se demostró que telmisartán reduce significativamente la producción de mediadores proinflamatorios y ROS por parte de las células microgliales murinas in vitro [63]. Además, el mismo estudio observó una reducción de la activación de macrófagos y microglía del hipocampo/cortical in vivo en ratones 5XFAD. Estos hallazgos proponen un papel importante de la microglía detrás de los efectos beneficiosos inducidos por RASi en el cerebro. Los bloqueadores/inhibidores centralmente activos de RAS pueden, por lo tanto, representar un tratamiento prometedor además de las terapias estándar para la EA, como los inhibidores de la colinesterasa. En apoyo de este punto de vista, se descubrió que la inhibición de RAS mejora los trastornos cognitivos al reducir la neuroinflamación relacionada con la microglía también en otros modelos animales de trastornos cerebrales, como el lupus neuropsiquiátrico y la depresión [79-81].

beneficio de la cistanche deserticola: antiinflamatorio
7. Nuevos medicamentos RAS
La modulación de aminopeptidasa-A (AP-A) y aminopeptidasa-N (AP-N) en el cerebro ha mostrado cambios efectivos en la PA sistémica a través de inyecciones intracerebroventriculares en ratas [82,83]. Los mecanismos de regulación de la PA propuestos en estos trabajos son la producción de AngIII [82] o el aumento de su metabolismo [83]. Otro estudio encontró que la actividad de la aminopeptidasa en el hipocampo podría hidrolizar péptidos neuroprotectores como la encefalina, lo que demuestra que el tratamiento con bestatina es neuroprotector contra la muerte neuronal CA1 inducida por la privación de oxígeno y glucosa [84]. Además de su actividad en el RAS del cerebro, AP-A se involucró recientemente en la agregación de amiloide a través del truncamiento N-terminal de A. En este estudio, la inhibición de AP-A con RB150 (descrito a continuación) restauró la densidad de las espinas dendríticas de hongos y redujo las espinas inmaduras similares a filopodios en cortes organotípicos del hipocampo. Además, el trabajo mostró una mayor actividad de AP-A en los primeros casos de EA [85]. Como se discutió anteriormente en esta revisión, se ha demostrado que los factores de riesgo ambientales para la EA, como los metabolitos del colesterol, alteran la expresión de AP-A y AP-N y se correlacionan con la disminución de la memoria espacial en ratones [24]. Así, AP-A y AP-N representan dianas farmacológicas con eficacia demostrada en la regulación de la presión arterial. Sin embargo, el efecto de su modulación en la cognición y como estrategia preventiva de la EA apenas ha comenzado a caracterizarse. Para cambiar la expresión de AP-A y AP-N en el cerebro, se están desarrollando diversos fármacos, y elaboraremos una nueva clase de moléculas pequeñas que pueden pasar la BBB, y vectores de nanopartículas que también pueden superar los problemas de barrera de entrega de cerebro.
7.1. Moléculas Pequeñas para Modulación APA y APN.
EC33 y su profármaco RB150/Firibastat EC33 ((S)-3-amino-4-ácido sulfónico de mercapto-butilo) es un inhibidor de AP-A administrado por vía oral que no puede atravesar la BBB [86]. Sin embargo, cuando se inyectó por vía intracerebral en los ventrículos (hasta 100 microgramos), EC33 inhibió la actividad AP-A cerebral en el rango de 12 a 50 microgramos en ratones conscientes [87] y, en un estudio diferente, inhibió la producción de AngIII como se observó. por radiomarcaje de [3H]Ang III [88]. Dado que EC33 no puede ingresar al cerebro, se desarrolló el profármaco RB150, también conocido como firibastat. Firibastat puede cruzar la BBB cuando se administra por vía oral y no altera la PA en ratas normotensas. Este profármaco puede cruzar la BBB y entrar en el cerebro, donde la escisión de su puente disulfuro central por las reductasas cerebrales libera dos moléculas de EC33. En ratas, mostró actividad reductora de la PA de 2 a 15 horas después de la administración [89]. Como se mencionó anteriormente en este trabajo, la actividad comprobada de firibastat para la neurodegeneración se basa en la inhibición de la actividad de la aminopeptidasa sobre A, lo que disminuye la abundancia de especies A tóxicas y su efecto sobre la fisiología neuronal [85].
También hemos mencionado que la vasoconstricción y la reducción del flujo linfático podrían promover la agregación de proteínas en el cerebro; por lo tanto, firibastat, a través de la actividad de EC33 en el cerebro, podría mejorar potencialmente estos factores de riesgo que influyen directamente en la cognición al reducir la actividad de AP-A y los niveles de AngIII. Firibastat alcanzó un ensayo clínico de fase IIb llamado NEW-HOPE (NCT03198793), en el que demostró actividad hipotensora segura y eficaz en poblaciones de alto riesgo [90].
7.2. NI929 y NI956/QGC006
EC33 se diseñó primero como un inhibidor sistémico de AP-A y demostró que la unión de AP-A era suficiente para disminuir su actividad [86]. El NI929 no peptídico ([3S,4S]-3-amino- 4-mercapto-6-fenil-hexano-1-ácido sulfónico), es una molécula pequeña con una potente actividad como AP-A inhibidor, 10 veces más potente que EC33 in vitro (Ki=30 nmol) y capaz de cruzar la BHE hacia el cerebro [91]. Cuando NI929 se dimeriza mediante un puente disulfuro, forma un dímero denominado NI956, cuya principal ventaja es la capacidad de cruzar la BBB cuando se administra por vía oral. Además, NI956 regularía a la baja de forma efectiva la actividad de AP-A sin alterar las concentraciones plasmáticas de sodio y potasio a una dosis de fracción 10- veces superior a la requerida para RB150. Desafortunadamente, este medicamento solo se ha probado en animales y no se ha informado de un ensayo clínico.
7.3. Vectores de administración multietapa (MDV) y nanopartículas para la terapia RASi
El desarrollo de MDV obedece a la necesidad de un sistema de entrega que pueda utilizar activamente los transportadores en la BHE, como la transferrina [92,93]. También sigue la necesidad de apuntar a un objetivo específico o a un grupo de objetivos presentes en las células, que también se pueden usar como objetivos específicos de células [94]. Los MDV se desarrollaron inicialmente para tratar ciertos tipos de tumores, que albergan células madre cancerosas en su núcleo y producen capas extensas de tejido conectivo y vascular [92]. En estos tumores, los MDV tienen un recubrimiento inicial que permitirá que el vector ingrese a la(s) primera(s) capa(s) de tejido, lo que libera el vector recubierto con un ligando que brinda especificidad de objetivo. Después de la unión ligando-receptor, el vector se internaliza en las células y libera el fármaco, que ejerce efectos terapéuticos. Sin embargo, la visualización de una capa tumoral como la BBB dio lugar a la idea de utilizar el revestimiento multietapa para administrarlo directamente en el cerebro [95,96].
Los MDV ya no parecen una idea novedosa; sin embargo, los descubrimientos recientes sobre la señalización lisosomal abren el camino para aplicaciones novedosas que pueden beneficiarse de la entrega de MDV. En ciertos tipos de cáncer, la señalización del dolor es transducida por receptores acoplados a G (GPCR), que al activarse se internalizan en vesículas en las células nerviosas [97]. Normalmente, este mecanismo conduce a una disminución en la señalización del dolor debido a la falta de disponibilidad de los GPCR para unirse a sus ligandos; sin embargo, en el cáncer, los GPCR internalizados pueden continuar emitiendo señales desde dentro de los lisosomas internalizados, lo que se traduce en un dolor crónico que no responde. al tratamiento con opioides [98]. Para abordar este problema, Jimenez-Vargas y sus colaboradores diseñaron un sistema de nanopartículas que aprovecha el pH ácido presente dentro de los lisosomas donde se internalizan los GPCR. Estas nanopartículas tienen un ligando que inactiva la señalización de la proteína G aguas abajo de los GPCR y solo se libera en condiciones ácidas del lisosoma, evitando la unión no específica asociada con los inhibidores de GPCR y disminuyendo la dosis efectiva en órdenes de magnitud [99].
La señalización de angiotensina depende, al menos parcialmente, de los GPCR que reclutan arrestinas para internalizar los receptores de angiotensina como una forma de desensibilización [1,100]. Los complejos receptor de angiotensina-arrestina se dirigen hacia el endosoma para ayudar en el reciclaje o la degradación de los receptores [101]. Sin embargo, la señalización y el andamiaje alternativos pueden ocurrir después de la formación de los complejos de detención de ATR, ya que las arrestinas pueden reclutar varias moléculas de señalización para los receptores ya acoplados en los endosomas [100]. Esto representa una posible ruta de señalización para el RAS cerebral que persiste incluso después de que los péptidos de angiotensina no estén presentes, lo que podría dificultar las terapias RASi. Por lo tanto, sería posible dirigir los bloqueadores de los receptores de angiotensina que se unirán solo en condiciones endosómicas ácidas, lo que permitiría regular la señalización de la presión arterial independientemente de las cantidades de isoformas de angiotensina presentes en el cerebro. Esto supondría alteraciones en el reciclaje endosómico de los ATR, ya que su bloqueo en los endosomas podría potenciar su degradación por el proteosoma o por mecanismos de autofagia. Además, dado que los bloqueadores de ATR pueden ser moléculas pequeñas, son adecuados para unirse a los MDV y potencialmente administrarse sistémicamente [101,102]. Proponemos que el efecto general de bloquear la señalización de angiotensina en el cerebro puede actuar para prevenir la activación glial (dada su expresión de solo AT1R) y posiblemente la vasoconstricción, mejorando el flujo sanguíneo y la disponibilidad de glucosa para la función neuronal. Las terapias de prueba de concepto en modelos animales demostraron que es posible unir inhibidores de RAS a nanopartículas basadas en polímeros con efectos reductores de la PA [103]. Además, las nanopartículas lipídicas que contienen siRNA para angiotensinógeno mostraron efectos reductores de la PA en ratas [104], aunque esta terapia se encuentra aguas arriba de la vía de señalización, mientras que proponemos regular la señalización después de que se hayan activado los ATR, asegurando una terapia más específica que, por ejemplo, inhiben la señalización de RAS en astrocitos pero no en células vasculares sin alterar los niveles globales de Ang.

efectos de la cistanche deserticola
8. Perspectivas futuras
A partir de los estudios mencionados aquí, se pueden identificar varias vías para la investigación en el cerebro RAS. Mencionamos el uso de nanopartículas para inhibir la señalización RAS después de la activación de ATR, sin embargo, los mecanismos que involucran la señalización lisosomal y el andamiaje en el cerebro RAS siguen sin explorarse en gran medida. Por ejemplo, la activación de AT1R conduce a la señalización de un segundo mensajero que estimula las proteasas de membrana como ADAM, que a su vez puede activar otros receptores de tirosina quinasa [105]. Hasta donde sabemos, no está claro si este fenómeno ocurre en los astrocitos o en las células vasculares del cerebro.
24-S-hidroxicolesterol (24-OH) y 27-OH son metabolitos de colesterol que pueden activar el RAS en células neuronales in vitro [24,106]. Además, estos oxiesteroles tienen claros efectos moduladores sobre la función sináptica, con la activación de CYP46A1 como neuroprotector [107–111] y niveles altos de 27-OH como perjudiciales [24,112–114]. Cuando se trata de modelos animales para la EA, hay muy pocos ejemplos que combinen factores de riesgo como la hipercolesterolemia con alteraciones genéticas conocidas que conducen a la amiloidosis. Los ratones CYP27Tg no tienen neurodegeneración por sí mismos, sin embargo, se desconoce cómo estos fenotipos se sinergizarían con los modelos genéticos que producen en exceso beta amiloide para promover la muerte neuronal. Por el contrario, la activación de CYP46A1 se estudió como diana farmacológica para la enfermedad de Alzheimer y la enfermedad de Huntington [107,109,110], pero los mecanismos que ofrecen neuroprotección aún no se conocen bien. CYP46Tg, un modelo de ratón que sobreexpresa CYP46A1 con altos niveles de 24-OH [115], no se ha estudiado en el contexto de la neurodegeneración de la EA, donde podría promover la neuroprotección y mantener la cognición durante el envejecimiento, como sugieren los estudios conductuales sobre CYP46Tg solo [107].
Recientes descubrimientos sobre la modulación circadiana del sistema de limpieza del cerebro abren el camino para estudiar nuevas terapias sobre proteinopatías. Los enfoques terapéuticos para tratar la amiloidosis nunca han considerado que se produce una mayor tasa de eliminación en el cerebro durante el sueño [116], lo que sugiere de inmediato que se podría encontrar alguna asociación entre la melatonina y las terapias RASi en pacientes. En ratas, la melatonina mostró modulación de la aminopeptidasa regulada por insulina (IRAP) en la glándula pineal [117], y anteriormente se sugirió que la inhibición de IRAP puede mejorar la cognición [118]. Sin embargo, la relación entre estas moléculas queda por estudiar en humanos.
Finalmente, existe una fuerte evidencia de que la EA puede ser multifactorial [119–122], lo que resalta la importancia de la estratificación de cohortes para las intervenciones de estudio en neurodegeneración. La estratificación por edad mejora el análisis de cohortes para estimar el riesgo del genotipo APOE [123]. Además, se estudió el perfil correcto de biomarcadores inflamatorios específicos del paciente como estrategia para mejorar el diagnóstico y el pronóstico en la EA y la enfermedad de Parkinson [124]. Por lo tanto, los estudios que analizan el uso de terapias RASi en humanos deben reforzarse con una estratificación de pacientes adecuada y relevante para encontrar asociaciones más claras entre la función cerebral RAS y la cognición. Esto seguramente conducirá al descubrimiento de mejores objetivos para mejorar la función cognitiva a través de la modulación del RAS cerebral y aumentará las alternativas para el tratamiento de la EA y otras enfermedades neurodegenerativas.








